Особенности медицинской реабилитации пациентов, перенесших пластику передней уретры с использованием слизистой щеки, при первично выявленной стриктуре передней уретры
- Аннотация
- Статья
- Ссылки
- English
Материал и методы. Проведено клиническое исследование пациентов после уретропластики с использованием буккального (щечного) графта при первично выявленной стриктуре передней уретры. Реабилитационная программа включала физиотерапевтическое воздействие (низкоинтенсивная лазерная терапия на область операционного вмешательства и донорскую зону), медикаментозное сопровождение и функциональный мониторинг. Эффективность терапии оценивалась по показателям уродинамики (Qmax), выраженности болевого синдрома, скорости эпителизации и частоте воспалительных осложнений.
Результаты. Применение низкоинтенсивной лазерной терапии способствовало ускорению процессов эпителизации, уменьшению болевого синдрома и снижению частоты воспалительных осложнений в послеоперационном периоде. Через шесть месяцев отмечалось повышение максимальной скорости потока мочи (Qmax) в среднем на 48% по сравнению с исходными данными, а также улучшение показателей эректильной функции и качества жизни.
Заключение. Комплексная медицинская реабилитация пациентов после уретропластики с использованием буккального графта, включающая низкоинтенсивную лазерную терапию, является эффективным и патогенетически обоснованным направлением восстановления. Такой мультидисциплинарный подход обеспечивает выраженный клинический эффект и должен рассматриваться как обязательный компонент ведения больных после реконструктивных операций на уретре.
Материал и методы. Проведено клиническое исследование пациентов после уретропластики с использованием буккального (щечного) графта при первично выявленной стриктуре передней уретры. Реабилитационная программа включала физиотерапевтическое воздействие (низкоинтенсивная лазерная терапия на область операционного вмешательства и донорскую зону), медикаментозное сопровождение и функциональный мониторинг. Эффективность терапии оценивалась по показателям уродинамики (Qmax), выраженности болевого синдрома, скорости эпителизации и частоте воспалительных осложнений.
Результаты. Применение низкоинтенсивной лазерной терапии способствовало ускорению процессов эпителизации, уменьшению болевого синдрома и снижению частоты воспалительных осложнений в послеоперационном периоде. Через шесть месяцев отмечалось повышение максимальной скорости потока мочи (Qmax) в среднем на 48% по сравнению с исходными данными, а также улучшение показателей эректильной функции и качества жизни.
Заключение. Комплексная медицинская реабилитация пациентов после уретропластики с использованием буккального графта, включающая низкоинтенсивную лазерную терапию, является эффективным и патогенетически обоснованным направлением восстановления. Такой мультидисциплинарный подход обеспечивает выраженный клинический эффект и должен рассматриваться как обязательный компонент ведения больных после реконструктивных операций на уретре.
Введение
Стриктура уретры представляет собой патологическое сужение мочеиспускательного канала, приводящее к серьезным нарушениям мочеиспускания, ухудшению качества жизни пациента и развитию различных осложнений. Среди хирургических методов лечения стриктур передней уретры одним из наиболее эффективных является уретропластика с использованием буккального (щечного) графта [1, 2].
Д.Ю. Пушкарь и соавт. в своем исследовании 2012 г. установили, что после буккальной уретропластики показатели по шкале IPSS и индексу качества жизни (Quality of Life, QoL) значительно улучшаются к третьему месяцу после операции и остаются стабильными в течение всего периода наблюдения [1]. С.И. Гамидов и соавт. (2017) подчеркивают важность этапной заместительной уретропластики с использованием слизистой оболочки ротовой полости, что позволяет эффективно восстанавливать проходимость мочеиспускательного канала и снижает частоту осложнений [3].
По данным исследования G. Barbagli и соавт. (2021), включавшего исследование 236 пациентов, применение буккального графта снизило частоту рецидивов на 31% и улучшило средние показатели Qmax на 42% через шесть месяцев после операции [4].
Систематический обзор оптимального лечения стриктур уретры представлен в работе S. Bugeja и соавт. [5], что позволило разработать базовый документ, который был одобрен секцией андрологии и мочеполовой хирургии Британской ассоциации хирургов-урологов (The British Association of Urological Surgeons, BAUS).
Однако даже при успешно проведенной операции важным аспектом остается послеоперационная медицинская реабилитация, направленная на восстановление функции уретры, улучшение мочеиспускания, профилактику осложнений и повышение качества жизни пациентов.
В ряде исследований отмечена важность физиотерапевтических методов для ускорения заживления тканей и восстановления уродинамических показателей [6, 7]. В метаанализе А.Г. Мартова 2020 г. авторы подчеркивают, что применение лазеротерапии и магнитотерапии позволяет улучшить показатели урофлоуметрии в среднем на 35% через шесть месяцев после операции [6].
Показано, что применение преформированных физических факторов после реконструктивных операций на уретре способствует улучшению микроциркуляции и снижению воспалительной реакции [8]. По данным одного из зарубежных исследований по лечению стриктур уретры, отмечено, что наиболее успешные результаты терапии достигнуты при комбинированном подходе [9].
В работах российских ученых и обзорных статьях подтверждена значимость комплексного подхода к медицинской реабилитации пациентов после уретропластики. Отмечено, что сочетание хирургического лечения с последующей программой реабилитации, включающей преформированные физические факторы, улучшает заживление, уродинамические показатели и снижает частоту послеоперационных осложнений по сравнению с изолированной хирургической тактикой [10, 11].
Включение преформированных факторов физиотерапии в комплекс реабилитационных мероприятий позволяет снизить риск осложнений, ускорить восстановление и повысить качество жизни пациентов после уретропластики [9].
Материал и методы
В исследование, проведенное на базе урологических клиник в течение пяти лет, были включены 63 пациента в возрасте от 35 до 65 лет (средний возраст 50,2 ± 8,1 года), перенесшие уретропластику по поводу стриктуры передней уретры. Средняя протяженность стриктуры у пациентов составила 2,5 ± 1,1 см. Оценку состояния проводили через один, три, шесть месяцев после операции, анализируя клинические и функциональные показатели.
Критерии включения:
- мужчины с подтвержденной стриктурой передней уретры;
- возраст – 35–65 лет;
- отсутствие тяжелых сопутствующих заболеваний, влияющих на процесс заживления;
- согласие пациента на участие в исследовании.
Критерии исключения:
- наличие тяжелых сопутствующих заболеваний (например, неконтролируемый сахарный диабет, онкологические заболевания);
- активные инфекционные заболевания мочеполовой системы;
- предыдущие неудачные попытки уретропластики в течение последнего года.
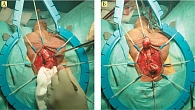
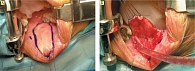
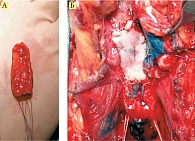
Хирургическое лечение
Во всех случаях выполнялась пластика передней уретры с использованием буккального графта (рис. 1–3). Пациенты, включенные в исследование, имели стриктуры уретры протяженностью более 1 см, что требовало применения свободного трансплантата для адекватного восстановления просвета мочеиспускательного канала. Для реконструкции пораженного участка уретры были использованы фрагменты слизистой оболочки щеки, что позволило обеспечить высокую степень васкуляризации, снизить риск рубцевания и рецидива стриктуры, а также улучшить долгосрочный прогноз после операции.
Медикаментозная терапия
В лекарственную терапию были включены противовоспалительные препараты (ибупрофен, диклофенак, мелоксикам), а также антиоксиданты и препараты, улучшающие микроциркуляцию. Проведена антибактериальная профилактика (цефтриаксон, 2 г ×1 р/сут в течение 5 дней).
Реабилитационные мероприятия
В лазеротерапии для стимуляции заживления тканей были использованы аппараты типа «Матрикс» и «Лазмик», обеспечивающие стабильное низкоинтенсивное воздействие. Для оптимального проникновения излучения в ткани и стимуляции регенерации были применены лазерные излучатели длиной волны 635 нм (красный спектр) и 850–904 нм (инфракрасный спектр). Воздействие лазером на область операционной раны и области забора трансплантата (слизистой щеки) проводили на уровне доступа к локализации стриктуры, что способствовало улучшению микроциркуляции, активизации клеточного метаболизма и репаративных процессов слизистой ткани в зоне оперативного вмешательства.
Были использованы специальные насадки: магнитно-лазерные (усиливающие терапевтический эффект благодаря комбинации лазерного и магнитного воздействия); фокусирующие оптические (обеспечивающие равномерное распределение лазерного пучка на обрабатываемой поверхности); сканирующие лазерные модули (для расширенного воздействия на область трансплантата).
Процедуры начинали со второго дня после операции, после первичного заживления операционной раны. Воздействие проводили ежедневно в течение первых 10 дней послеоперационного периода. Курс лечения включал 10 сеансов с экспозицией 5–7 минут на каждую зону с общим объемом воздействия – 50–80 Дж/сеанс. Параметры излучения были подобраны индивидуально в зависимости от скорости заживления тканей пациента. После окончания всех процедур удаляли уретральный катетер и проводили урофлоуметрию для контроля результата.
Применение данной методики позволило существенно ускорить эпителизацию слизистой щеки, снизить риск воспалительных осложнений и уменьшить болевой синдром у пациентов. Согласно данным клинических наблюдений, время полной эпителизации слизистой уменьшилось на 25% (среднее время 12,3 ± 2,1 дня против 16,5 ± 3,4 дня в контрольной группе). Частота воспалительных осложнений снизилась до 8,7% против 15,4% у пациентов, не получавших лазерную терапию. Пациенты, получившие данное лечение, отметили снижение болевого синдрома на 30–40% по шкале ВАШ (от 7,2 ± 1,1 до 4,3 ± 0,9 балла) по сравнению с контрольной группой, что подтверждает эффективность низкоинтенсивной лазерной терапии в послеоперационной реабилитации.
Для оценки результатов лечения проводили урофлоуметрию через один, три, шесть месяцев после операции; классифицировали уровень эректильной функции по шкале IIEF-5; определяли выраженность симптомов нарушения мочеиспускания по шкале IPSS и качество жизни с помощью опроса по шкале QoL. Статистическую обработку данных осуществляли с использованием методов описательной и сравнительной статистики. Количественные показатели представляли в виде среднего значения и стандартного отклонения (M ± SD). Для оценки различий между показателями до и после операции применяли парный t-критерий Стьюдента или критерий Уилкоксона при отсутствии нормального распределения.
Результаты
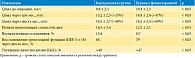
На основе собранных данных и анализа других исследований [5] получены следующие результаты (таблица).
Через три месяца после операции средний объемный поток мочи (Qmax) увеличился на 35% по сравнению с предоперационными показателями, что подтверждает эффективность хирургического вмешательства и последующей реабилитации. Через шесть месяцев после операции показатель Qmax продолжал расти и достиг увеличения на 48% по сравнению с предоперационными данными. У пациентов, проходивших дополнительную физиотерапию, этот показатель был выше на 12% по сравнению с контрольной группой, что свидетельствует о стойком положительном эффекте комплексного лечения и реабилитации.
В группе с дополнительно назначенной физиотерапией у 87% пациентов было отмечено значительное улучшение мочеиспускания и исчезновение дизурических расстройств. В контрольной группе этот показатель составил 78%, что подчеркивает пользу физиотерапии в восстановительном процессе.
Лазерная терапия области забора трансплантата (слизистой щеки) способствовала ускорению регенерации тканей, снижению воспалительных реакций и уменьшению болевого синдрома. В группе с дополнительно назначенной физиотерапией среднее время полной эпителизации слизистой составило 12,3 ± 2,1 дня против 16,5 ± 3,4 дня в контрольной группе. Частота воспалительных осложнений снизилась до 8,7% против 15,4% соответственно.
Оценка по шкале IIEF-5 показала умеренное снижение эректильной функции в раннем послеоперационном периоде, однако у 79% пациентов из группы с дополнительно назначенной физиотерапией через шесть месяцев наблюдалось полное восстановление сексуальной функции. В контрольной группе этот показатель составил 68%.
Качество жизни (по шкале QoL) в контрольной группе улучшилось на 40% по сравнению с предоперационным уровнем. В группе пациентов, получавших дополнительную физиотерапию, данный показатель вырос на 47%.
Обсуждение
Результаты исследования подтверждают высокую эффективность комплексной медицинской реабилитации после уретропластики с использованием буккального графта. Применение физиотерапевтических методов, таких как магнитно-лазерная терапия области забора трансплантата (слизистой щеки), играет ключевую роль в ускорении процессов заживления и снижении воспалительных реакций [9]. Лазерное воздействие способствует регенерации тканей, минимизации болевого синдрома и улучшению микроциркуляции, что позволяет избежать развития послеоперационных осложнений.
Сравнительный анализ данных исследований показывает, что включение комплексных реабилитационных программ значительно улучшает прогноз у пациентов. В исследовании D. Ambrosio и соавт. [7] выявлено, что лазеротерапия сокращает период заживления донорской зоны, снижая риск инфекционных осложнений и дискомфорта у пациентов. Согласно клиническим рекомендациям РФ (2024), после уретропластики показано регулярное динамическое наблюдение (1, 3, 6, 9, 12 месяцев в первый год, затем ежегодно) с использованием IPSS/IIEF-5 и урофлоуметрии. Включение физиотерапевтических методик может быть рассмотрено по клиническим показаниям для оптимизации восстановления уродинамических показателей.
Заключение
В восстановительном периоде после уретропластики с использованием слизистой щеки рекомендуется использовать не только стандартные хирургические и медикаментозные методы, но и физиотерапевтические мероприятия, направленные на улучшение кровоснабжения, регенерацию тканей и восстановление функций. Комплексный подход к реабилитационным мероприятиям позволяет достичь более высоких результатов в лечении стриктуры передней уретры, повышая качество жизни пациентов и снижая риск рецидива.
V.A. Shchekochikhin, L.S. Kruglova, PhD, Prof., S.P. Darenkov, PhD, Prof.
Central State Medical Academy of the Presidential Administration of the Russian Federation, Moscow
Clinical Hospital of the Presidential Administration of the Russian Federation, Moscow
Contact person: Vladimir A. Shchekochikhin, shch.v@mail.ru
Aim. To evaluate the effectiveness of a comprehensive postoperative rehabilitation program, including low-intensity laser therapy, in improving uroflowmetry parameters, erectile function, and quality of life in patients undergoing buccal mucosa graft urethroplasty for anterior urethral stricture.
Material and methods. A clinical study was conducted in patients undergoing urethroplasty with a buccal mucosa graft for primary anterior urethral stricture. The rehabilitation protocol included physiotherapy (low-intensity laser therapy applied to the surgical and donor areas), pharmacological treatment, and functional monitoring. The efficacy of the approach was evaluated by uroflowmetry parameters (Qmax), pain intensity, epithelialization rate, and incidence of inflammatory complications.
Results. Low-intensity laser therapy significantly accelerated epithelialization, reduced pain intensity, and decreased the rate of postoperative inflammatory complications. Six months after surgery, maximum urinary flow rate (Qmax) increased by an average of 48%, accompanied by improvement in erectile function and overall quality of life.
Conclusion. Comprehensive medical rehabilitation after buccal mucosa urethroplasty, including low-intensity laser therapy, represents an effective and pathogenetically justified strategy for functional recovery. This multidisciplinary approach provides significant clinical benefits and should be considered an integral component of postoperative management in urethral reconstruction patients.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.