Неспецифические вагиниты: стратегия комплексной локальной терапии
- Аннотация
- Статья
- Ссылки
- English
Цель – оценить эффективность и безопасность применения препарата Суперлимф 25 ЕД с антисептиком деквалиния хлоридом, таблетки вагинальные 10 мг, в комплексной терапии женщин репродуктивного возраста с неспецифическим вагинитом/вагинозом.
Материал и методы. Под наблюдением находилось 60 пациенток в возрасте 20–45 лет с диагностированным вульвовагинитом, обратившихся к гинекологам двух лечебно-диагностических центров по поводу патологических выделений из половых путей. Диагноз подтвержден клинически, микроскопически и методом полимеразной цепной реакции.
Результаты. Согласно результатам клинико-лабораторных исследований и наблюдениям, эффективность терапии была высокой в группах, в которых пациентки одновременно с базовой терапией получали иммуноцитокиновый препарат Суперлимф 25 ЕД, суппозитории ректальные и вагинальные. После лечения отмечался длительный безрецидивный период. Переносимость препарата была хорошей, нежелательных реакций не зарегистрировано.
Цель – оценить эффективность и безопасность применения препарата Суперлимф 25 ЕД с антисептиком деквалиния хлоридом, таблетки вагинальные 10 мг, в комплексной терапии женщин репродуктивного возраста с неспецифическим вагинитом/вагинозом.
Материал и методы. Под наблюдением находилось 60 пациенток в возрасте 20–45 лет с диагностированным вульвовагинитом, обратившихся к гинекологам двух лечебно-диагностических центров по поводу патологических выделений из половых путей. Диагноз подтвержден клинически, микроскопически и методом полимеразной цепной реакции.
Результаты. Согласно результатам клинико-лабораторных исследований и наблюдениям, эффективность терапии была высокой в группах, в которых пациентки одновременно с базовой терапией получали иммуноцитокиновый препарат Суперлимф 25 ЕД, суппозитории ректальные и вагинальные. После лечения отмечался длительный безрецидивный период. Переносимость препарата была хорошей, нежелательных реакций не зарегистрировано.







Введение
Использованию у пациенток с вагинальной инфекцией современных препаратов, нормализующих микробиоту урогенитального тракта, на фоне комбинированной терапии посвящен ряд исследований разного уровня доказательности. Сегодня ученые активно изучают микробиом человека, влияние мукозального иммунитета на бактериальные ассоциации и биопленки при вагинальной инфекции, нарушение эубиоза вульвовагинального тракта и пути его коррекции [1].
Неспецифические вагиниты становятся все более серьезной проблемой в акушерстве и гинекологии в силу не только рецидивирующего течения, но и очевидного влияния на состояние репродуктивной системы женщин фертильного возраста.
Согласно данным литературы, основными клинико-лабораторными синдромами воспаления и дисбаланса микробиоты влагалища являются:
- дисбиоз со снижением количества лактобактерий и заменой грибковой микробиотой с развитием кандидозного вульвовагинита (КВВ);
- дисбаланс с преобладанием анаэробной биоты, который приводит к развитию бактериального вагиноза (БВ);
- дисбаланс с преобладанием аэробной биоты над другими постоянными симбионтами микрофлоры влагалища – неспецифический вагинит [2, 3].
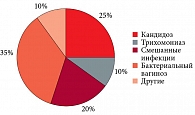
Как показывают результаты исследований, в структуре вульвовагинальных инфекций (ВВИ) на долю БВ приходится 24–35%, на долю КВВ – 6,5–25% [4, 5]. При этом самой частой причиной патологических вагинальных выделений является БВ [6, 7]. Из коинфекций наиболее часто встречаются БВ и КВВ (0,8–25%) и смешанные инфекции (0,1–20%) [4, 8] (рис. 1).
Наряду с ростом заболеваемости отмечаются развитие лекарственной устойчивости к большинству антибиотиков, изменение иммунологической реактивности организма и, как следствие, уменьшение концентрации факультативных лактобактерий. В результате снижается содержание молочной кислоты, кислотность влагалищного секрета, возрастает количество анаэробов и развиваются дисбиотические процессы вульвовагинального тракта.
Изменение гомеостаза слизистой оболочки влагалища и эктоцервикса сопровождается избыточным ростом чужеродных для индивидуального микробиома условно патогенных микроорганизмов (УПМ) и нарушением вагинального биотопа [9]. Снижение неспецифической резистентности больных является одной из причин воспалительного процесса, его рецидивирующего течения, торможения регенерации и восстановления функции инфицированных органов с формированием патологических биопленок [5, 10, 11].
Анаэробный дисбиоз способен трансформироваться не только в БВ, но и в вагиниты смешанного характера. В подобной ситуации прослеживается универсальный патогенетический сценарий со сменой биотопа: лактобактерии и анаэробы подавляются, а аэробная флора приобретает качественные конкурентные преимущества, что способствует ее активному размножению [2, 3, 7].
Способность вытеснять адгезированные на вагинальном эпителии лактобактерии определяет развитие и персистенцию ВВИ в ассоциации с УПМ, которая приобретает большую инфекционность и выявляется у 70% пациенток с патологическими вагинальными выделениями.
Наиболее часто нормофлора замещается сообществами анаэробных бактерий или смешанной аэробно-анаэробной микрофлорой. Чистый аэробный дисбиоз встречается редко [2, 3, 8, 12]. Утрачивается доминирующий статус Lactobacillus, и проявляется избыточный рост облигатных и факультативных анаэробов, таких как Gardnerella vaginalis, Prevotella spp., Atopobium vaginae и Mobiluncus spp., различающихся вирулентностью, цитотоксичностью и способностью к адгезии [4, 5, 13].
Дисбаланс количественного и качественного состава микробиоты приводит к утрате иммунологического контроля на фоне каскада метаболических изменений и нарушению колонизационной резистентности биотопа, что реализуется в симптоматике ВВИ у значительной части пациенток.
С учетом сказанного при ВВИ должны применяться не только антибиотики [14] и пробиотики, но и препараты метаболической терапии, потенцирующие рост резидентной микрофлоры и способствующие регенерации вагинального эпителиального матрикса [9, 15].
В соответствии с российскими клиническими рекомендациями, для диагностики неспецифических смешанных вульвовагинитов применяются микробиологические исследования, определяющие микроэкологические нарушения вагинального биотопа, и общепринятые критерии Амселя с оценкой по критерию Ньюджента: полуколичественный подсчет морфотипов бактерий в мазках вагинального секрета, окрашенных по Граму [16]. Десятибалльную шкалу используют в качестве золотого стандарта (количество баллов в пределах 7–10 считается патогномоничным для БВ).
Таким образом, клинические признаки и данные лабораторных исследований служат основой для постановки диагноза и выбора этиотропного лечения. Показаниями к назначению такого лечения в конечном итоге служат три объективно значимых критерия [2, 5, 6]:
- инфекции, передаваемые половым путем (ИППП);
- специфические жалобы (выделения, запах, зуд, жжение и др.);
- клинические признаки, характерные для воспалительных процессов во влагалище.
Своевременная комбинированная этиотропная терапия вагинитов, направленная на быструю элиминацию возбудителей за счет непосредственного влияния на инфекционный агент, и препараты, активно воздействующие на биопленки и метаболизм бактерий, выполняют сочетанную антимикробную и иммуномодулирующую функцию.
За счет стимулирующего воздействия комменсалов на мукозальный иммунитет восстанавливается колонизационная резистентность влагалищного биотопа, формируется устойчивое равновесие системы и обеспечивается длительный безрецидивный эффект после лечения.
Лекарственные препараты с разным механизмом действия, не повреждающие эпителий и резидентную микробиоту, нормализующие рН вагинального секрета с одновременной стимуляцией мукозального иммунитета, считаются наиболее перспективными в лечении ВВИ. Указанным критериям отвечает отечественный препарат Суперлимф 25 ЕД, суппозитории ректальные и вагинальные, в состав которого входит стандартизированный комплекс природных цитокинов необходимой концентрации: интерлейкин (ИЛ) 1, фактор некроза опухоли альфа, макрофагальный фактор, ИЛ-6, ряд минорных компонентов цитокинов, хемокинов и антимикробных пептидов.
Цель – оценить эффективность и безопасность трех схем применения препарата Суперлимф 25 ЕД (производитель – ООО «Альтфарм», разработчик и держатель регистрационного удостоверения в ЕАЭС – ООО «Центр иммунотерапии ИММУНОХЕЛП», дистрибьютор – ООО «Биотехфарм») с антисептиком деквалиния хлоридом, таблетки вагинальные 10 мг, в комплексной терапии пациенток репродуктивного возраста с неспецифическим вагинитом/вагинозом.
Материал и методы
В исследовании участвовало 60 пациенток в возрасте 20–45 лет, обратившихся к гинекологам двух лечебно-диагностических центров Центрального федерального округа и Москвы.
На основании специфических жалоб, визуальных клинических признаков и результатов лабораторного тестирования у всех обследованных диагностирована ВВИ.
При первичном осмотре выполнено полное клинико-лабораторное обследование: бактериоскопия отделяемого цервикального канала и влагалища с окраской по граму, оценка по критериям Амселя вагинального содержимого, гинекологический осмотр.
Критериями включения в исследование были:
- возраст от 20 до 45 лет;
- неспецифическая вульвовагинальная инфекция, подтвержденная в мазках, окрашенных по граму, рН-метрией вагинального секрета, аминным тестом и ПЦР-диагностикой (Фемофлор-16);
- желание и способность выполнять требования протокола на протяжении всего исследования;
- заполненное и подписанное информированное согласие на участие в исследовании.
Критерии невключения:
- гиперчувствительность к любому компоненту, входящему в состав исследуемых препаратов;
- ИППП;
- ВПЧ-положительный статус с тяжелой дисплазией шейки матки;
- любое клинически значимое состояние, из-за которого, по мнению исследователя, пациентка не может участвовать в исследовании.
На протяжении всего исследования в целях контрацепции женщины использовали барьерные методы (презерватив).
Согласно дизайну исследования, пациенткам назначали терапию с учетом клинических симптомов вагинальной инфекции, результатов микроскопии влагалищных мазков, окрашенных по граму, с балльной оценкой по Ньюдженту, рН-метрии вагинального секрета, исследования микробиоты с помощью теста Фемофлор-16, в совокупности подтверждающих наличие ВВИ.
Методом случайной выборки участницы исследования были разделены на три равные группы (по 20 пациенток в каждой). В первой группе назначали базовую терапию вагинита в соответствии с клиническими рекомендациями – деквалиния хлорид, таблетки вагинальные, шесть дней на ночь. Пациентки второй группы помимо базовой терапии антисептическим препаратом деквалиния хлоридом, таблетки вагинальные, утром шесть дней, применяли препарат Суперлимф 25 ЕД, суппозитории ректальные и вагинальные, на ночь по одной свече вагинально десять дней. В третьей группе помимо базовой терапии антисептическим препаратом деквалиния хлоридом, таблетки вагинальные, шесть дней на ночь, использовали препарат Суперлимф 25 ЕД, суппозитории ректальные и вагинальные, на ночь по одной свече ректально десять дней.
Пациентки трех групп были сопоставимы по возрасту, экстрагенитальному статусу, акушерско-гинекологическому анамнезу, паритету и характеру местного смешанного воспалительного синдрома.
Эффективность терапии оценивали на основании клинических и лабораторных данных после лечения и с помощью визуальной аналоговой шкалы (ВАШ) через неделю (визит 1), месяц (визит 2) и три месяца от начала терапии (визит 3).
Телемедицинское консультирование, анализ и детализация жалоб с методикой самоконтроля (кольпо-тест – полуколичественная рН-метрия вагинального секрета индикаторными полосками ООО «Биосенсор», Россия), отслеживание рецидивов в группах осуществлялись через три (визит 4) и шесть месяцев (визит 5) после завершения лечения.
Безопасность терапии оценивали исходя из анализа всех нежелательных явлений (НЯ) и серьезных НЯ (СНЯ) за весь период лечения и наблюдения (визиты 1–5).
Об удовлетворенности врача и пациента терапевтическим эффектом и клиническими результатами судили по опроснику шкалы Гуттмана (пять пунктов). За основу принимали одномерность и иерархическую связанность суждений респондентов.
Полученные результаты обрабатывали методом вариационной статистики с использованием Microsoft Office Excel 2010. Вычисляли среднее значение (М), среднеквадратическое отклонение (Q), ошибку средней арифметической (m). Бинарные показатели, характеризующие более двух связанных совокупностей, сравнивали с помощью Q-критерия Кохрена. Апостериорный анализ проводили с использованием теста Мак-Немара c поправкой Холма.
Результаты
При изучении гинекологического анамнеза установлено, что возраст менархе у пациенток значительно не отличался – 12,4 ± 1,2 года. Роды в анамнезе были у 41 (70,6%) женщины, медицинские аборты – у 19 (27,2%). Ранее малые гинекологические операции перенесли 8 (13,7%) пациенток.
Данные клинико-лабораторного обследования представлены в табл. 1.
Результаты обследования подтвердили наличие у 95% обследованных инфекционно-воспалительного процесса во влагалище с участием трех и более возбудителей.
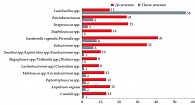
В тестируемых персональных образцах вагинального отделяемого доминировали облигатно-анаэробные микроорганизмы Enterobacteriaceae, Eubacterium spp., Streptococcus spp. Дефицит резидентной лактофлоры выявлен у каждой второй пациентки (рис. 2, табл. 2).
Микроскопия вагинальных мазков, окрашенных по граму, продемонстрировала высокую микробную концентрацию различных морфотипов облигатных анаэробов, морфологически сходных с бактероидами, мобилункусом, лептотриксом, что соответствовало результатам микробиологических посевов и данным литературы [3, 10, 12].
Оценка по ВАШ показала, что у большинства пациенток к концу первой недели (визит 1) от начала лечения клинические симптомы вульвовагинита купировались или значительно уменьшилась их выраженность, что в среднем на три-четыре дня опережало микробиологическую деконтаминацию.
Вагинальная микробиота отреагировала уменьшением микробных ассоциаций и повышением количества морфотипов лактобактерий (15 до лечения, 56 – после) на фоне хорошей переносимости препарата (рис. 2).
В нашем исследовании эффективность комбинированной терапии с микробиологической точки зрения составила 97%, о чем наглядно свидетельствовали снижение микробной контаминации и увеличение титра лактобактерий вагинального тракта. Подтверждение тому – результаты теста Фемофлор-16, проведенного через 30 дней после завершения курса лечения (рис. 2).
По критериям Амселя восстановление микрофлоры и нормализация концентрации водородных ионов зафиксированы во второй и третьей группах во время контрольного обследования через 30 дней от начала лечения (визит 2) (рис. 3).
Согласно критериям Амселя, в группах отмечалась общая положительная динамика с уменьшением количества ключевых клеток, восстановлением рН вагинального секрета даже при наличии условного нормоценоза через 30 дней от начала лечения на основании данных теста Фемофлор-16 (рис. 3–5).
Критерии эффективности, такие как отсутствие жалоб, изменение характера выделений и нивелирование симптомов диспареунии, были наиболее выражены во второй группе, несколько меньше в третьей группе, где отмечались симптомы вульварного дискомфорта без критического пика лейкоцитарного компонента в лабораторных исследованиях.
Общая продолжительность бессимптомного временного интервала превысила пять недель на фоне снижения количества коккобациллярной флоры и лейкоцитов в мазках, окрашенных по граму, до референсных значений (табл. 2).
Через три месяца после окончания лечения у всех пациенток второй группы наблюдались восстановление референсных значений рН и снижение количества ключевых клеток – до 5 в поле зрения и менее. В третьей группе аналогичные показатели составили 95 и 90%, во второй – 60 и 75% соответственно (табл. 3).
Через три месяца от начала лечения (визит 3) рецидив дисбиоза отмечался у 25% пациенток первой группы. Во второй и третьей группах этот показатель составил 5 и 10% соответственно.
В лабораторных исследованиях положительный аминный тест и наличие ключевых клеток коррелировали с жалобами пациенток первой и третьей групп на симптомы вульварного дискомфорта и вагинальные бели, что указывало на относительный дисбиоз (визит 3).
Частота вагинальных жалоб у пациенток в течение полугода после окончания лечения представлена на рис. 6. Как показал телемедицинский опрос, симптомокомплекс, ассоциированный с относительным дисбиозом, выявлен при самоконтроле рН у восьми пациенток первой группы, одной пациентки второй группы и двух пациенток третьей группы через три месяца после окончания лечения (визит 4).
Симптомы аногенитального дискомфорта, отмеченные на визите 4 во время телеконсультирования у двух пациенток третьей группы, скорее всего были обусловлены индивидуальной местной реакцией на применение интимного эмолента – геля. После консультации дерматолога и отмены геля указанные симптомы были зафиксированы при телеконсультировании только у одной пациентки данной группы. При этом персональные жалобы на патологические бели отсутствовали, значение рН – около 4,5 (визит 5).
Анализ клинических симптомов и результаты микробиологических и лабораторных исследований в динамике продемонстрировали высокую эффективность терапии во второй и третьей группах, причем более длительный безрецидивный эффект зафиксирован во второй группе, в которой пациентки в комплексе с базовой терапией применяли вагинально препарат Суперлимф 25 ЕД.
Проанализировав результаты телемедицинского опроса (оценка по ВАШ) на визитах 4 и 5, можно констатировать, что эффективность комплексной терапии в исследуемых группах составила от 75 до 97%. Переносимость препарата была хорошей.
Полученные результаты позволяют сделать вывод, что применение препарата Суперлимф в суппозиториях в течение десяти дней в качестве дополнения к этиотропной терапии эффективно и может быть рекомендовано в комплексной терапии неспецифического вульвовагинита.
В настоящем исследовании не зафиксировано ни одного случая развития НЯ, СНЯ и отказа от продолжения комплексного лечения.
Удовлетворенность врача клиническим результатом лечения была достоверно выше, чем удовлетворенность пациенток эффективностью и удобством применения препаратов два раза в день, – 92 и 83% соответственно по шкале Гуттмана.
Обсуждение
Проведенное исследование еще раз подтвердило, что инфекционно-воспалительный процесс вульвовагинального тракта обусловлен комбинацией нескольких возбудителей с разным потенциалом вирулентности.
Клинические наблюдения показывают, что смешанные вагиниты наряду с достаточно яркой клинической симптоматикой характеризуются длительным и упорным течением, высокой частотой рецидивов. Эффект от классической антибактериальной терапии может быть неполным или кратковременным.
Неудовлетворенность результатами супрессивной терапии требует поиска новых альтернативных вариантов этиотропной терапии, в том числе применения препаратов на основе цитокинов с широким спектром действия, эффективных при воспалительных заболеваниях вульвовагинального тракта.
По нашему мнению, такой подход к лечению ВВИ представляется разумной альтернативой длительной антибиотикотерапии.
Согласно полученным данным, во всех группах ведущим клиническим симптомом были патологические бели. Частота их возникновения в группах достигала 78,9–85,5%. Диспареуния, равно как зуд и жжение, на фоне воспаления имела место у каждой третьей пациентки – от 25 до 37% во всех группах.
По совокупности клинико-лабораторных данных у каждой третьей пациентки с вагинитом превалировал микст бактериальных ассоциантов, характерных для БВ, у каждой второй (36,7%) – смешанные аэробно-анаэробные ассоциации микроорганизмов, что согласуется с современными представлениями о роли сочетанной инфекции в формировании хронических вагинитов.
Анализ лабораторных обследований наглядно продемонстрировал значимую и более быструю элиминацию бактериальных комплексов в совокупности с нормализацией критериев Амселя. Положительный аминный тест отмечался у всех обследованных на старте лечения. К визиту 2 в зависимости от варианта лечения количество пациенток с положительным аминным тестом снизилось. Зафиксировано значимое снижение количества лейкоцитов в мазках, окрашенных по граму, и ключевых клеток – до 5 в поле зрения и менее, что четко коррелировало с уменьшением или отсутствием жалоб на вагинальные выделения и дискомфорт в аногенитальной зоне.
Комбинация антибактериального препарата и препарата Суперлимф интравагинально (вторая группа) оказалась в три раза эффективнее по сравнению с лечением только антисептиком (первая группа).
Эффективность лечения вульвовагинита в третьей группе, где использовали препарат Суперлимф ректально, в два раза превысила эффективность в первой группе, в которой применяли только деквалиния хлорид 10 мг.
Вероятно, монотерапия антибактериальными препаратами способна менять резистентность и патогенность бактериальных популяций, что обеспечивает кратковременный эффект антибактериального лечения, увеличение частоты рецидивов вагинитов (первая группа).
Анализ клинических симптомов, а также результаты микробиологических и лабораторных исследований в динамике подтверждают высокую эффективность лечения во второй и третьей группах, причем более длительный безрецидивный эффект прослеживался во второй группе, где пациентки в комплексе с базовой терапией применяли иммуноцитокиновый препарат Суперлимф вагинально.
Аналогичный, но менее длительный эффект с сохраняющимся, правда меньшей интенсивности, дискофортом в аногенитальной области зарегистрирован у двух пациенток третьей группы, где применялись базовая терапия деквалиния хлоридом вагинально и суппозитории Суперлимф ректально (визит 3).
При уточнении анамнеза и причин возникновения симптомов дискомфорта, озвученных при телеконсультировании, выяснилось, что две пациентки третьей группы использовали новый лубрикант-эмолент при половом контакте. После рекомендованной дерматологами отмены вагинального геля указанные симптомы купировались самостоятельно, что было зафиксировано при повторном телемедицинском консультировании (визит 5).
Учитывая результаты телемедицинского контрольного опроса в исследуемых группах, можно констатировать достаточно длительный безрецидивный эффект по окончании лечения во второй и третьей группах (рис. 6).
Пролонгированный результат в отсутствие клинических жалоб отмечался у пациенток второй группы (визиты 4 и 5). Нормализация рН вагинального отделяемого (> 4,5) выявлена при самоконтроле у 11 пациенток первой группы, двух пациенток второй группы и четырех пациенток третьей группы. Это свидетельствует о длительном положительном эффекте комплексной терапии с формированием нормобиоценоза вагинального тракта.
Таким образом, своевременно назначенная противомикробная терапия в комбинации с цитокиновым комплексом Суперлимф 25 ЕД обеспечивает стойкий безрецидивный клинико-лабораторный эффект при благоприятном профиле безопасности. Основание – результаты проведенного нами исследования.
Заключение
Суперлимф 25 ЕД, суппозитории ректальные и вагинальные, является эффективным и безопасным препаратом и может быть рекомендован в комплексной терапии неспецифических вагинитов у женщин репродуктивного возраста.
Yu.Ye. Kizhaev, PhD, L.G. Sozaeva, PhD, M.B. Obukhova, S.S. Ismailova, A.N. Kalinskaya, Ye.Ye. Mass
Russian Medical Academy of Continuous Professional Education
Moscow Multidisciplinary Scientific and Clinical Center named after S.P. Botkin
Contact person: Larisa G. Sozaeva, sozaewa@mail.ru
Relevance. The use of modern medicines to normalize the microflora of the genitourinary system in the complex treatment of vaginal infections has always been the subject of extensive research at various levels of evidence. In recent years, special attention has been paid to the use of corrective drugs with a wide spectrum of action, in particular, based on cytokines.
The aim is to evaluate the efficacy and safety of using Superlimph 25 units with dequalinium chloride antiseptic, 10 mg vaginal tablets, in the complex therapy of women of reproductive age with nonspecific vaginitis/vaginosis.
Material and methods. 60 patients aged 20–45 years with diagnosed vulvovaginitis were under observation, who contacted gynecologists at two diagnostic and treatment centers for pathological discharge from the genital tract. The diagnosis was confirmed clinically, microscopically, and by polymerase chain reaction.
Results. According to the results of clinical laboratory studies and observations, the effectiveness of therapy was high in groups in which patients received the immunocytokine drug Superlimph 25 units, suppositories, rectally or vaginally simultaneously with basic therapy. After treatment, there was a long relapse-free period. The drug was well tolerated, and no adverse reactions were reported.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.