Пансклеротическая склеродермия
- Аннотация
- Статья
- Ссылки
- English
В работе представлен случай пансклеротической склеродермии у мужчины 37 лет, дебютировавшей после тяжелой травмы с множественными переломами. Клиническая картина включала обширные индуративные очаги на коже туловища, конечностей и лица с восковидным блеском, деформацией суставов и развитием контрактур. Диагностические исследования выявили высокий титр антинуклеарного фактора и отсутствие специфических антител к системной склеродермии. В биоптате кожи обнаружены утолщение коллагеновых волокон и плотные воспалительные инфильтраты с преобладанием лимфоцитов. Системная терапия была начата поздно, когда большая часть очагов сформировалась, что не позволило достичь стабилизации патологического процесса.
Особо подчеркивается критическая необходимость раннего назначения базисной иммуносупрессивной терапии и комплексной диагностики для исключения системного процесса. Представленный случай демонстрирует сложности ведения пациентов с пансклеротической склеродермией и важность индивидуализированного подхода для оптимизации лечения и прогноза.
В работе представлен случай пансклеротической склеродермии у мужчины 37 лет, дебютировавшей после тяжелой травмы с множественными переломами. Клиническая картина включала обширные индуративные очаги на коже туловища, конечностей и лица с восковидным блеском, деформацией суставов и развитием контрактур. Диагностические исследования выявили высокий титр антинуклеарного фактора и отсутствие специфических антител к системной склеродермии. В биоптате кожи обнаружены утолщение коллагеновых волокон и плотные воспалительные инфильтраты с преобладанием лимфоцитов. Системная терапия была начата поздно, когда большая часть очагов сформировалась, что не позволило достичь стабилизации патологического процесса.
Особо подчеркивается критическая необходимость раннего назначения базисной иммуносупрессивной терапии и комплексной диагностики для исключения системного процесса. Представленный случай демонстрирует сложности ведения пациентов с пансклеротической склеродермией и важность индивидуализированного подхода для оптимизации лечения и прогноза.
Введение
Пансклеротическая склеродермия, или пансклеротическая морфеа, (PSM) является редкой и тяжелой формой локализованной склеродермии, характеризующейся генерализованным поражением кожи и подлежащих тканей и неблагоприятным долгосрочным прогнозом из-за прогрессирующего характера заболевания. Лечение таких пациентов должно быть своевременным, системным и длительным [1].
Эпидемиологические данные по этому заболеванию ограниченны из-за его редкости, однако они свидетельствуют о том, что среди всех случаев локализованной склеродермии пансклеротическая форма составляет не более 5%. Заболевание чаще встречается у детей и подростков, хотя описаны случаи и у взрослых пациентов с преобладанием лиц женского пола в соотношении примерно 2,4 : 1. Данная форма чаще описана у представителей европеоидной расы [1, 2].
Этиология пансклеротической склеродермии до сих пор остается в значительной степени неизвестной, но современные исследования предполагают сложное взаимодействие генетической предрасположенности, факторов окружающей среды и нарушения иммунной регуляции [3, 4]. Генетические факторы, вероятно, играют определенную роль, поскольку у пациентов с морфеа наблюдается более высокая частота семейного анамнеза аутоиммунных заболеваний, включая PSM. Некоторые исследования показали повышенную частоту определенных аутоантител, таких как антитела к гистонам и топоизомеразе IIa, у пациентов с морфеа. Экологические триггеры также могут способствовать развитию PSM. Отчеты о случаях связывают морфеа с различными факторами, включая инфекции, в частности Borrelia burgdorferi, травмы, хирургические операции, лучевую терапию, вакцинацию БЦЖ [3, 5, 6].
Патогенез PSM включает сложные иммунные механизмы. Недавние исследования с использованием одноклеточного и пространственного секвенирования РНК выявили выраженный ответ интерферона II типа (ИФН) в PSM, характеризующийся инфильтрацией миелоидных клеток, B-клеток и T-клеток, причем T-клетки являются основным источником ИФН-γ [7].
В этом исследовании были выявлены уникальные фибробласты CXCL9+ в PSM, которые показали повышенную экспрессию хемокинов, таких как CXCL9, CXCL10 и CCL2 [7]. Более того, взаимодействие между различными цитокинами, по-видимому, имеет решающее значение в развитии PSM. Было показано, что трансформирующий фактор роста бета и ИФН-γ синергически увеличивают экспрессию CXCL9 и CXCL10, способствуя сохранению ответов ИФН-γ. Другие профибротические цитокины, включая интерлейкины (ИЛ) 4 и 6, также играют важную роль в патогенезе. Аутоиммунная природа PSM подтверждается сосуществованием ее с другими аутоиммунными заболеваниями, такими как первичный билиарный цирроз, витилиго и в некоторых случаях системная красная волчанка [5].
Цель – описание редкой формы склеродермии – пансклеротической – на конкретном клиническом примере, анализ применявшихся к пациенту методов лечения при данной форме заболевания.
Исследование проведено по данным медицинской документации, включая инструментальное и физикальное обследования пациента.
Клинический случай
На рассмотрении случай пансклеротической склеродермии у мужчины 37 лет.
В феврале 2025 г. в Областной кожно-венерологический диспансер г. Ярославля поступил пациент С., 37 лет, с жалобами на обширные высыпания в области туловища и конечностей, чувство стягивания кожи, ограничение подвижности суставов, боль в области суставов правой нижней конечности.
Из анамнеза заболевания известно, что заболевание началось в 2012 г. после дорожно-транспортного происшествия (ДТП), в результате которого мужчина получил множественные открытые переломы правой ноги и лицевого отдела черепа, рваные раны лица, конечностей. По данному поводу было проведено хирургическое лечение методом остеосинтеза. Через месяц стал отмечать появление высыпаний в области грудной клетки, верхних и нижних конечностей, которые сопровождались чувством стягивания. С данными жалобами пациент был направлен к дерматовенерологу в поликлинику по месту жительства, где ему был выставлен впервые диагноз склеродермии. С течением времени площадь поражения увеличивалась, затрагивая новые анатомические зоны.
Пациент многократно лечился амбулаторно (назначались пентоксифиллин, введение в очаги поражения и внутримышечно раствора гиалуронидазы в комбинации с раствором новокаина 1%, топические глюкокортикостероиды (ГКС). С 2012 по 2020 г. заболевание неуклонно прогрессировало, появлялись новые очаги на коже, скованность в движениях из-за нарушения эластичности кожи, форма склеродермии из бляшечной формы трансформировалось в пансклеротическую.
Лишь в 2020 г. пациенту была впервые назначена системная терапия дексаметазоном в суточной дозе 2,5 мг (пять таблеток) до полной отмены в течение одного месяца, также внутриочаговое и внутримышечное введение раствора гиалуронидазы (64 Ед) в комбинации с раствором новокаина 1%. Курс системных стероидов в той же дозировке повторили в 2023 г. в связи с ухудшением и дальнейшим прогрессированием процесса на коже. Улучшений от проводимой терапии пациент не отмечал, прием системных ГКС сопровождался побочными эффектами в виде подъемов артериального давления и уровня глюкозы крови, увеличения массы тела. Во время последней госпитализации, в 2023 г., был произведен ряд исследований: анализ крови на антитела к антигену Scl-70 – отрицательный, анализ крови на B. burgdorferi методом ИФА (IgM, IgG) – отрицательный.
У пациента, помимо основного клинического диагноза, имелся ряд сопутствующих патологий: гипертоническая болезнь второй стадии, риск 3, достигнуты целевые показатели артериального давления; сахарный диабет 2-го типа (HbA1C целевой уровень < 7,5); ожирение третьей степени; остеоартроз, хронический синовит коленных суставов; анкилоз правого голеностопного сустава, функциональная недостаточность сустава второй степени. Для коррекции перечисленных патологических состояний пациент получал терапию: метформин по 1000 мг два раза в сутки, вилдаглиптин по 50 мг один раз в сутки, метопролол по 50 мг один раз в сутки, препарат Ко-Перинева 8 мг + 2,5 мг в сутки.
На момент поступления в стационар: состояние пациента удовлетворительное, сознание ясное. Пациент передвигается при помощи костылей. Видимые и скрытые отеки не определяются. Видимые слизистые чистые, влажные, ярко-розового цвета. Подкожно-жировая клетчатка развита избыточно. Рост – 170 см, вес – 120 кг, индекс массы тела – 41,52 (ожирение третьей степени). Лимфатические узлы не пальпируются. Изменения в костно-мышечной системе: деформация правого голеностопного сустава, контрактура правого голеностопного сустава. Атрофия мышц правой ноги, укорочение правой ноги. При аускультации легких: дыхание везикулярное, проводится во все отделы, хрипов нет. Частота дыхательных движений – 20 в минуту, SpO2 – 97%. При аускультации сердца: тоны сердца приглушены, ритмичные, патологические шумы не определяются. Частота сердечных сокращений – 80 в минуту, артериальное давление – 140/90 мм рт. ст. на обеих руках. Пальпация органов брюшной полости безболезненная, живот мягкий, печень не увеличена, край мягкий, эластичный. Селезенка не пальпируется. Симптомы раздражения брюшины отсутствуют.
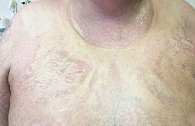
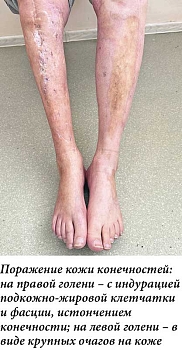
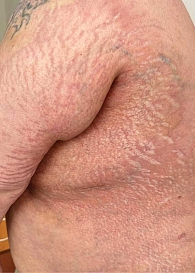
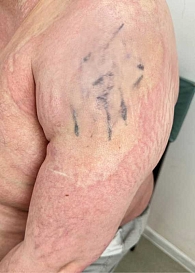
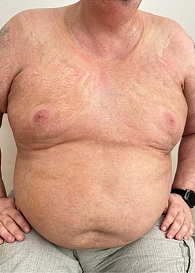
Кожный процесс носит распространенный характер (рис. 1). На коже груди, спины, поясницы кожа цвета слоновой кости, с восковидным блеском, в состоянии индурации; в области шеи напоминающая панцирь; границы поражения четкие; кожа в складку не собирается; пушковые волосы отсутствуют; в пораженных участках фолликулярный аппарат при дерматоскопии также не выявляется; прослеживаются множественные телеангиэктазии и древовидно-ветвящиеся мелкие капилляры. На коже верхних и нижних конечностей (рис. 2) присутствуют множественные крупные очаги округлой и овальной формы, в диаметре до 12 см, цвета слоновой кости, плотные, малоподвижные по отношению к подлежащим тканям. На коже верхних конечностей и живота очаги представлены синюшно-розовыми пятнами с уплотнением в центральной части, в области плеч – линейные стрии белого и фиолетового цвета длиной 3–5 мм (рис. 3, 4). На коже лица множественные рубцы неправильной формы темно-серого и белого цвета (рис. 5). На коже внешней поверхности бедер, боковых поверхностей туловища, на животе – множественные красные и белые стрии длиной 1–10 см, шириной 5–10 мм.
В период нахождения в стационаре пациенту проведены следующие диагностические исследования:
- общий анализ крови (патологических изменений показателей не выявлено);
- общий анализ мочи (патологических изменений показателей не выявлено);
- биохимический анализ крови (повышен уровень щелочной фосфотазы – 369 Ед/л, аланинаминотрансферазы – 59,5 Ед/л, аспартатаминотрансферазы – 48,3 Ед/л, билирубина общего – 42,0 мкмоль/л, мочевой кислоты – 473 мкмоль/л; выявлены нарушения в белковых фракциях крови: повышен уровень альбумина – 49,1 г/л, альфа-1-глобулина – 3,6 г/л, бета-1-глобулина – 5,5 г/л, гамма-глобулина –17,6 г/л, общего белка – 86,6 г/л, иммуноглобулина G – 1781 мг/дл; глюкоза крови: за период нахождения в стационаре максимальное значение составило 7,9 ммоль/л, минимальное – 6,12 ммоль/л);
- анализы крови на сифилис, вирус иммунодефицита человека, гепатиты В и С, паразитов (токсокара, описторх, трихинелла, аскарида, эхинококк, лямблии а/т суммарные, клонорхис) – отрицательные;
- анализ крови на гормоны: все показатели находятся в пределах референсных значений (тиреотропный гормон – 1,6890 мкМЕ/мл, пролактин – 234,92 мМЕ/л, эстрадиол – 82,0 пмоль/л, тестостерон общий – 14,356 нмоль/л;
- коагулограмма (повышен уровень антитромбина III – 132,0%, волчаночный антикоагулянт не обнаружен);
- на серологические маркеры инфекций (антитела к B. burgdorferi, IgM, IgG) – не обнаружены;
- на антинуклеарные антитела методом иммуноблота – не обнаружены;
- на фактор некроза опухоли альфа – менее 1,00 пг/мл;
- анализ крови на антинуклеарный фактор на клеточной линии HEp-2 – 1280 (ядерный гранулярный тип свечения (АС-2,4));
- ультразвуковое исследование (УЗИ) органов брюшной полости и почек: увеличение и диффузные изменения печени (УЗ-признаки жирового гепатоза); диффузные изменения поджелудочной железы; спленомегалия; утолщение подкожно-жировой клетчатки в области верхних отделов грудной клетки;
- УЗИ щитовидной железы: узлы обеих долей щитовидной железы (TIRADS-5);
- рентген таза: состояние после остеосинтеза перелома шейки правой бедренной кости; рентгенологические признаки двустороннего коксартроза первой степени; рентгенологические признаки не исключают асептический некроз головки левой бедренной кости первой/второй степени и правосторонний сакроилеит второй степени;
- ЭХО-КС: дилатация левого предсердия; фракция выброса левого желудочка по Симпсону – 55%;
- рентгеноскопия пищевода: рентгенологические признаки функциональной недостаточности кардии, гастроэзофагеальный рефлюкс, признаки хронического гастродуоденита;
- компьютерная томограмма органов грудной клетки: пневмофиброз;
- прижизненное патологоанатомическое исследование биопсийного материала кожи: в биоптате кожи определяются утолщение коллагеновых пучков внутри ретикулярной дермы, идущих параллельно поверхности кожи, наличие плотных воспалительных инфильтратов между коллагеновыми пучками, вокруг кровеносных сосудов и потовых желез; в воспалительных инфильтратах преобладают лимфоциты, плазматические клетки, гистиоциты; вышележащий эпидермис тонкий и атрофичный; отмечается атрофия эккринных желез, окружающая их жировая ткань отсутствует, потовые железы имеют более поверхностное расположение; волосяные фолликулы атрофичны, наблюдается резкая гидропическая дистрофия мышц, поднимающих волосы.
Проходил обследование и лечение в ревматологическом стационаре. Данных о системной склеродермии у пациента нет.
Диагноз основной: «генерализованная (пансклеротическая) склеродермия, стадия отека, уплотнения, атрофии».
Осложнения: «функциональная недостаточность крупных суставов нижних конечностей второй степени. Нарушение функции опоры и ходьбы».
Сопутствующие диагнозы: «сахарный диабет 2-го типа (HbA1C целевой уровень < 7,5); узловой зоб, эутиреоз; гипертоническая болезнь третьей степени, риск 4; ожирение третьей степени; анкилоз посттравматический правого голеностопного сустава; синовит коленного сустава; состояние после остеосинтеза перелома шейки правой бедренной кости (травма в результате ДТП); двусторонний коксартроз первой степени; асептический некроз головки левой бедренной кости; правосторонний сакроилеит второй степени».
При выписке из стационара пациенту даны следующие рекомендации:
- сахароснижающая терапия (метформин по 1000 мг два раза в сутки);
- гипотензивная терапия (лозартан по 25 мг два раза в сутки, бисопролол 5 мг один раз в сутки в утреннее время);
- уратснижающая терапия (аллопуринол 150 мг один раз в сутки);
- при усилении боли в суставах прием нестероидных противовоспалительных средств (Аэртал 100 мг два раза в сутки, или Целебрекс 100–200 мг два раза сутки, или ибупрофен 400 мг три раза в сутки).
С учетом наличия полиморбидного состояния пациенту было рекомендовано регулярное наблюдение дерматолога, кардиолога, хирурга-ортопеда, ревматолога, эндокринолога в поликлинике по месту жительства, а также консультация в центре остеопороза.
Представленный клинический случай пансклеротической склеродермии демонстрирует сложность диагностики и лечения данной редкой и тяжелой формы заболевания. Пансклеротическая склеродермия составляет не более 5% всех случаев локализованной склеродермии и характеризуется генерализованным поражением кожи и подлежащих тканей. В данном случае заболевание дебютировало после травмы, полученной в результате ДТП, что согласуется с литературными данными о возможной роли травмы как триггерного фактора в развитии склеродермии. Однако стоит отметить, что этиология пансклеротической склеродермии остается не до конца изученной и предполагает сложное взаимодействие генетической предрасположенности, факторов окружающей среды и нарушений иммунной регуляции.
Патогенез заболевания включает сложные иммунные механизмы. Недавние исследования выявили выраженный ответ ИФН типа II при пансклеротической склеродермии, характеризующейся инфильтрацией миелоидных клеток, B-клеток и T-клеток, причем T-клетки являются основным источником ИФН-γ. Эти данные подтверждаются результатами гистологического исследования в представленном случае, где наблюдались плотные воспалительные инфильтраты с преобладанием лимфоцитов, плазматических клеток и гистиоцитов.
Особого внимания заслуживает длительный период (около восьми лет) от начала заболевания до назначения системной терапии. Это подчеркивает необходимость раннего распознавания тяжелых форм склеродермии и своевременного начала адекватного лечения. В данном случае позднее назначение системных глюкокортикостероидов не привело к значительному улучшению состояния пациента в связи с формированием необратимых изменений кожи.
Наличие у пациента множественных сопутствующих патологий, включая сахарный диабет 2-го типа, гипертоническую болезнь и ожирение третьей степени, существенно осложняет выбор терапевтической тактики и повышает риск развития побочных эффектов при лечении. Лабораторные исследования выявили повышенный титр антинуклеарного фактора, однако стоит подчеркнуть, что даже при такой тяжелой форме ограниченной склеродермии отсутствовали специфические антитела, характерные для системной склеродермии (анти-Scl-70).
Данный клинический случай подчеркивает необходимость мультидисциплинарного подхода к ведению пациентов с пансклеротической склеродермией. С учетом прогрессирующего характера заболевания и риска развития функциональных нарушений крайне важно раннее назначение системной иммуносупрессивной терапии. В современной литературе описаны различные схемы лечения тяжелых форм склеродермии, включая микофенолата мофетил, комбинацию метотрексата с системными глюкокортикостероидами и биологические препараты. Выбор оптимальной терапевтической стратегии должен основываться на индивидуальных особенностях пациента, тяжести заболевания и наличии сопутствующих патологий.
Выводы
- Продемонстрирована необходимость раннего назначения базисной терапии тяжелых, распространенных и прогрессирующих форм склеродермии, таких как пансклеротическая.
- Необходимы полноценные клинико-лабораторное и инструментальное обследования пациентов для исключения системного течения заболевания. К сожалению, по-прежнему в большинстве случаев врачи-дерматологи недооценивают возможную прогрессию и потенциальную инвалидизацию больных, предпочитают устаревшие методы лечения (такие как пенициллинотерапия, ферментные препараты для внутримышечного введения), не назначая системную иммуносупрессивную терапию. Промедление в таком случае может пагубно сказаться на качестве жизни пациента, его дальнейшей работоспособности.
- Назначение курсов системных ГКС не всегда рационально, как у пациента в представленном клиническом случае, ввиду наличия коморбидности и высоких рисков ухудшения сопутствующих патологий.
Таким образом, в представленном клиническом случае продемонстрирована сложность ведения пациентов с пансклеротической склеродермией, что обусловливает необходимость дальнейших исследований для разработки эффективных методов лечения этой редкой и тяжелой формы заболевания.
N.V. Romanova, PhD
Yaroslavl State Medical University
Contact person: Nadezhda V. Romanova, n.v.romanova@mail.ru
Pansclerotic morphea is one of the rarest and most severe forms of localized scleroderma, characterized by generalized involvement of the skin and underlying tissues, resulting in significant functional limitations and reduced quality of life. The relevance of presenting this clinical case lies in the insufficient understanding of pathogenetic mechanisms, triggering factors of disease onset, and the lack of established therapeutic strategies in adult patients.
This report presents a case of pansclerotic morphea in a 37-year-old man, with disease onset following severe trauma with multiple fractures. The clinical picture included extensive indurated areas on the trunk, limbs, and face with typical waxy shine, joint deformities, and contracture development.
Diagnostic tests revealed a high titer of antinuclear factor and absence of specific antibodies to systemic scleroderma. Skin biopsy showed thickened collagen fibers and dense inflammatory infiltrates predominantly composed of lymphocytes. Systemic therapy was initiated late, when most lesions were already formed, and failed to achieve stabilization of the pathological process.
The conclusions emphasize the critical need for early initiation of basic immunosuppressive therapy and comprehensive diagnostics to exclude systemic involvement. This case demonstrates the complexities of managing patients with pansclerotic morphea and the importance of an individualized approach to optimize treatment and prognosis.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.


