Периферическая и автономная нейропатия: алгоритмы для практической работы
- Аннотация
- Статья
- Ссылки






Роль продуктов конечного гликирования в развитии поздних осложнений сахарного диабета
В настоящее время установлено, что огромную роль в развитии поздних осложнений сахарного диабета играют продукты конечного гликирования (КПГ). Это модифицированные белки, которые образуются в основном вследствие гипергликемии. Они так же носят название гликотоксинов – веществ, крайне насыщенных активными радикалами и представляющих собой оксиданты.
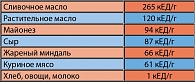
Существует два источника образования продуктов конечного гликирования. Первый путь – пищевой. Образованию КПГ способствует кулинарная обработка пищи, особенно воздействие высоких температур. А так же воздействие никотина во время курения и неблагоприятных факторов внешней среды. Содержание КПГ неодинаково в различных продуктах. Основным источником является сливочное масло, майонез, сыр, орехи. Малым содержанием КПГ отличаются овощи, хлебобулочные изделия и молоко (таблица 1).
В последние годы пищевые технологи и эндокринологи в различных лабораториях, особенно в США, активно занимаются изучением продуктов конечного гликирования. И было обнаружено, что термическая обработка пищи оказывает огромное влияние на количество этих продуктов. Чем выше температура и дольше проходит кулинарная обработка, тем выше уровень вредных веществ в готовом блюде. Также было доказано, что после употребления человеком жареной пищи, в его организме регистрируется чрезвычайно высокий уровень продуктов-оксидантов, определяются молекулы адгезии, факторы, повреждающие эндотелий, и различные цитокины. Также на фоне употребления такой пищи заметно снижается уровень лептина и адипонектина, что косвенно указывает не только на нарушение микроциркуляции, но и сигнализирует об адипоцитарной дисфункции. А это уже прямой путь к развитию инсулинорезистентности.
Что же касается второго, эндогенного пути, то в его основе лежит хроническая гипергликемия. Накопление КПГ в данной ситуации связано с тем, что при гипергликемии нарушается нормальная последовательность биохимических превращений глюкозы. Так, за счет образования супероксида в митохондриях, тормозится работа фермента глицеропептидфосфатдегидрогеназы, что приводит к накоплению промежуточных, вредных продуктов обмена глюкозы.
Научно установлено, что люди с повышенным уровнем КПГ меньше поддаются лечению и больше страдают от поздних осложнений диабета. Подтверждением этому служит такое понятие, как гипергликемическая память. В качестве доказательства приводятся исследования двух групп людей. В первой уровень КПГ был выше, чем во второй. Все пациенты получали примерно одинаковое лечение, но после обследования, проведенного через несколько лет, были получены следующие данные. У пациентов первой группы был выявлен более высокий уровень поздних осложнений сахарного диабета. Это объясняется как раз таки гипергликемической памятью. Она основывается на накоплении КПГ в клетках и образовании в них продуктов оксидативного стресса. Это приводит к труднообратимым изменениям, которые спустя несколько лет продолжают ухудшать течение болезни, способствуя появлению осложнений.
Таким образом, можно сделать вывод, что влияние продуктов конечного гликирования чрезвычайно важно. Они тесно связаны с образованием цитокинов и развитием митохондриального стресса, с мощным синтезом свободных жирных кислот и оксидации липопротеинов в эндотелии сосудистой стенки. Эндотелиальная дисфункция и нарушение дилатации мелких сосудов приводит к гибели клеток и раннему прогрессированию хронических осложнений сахарного диабета.
Выявление уровня КПГ – это эффективное и достоверное прогнозирование риска развития поздних осложнений. 18-летнее популяционное проспективное исследование показало, что уровень этих продуктов коррелирует с уровнем смертности при сахарном диабете.
Как же мы можем достигнуть контроля за образованием конечных продуктов гликирования? В первую очередь, по данным профессора Глоссара, успеху способствует соблюдение правильной диеты. То есть, если мы на 50% снизим содержание этих продуктов в пищевом рационе, то автоматически уменьшим их количество в крови.
Так же важен и второй путь – необходимо попробовать уменьшить эндогенное образование конечных продуктов гликирования. Чем раньше и строже осуществляется этот контроль, тем выше вероятность отдалить развитие микрососудистых повреждений.
В настоящее время на первое место среди ингибиторов конечных продуктов гликирования выходит активатор транскетолазы – бенфотиамин. Бенфотиамин – это предшественник тиаминпирофосфата. Обладает повышенной биодоступностью и блокирует образование неферментных продуктов гликирования. Экспериментально была доказана его эффективность в замедлении прогрессирования осложнений сахарного диабета. И в настоящее время препарат используется в лечении диабетической невропатии.
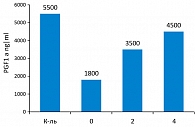
Бенфотиамин – основное действующее вещество препарата Мильгамма композитум. У этого препарата – большое будущее. Уже существуют экспериментальные подтверждения преимущества воздействия комбинации бенфотиамина с другими препаратами. В частности, опубликовано исследование о комбинированном воздействии бенфотиамина и α-липоевой кислоты. Такое мощное комбинированное воздействие восстанавливает простациклинсинтазу в эндотелии у больных сахарным диабетом 1 типа. В исследование вошло 9 пациентов, и 4 недели лечения фактически почти до нормы восстановили содержание простациклинсинтазы в эндотелии (рисунок 1).
В заключение еще раз хочется подчеркнуть, что чем раньше мы с вами будем компенсировать диабет, чем раньше будем назначать дополнительные вещества, которые блокируют образование КПГ, тем на более долгий срок мы отсрочим поздние осложнения заболевания. Комплексный подход, состоящий из правильной диеты и назначения препаратов, снижающих образование КПГ в организме, в частности препарата Мильгамма композитум, содержащего бенфотиамин, могут значительно улучшить прогноз пациентов, страдающих сахарным диабетом.
Патогенетическая терапия диабетической полиневропатии
В последние годы были проведены исследования, касающиеся влияния α-липоевой кислоты на основные показатели и основные характеристики диабетической полиневропатии. В частности, исследование Sydney, в котором приняло участие 120 человек. Длительность лечения составила 3 недели. Альфа-липоевая кислота вводилась больным в вену в дозе 600 мг, было сделано 15 инфузий. Был период, когда всем больным без исключения давали плацебо. И если за это время состояние кого-то из них улучшалось, то человека исключали из этого исследования. Действительно, плацебо работает, но есть высокодостоверная разница препаратов и плацебо. Что тут важно? Очень часто врачи ограничиваются назначением 10 инфузий своим больным, и результат не очень-то отличается в конечной точке от плацебо. Надо делать 15 инфузий или 14 по крайней мере, тогда будет различие.
Прием таблеток. Можно ли принимать только таблетки, будут ли они работать – тоже очень важный фактор, который нужно осветить. Было проведено несколько исследований. В одном из них мы принимали участие. Больным давали различные дозы α-липоевой кислоты, сравнивали с плацебо. Около 4 лет проходило это исследование. Целью было выяснить, как работают разные дозы. Выяснилось, что есть разница между 1800 мг α-липоевой кислоты в таблетках и плацебо! Было показано, что если принять 1800 мг в таблетках и ввести 600 мг кислоты в вену в виде инфузии, то будут приблизительно одинаковые концентрации. Отсюда возникла мысль о том, что 1800 мг в таблетках – это то же самое, что 600 мг кислоты, вводимые в вену.
В исследовании Sydney 2, в котором принял участие 181 больной, мы сравнили действие 1800 мг, 1200 мг и 600 мг с плацебо. Безусловно, α-липоевая кислота в таблетках работает, но 600 мг дают такой же эффект, как и у 1800 мг в таблетках. Не надо давать больших доз. В общем-то, все согласны, что этого делать не следует. Препарат хорошо работает и в меньших дозах.
Внутривенное введение с последующим приемом таблеток. Были проведены два исследования, которые показали, что по сравнению с плацебо эффективность такого применения α-липоевой кислоты существенна. Если мы даем таблетки после внутривенного введения, то они достаточно долго работают. Очень важно было посмотреть не только реакцию позитивной или негативной полиневропатической симптоматики, но и функцию нерва. При лечении, которое сочетает внутривенное введение α-липоевой кислоты, а потом прием таблеток, возникает улучшение: было показано, что длительный прием действительно замедляет прогрессирование диабетической полиневропатии.
Почему больным дается не тиамин, а жирорастворимый бенфотиамин? У него значительно более высокая биодоступность. Биодоступность водорастворимых тиаминов очень низкая, а если они принимаются в виде таблеток – ничтожная. Вы даете огромную дозу, а препарат не поступает в кровь. Всего этого лишен бенфотиамин.
Бенфотиамин защищает нерв от нарушения функции. Также в одном из исследований было показано, что происходит влияние бенфотиамина на скорость проведения возбуждения по нерву. При применении бенфотиамина состояние отчетливо улучшается.
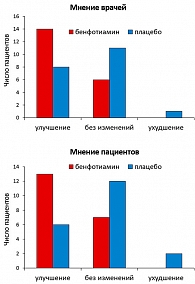
Одно из исследований BEDIP включало 40 больных (2 группы по 20 больных). Лечение проводилось 3 недели. Одним больным давали 400 мг бенфотиамина, другим – плацебо. Было значительное улучшение общего счета, наилучший эффект в отношении симптома «Боль». Большинство больных и врачей отметили улучшение после лечения бенфотиамином (рисунок 2).
В другом исследовании BENDIP, в котором приняли участие 133 человека, больным давали разные дозы бенфотиамина (300 мг и 600 мг) в течение 6 недель. Бенфотиамин в дозе 600 мг оказывал лучшее влияние.
Что касается действия на другие осложнения диабета, то есть результаты экспериментальных исследований.
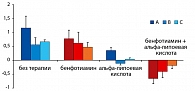
В исследовании с участием 144 больных одной группе давали только бенфотиамин; другой – только α-липоевую кислоту; третьей – комбинацию препаратов; четвертая группа наблюдалась без лечения. В течение 6 месяцев наблюдали и оценивали порог чувствительности различных тонких и толстых волокон. Лучший эффект в виде снижения порога был получен именно при комбинации препаратов (рисунок 3).
В другом исследовании тоже было показано, что наилучший эффект в отношении функции нерва наблюдается именно при комбинации α-липоевой кислоты и бенфотиамина.
Рекомендации по лечению. Начинать надо с внутривенного введения α-липоевой кислоты (Тиогамма) в течение 3 недель. Дальше – проводится поддерживающая терапия по 600 мг ежедневно – одна таблетка Тиогаммы в течение 2-3 месяцев.
Если не получили эффекта, а это оценивают через 3 месяца, то добавляются высокие дозы либо только бенфотиамина (препарат Бенфогамма – 150 мг в одной таблетке назначается в дозе 3-4 таблетки в день), либо инъекции комбинации витаминов группы В, т.е. 1 ампула Мильгаммы в день в течение 10 дней. Или же назначается препарат Мильгамма композитум, который кроме бенфотиамина дополнительно содержит пиридоксин, что очень важно для обеспечения энергетики нерва. Итак, Мильгамма композитум по 1 драже 4 раза в день в течение недели.
Затем поддерживающая терапия. Это постоянный прием Бенфогаммы по 1 таблетке ежедневно или Мильгаммы композитум по 1 драже 3 раза в день.
В тяжелых случаях применяют комбинацию бенфотиамина и α-липоевой кислоты, то есть препаратов Мильгамма композитум и Тиогамма. И одновременно нужно давать 1-2 ампулы α-липоевой кислоты (600 мг) в течение 3-4 недель.
Затем поддерживающая терапия: постоянный прием Бенфогаммы и Мильгаммы композитум в стандартных дозах и дополнительно прием 1-3 таблеток α-липоевой кислоты. Подчеркну, что эти препараты действуют на совершенно разные звенья патогенеза, поэтому их не только можно, но и нужно совмещать.
Тоннельные невропатии рук у больных сахарным диабетом
Билатеральные сенсорные нарушения и болевой синдром у больных сахарным диабетом чаще всего обусловлен тоннельной невропатией. Тоннельная невропатия среди больных сахарным диабетом встречается в 2,3 раза чаще, чем в общей популяции населения. Когда мы проводили исследование Sydney, в котором участвовало около 500 больных, оказалось, что больше, чем у 40% больных, имеются неприятные ощущения не только в ногах, но и в руках. Нас это заинтересовало. И мы провели исследование по выяснению причин появления болей в руках, по диагностике различных состояний, которые вызывают такие феномены, по лечению. Наиболее часто боли в руках при сахарном диабете связаны с так называемыми тоннельными невропатиями. Периферический нерв проходит через участки, где он очень тесно окружен костными, мышечными, структурными сухожилиями, сосудами и так далее, и в этих типичных местах он легко подвергается компремации, давлению. Такие невропатии называются тоннельными.
Допустим, пришел на прием пожилой человек, бабушка с диабетом. Она жалуется, что у нее немеют руки. Она встает, должна потрясти руками, растереть их, и тогда неприятные ощущения уменьшаются. Какой диагноз чаще всего ставят? Остеохондроз позвоночника. Однако остеохондроз позвоночника не может вызывать таких ощущений, он просто не способен. Корешковая патология дает совершенно другие ощущения и совершенно иначе себя проявляет. Поэтому эта тема с практической точки зрения действительно очень важна. В нашем исследовании мы решили исключить физиологические особенности у больных с диабетом, потому что очень часто имеет место ошибочная диагностика.
Итак, целью нашего исследования было изучение клинических и нейрофизиологических особенностей тоннельных невропатий верхних конечностей у пациентов с сахарным диабетом 1 и 2 типов и оценка эффективности консервативных методов их терапии. Мы взяли достаточно большую группу – 250 пациентов. 106 из них имели жалобы на боли в руках. Тоннельные невропатии были у 88 пациентов. Еще 60 пациентов имели сочетание тоннельных невропатий и диабетическую невропатию. У нас была группа сравнения (100 человек), мы взяли этих людей в обычных терапевтических стационарах. Они не имели диабета, а вот типичные жалобы на боли в руках у них были. И контрольная группа состояла из 15 здоровых испытуемых. Группы достоверно не различались друг от друга по полу, возрасту, типу и длительности сахарного диабета, уровню HbA1c.
Методы исследования
- Клиническое обследование: характеристика субъективных ощущений; шкала степени выраженности тоннельных невропатий; опросник диагностики невропатической боли ДН4; четырехбальная шкала оценки эффективности лечения; диагностические (провокационные) тесты.
- Неврологическое обследование: сухожильные рефлексы; мышечная сила; поверхностная чувствительность (тактильная, болевая, температурная); глубокая чувствительность (вибрационная, суставно-мышечное чувство).
- Стимуляционная ЭМГ.
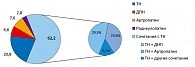
Всем больным проводилось микробиологическое лечение, контролировали у них уровень гликемии и гемоглобин для того, чтобы оценить роль нарушений углеводного обмена. И оказалось, что диабетическая полиневропатия в чистом виде, без наличия дополнительных факторов, была всего у 8% больных. Вот только в 8% случаев диабетическая полиневропатия может вызвать какие-либо сенсорные феномены в руках. Только тоннельные невропатии были в 20% случаев, в очень небольшом проценте случаев (6,6%) – артропатии. Всего в 3% случаев, то есть у нескольких больных, имели место радикулопатии (рисунок 4). При радикулопатиях возникает «длинная» боль, они не дают боль в кистях. Обычно это боли, идущие от плеча, которые могут доходить до пальцев. При тоннельных невропатиях помогает опускание рук вниз, растирание рук, покой руки.
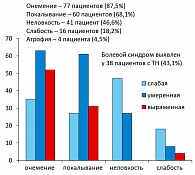
И было достаточно много случаев, когда тоннельные невропатии сочетались с другой патологией, которая тоже могла вызывать различные феномены. Чаще всего у больных встречались онемение, покалывание, неловкость, двигательные эффекты, слабость (рисунок 5). Например, у достаточно высокого процента больных было нарушение застегивания пуговиц. Оказалось, что атрофии при диабете встречаются очень редко.
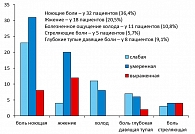
Болевой синдром был выражен у 40% больных. Часто встречались ноющие боли, жжение, болезненное ощущение холода. Стреляющие и глубокие тупые давящие боли встречались реже (рисунок 6).
Невропатическую боль выявили только у 9 пациентов, ноцицептивную боль – у 6, а сочетанную боль – у 23 пациентов.
Распространенность тоннельных невропатий среди больных диабетом составляла 35%, это высокий показатель; карпальной тоннельной невропатии – 22,8%; кубитальной – 19,2%. Мы сравнили больных с диабетом, которые имели жалобы на боли в руках и другие сенсорные феномены в руках, с теми, кто не имел диабета. Тоннельные невропатии среди больных сахарным диабетом встречаются достоверно чаще. Чаще всего эта патология возникает в возрасте от 40 до 60 лет, в молодом возрасте это большая редкость. Мы разработали шкалу степени выраженности тоннельной невропатии от легкой и до самой тяжелой.
При диабете чаще встречаются легкие формы, тяжелые формы – реже, промежуточные стадии одинаково встречаются при диабете и без диабета. Была рассчитана зависимость между длительностью неприятных ощущений в руках и скоростью проведения возбуждения по нерву на ладони.
Длительность диабета, естественно, влияла на распространенность невропатии. Чем больше длительность диабета, тем больше вероятность формирования тоннельных невропатий. И тяжесть невропатии тоже напрямую от этого зависит: была прямая зависимость между длительностью диабета и тяжестью невропатии. Вместе с тем болевой синдром не зависел от характеристики углеводного обмена. Это понятно, потому что он определяется в первую очередь характером поражения нерва, а не нарушением метаболизма. Очень сложно бывает различить тоннельные невропатии и полиневропатии.
Анализ соотношения скорости проведения по срединному и локтевому нервам показал, что в том случае, если на фоне диабетической полиневропатии есть, скажем, кубитальный синдром, то имеется более высокое соотношение. Мы построили кривую и показали, что если это соотношение выше, чем 1,6, то в 8 раз более вероятно, что мы имеем в этом случае на фоне диабетической полиневропатии компрессию, компрессионную мононевропатию в частности, или кубитальный синдром. Это очень важно.
Мы решили проверить эффективность лечения. Было создано 3 группы. Мы делали аппликации димексида и новокаина на область давления. Это снимает отек и воспаление, улучшает кровоток. Проводили классическое консервативное лечение, вводили кортикостероиды в зону тоннеля.
Если нет диабета, то положено вводить пролонгированные препараты. Но это были больные с диабетом, поэтому мы им вводили короткодействующие препараты. Мы не получили серьезных нарушений углеводного обмена, чуть поднималась гликемия. Делали 4 инъекции через 3-4 дня. И вводили препарат α-липоевой кислоты – Тиогамма.
Мы считали, что столь высокая частота образования тоннельных невропатий при диабете связана не столько с изменением стенок тоннеля, сколько с изменением состояния периферического нерва. Оказалось, что наилучший эффект был получен не при введении кортикостероидных препаратов, а при инфузии α-липоевой кислоты.
Подчеркиваю, исходное состояние нерва играет большую роль в развитии компрессии. При диабете не делают хирургической декомпрессии нерва. Было показано, что это неэффективно, так как велика частота рецидивов, и от этого отказались. Поэтому применение α-липоевой кислоты (Тиогамма) помогает больным, и это очень важно.
Все это позволило сделать нам следующие выводы.
- Боли, парестезии и онемение в кистях при сахарном диабете формируются в подавляющем большинстве случаев из-за наличия тоннельных невропатий.
- Развитие тоннельных невропатий при сахарном диабете связано с исходным неблагополучием периферических нервов.
- Наилучший эффект при лечении тоннельных невропатий рук у больных сахарным диабетом получен при использовании препарата Тиогамма.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.