Персистирующее постуральное перцептивное головокружение и коморбидные нарушения: современные подходы к диагностике и лечению
- Аннотация
- Статья
- Ссылки
- English
Материал и методы. Обследовано 60 пациентов в возрасте 42,5 ± 13,8 года с ПППГ согласно диагностическим критериям Общества Барани и коморбидными нарушениями. Пациенты с ПППГ были разделены на три группы с учетом коморбидной патологии. 30 (50%) пациентов с сопутствующими тревожными расстройствами составили первую группу, 8 (13,3%) пациентов с периферическими вестибулярными расстройствами – вторую, 22 (36,7%) пациента с мигренью – третью. В ходе исследования использовались госпитальная шкала тревоги и депрессии, шкала депрессии Бека, шкала тревоги Спилбергера, клиническое отоневрологическое обследование, отоневрологический опросник и шкала оценки головокружения, видеонистагмография. После постановки диагноза пациентам назначали комплексное лечение, включавшее ингибиторы обратного захвата серотонина, противотревожные средства, вестибулярную гимнастику, для купирования острого приступа головокружения – комбинированный препарат циннаризина 20 мг + дименгидрината 40 мг Арлеверт, который показал высокую эффективность и хорошую переносимость. Осмотр в динамике проводился через месяц.
Результаты. Диагнозы ПППГ, вестибулярной мигрени, вестибулярного нейронита, доброкачественного пароксизмального позиционного головокружения (ДППГ) не были ранее установлены ни одному из обследованных нами пациентов. В 75% случаев пациенты с ПППГ лечились с диагнозом цереброваскулярного заболевания: хронической ишемии мозга, вертебробазилярной недостаточности. В 11,7% головокружение расценивалось как проявление нестабильности шейного отдела позвоночника, в 13,3% – как проявление синдрома вегетативной дистонии. Уровень ситуационной и личностной тревоги по шкале Спилбергера был достоверно выше в группе пациентов с ПППГ и периферическими вестибулярными расстройствами (p < 0,001). Средний суммарный балл по отоневрологическому опроснику и шкале оценки головокружения при первичном осмотре соответствовал умеренной выраженности головокружения во всех трех группах (в группе с ПППГ и тревожными расстройствами – 44,5 ± 15,6 балла, в группе с ПППГ и периферическими вестибулярными расстройствами – 61,3 ± 8,3 балла, в группе с ПППГ и мигренью – 43,6 ± 14,1 балла).
При повторном осмотре через месяц на фоне проводимой терапии средний суммарный балл по отоневрологическому опроснику и шкале оценки головокружения составил в группе с ПППГ и тревожными расстройствами 29,6 ± 12,8 балла, в группе с ПППГ и периферическими вестибулярными расстройствами – 46,3 ± 8,9 балла, в группе с ПППГ и мигренью – 28,5 ± 7,2 балла. Выявлено достоверное уменьшение выраженности головокружения во всех группах (p < 0,001).
Выводы. Исследование показало низкий уровень диагностики ПППГ, вестибулярной мигрени, вестибулярного нейронита, ДППГ врачами. Эти заболевания не были диагностированы ни у одного из обследованных пациентов. К наиболее частым коморбидным расстройствам при ПППГ относятся тревожные расстройства и мигрень. Уровень тревоги был повышен у всех пациентов с ПППГ, но выраженность тревоги была достоверно выше у пациентов с ПППГ и периферическими вестибулярными расстройствами. На фоне комплексной терапии выраженность головокружения у всех пациентов с ПППГ достоверно уменьшилась.
Материал и методы. Обследовано 60 пациентов в возрасте 42,5 ± 13,8 года с ПППГ согласно диагностическим критериям Общества Барани и коморбидными нарушениями. Пациенты с ПППГ были разделены на три группы с учетом коморбидной патологии. 30 (50%) пациентов с сопутствующими тревожными расстройствами составили первую группу, 8 (13,3%) пациентов с периферическими вестибулярными расстройствами – вторую, 22 (36,7%) пациента с мигренью – третью. В ходе исследования использовались госпитальная шкала тревоги и депрессии, шкала депрессии Бека, шкала тревоги Спилбергера, клиническое отоневрологическое обследование, отоневрологический опросник и шкала оценки головокружения, видеонистагмография. После постановки диагноза пациентам назначали комплексное лечение, включавшее ингибиторы обратного захвата серотонина, противотревожные средства, вестибулярную гимнастику, для купирования острого приступа головокружения – комбинированный препарат циннаризина 20 мг + дименгидрината 40 мг Арлеверт, который показал высокую эффективность и хорошую переносимость. Осмотр в динамике проводился через месяц.
Результаты. Диагнозы ПППГ, вестибулярной мигрени, вестибулярного нейронита, доброкачественного пароксизмального позиционного головокружения (ДППГ) не были ранее установлены ни одному из обследованных нами пациентов. В 75% случаев пациенты с ПППГ лечились с диагнозом цереброваскулярного заболевания: хронической ишемии мозга, вертебробазилярной недостаточности. В 11,7% головокружение расценивалось как проявление нестабильности шейного отдела позвоночника, в 13,3% – как проявление синдрома вегетативной дистонии. Уровень ситуационной и личностной тревоги по шкале Спилбергера был достоверно выше в группе пациентов с ПППГ и периферическими вестибулярными расстройствами (p < 0,001). Средний суммарный балл по отоневрологическому опроснику и шкале оценки головокружения при первичном осмотре соответствовал умеренной выраженности головокружения во всех трех группах (в группе с ПППГ и тревожными расстройствами – 44,5 ± 15,6 балла, в группе с ПППГ и периферическими вестибулярными расстройствами – 61,3 ± 8,3 балла, в группе с ПППГ и мигренью – 43,6 ± 14,1 балла).
При повторном осмотре через месяц на фоне проводимой терапии средний суммарный балл по отоневрологическому опроснику и шкале оценки головокружения составил в группе с ПППГ и тревожными расстройствами 29,6 ± 12,8 балла, в группе с ПППГ и периферическими вестибулярными расстройствами – 46,3 ± 8,9 балла, в группе с ПППГ и мигренью – 28,5 ± 7,2 балла. Выявлено достоверное уменьшение выраженности головокружения во всех группах (p < 0,001).
Выводы. Исследование показало низкий уровень диагностики ПППГ, вестибулярной мигрени, вестибулярного нейронита, ДППГ врачами. Эти заболевания не были диагностированы ни у одного из обследованных пациентов. К наиболее частым коморбидным расстройствам при ПППГ относятся тревожные расстройства и мигрень. Уровень тревоги был повышен у всех пациентов с ПППГ, но выраженность тревоги была достоверно выше у пациентов с ПППГ и периферическими вестибулярными расстройствами. На фоне комплексной терапии выраженность головокружения у всех пациентов с ПППГ достоверно уменьшилась.


Введение
Персистирующее постуральное перцептивное головокружение (ПППГ) представляет собой функциональное вестибулярное расстройство, которое вызывает хроническое головокружение, мешающее повседневной деятельности [1–3]. Один или несколько симптомов головокружения либо неустойчивости присутствуют как минимум 15 дней в месяц в течение трех месяцев или более. Вертикальное положение, активные или пассивные движения и воздействие движущихся визуальных стимулов или сложных визуальных образов усугубляют симптомы заболевания [4]. Клинически ПППГ проявляется в виде невращательного головокружения, которое может возникать приступообразно с кратковременными эпизодами неустойчивости с ощущением оцепенения, замирания, легкости в голове (дурноты) при стоянии или ходьбе или в виде постоянного различной степени выраженности ощущения головокружения внутри головы, уменьшающегося или продолжающегося в положении лежа [1–4].
Расстройство провоцируется состояниями, которые вызывают головокружение, неустойчивость или проблемы с равновесием, включая острые, эпизодические или хронические вестибулярные синдромы, другие неврологические, соматические или психологические расстройства. При этом симптомы вызывают значительные функциональные нарушения [2, 4–6]. У пациентов с ПППГ усиливается постуральный контроль в ответ на вызывающие головокружение триггерные события, затем эта патологическая адаптивная стратегия постоянно поддерживается, даже если триггерные факторы исчезают [7, 8]. Важно, что ПППГ не является диагнозом исключения [1–4].
В патогенезе заболевания ведущую роль играет нарушение адаптации мозга к вестибулярному дефициту с увеличением зависимости от визуальной информации о самодвижении [5–10]. Причиной рассогласования, лежащего в основе ПППГ, может быть постоянный тревожный контроль за собственной постуральной устойчивостью из-за страха перед возможным падением. Страх может сформироваться, например, вследствие перенесенного приступа вестибулярного головокружения, обморока, панической атаки. Любые ситуации, приводящие к напряжению постуральных механизмов, усиливают ощущение неустойчивости, нестабильности, воспринимаемой как головокружение. В результате обычная ходьба, пересечение открытых пространств или посещение многолюдных мест сопровождаются усилением ощущения головокружения. При этом нарушение адаптации приводит к хронизации симптомов, хотя пусковое событие может уже исчезнуть [7, 11]. Проведенные исследования выявили изменение функциональных связей в головном мозге [10, 12]: снижение взаимосвязи между (пре)клиновидной и премоторной корой [12] и увеличение активации зрительной коры при вестибулярных нагрузках [13]. Первое нарушает регуляцию позы и движения тела, второе приводит к усилению зрительной зависимости [10, 12–14]. Чрезмерная зависимость от визуальной информации часто вызывает головокружение и/или постуральную неустойчивость в ситуациях с нестабильными визуальными стимулами (движущийся поток машин, мелькание витрин и т.д.) [10, 11]. Остается открытым вопрос, что именно приводит к развитию симптомов ПППГ у части пациентов, поскольку после одних и тех же вестибулярных нарушений у других больных эта дисфункция не развивается [5, 15–17].
Понятие коморбидности включает в себя сочетание у одного больного двух или более хронических заболеваний, патогенетически взаимосвязанных между собой или совпадающих по времени независимо от активности каждого из них. Отсутствие единого комплексного научного подхода к оценке коморбидности влечет за собой пробелы в клинической практике. Коморбидность значительно затрудняет диагностику заболеваний. Однако остается крайне важным выявление коморбидных нарушений для разработки оптимальной стратегии ведения пациентов [18].
В качестве коморбидных расстройств при ПППГ рассматриваются структурные, метаболические и психические заболевания. Обычно ПППГ наблюдается при доброкачественном позиционном пароксизмальном головокружении (ДППГ), вестибулярном нейроните, вестибулярной мигрени, паническом расстройстве и других тревожных расстройствах. При этом коморбидные заболевания могут как предшествовать началу ПППГ, так и ухудшать состояние, когда ПППГ вызвано иной причиной. Своевременная диагностика ПППГ и как самостоятельного заболевания, и как вторичного расстройства после структурного вестибулярного синдрома очень важна для предотвращения дальнейшей хронизации процесса и обеспечения адекватного лечения [16–19].
Подбор адекватной стратегии лечения пациентов с ПППГ сопряжен с трудностями, обусловленными патогенетическими особенностями ПППГ и частым сочетанием с коморбидными нарушениями. Проведенное сравнительное исследование эффективности только лекарственной терапии и лекарственной терапии совместно с психотерапией и вестибулярной реабилитацией показало преимущество комплексного подхода к лечению этого заболевания [20, 21]. В ранее проведенных исследованиях показана целесообразность использования селективных ингибиторов обратного захвата серотонина (СИОЗС) [21–24]. К важным аспектам лечения пациентов с ПППГ относятся своевременная диагностика и эффективное лечение коморбидных нарушений: ДППГ, периферической вестибулопатии, вестибулярной мигрени, тревожных расстройств [25].
Цель – анализ типичной практики ведения пациентов с ПППГ и коморбидными нарушениями и ее оптимизация.
Материал и методы
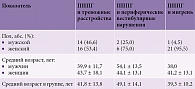
Обследовано 60 пациентов с коморбидными нарушениями при ПППГ, которые были разделены на три группы. 30 (50%) пациентов с тревожными расстройствами вошли в первую группу, 8 (13,3%) пациентов с периферическими вестибулярными расстройствами (вестибулярный нейронит, ДППГ) – во вторую, 22 (36,7%) пациента с мигренью – в третью. Половозрастные характеристики обследованных пациентов представлены в табл. 1.
Критериями включения в исследование были возраст старше 18 лет и наличие жалоб на головокружение и неустойчивость.
В исследование не включались пациенты:
- с выраженными когнитивными нарушениями (деменцией);
- выраженной депрессией;
- ортостатической гипотензией;
- синкопальными пароксизмами;
- эпилептическими припадками;
- демиелинизирующими, дегенеративными заболеваниями центральной нервной системы;
- онкологическими заболеваниями;
- тяжелой аритмией, нестабильной стенокардией, инфарктом миокарда;
- анемией (гемоглобин ≤ 10,5 г/дл для женщин и ≤ 11,5 г/дл для мужчин);
- беременные;
- страдающие алкоголизмом, токсикоманией и наркоманией.
Для постановки диагноза и исключения других причин головокружения проведено стандартное соматическое, неврологическое и нейровестибулярное обследование: проба Хальмаги, проба с встряхиванием головы, проба Унтербергера, проба Вальсальвы и гипервентиляционная проба. Всем пациентам выполнена видеонистагмография с исследованием спонтанного, установочного и позиционного нистагма. Для оценки выраженности тревоги и депрессии использовались госпитальная шкала тревоги и депрессии (Hospital Anxiety and Depression Scale, HADS), шкала депрессии Бека (Beck Depression Inventory, BDI), шкала тревоги Спилбергера (State-Trait Anxiety Inventory, STAI), для оценки выраженности головокружения – отоневрологический опросник и шкала оценки головокружения (Dizziness Handicap Inventory, DHI).
Проанализирована информация о течении заболевания до обращения в клинику: давность и характер головокружения, провоцирующие факторы, устанавливаемые ранее диагнозы, назначенное лечение и его эффективность. После обследования и постановки диагноза пациентам назначали комплексное лечение, включавшее СИОЗС, противотревожные средства, вестибулярную гимнастику. Профилактическое лечение мигрени назначалось индивидуально и могло дополнительно к антидепрессантам включать бета-блокаторы, Вазобрал. Для купирования острого приступа головокружения при ДППГ проводились лечебные маневры. Лечение периферической вестибулярной дисфункции включало назначение комбинированного препарата циннаризина 20 мг + дименгидрината 40 мг Арлеверт, который также использовался при острых приступах вестибулярной мигрени наряду с нестероидными противовоспалительными средствами, триптанами, препаратами эрготамина для купирования головной боли.
Все пациенты подписали информированное согласие. Повторное обследование проводилось после курса лечения (в среднем через месяц).
Статистическая обработка полученных данных осуществлялась с помощью компьютерной программы Statistica (StatsoftInc), версия 10.0. Для количественных показателей с нормальным распределением описательная статистика представлена как среднее арифметическое и стандартное отклонение (М ± σ). Для сравнения количественных показателей между двумя группами применялся непараметрический критерий Манна – Уитни.
Результаты
Длительность заболевания в первой группе (ПППГ и тревожные расстройства) составила от трех месяцев до 11 лет, во второй (ПППГ и периферические вестибулярные нарушения) – от трех месяцев до полутора лет, в третьей (ПППГ и мигрень) – от трех месяцев до шести лет.
Несмотря на характерные клинические проявления ПППГ, вестибулярной мигрени, вестибулярного нейронита, ДППГ, эти диагнозы не были установлены ни одному из обследованных пациентов. Головокружение расценивалось как следствие других заболеваний.
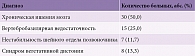
Направительные диагнозы участников исследования приведены в табл. 2.
В 75% случаев пациенты с ПППГ и мигренью лечились амбулаторно с диагнозом цереброваскулярного заболевания: хронической ишемией мозга, вертебробазилярной недостаточностью. В 11,7% случаев головокружение расценивалось как проявление нестабильности шейного отдела позвоночника, в 13,3% – как проявление синдрома вегетативной дистонии.
Пусковым механизмом ПППГ у 15 (25%) пациентов послужило вестибулярное расстройство: у 3 (5%) – вестибулярный нейронит, у 5 (8,3%) – ДППГ, у 7 (11,7%) – вестибулярная мигрень. У остальных 45 (75%) пациентов ПППГ развивалось на фоне хронического стресса и сочеталось только с тревожным расстройством у 30 (50%) пациентов, с простой мигренью и мигренью с аурой – у 15 (25%) пациентов.
У 57 (95%) пациентов не обнаружено значимых нарушений при клиническом отоневрологическом обследовании и в ходе видеонистагмографии. У этих пациентов при исследовании походки не выявлены нарушения устойчивости и ходьбы. У 3 (5%) больных отмечалась слабоположительная проба Хальмаги и Унтербергера, у 2 (3,3%) – положительная проба с встряхиванием головы, что указывало на легкие остаточные явления перенесенного вестибулярного нейронита. У таких пациентов зафиксированы минимальные трудности при выполнении усложненных тестов на устойчивость.
Выраженность тревоги и депрессии в группах пациентов с ПППГ и коморбидными нарушениями до и после лечения представлена в табл. 3. Как видно из таблицы, ситуационная и личностная тревога по шкале Спилбергера была достоверно выше в группе пациентов с ПППГ и периферическими вестибулярными нарушениями. После лечения отмечалось достоверное уменьшение выраженности тревоги во всех группах пациентов.
Выраженность головокружения в группах пациентов с ПППГ и коморбидными расстройствами до и после лечения представлена в табл. 4.
Таким образом, на фоне комплексного лечения отмечалось достоверное уменьшение выраженности головокружения во всех группах пациентов с ПППГ и коморбидными нарушениями.
Обсуждение
Зафиксирован низкий уровень диагностики ПППГ, вестибулярной мигрени, вестибулярного нейронита, ДППГ врачами общей практики и неврологами. Правильные диагнозы не установлены ни одному из обследованных нами пациентов. При этом периферическая и центральная вестибулярная дисфункция ошибочно расценивалась врачами как проявление сосудистой патологии головного мозга, дегенеративных заболеваний позвоночника, вегетативной дисфункции. Как следствие – неверный выбор терапевтической тактики, что не уменьшало выраженности головокружения, а усиливало тревогу и ухудшало течение ПППГ. Во многих исследованиях был показан низкий уровень диагностики вестибулярных нарушений: ПППГ, вестибулярной мигрени, вестибулярного нейронита, ДППГ [26]. Следует отметить, что поздняя диагностика вестибулярного расстройства служит важным аспектом хронизации головокружения и развития вторичных функциональных нарушений [1–3,15–17, 25, 26].
В ходе исследования тревожные расстройства разной степени выраженности выявлены во всех группах пациентов, которые в свою очередь являются коморбидными как для ПППГ, так и для мигрени. Следует отметить, что повышенный уровень тревоги часто наблюдается при ДППГ, вестибулярном нейроните, болезни Меньера. Это обусловлено тесной связью вестибулярной системы с вегетативными центрами головного мозга, что может способствовать возникновению тревожного расстройства при любой вестибулярной дисфункции [3, 15–17, 25, 26]. Психиатрические факторы (тревожность, паническое расстройство) могут играть важную роль в возникновении и поддержании ПППГ, тогда как ПППГ поддерживает и усиливает уровень тревоги [27–29]. Высокий уровень тревоги ассоциируется с худшим прогнозом у пациентов с ПППГ. Это необходимо учитывать при выборе методов лечения. Важно одновременно воздействовать на вестибулярную дисфункцию и эмоциональные расстройства [30].
Проведенные ранее исследования эффективности терапии ПППГ показали более значимую эффективность комбинированной терапии, состоящей из рациональной и когнитивно-поведенческой терапии, вестибулярной реабилитации и назначения СИОЗС [1, 31–34]. В нашем исследовании пациенты получали комплексное лечение ПППГ, включавшее рациональную психотерапию, СИОЗС, противотревожные средства, вестибулярную гимнастику. При коморбидных расстройствах использовались современные эффективные методы. Высокую эффективность и хорошую переносимость показал низкодозовый комбинированный препарат циннаризина 20 мг + дименгидрината 40 мг (Арлеверт). Он использовался для купирования острых приступов вестибулярной мигрени, назначался после лечебных маневров при ДППГ. Входящий в состав препарата циннаризин блокирует кальциевые каналы преимущественно на уровне рецепторного отдела вестибулярной системы, что уменьшает чувствительность волосковых клеток к вестибулярным раздражителям [35–37]. Дименгидринат обладает антигистаминными и холинолитическими свойствами и действует преимущественно на уровне центральных отделов вестибулярной системы [35–37]. Эффективность Арлеверта обусловлена синергичным действием входящих в его состав компонентов, усиливающих действие друг друга. Во многих исследованиях препарат показал высокую эффективность и хорошую переносимость у пациентов с вестибулярным головокружением центрального и/или периферического генеза [35–37]. Зарегистрировано достоверно более значимое снижение выраженности головокружения на фоне применения препарата по сравнению с плацебо или лечением циннаризином и дименгидринатом, которые назначались отдельно, даже в более высоких дозах. Арлеверт показал высокую эффективность у пациентов с вестибулярным нейронитом. Достоверное улучшение отмечалось через одну и четыре недели приема. При этом серьезных нежелательных явлений не зафиксировано ни у одного пациента [36, 37]. Профилактическое лечение мигрени было индивидуальным и могло дополнительно к антидепрессантам включать бета-блокаторы, Вазобрал.
Назначение комплексного лечения пациентам с ПППГ и коморбидными расстройствами привело к достоверному уменьшению выраженности головокружения во всех группах уже через месяц лечения.
Заключение
Исследование показало низкий уровень диагностики ПППГ, центральных и периферических вестибулярных расстройств. Как следствие – неадекватная тактика ведения пациентов, усиление тревоги и головокружения. К самым частым коморбидным заболеваниям у пациентов с ПППГ относятся мигрень и тревожное расстройство, которые необходимо своевременно диагностировать и лечить. Большое значение имеет подбор адекватной терапии острых приступов периферического и центрального головокружения, которые могут служить как пусковыми, так и поддерживающими факторами ПППГ. Высокую эффективность у пациентов с головокружением различного генеза показал низкодозовый комбинированный препарат циннаризина 20 мг + дименгидрината 40 мг (Арлеверт).
Ye.N. Zastenskaya, L.M. Antonenko, PhD, Prof.
I.M. Sechenov First Moscow State Medical University
Contact person: Yekaterina N. Zastenskaya, zastik26@mail.ru
The aim is to analyze and optimize the typical practice of managing patients with persistent postural perceptual vertigo (PPPV) and comorbid disorders.
Material and methods. 60 patients aged 42.5 ± 13.8 years with PPPV were examined according to the diagnostic criteria of the Barani Society and comorbid disorders. Patients with PPPV were divided into three groups, taking into account comorbid pathology. 30 (50%) patients with concomitant anxiety disorders made up the first group, 8 (13.3%) patients with peripheral vestibular disorders – the second, 22 (36.7%) patients with migraine – the third. The study used the hospital anxiety and depression scale, Beck depression scale, Spielberger anxiety scale, clinical otoneurological examination, otoneurological questionnaire and vertigo assessment scale, videonystagmography. After the diagnosis, patients were prescribed complex treatment, which included serotonin reuptake inhibitors, anti-anxiety agents, vestibular gymnastics, for the relief of an acute attack of dizziness – a combined preparation of cinnarizine 20 mg + dimenhydrinate 40 mg Arlevert, which showed high efficacy and good tolerability. The dynamic inspection was carried out a month later.
Results. The diagnoses of PPPV, vestibular migraine, vestibular neuritis, benign paroxysmal positional vertigo (BPPV) were not previously established in any of the examined patients. In 75% of cases, patients with PPH were treated with a diagnosis of cerebrovascular disease: chronic cerebral ischemia, vertebral-basilar insufficiency. In 11.7%, dizziness was regarded as a manifestation of instability of the cervical spine, in 13.3% – as a manifestation of vegetative dystonia syndrome. The level of situational and personal anxiety on the Spielberger scale was significantly higher in the group of patients with PPPV and peripheral vestibular disorders (p < 0.001). The average total score according to the otoneurological questionnaire and the dizziness assessment scale at the initial examination corresponded to moderate severity of dizziness in all three groups (in the group with PPPV and anxiety disorders – 44.5 ± 15.6 points, in the group with PPPV and peripheral vestibular disorders – 61.3 ± 8.3 points, in the group with PPPV and migraine – 43.6 ± 14.1 points).
When re-examined a month later against the background of therapy, the average total score according to the otoneurological questionnaire and the dizziness assessment scale was 29.6 ± 12.8 points in the group with PPPV and anxiety disorders, 46.3 ± 8.9 points in the group with PPPV and peripheral vestibular disorders, 28.5 ± 7.2 points in the group with PPPV and migraine. There was a significant decrease in the severity of dizziness in all groups (p < 0.001).
Conclusions. The study showed a low level of diagnosis of PPPV, vestibular migraine, vestibular neuritis, BPPV by doctors. These diseases were not diagnosed in any of the examined patients. The most common comorbid disorders in PPPV include anxiety disorders and migraines. The level of anxiety was increased in all patients with PPPV, but the severity of anxiety was significantly higher in patients with PPPV and peripheral vestibular disorders. Against the background of complex therapy, the severity of dizziness in all patients with PPPV significantly decreased.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.