Перспективы применения алендроната для лечения постменопаузального остеопороза
- Аннотация
- Статья
- Ссылки
- English
Остеопороз (ОП) называют немой эпидемией в связи с широкой распространенностью и асимптоматичным течением. Основной задачей терапии ОП является предотвращение переломов, которые развиваются на фоне снижения минеральной плотности кости (МПК), нарушения микроархитектоники костной ткани и ассоциируются с увеличением риска инвалидности и смерти. По прогнозам, количество переломов, обусловленных хрупкостью костной ткани, будет возрастать, что связано с повышением продолжительности жизни и изменением демографической ситуации в мире.
Эпидемиологические исследования показали, что около 40–50% женщин и 13–30% мужчин после 50 лет имеют один или более переломов, связанных с ОП. Эти данные эквивалентны риску сердечно-сосудистых заболеваний, обусловленных атеросклерозом [1, 2].
В мире ежегодно происходит 8,9 млн переломов, связанных с ОП, из них 4,5 млн приходится на Америку и Европу [3]. К сожалению, в России нет полных эпидемиологических данных. Однако с помощью моделирования эпидемиологической ситуации показано, что свыше 9 млн человек имеют периферические переломы и ежегодно происходит 3,8 млн переломов позвонков [4].
Затраты на лечение всех остеопоротических переломов в странах Европейского союза составляют 38,7 млн евро в год [5], на лечение и реабилитацию больных после перелома бедра – более 85% всех расходов, связанных с ОП [6].
Поскольку продолжительность жизни в большинстве стран увеличивается, финансовые и другие затраты, связанные с остеопоротическими переломами, будут только расти, если не предпринять превентивные меры.
Высокая распространенность ОП и связанных с ним переломов приводят к инвалидизации и значительному снижению качества жизни.
Большие затраты на лечение переломов ставят ОП в разряд социально значимых заболеваний и в настоящее время являются одной из важных проблем общественного здоровья, однако в России до сих пор данное заболевание не удостоено статуса социально значимого. Пациенты не получают бесплатного обследования и лекарственного обеспечения. 76% больных приобретают препараты за счет личных средств [7].
Результаты рандомизированных клинических исследований (РКИ) показали, что для лечения ОП и профилактики как первичных, так и повторных переломов можно использовать разные классы препаратов: снижающие разрушение костной ткани (антирезорбтивные) или повышающие ее образование. Бисфосфонаты рассматриваются сегодня в качестве препаратов первой линии в лечении ОП. Золотым стандартом терапии ОП признан алендронат.
Увеличение назначений бисфосфонатов врачами в последнее время связано с обширной доказательной базой, демонстрирующей эффективность и оптимальный профиль безопасности, а также с отсутствием необходимости постоянного мониторинга лабораторных показателей для оценки риска развития нежелательных явлений. Однако приверженность пациентов лечению ими, как и другими антиостеопоротическими средствами, остается низкой. Среди причин отказа от приема препарата выделяют плохую информированность пациентов о положительном эффекте, общую стоимость лечения, развитие нежелательных явлений и слабую мотивацию, что связано с недостаточным качеством медицинской помощи при ОП [8, 9]. Через год после назначения препарата менее 50% пациентов продолжают им лечение [10]. В то же время слабая приверженность терапии (менее 50%) ассоциируется с повышением риска переломов – на 40% (по сравнению с пациентами, приверженность которых лечению достигает 90%) [11]. Необходимо отметить, что если приверженность лечению составляет менее 50%, то эффективность терапии приравнивается к нулю [12]. Кроме того, у пациентов, не приверженных лечению, увеличивается риск госпитализаций, связанных с переломами и вторичными осложнениями, такими как выраженный болевой синдром, вторичная госпитальная инфекция и легочная тромбоэмболия; значительно ухудшается качество жизни [13, 14].
В России одна из ведущих причин прекращения терапии – высокая стоимость большинства оригинальных антиостеопоротических препаратов. Так, по результатам годичного наблюдения в первичном звене здравоохранения за 427 пациентками с постменопаузальным ОП, которым был назначен Фосамакс® 70 мг один раз в неделю, в 35,8% случаев отмена препарата была связана с его высокой стоимостью [16].
Указанные препараты недоступны пациентам с ограниченными материальными возможностями, прежде всего пенсионерам, которые составляют большую долю пациентов с ОП.
Несмотря на тот факт, что в настоящее время наряду с таблетированными препаратами существуют препараты для подкожного, внутримышечного и внутривенного введения, наиболее широко используются первые [17].
Важно напомнить, что при выборе оптимальной формы препарата для пациента необходимо учитывать сопутствующие заболевания, индивидуальные особенности и предпочтения в режиме приема препарата.
Фармакоэкономический анализ, проводимый в разных странах с целью выявления наименее затратных способов лечения ОП, показал, что наиболее целесообразна вторичная профилактика переломов у женщин и мужчин старше 70 лет, имеющих предшествующие переломы, низкую МПК (-2,5 стандартного отклонения по Т-критерию) или другие факторы риска (например, низкая масса тела, инсульт в анамнезе) [18]. Необходимо отметить: именно на примере алендроната была показана наибольшая экономическая эффективность бисфосфонатов в группах высокого риска [19–21].
Цель профилактики и лечения остеопороза – обеспечить прирост массы кости, снизить частоту и риск переломов, улучшить качество жизни пациентов. Это потребовало организации трех – пятилетних рандомизированных исследований для доказательства эффективности алендроната. Наиболее крупные из них FOSIT – многоцентровое (34 страны) рандомизированное двойное слепое плацебоконтролируемое исследование, включавшее 1908 постменопаузальных женщин с ОП, которые получали ежедневно в течение 12 месяцев алендронат в дозе 10 мг, и FIT – многоцентровое (11 центров США) рандомизированное двойное слепое плацебоконтролируемое исследование 2027 постменопаузальных женщин, получавших алендронат в дозах 5 и 10 мг в течение трех лет, а также десятилетнее наблюдение пациентов, продолжавших получать алендронат в тех же дозах либо плацебо. Алендронат показал высокую эффективность: повышая МПК во всех областях измерения – от 5,4% в шейке бедра до 13,7% в позвоночнике (уровень доказательности А), он достоверно снижал частоту переломов в позвоночнике (на 47%), бедре (на 51–56%), предплечье (на 48%). У 64% больных уменьшилось прогрессирование деформаций позвонков (уровень доказательности А).
Однако в России группы высокого риска ОП представлены в основном малообеспеченными гражданами, которым приходится самим нести бремя расходов на лекарственные средства. Таким образом, наличие на российском фармацевтическом рынке более доступных препаратов уменьшит затраты самих пациентов и позволит получать адекватную терапию большему числу больных.
В связи с доступностью и оптимальным соотношением «эффективность/стоимость» дженерики алендроната стали широко назначаться при ОП, однако качество препаратов неодинаково и требует тщательной оценки. В первую очередь необходимо выяснить, насколько аналог соответствует оригинальному препарату.
Минимизировать риски при применении дженериков возможно при использовании легальной копии (того же действующего вещества, что и в исследованиях) с доказанной биоэквивалентностью.
Два фармацевтических продукта биоэквивалентны, если они эквивалентны фармацевтически и параметры их биодоступности (скорость и степень доступности) после введения в одинаковой дозе сходны в такой степени, которая позволяет предполагать, что их воздействие будет одинаковым. Оценка фармакокинетической эквивалентности предполагает, что биоэквивалентные оригиналу воспроизведенные лекарственные средства обеспечивают одинаковую эффективность и безопасность фармакотерапии, то есть являются терапевтически эквивалентными.
В настоящее время появились публикации о различиях в переносимости оригинальных и воспроизведенных бисфосфонатов больными ОП. Как следствие, снижаются приверженность терапии и ее эффективность. В отдельных исследованиях показано снижение МПК или уменьшение темпов прироста костной массы при лечении дженериком алендроната по сравнению с оригинальным препаратом [22, 23]. В других работах отмечалось повышение частоты побочных реакций и ухудшение приверженности терапии [24, 25]. В связи с полученными данными обсуждается необходимость проведения проспективных сравнительных исследований, в которых можно установить терапевтическую эквивалентность оригинального и воспроизведенного препаратов [26].
Очевидно, что исследования биоэквивалентности лекарственных средств не заменяют РКИ, в которых оценивается эффективность препаратов. В то же время исследование терапевтической эквивалентности при ОП экономически не оправдано, поскольку для доказательства антипереломного эффекта требуется не менее трех – пяти лет и участие больших групп пациентов. В случае регламентации таковых произойдет значительное повышение стоимости дженериков. В такой ситуации они уже не будут обладать преимуществами в плане сокращения финансовых затрат.
Использование дженериков должно основываться на доверии к фармацевтической компании. Именно поэтому в клинической практике надо пользоваться препаратами известных и хорошо зарекомендовавших себя на фармацевтическом рынке компаний. Одним из таких препаратов является Фороза® («Сандоз», Швейцария). В одной таблетке Форозы содержится 70 мг алендроната натрия. Режим применения – один раз в неделю.
Алендронат относится к аминобисфосфонатам. Основной механизм действия – подавление фарнезилпирофосфатсинтетазы. Это ключевой фермент мевалонатного пути синтеза холестерина и изопреноидных липидов, которые способствуют пренилированию сигнальных G-белков, регулирующих клеточные процессы, необходимые для функционирования и выживаемости остеокластов [27].
Алендронат обладает высоким сродством (аффинностью) с костной тканью. Он быстро связывается с гидроксиапатитом. Вещество медленно всасывается в костную ткань и длительно сохраняется в ней даже после отмены препарата. У алендроната отмечается большая десорбция на костной поверхности [28]. Максимальный период полужизни алендроната в организме человека составляет около десяти лет [29]. Этот препарат в условиях in vivo не образует метаболитов, что объясняет небольшое количество побочных эффектов. Аминобисфосфонаты связываются с белками сыворотки и элиминируются посредством почечной экскреции [30].
Эффективность алендроната в отношении снижения риска позвоночных и непозвоночных переломов была показана в исследовании FIT – многоцентровое (11 центров) рандомизированное двойное слепое плацебоконтролируемое исследование 2027 женщин в постменопаузе, которые принимали 5 и 10 мг алендроната в течение трех лет, а также десятилетнее наблюдение пациентов, продолжавших получать алендронат в тех же дозах либо плацебо [31, 32].
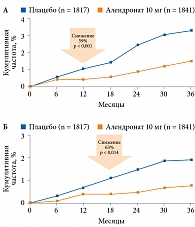
Результаты исследований свидетельствовали о снижении риска позвоночных переломов на 59% (р < 0,001) и проксимального отдела бедра на 63% (p < 0,002) (рис. 1) [31, 32]. В ходе метаанализа шести РКИ также была доказана эффективность алендроната в предотвращении перелома бедра – снижение риска перелома на 55% в группе пациенток с МПК -2,5 и ниже стандартного отклонения по Т-критерию [33].
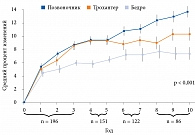
Отдаленные эффекты алендроната изучены в исследовании FLEX, в которое было включено 1099 пациентов из исследования фазы III [34]. Часть пациентов продолжила прием алендроната (длительность терапии – до десяти лет). За период наблюдения отмечалось стойкое повышение МПК (рис. 2) [35]. У пациенток, которые прекратили прием препарата через пять лет, зафиксировано небольшое снижение МПК и повышение маркеров костного обмена. При этом риск переломов не увеличивался по сравнению с пациентками, которые продолжали принимать алендронат. Был сделан вывод: при прекращении приема препарата у женщин со средним риском развития переломов риск последующих переломов не повышается. Тем не менее пациенткам с высоким и очень высоким риском переломов лучше не прекращать терапию через пять лет [34].
Для уменьшения побочных явлений и улучшения приверженности больных терапии была разработана форма алендроната для еженедельного приема (70 мг/нед). Эффективность новой формы доказана в одно- и двухлетних исследованиях с меньшим числом пациентов и менее продолжительных, чем РКИ фазы III, но с эквивалентным изменением суррогатных точек (МПК и биохимических маркеров костного обмена) [36].
При оценке предпочтений пациентов в использовании разных режимов лечения – ежедневного и раз в неделю – более 85% пациентов выбрали второй вариант, 9,2% – первый [37].
Поскольку алендронат применяется в России более 15 лет, накоплены данные об эффективности лечения препаратом в разных режимах. Работы показывают влияние алендроната на суррогатные показатели (МПК и биохимические маркеры костного обмена) и хорошую переносимость препарата, что согласуется с результатами зарубежных исследований [38–41].
Особенностью бисфосфонатов является их чрезвычайно низкая биодоступность при приеме таблетированных форм (0,7–1,8%). Поэтому их концентрация в плазме крови настолько низка, что ее невозможно оценить.
Большая часть препарата (40–70%) связывается с гидроксиапатитом костной ткани, оставшаяся – выводится из организма через почки. Поэтому для определения биоэквивалентности оригинального препарата и дженерика используют параметры экскреции с мочой: Ае0-72, Rmax , Tmax, где Ае0-72 – кумулятивная почечная экскреция за 72 часа наблюдения после однократного приема препарата, Rmax – максимальная почечная экскреция, Tmax – среднее время достижения максимальной экскреции.
Для определения биоэквивалентности препарата Фороза® – алендроната натрия 70 мг в таблетке («Сандоз», Швейцария) и оригинального алендроната Фосамакс® 70 мг в таблетке («Мерк Шарп&Доме», США) в независимой лаборатории Anapharm (Канада), специализирующейся на проведении исследований фазы I и биоэквивалентности препаратов, проведено одноцентровое открытое рандомизированное двукратно перекрестное исследование с участием 106 здоровых, некурящих мужчин в возрасте 18–55 лет. Полученные результаты свидетельствовали о биоэквивалентности алендроната натрия (Фороза®) референс-стандарту и возможности его использования для лечения постменопаузального, глюкокортикостероидного ОП и снижения костной массы у мужчин: биодоступность алендроновой кислоты существенно не различалась у пожилых и молодых пациентов.
Препарат Фороза® следует применять при удовлетворении суточной потребности в кальции и витамине D. Оптимальная длительность терапии не установлена. Продолжительность терапии бисфосфонатами должна оцениваться на регулярной основе, особенно после пяти или более лет применения. Для обеспечения надлежащего всасывания препарата Фороза® таблетки необходимо принимать утром натощак, не менее чем за 30 минут до первого приема пищи, напитков или других лекарственных препаратов, запивая не менее чем 200 мл воды. Одновременный прием алендроновой кислоты с пищей или в течение 2 часов после еды резко снижает абсорбцию препарата. Биодоступность характеризуется как незначительная. При совместном приеме с кофе или апельсиновым соком она уменьшается приблизительно на 60% [42].
Различия в эффективности оригинальных и воспроизведенных препаратов также могут быть обусловлены входящими в их состав вспомогательными веществами. Таковыми в препарате Фороза® являются микрокристаллическая целлюлоза, кремния диоксид коллоидный безводный, кроскармеллоза натрия и магния стеарат. Эти вещества индифферентны к костной ткани.
Преимуществом препарата Фороза® является запатентованная пленочная оболочка, которая помимо микрокристаллической целлюлозы содержит каррагинан и макрогол, защищающие слизистую пищевода от повреждения, способствуя высвобождению основного вещества уже в тонком кишечнике.
Применение алендронатов (Фороза®) актуально у женщин в постменопаузе для снижения риска компрессионных переломов позвоночника и переломов шейки бедра; у мужчин с целью лечения ОП и предупреждения переломов, а также при глюкокортикостероидном ОП.
Использование воспроизведенных препаратов позволяет сократить расходы на здравоохранение и прежде всего расходы самих граждан, что особенно актуально для стран с несовершенной системой обязательного медицинского страхования и социального обеспечения.
Применение качественных алендронатов с доказанной биоэквивалентностью позволит выполнить стратегическую цель Всемирной организации здравоохранения по обеспечению широкого доступа населения к медицинской помощи и расширению объема профилактических мероприятий, что в итоге должно привести к уменьшению распространенности остеопоротических переломов и улучшению качества жизни.
I.A. Skripnikova
State Research Center of Preventive Medicine
Contact person: Irina Anatolyevna Skripnikova, ISkripnikova@gnicpm.ru
Bisphosphonates are considered as the first line drugs for treatment of osteoporosis (OP) and prevention of fractures. However, patients still display low compliance to treatment with such drugs. High cost of brand anti-osteoporotic drugs is among lead reasons in Russia for discontinuing therapy. Due to availability and optimal efficacy/cost ratio for alendronate its generic forms has become widely prescribed during OP. However, quality of the drugs varies and demands through evaluation. Primarily, it must be found out do they correspond to the brand drug. Here, an opportunity and rationale of using generic alendronate, particularly Forosa®, in patients with OP are discussed.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.