Поражения легких у больных ревматоидным артритом и серонегативными спондилоартритами
- Аннотация
- Статья
- Ссылки
В статье представлен обзор литературных данных о характере и частоте различных видов поражения дыхательной системы при воспалительных заболеваниях суставов. Приводятся результаты предварительного анализа частоты встречаемости различных пульмонологических симптомов в терапевтическом и ревматологическом отделениях и их связи с активностью основного заболевания.
В статье представлен обзор литературных данных о характере и частоте различных видов поражения дыхательной системы при воспалительных заболеваниях суставов. Приводятся результаты предварительного анализа частоты встречаемости различных пульмонологических симптомов в терапевтическом и ревматологическом отделениях и их связи с активностью основного заболевания.

Поражение дыхательной системы является одним из наиболее часто встречающихся системных проявлений ревматоидного артрита (РА). В то же время их своевременное выявление и дифференциальная диагностика представляют собой достаточно сложную задачу. Типичные клинические симптомы, как и используемые рутинные методики, позволяют диагностировать в основном лишь далеко зашедшие изменения. Наибольшей информативностью обладает дорогостоящая методика КТ высокого разрешения (50–80%) и биопсия легких [1, 4, 6]. В то же время информативность рутинной рентгенограммы составляет не более 6% [4, 6]. Специфические клинические симптомы поражения легких выявляются лишь у 6,5–10% пациентов [4, 5]. Основные формы поражения легких и соответствующие им клинические синдромы представлены на рисунке 1. Согласно литературным данным, наиболее часто диагностируются поражения плевры, большая часть которых бессимптомны (40–75% аутопсий и 20% – рентгенологические изменения) или сопровождаются умеренным болевым синдромом (около 25%) [6]. Вторым по частоте заболеванием паренхимы легких является ассоциированная с ревматоидным артритом интерстициальная болезнь легких (RA-ILD) [1–7]. Наиболее часто встречается обыкновенная интерстициальная пневмония – UIP, один из самых неблагоприятных вариантов RA-ILD [6–8]. Реже диагностируется неспецифическая интерстициальная пневмония, в большей степени типичная для системных заболеваний соединительной ткани [7, 8]. Встречаются также смешанные варианты с элементами лимфоцитарной интерстициальной пневмонии [6, 7]. Указанным состояниям сопутствуют рестриктивные изменения. Ранняя клиническая симптоматика RA-ILD в этих случаях может включать сухой кашель и одышку инспираторного типа. При некоторых вариантах RA-ILD (криптогенная организующая пневмония – СОР [9] и крайне редко ассоциирующаяся с ревматоидным артритом респираторная бронхиолит-интерстициальная болезнь легких – RB-ILD) одышка может быть смешанной или экспираторной, а при физикальном обследовании могут определяться признаки обструкции (жесткое дыхание, коробочный перкуторный тон). Обструктивный и бронхитический синдромы при RA-ILD могут быть следствием развития тракционных бронхоэктазов на фоне значительного фиброза легочной ткани [6]. Реже RA-ILD развивается как осложнение базисной терапии (метотрексат, препараты золота, D-пеницилламин) [1, 2, 6, 7]. Достаточно редко встречается эозинофильная пневмония (острая или хроническая), в том числе в дебюте заболевания [10].
Другой наиболее частый вариант поражения паренхимы – ревматоидные узелки – в подавляющем большинстве случаев является бессимптомным [1, 2]. При рутинной рентгенографии они выявляются всего у 1% пациентов, в то время как при КТ высокого разрешения частота выявления достигает 22% случаев. По данным аутопсии, узелки в легких обнаруживаются у 32,5% умерших больных с РА [4, 6]. Осложнениями ревматоидных узелков может быть развитие некроза с образованием полости, кровохарканьем, спонтанным пневмотораксом или эмпиемой плевры. Описаны случаи микозного поражения узелка с развитием мицетомы [4]. Дифференциальная диагностика очаговых изменений в легких у больных РА представляет особую диагностическую проблему в связи с высоким риском туберкулезного процесса не только у больных, получающих биологическую терапию (в 30 раз выше, чем в общей популяции), но и пациентов, получающих традиционное лечение метотрексатом и преднизолоном (в 4–8 раз выше, чем в популяции) [11, 12]. Некоторыми авторами обсуждается проблема роста ревматоидных узелков на фоне биологической терапии (инфликсимаб, этанерцепт) или лечения лефлюнамидом, однако в других публикациях этот феномен не подтверждается, тем более что продолжение терапии не приводит к клиническому ухудшению состояния пациента [13, 14, 20]. Редкой причиной очаговых изменений в легких при РА может быть перекрест-синдром с ограниченными легочной паренхимой проявлениями гранулематоза Вегенера [16]. Необходимо отметить, что как интерстициальная болезнь легких, так и ревматоидные узелки значительно чаще обнаруживаются у курящих пациентов по сравнению с некурящими [6]. Тем не менее наличие соответствующего анамнеза не должно рассматриваться как фактор, позволяющий полностью объяснить имеющиеся пульмонологические симптомы и исключить наличие поражения дыхательных путей, обусловленное РА.
Несколько реже встречаются поражения дыхательных путей, проявляющиеся обструктивным и бронхитическим синдромом. К ним относятся бронхоэктазы (в большинстве случаев тракционного характера на фоне RA-ILD), облитерирующий бронхиолит, фолликулярный бронхиолит и бронхоцентрический гранулематоз [6]. В целом частота развития патологии бронхиального дерева (включая тракционные бронхоэктазы) составляет около 30% [1–3, 6]. Обструктивные нарушения функции внешнего дыхания диагностируются примерно у 38% пациентов с нормальными результатами рентгенограммы [15]. Достаточно редки, но опасны начальные проявления легочного васкулита – кровохарканье, одышка или легочная гипертензия – и его потенциально фатальное осложнение – диффузное альвеолярное кровотечение, клинически и морфологически сходное с аналогичным состоянием при системной красной волчанке и обусловленное некротизирующим капилляритом с отложением иммунных комплексов. Клинические симптомы диффузного альвеолярного кровотечения включают острое развитие выраженной инспираторной одышки с резкой гипоксемией, кровохаркание, анемии [6].
При анкилозирующем спондилоартрите пульмонологические симптомы встречаются реже – примерно у 10% пациентов. Рестриктивный характер изменений обнаруживается при наиболее типичном осложнении – двустороннем апикальном фиброзе верхних долей, развитии буллезных изменений (как правило, той же локализации), а также при анкилозе костовертебральных суставов. Описаны случаи развития интерстициальной болезни легких, сходной с таковой при РА, однако в этих публикациях отсутствуют сведения о вариантах данного заболевания. Обструктивный синдром и смешанный характер изменений могут быть обусловлены тракционными бронхоэктазами или парасептальной эмфиземой [16–18]. У больных псориатическим артритом могут встречаться узловые образования в легких, сходные с таковыми у пациентов с РА. Подобные узелки, так же как и при РА, могут осложняться некрозом и спонтанным пневмотораксом [19].
Таким образом, при РА и серонегативных спондилоартритах (ССА) достаточно часто встречается поражение дыхательной системы. При этом ранняя диагностика указанных изменений затруднена в связи с неспецифичностью симптомов и поздним появлением изменений, определяемых рутинными методами, доступными практическому здравоохранению. В связи с этим представляется актуальным анализ диагностической значимости неспецифических пульмонологических симптомов (кашель, одышка, изменения перкуторной или аускультативной картины легких), позволяющих заподозрить вовлеченность легких в патологический процесс и, соответственно, планировать дальнейшее обследование пациентов с помощью высокотехнологичных методов.
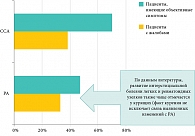
С целью поиска наиболее информативных клинических симптомов, определяемых рутинной диагностикой, проведен анализ историй болезни 29 больных ревматоидным артритом и 24 пациентов с серонегативными артритами, находившихся на лечении в клинике госпитальной терапии в период с 2006 по 2009 г. Средний возраст больных составлял 51,4 года, средняя длительность заболевания – 7,6 лет. Средний показатель активности заболевания составил 2,23, значения индекса DAS4 – 3,3 DAS28 – 4,9. Из 28 пациентов отрицательные значения ревматоидного фактора отмечались у 6, у 2 серонегативных пациентов не выявлялись антитела к циклическому цитруллиновому пептиду (АЦЦП). Системные проявления отмечались у 18 серопозитивных и 3 серонегативных пациентов. Наиболее частыми проявлениями у серопозитивных пациентов были лихорадка [9] и лимфаденопатия [5]. Анемия выявлена у 3 больных, еще у 3 – ревматоидные узелки и полинейропатия. У 2 пациентов документировано поражение дыхательной системы (интерстициальная болезнь легких и выпотной плеврит), у 1 – синдром Шегрена. В целом 3 и более системных проявлений имели место у 4 пациентов. У серонегативных пациентов имели место лихорадка [2], лимфаденопатия [2], амиотрофия и синдром Рейно [1]; 3 и более системных проявлений отмечалось у 1 пациента. Несмотря на то что диагностированное поражение легких отмечалось лишь у 2 серопозитивных пациентов с высокой степенью активности заболевания, такие симптомы, как кашель, одышка, отмечались у 8 пациентов (28,6%), объективные изменения в легких (коробочный тон, жесткое дыхание) – у 20 (71%). Реже указанные симптомы наблюдались у больных ССА. Одышка, затруднение дыхания и кашель встречались у 7 (29,1%), объективные изменения в легких зарегистрированы у 11 (45,8%) пациентов (рис. 2).
Обращает на себя внимание тот факт, что 10 больных РА и 4 ССА, у которых выявлялись объективные симптомы со стороны легких, не курили (рис. 3). Таким образом, примерно у половины пациентов с РА и более чем у 3 с ССА наличие симптомов не может быть объяснено ХОБЛ. Кроме того, как уже указывалось выше, пульмонологические симптомы при РА чаще отмечаются у курящих больных, что требует включения таких пациентов в диагностический поиск.
Анализируя связь перечисленных симптомов с активностью заболевания, было обнаружено, что у больных РА, предъявляющих пульмонологические жалобы, по сравнению с пациентами, не имеющими симптомов поражений легких, отмечались более высокие показатели активности заболевания – 2,8 и 2,0 – и значения индекса DAS4 – 4 и 2,9 соответственно. Эти больные были старше по возрасту – 55,9 и 49,6 – и имели большую длительность заболевания – 8,6 и 7,6 лет соответственно. Та же тенденция отмечалась и у пациентов с ССА: больные, предъявляющие пульмонологические жалобы, отличались большей активностью заболевания, у 49,5% из них определялось 2 и более системных проявлений против 26,7% пациентов без жалоб.
Из 12 пациентов с РА, которым производилось рентгенологическое исследование в клинике, только у 4 не было диагностировано каких-либо изменений. Изменения плевры обнаружены у 2 больных (экссудативный плеврит, плевральные шварты), у 5 – паренхиматозные изменения (диффузные интерстициальные изменения с субплевральным фиброзом, множественные субплевральные округлые образования в нижней доле, лимфаденопатия, субплевральный тяж в паренхиме одного из сегментов, диск-ателектаз, посттуберкулезные изменения). У одного пациента выявлены перибронхиальные изменения (подчеркнутость структуры бронхов). Таким образом, только у 2 пациентов были выявлены достоверные признаки, позволяющие диагностировать ревматоидное поражение легких. В то же время наличие множественных очаговых образований, плевральных шварт, лимфаденопатии и субплеврального тяжа требовали проведения дифференциальной диагностики между специфическим процессом (туберкулез), проявлениями ревматоидного артрита (в том числе последствиями криптогенной организующей пневмонии) и неспецифическими постпневмоническими изменениями (плевральные шварты). Наличие дисковидного ателектаза у больной 49 лет с высокой (3-я степень) активностью заболевания и ревматоидными узелками без признаков варикозной болезни нижних конечностей может быть обусловлено эпизодом тромбоэмболии на фоне активации эндотелия и внутрисосудистой гемокоагуляции. Из 12 пациентов ССА, у которых производилось рентгенологическое исследование, не обнаружены изменения в легких у 7 (58,3%), у 3 (25%) определялись паренхиматозные (посттуберкулезные у 2, диск-ателектазы у 1), у 1 (8,3%) – перибронхиальные изменения. Ни у одного из пациентов не были определены признаки поражения плевры. Таким образом, как при РА, так и, в меньшей степени, при ССА достаточно часто выявляются как клинические пульмонологические симптомы, так и рентгенологические изменения в паренхиме легких. При этом у пациентов, предъявляющих жалобы со стороны дыхательной системы, отмечается более высокая активность заболевания, чаще диагностируются системные проявления. В связи с этим можно предположить, что неспецифические пульмонологические симптомы могут быть начальными проявлениеми поражения легких в рамках РА или ССА, что требует проведения у этих пациентов углубленного обследования дыхательной системы, в том числе с применением высокотехнологичных методов.
Необходимо отметить, что при наличии рентгенологических изменений в легких (фиброзные тяжи, шварты, очаговые образования) требуется проведение дифференциальной диагностики с туберкулезным процессом, в том числе определение уровня антител к туберкулезной микобактерии. У 24,1% пациентов с РА и 18,1% больных ССА был контакт с больными туберкулезом в анамнезе и/или выявлены признаки, свидетельствующие об активации туберкулезной инфекции (посттуберкулезные изменения на рентгенограмме или положительная реакция Манту на пробу с 2ТЕ ППД-Л). С учетом приведенных ранее литературных данных о повышенном риске развития туберкулеза у больных РА (в том числе не получающих биологическую терапию), это свидетельствует о возможности развития у данных пациентов осложнений на фоне терапии биопрепаратами. Профилактический курс лечения изониазидом в противотуберкулезном диспансере по месту жительства проводился у 10% больных РА и 13,6% ССА. Ни у одного пациента не обнаружено признаков активации туберкулезной инфекции на фоне лечения инфликсимабом. Таким образом, при правильном отборе пациентов для проведения терапии антагонистами ФНО применение биологической терапии является достаточно безопасным и не приводит к активизации туберкулезной инфекции.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.