Принципы терапии формирующегося синдрома поликистозных яичников у подростков
- Аннотация
- Статья
- Ссылки



Лечебная тактика при синдроме поликистозных яичников (СПКЯ) в течение последних лет претерпела существенные изменения, однако окончательно она еще не определилась. В заключительном документе Роттердамского консенсуса (2003) СПКЯ был охарактеризован как синдром овариальной дисфункции, к специфическим проявлениям которой относятся гиперандрогения, нарушения менструального цикла, «поликистозная» морфология яичников. В этой связи логично, что лечение СПКЯ в значительной степени зависит от возраста больной.
Традиционные схемы лечебных мероприятий у девушек и молодых женщин, не планирующих беременность, направлены на нормализацию менструального цикла, устранение клинических проявлений гиперандрогении, а также на профилактику гиперпластических процессов в органах-мишенях. Своевременное и адекватное лечение гиперандрогении и ановуляции у пациенток с СПКЯ уже в подростковом периоде решает не только текущие медицинские задачи, но и является профилактикой отдаленных осложнений этого состояния, способствует улучшению репродуктивной функции в дальнейшем, повышению качества жизни, снижению заболеваемости и смертности.
В современных публикациях описаны многочисленные варианты лечения – от витаминов и прочих негормональных препаратов до комбинированных оральных контрацептивов (КОК) и агонистов гонадотропин-рилизинг гормона (ГнРГ) [2, 5]. В последние годы в иностранных и отечественных источниках, включая руководства для врачей, при лечении СПКЯ (в том числе у подростков) рекомендовано применение ингибиторов синтеза пролактина, бигуанидов, сенситайзеров инсулина и др. [3, 8]. Однако, несмотря на многочисленность используемых схем лечения, ожидаемый результат достигается далеко не во всех случаях [4].
В соответствии с патогенезом заболевания, в пубертатном периоде наиболее оправданным является применение КОК. Этинил-
эстрадиол в комбинации с прогестагеном повышает синтез глобулинов, связывающих половые гормоны (ГСПГ) в клетках печени, снижает секрецию тестостерона и андростендиона яичниками. Прогестагены снижают выброс ГнРГ гипоталамусом и как следствие – секрецию лютеинизирующего гормона (ЛГ) гипофизом, в результате чего снижается синтез андрогенов яичниками [1]. К тому же прогестагенный компонент конкурентно связывается с рецепторами андрогенов и может оказывать антиандрогенное действие на ткани-мишени. Результаты современных исследований показали, что при использовании КОК в непрерывном режиме в течение 3 циклов имеет место более полноценное торможение секреции ФСГ и отсутствие фолликулярного роста [6, 7], однако в подростковом периоде оценка подобного способа лечения не проводилась.
Целью проведенного нами исследования явилось определение эффективности и безопасности использования КОК в пролонгированном режиме у девочек с диагностированным СПКЯ.
Материалы и методы
В исследование включено 47 девочек-подростков наблюдавшихся в НЦАГиП им. В.И. Кулакова в 2008–2010 гг. с диагнозом формирующийся СПКЯ, подтвержденным клинико-лабораторными данными (нарушение менструального цикла, андрогензависимая дермопатия, уровень гормонов: ЛГ > 10 МЕ/л, отношение ЛГ/ФСГ > 2,5, общий тестостерон > 2,5 нмоль/л) и результатами эхографии (увеличение объема яичников более 10 см3, наличие в ткани множества (> 10) мелких анэхогенных образований до 10 мм в диаметре, увеличение яичниково-маточного индекса > 3,5). После получения информированного согласия на лечение и исключения противопоказаний к использованию гормональной терапии всем девочкам назначен монофазный низкодозированный контрацептив, содержащий в каждой таблетке 30 мкг этинилэстрадиола и 150 мкг дезогестрела (препарат Регулон® фирмы «Гедеон Рихтер», Венгрия) в пролонгированном режиме в течение трех 63-дневных курсов с семидневными перерывами между ними. Этот препарат выбран на основании имеющихся данных о высокой прогестагенной активности, сохранении биологического действия эстрогеновых рецепторов дезогестрелом, отсутствии метаболического и андрогенного эффектов.
Лечение начиналось с первого дня спонтанного или индуцированного приемом дидрогестерона менструального цикла (по 10 мг х 2 раза в день в течение 10 дней) при наличии задержки менструаций более чем на 40 дней.
Клиническая эффективность терапии оценивалась на основании изучения меноциклограммы и степени выраженности симптомов гиперандрогении у пациенток в течение 6 месяцев после окончания приема КОК. Оценка ритма самостоятельных менструаций была сопоставима с данными меноциклограммы до включения пациенток в исследование. Каждая девочка вела дневник, где отмечала прием таблеток, кровяные выделения и побочные эффекты (головная боль, головокружение, тошнота, метеоризм, депрессия). Ациклическими кровяными выделениями считались скудные «мажущие» кровяные выделения или кровотечения «прорыва». Скудные кровяные выделения на фоне приема КОК, требующие использования максимум одной ежедневной прокладки или вообще не требующие применения дополнительных средств гигиены, расценивались как «мажущие», а кровяные выделения, требующие использования как минимум двух ежедневных прокладок, считались кровотечением «прорыва».
Адекватность, приемлемость и наличие побочных эффектов проводимой терапии оценивали по результатам динамического контроля уровней гормонов крови, эхографии органов малого таза и показателей гемостаза и липидного спектра крови на 5–7-й день отмены первого и третьего 63-дневного курса приема КОК, а также спустя 3 и 6 месяцев после окончания гормонотерапии на 3–5-й день менструального цикла. В эти дни определяли концентрацию в крови ЛГ, ФСГ, тестостерона, эстрадиола, кортизола, ДГАС, пролактина, тестостерон-эстрадиол-связывающего глобулина (ТЭСГ).
Эхография проводилась с помощью датчика внутриполостного сканирования с возможностью автоматического сбора информации для получения трехмерного изображения и диапазоном частот 3,7–9,3 МГц на стационарном аппарате «Voluson 730 Pro» (GE Medical Systems Kretztechnik, Австрия), оснащенном режимами цветового допплеровского картирования (ЦДК), трехмерной эхографии. Во время сонографического исследования особое внимание уделяли размерам и форме яичников, количеству и характеру расположения в них фолликулов. В режиме трехмерной реконструкции сосудов (3D-эхоангиографии) была получена пространственная карта сосудистых структур органов малого таза, позволяющая выявить их анатомо-топографическое расположение, а также оценить локализацию и количество внутриорганных кровеносных сосудов. На третьем этапе исследования проводилась допплерометрия сосудов с регистрацией кривых скоростей кровотока и анализом допплеровского спектра эхосигналов. Допплеровский анализ включал определение характера кровотока, количество цветовых сигналов от сосудов в исследуемой зоне.
Результаты
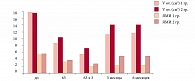
Обследовано 47 девственниц в возрасте от 12 до 19 лет (средний возраст 17,13 ± 0,18 лет). По возрасту больные распределились следующим образом: до 13 лет – 3 девочки (6,3%), 14–16 лет – 12 девушек (25,5%), 17–19 лет – 32 девушки (68,2%).
В зависимости от полученных результатов все пациентки были разделены на две группы: в 1-ю группу (группа эффективного лечения) включены 35 девушек с регулярным менструальным циклом, нормативными значениями изучаемых гормональных и эхографических показателей; во 2-ю группу (группа неэффективного лечения) вошли 12 пациенток с возобновившимися расстройствами менструаций, гормональными и эхографическими отклонениями, выявленными в исходном цикле обследования до начала лечения. При этом пациентки 2-й группы оказались в среднем на 1 год старше девушек из 1-й группы (18,5 ± 0,1 лет и 17,1 ± 0,3 соответственно).
Большинство пациенток (85,1%) наблюдались по месту жительства и получали различное лечение по поводу расстройств менструаций. Анализ предшествующей терапии показал, что комбинированные оральные контрацептивы в 21-дневном режиме получили 17 девушек, прогестагены (преимущественно дидрогестерон 20 мг/сутки во вторую фазу цикла) – 5, причем указанные препараты назначались, как правило, не более чем на 3 месяца. Негормональная коррекция нарушений ритма менструаций проведена 12 девушкам. Из их числа 4 пациентки получили витаминотерапию в циклическом режиме (ЦВТ), 5 – препараты растительного происхождения, трем пациенткам ранее не назначалось лечение, а была предложена выжидательная тактика, несмотря на то что после менархе у каждой из них прошло более года.
Анализ особенностей менструального цикла показал, что 39 (83%) девушек имели своевременное менархе в возрасте от 11,8 до 14 лет, в среднем – 13,6 ± 0,24 лет. У одной девушки менархе возникло в 9 лет, у 35 (87,5%) пациенток нарушения менструального цикла начались с менархе и у 5 (12,5%) – через 2–6 месяцев после менархе. Задержки менструаций до 6 месяцев имели место у 23 (57,5%), более полугода – у 14 (35%), маточные кровотечения – у 3 (7,5%) из 40 больных. Продолжительность менструации колебалась от 3 до 7 дней и в среднем составила 4 дня. При этом умеренное количество кровяных выделений отметили 27 (67,5%), обильные менструации – 6 (15%), скудные менструальные выделения – 7 (17,5%) девушек.
У 7 пациенток имела место первичная аменорея. Для определения реактивности эндометрия и исключения маточной формы первичной аменореи этим девочкам была проведена проба с гестагенами. В качестве гестагена использовался дидрогестерон, который по своей молекулярной структуре, химическим и фармакологическим свойствам весьма близок к природному прогестерону, но не обладает эстрогенной, андрогенной и термогенной активностью. Дидрогестерон использовался в форме таблетированного препарата Дюфастон для перорального применения по 10 мг х 2 раза в день (максимальная доза) в течение 10 дней. Появление кровяных выделений из половых путей пациенток до окончания цикла приема гестагена расценивалось нами как начало индуцированной менструации, что требовало отмены препарата. К достоинствам Дюфастона относится отсутствие анаболического эффекта, минералокортикоидной и глюкокортикоидной активности, а также отрицательного влияния на метаболизм белков, углеводов, на уровень липидов крови. Препарат не оказывает отрицательного влияния на функцию печени, не влияет на тромбоцитарную агрегацию, активность факторов коагуляции и систему фибринолиза. Менструально-подобная реакция возникла на 2–8-й день (положительная проба) после отмены препарата у всех семи девочек, что исключило маточную форму аменореи I.
Все 47 пациенток получили терапию в полном объеме. В единичных случаях наблюдались кратковременные побочные эффекты, не требовавшие отмены препарата. Так, в течение первых нескольких дней на фоне лечения 3 девочки предъявляли жалобы на преходящую тошноту, 3 – на умеренные и непродолжительные головные боли, 2 – на редкие головокружения без обмороков. Жалобы на кратковременную (за 2–3 месяца) прибавку массы тела на 1–2 кг в первые 2–3 месяца от начала терапии предъявили 4 (8,5%) пациентки. У всех больных печеночные ферменты на фоне терапии остались в пределах нормативных значений (АЛТ; АСТ; ЩФ до/после лечения: 21,7 ± 3,1 / 22,4 ± 4,6; 22,7 ± 2,5 / 22,4 ± 2,3; 156,7 ± 7,1 / 158,5 ± 10,6 соответственно). На фоне применения КОК не выявлено заметных изменений в показателях гемостазиограммы (изокоагуляция наблюдалась после лечения у всех девушек).
Прием гормональных препаратов существенно не повлиял на показатели пролактина (ПРЛ) в сыворотке крови пациенток и находился в пределах нормативных значений на протяжении всего времени наблюдения. В то же время исследование уровня кортизола свидетельствовало о значительном увеличении его содержания в сыворотке крови на протяжении всего курса лечения, что было расценено нами как закономерные изменения гомеостаза на фоне приема гормональных препаратов. Однако уже через 3 месяца после отмены лечения уровень кортизола снизился до нормативных возрастных значений (рис. 1).
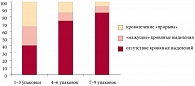
У всех пациенток наблюдались менструальноподобные реакции на отмену препарата, аменорея не отмечена ни в одном случае. Кровотечения «прорыва» возникали после приема различного количества таблеток, однако со временем постепенно снижалась их частота и интенсивность. Так, в начале исследования, в период приема первых трех упаковок они выявлены у 16 (34%) девушек и средняя продолжительность кровотечений составила 2,1 дня, однако к концу исследования, за время приема последних трех упаковок этот показатель снизился до 0,3 дней и кровотечения отмечены лишь 3 (6%) девушками. «Мажущие» кровяные выделения наблюдались в основном в течение приема первых трех упаковок у 12 (26%) пациенток со средней продолжительностью 6,27 дней. Однако во время приема последних трех упаковок число больных с указанными жалобами уменьшилось до 4 (9%) пациенток, а средняя продолжительность кровотечений составила 0,9 дней (рис. 2).
Значительное уменьшение выраженности гирсутизма и исчезновение угревых высыпаний отмечено уже через 3 месяца приема КОК у 24 (51%) и у 18 (38,3%) девушек соответственно, положительный результат сохранялся спустя 6 месяцев после окончания лечения.
Положительная динамика в характере менструального цикла (4 самостоятельные менструации за 6 месяцев) отмечена нами у 37 (78,7%) пациенток после лечения (табл. 1).
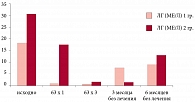
На фоне применения КОК у пациенток обеих групп произошло одинаковое снижение ЛГ и Т – основных маркеров формирующегося СПКЯ – уже после первого 63-дневного курса, при этом достигнутые показатели ЛГ и Т остались неизменными до окончания гормонотерапии. Спустя 3 месяца после отмены препаратов было отмечено увеличение уровня ЛГ и Т, причем в группе с положительным эффектом, несмотря на некоторое плавное увеличение изучаемых гормональных показателей, их значения находились в нормативных пределах и через 6 месяцев после лечения, тогда как у девушек 2-й группы было отмечено стойкое значительное повышение уровня ЛГ и Т, превышающее верхнюю границу нормативных значений (рис. 3, 4).
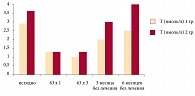
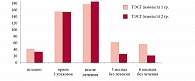
Несмотря на закономерное увеличение содержания ТЭСГ в сыворотке крови пациенток в ходе лечения, снижение данного показателя после отмены терапии у девушек из обеих подгрупп было различным. Так, у пациенток в группе с положительным эффектом снижение данного показателя не выходило за рамки референсных значений, тогда как у пациенток 2-й группы на 3-й и 6-й месяцы без лечения наблюдалось снижение ТЭСГ до 22,46 ± 4,3 нмоль/л и 17,55 ± 0,34 нмоль/л соответственно, что выходит за рамки нормативных показателей (рис. 5).
Клиническая эффективность терапии четко коррелировала с изменениями изучаемых эхографических параметров органов малого таза (рис. 6). У пациенток 1-й группы в ходе лечения отмечалось более выраженное уменьшение объема яичников по сравнению с больными 2-й группы (после приема 1 курса терапии: 8,6 см3 и 10,4 см3 соответственно; после окончания лечения: 5,5 см3 и 7,2 см3 соответственно). Более того, у девушек в группе неэффективной терапии данный показатель, хотя и не соответствовал прежним значениям, регистрировался как высокий – 14,1 см3. Кроме того, через 6 месяцев после лечения у них сохранялись явления асимметрии яичников (Vправого яичника > V левого яичника в среднем на 4,1 ± 0,9), ранее нивелировавшиеся на фоне терапии. У пациенток с восстановленным менструальным циклом и нивелированием признаков гиперандрогении через 6 месяцев после окончания терапии объем яичников незначительно превышал допустимое значение (11,2 см3), что, скорее всего, связано с визуализацией у большинства из них желтого тела в стадии обратного развития. У пациенток этой группы даже при отсутствии признаков свершившейся овуляции (12 и 9 больных соответственно через 3 и 6 месяцев обследования без лечения) разница в объеме правого и левого яичника была незначительной и составила в среднем 1,9 ± 0,3 см3. В этой группе также не наблюдалось сгруппированности фолликулов, их контуры при этом расценивались нами как изоэхогенные, отмечался менее выраженный сосудистый рисунок в сравнении с прежними результатами при цветовом допплеровском картировании. В ходе проведения импульсной допплерометрии у пациенток 1-й группы выявлены нормативные значения индекса резистентности (ИР) (0,50 ± 0,05 в яичниках с признаками свершившейся овуляции и 0,52 ± 0,06 в неовулирующих яичниках). У пациенток 2-й группы отмечались повышенные, монотонные значения ИР (0,62 ± 0,05), при этом признаки овуляции отсутствовали.
Заключение
Применение КОК в 63-дневном режиме в течение 29 недель позволяет достичь положительного клинико-лабораторного эффекта у 78,7% подростков с формирующимся СПКЯ. Достоверными критериями эффективного лечения являются формирование регулярного ритма менструации после отмены КОК, стойкое улучшение состояния кожи, нормализация уровня ЛГ, Т, ТЭСГ, объема и структуры яичников, уменьшение васкуляризации стромы, цикличное выявление желтых тел. Высокая эффективность предложенной схемы лечения, низкий процент побочных эффектов и в целом хорошая переносимость препарата позволяют рекомендовать Регулон® для лечения СПКЯ у подростков. Пациентки группы неэффективного лечения нуждаются в дальнейшем углубленном обследовании для уточнения природы заболевания и более точного подбора патогенетически оправданного лечебного воздействия.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.