количество статей
7376
Загрузка...
Пожалуйста, авторизуйтесь:
Исследования
Проблема использования дженериков при остеопорозе
Эффективная фармакотерапия. Эндокринология. СПЕЦВЫПУСК № 2.
- Аннотация
- Статья
- Ссылки
Основным проявлением остеопороза (ОП) являются переломы различной локализации, возникающие при низкоэнергетической травме. Фармакотерапия ОП нацелена на снижение риска переломов, которые ассоциируются с временной утратой трудоспособности, инвалидностью и, в некоторых случаях, увеличением смертности. В связи с неуклонным ростом числа переломов, связанных с ОП, возрастают затраты на их лечение. Одним из возможных способов снижения затрат на фармакотерапию ОП является использование воспроизведенных препаратов (дженериков), цена которых ниже по сравнению с оригинальными (брендовыми) лекарственными средствами. В статье обсуждается проблема терапевтической эквивалентности оригинальных и воспроизведенных противоостеопоротических препаратов. На примере препаратов группы бисфосфонатов показано, что к настоящему времени завершены продленные исследования, доказавшие возможность безопасного длительного применения оригинальных бисфосфонатов (вне зависимости от способа назначения) при ОП. Авторы подчеркивают, что широкому внедрению в клиническую практику дженериковых аналогов должны предшествовать исследования, подтверждающие их терапевтическую эффективность и хорошую переносимость, сопоставимую с брендовыми препаратами.
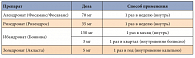
Таблица. Перечень бисфосфонатов и способ их применения
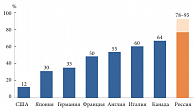
Рис. Доля дженериков на фармацевтическом рынке различных стран
Остеопороз относится к наиболее распространенным заболеваниям людей старшего возраста. В связи с этим перед органами здравоохранения стоит важная задача по организации медицинской помощи пациентам с данной патологией. В большинстве стран Европы и Северной Америки основную нагрузку по диагностике, профилактике и лечению ОП берут на себя врачи общей практики первичного звена здравоохранения. Действительно, трудно представить, что оказывать адекватную и всеобъемлющую помощь пациентам с ОП смогут врачи-специалисты, однако именно они (эндокринологи, ревматологи, травматологи, гинекологи и др.) должны проводить консультативно-диагностическую работу на высоком качественном уровне, помогая врачу общей практики (а в России и участковому терапевту) в сложных клинических ситуациях. Например, врач-специалист может выступать в качестве эксперта в случаях, когда: 1) отсутствует клинический эффект при длительном применении антиостеопоротических препаратов (нет нарастания минеральной плотности кости (МПК), на фоне лекарственной терапии развиваются новые переломы); 2) на первый план выходят тяжелые побочные реакции при последовательном применении нескольких антиостеопоротических препаратов; 3) остеопороз диагностирован на фоне сопутствующей патологии, которая может ограничивать применение лекарственных средств, и др.
В настоящее время в соответствии с приказом Министерства здравоохранения Российской Федерации № 239 от 11.08.1997 «Об организации центров профилактики остеопороза» успешно осуществляют свою деятельность более 40 региональных консультативно-диагностических центров, которые рассматриваются в качестве специализированных подразделений, отвечающих за внедрение современных методов профилактики, диагностики и лечения ОП на основе национальных клинических рекомендаций и разрабатываемых методических указаний.
Эпидемиология остеопороза и переломов
Эпидемиологические исследования показали, что нет страны, расы или нации, свободной от остеопороза. ОП диагностируется примерно у 30% людей старше 50 лет, с некоторым преобладанием среди женщин. При этом медико-социальное значение болезни определяется числом и риском переломов различной локализации. Так, суммарный риск переломов бедра, предплечья и позвоночника после 50 лет составляет около 50%, что сравнимо с рисками кардиоваскулярных событий (инфарктов и инсультов) [1].
Эпидемиологические исследования, проводимые в различных странах, позволили подсчитать количество случаев переломов бедра в мире. В 1990 г., например, было зарегистрировано 1,66 млн переломов данной локализации. Согласно прогнозам экспертов, к 2050 г. число переломов бедра должно увеличиться в несколько раз и составить 6,26 млн случаев с учетом только фактора постарения населения. Наиболее высока частота переломов бедра в Северной Америке и скандинавских странах. В Европе число переломов бедра с поправкой на возраст варьирует в диапазоне от 50 случаев на 10 тыс. населения на Мальте и в Польше до 500 случаев в Швеции. При этом в разных государствах Европы наблюдаются существенные расхождения в значении такого показателя, как соотношение числа переломов бедра между женщинами и мужчинами: от 1,6 в Польше до 4,2 в Ирландии [2].
Затраты на лечение остеопороза
Прямые расходы на лечение переломов в Европе составили 31,7 млрд евро в 2000 г. Ожидается, что к 2050 г. они могут удвоиться, что будет обусловлено демографическими изменениями в структуре населения [3]. В России анализ экономических затрат на лечение переломов представлен единичными работами. Так, по данным, полученным в Екатеринбурге (население 1,4 млн человек), общие затраты на лечение только переломов шейки бедра и дистального отдела предплечья у лиц в возрасте 50 лет и старше составили 10 млн рублей в год, что значительно ниже, чем в зарубежных странах [4]. Исследование, проведенное в Санкт-Петербурге, показало, что прямые затраты на лечение одного случая перелома дистального отдела предплечья составили около 18 тыс. рублей [5].
Фармакотерапия остеопороза
Разработка и внедрение в клиническую практику эффективных и безопасных способов лечения потенциально могут сократить затраты. В настоящее время на рынке представлен широкий спектр лекарственных средств, которые при длительном применении способны снижать относительный риск вертебральных переломов на 40–75%, невертебральных переломов – примерно на 20%, а переломов бедра – на 40%. Как и для большинства хронических неинфекционных заболеваний, фармакотерапия ОП должна основываться на балансе между эффективностью и переносимостью, быть направленной на снижение риска осложнений. Применительно к ОП это означает снижение риска вертебральных и невертебральных переломов, включая переломы бедра, что ассоциируется со снижением смертности и инвалидности [6, 7]. Ответственность за выбор тактики ведения пациента с ОП в полной мере ложится на лечащего врача, который должен руководствоваться принятыми клиническими рекомендациями.
Основными фармакологическими средствами для профилактики и лечения постменопаузального ОП с доказанной клинической эффективностью на основании проведенных рандомизированных контролируемых исследований являются бисфосфонаты, стронция ранелат, деносумаб, селективные блокаторы эстрогеновых рецепторов, пептиды паратиреоидного гормона (последние две группы в России не зарегистрированы). Бисфосфонаты относятся к препаратам первой линии в лечении постменопаузального ОП. В России зарегистрированы препараты алендроната (Фосамакс, Фосаванс – оригинальные препараты; Осталон, Теванат, Фороза – воспроизведенные препараты), ибандроната (Бонвива – оригинальный препарат), золедроновой кислоты (Акласта – оригинальный препарат), ризедроната (Ризендрос – воспроизведенный препарат). Следует отметить, что бисфосфонаты производятся как для приема внутрь, так и для внутривенного введения (Бонвива 3 мг 1 раз в квартал, Акласта 5 мг 1 раз в год) (табл.). Некоторые бисфосфонаты (алендронат, ризедронат и золедроновая кислота) также могут применяться и для профилактики, и для лечения глюкокортикоидного ОП. Доказано, что бисфосфонаты, стронция ранелат и терипаратид эффективны при лечении ОП у мужчин. Все перечисленные препараты снижают риски вертебральных и невертебральных переломов в комбинации с препаратами кальция и витамина D.
Несмотря на некоторые различия в антипереломном эффекте этих препаратов, все они могут использоваться для предотвращения переломов. Достижение этой цели крайне важно, поскольку при возникновении низкоэнергетического перелома риск новых переломов возрастает независимо от МПК. Поскольку прямых сравнительных исследований антиостеопоротических препаратов, в которых конечной точкой являлись бы переломы, не проводилось, невозможно решить, какой из указанных препаратов обладает более мощным антипереломным эффектом.
Воспроизведенные препараты (дженерики) в лечении остеопороза
Появление на фармацевтическом рынке дженериков обусловлено значительным ростом расходов со стороны государства и страховых медицинских компаний на лекарственное обеспечение граждан. Известно, что рост заболеваемости, прежде всего, связан с постарением населения практически во всех странах мира. Люди старшего возраста страдают различными хроническими заболеваниями, среди которых преобладают сердечно-сосудистые, ревматические, метаболические и эндокринные болезни. Вместе с тем создание инновационных лекарственных средств на основе современных технологий, их экспериментальное и клиническое исследование требуют огромных затрат со стороны фармацевтических компаний. Таким образом, существуют две противоположные тенденции – увеличение стоимости новых высокоэффективных лекарств и стремление снизить затраты на лекарственное обеспечение.
Безусловно, определенным выходом из существующей ситуации является создание дженериков и замена брендовых препаратов на воспроизведенные в широкой клинической практике. В России требования к регистрации дженериков регламентируются следующими документами: 1) Федеральным законом «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ; 2) Национальным стандартом РФ «Надлежащая клиническая практика» (ГОСТ Р 52379-2005); 3) Методическими указаниями МЗСР «Оценка биоэквивалентности лекарственных средств» (2008). Проведение исследований биоэквивалентности считается обязательным для препаратов, назначаемых внутрь.
Оценка биоэквивалентности («фармакокинетической эквивалентности») лекарственных средств является основным видом медико-биологического контроля воспроизведенных (дженерических) лекарственных средств, не отличающихся лекарственной формой и содержанием действующих веществ от соответствующих оригинальных лекарственных средств. Исследования биоэквивалентности позволяют сделать обоснованные заключения о качестве сравниваемых препаратов по относительно меньшему объему первичной информации и в более сжатые сроки, чем при проведении клинических исследований, однако эти исследования не оценивают эффективность препарата при его длительном применении. Имеются также сведения о большем числе побочных эффектов среди дженериков по сравнению с оригинальными препаратами.
В ряде публикаций приводятся данные о том, что при замене оригинальных препаратов на дженерики можно сократить бюджет на лекарственное обеспечение примерно на 11%. Вместе с тем крупные фармацевтические компании, занимающиеся разработками новых препаратов, косвенно несут убытки, соответственно, это может сдерживать новые разработки [8].
В настоящее время на мировом фармацевтическом рынке наблюдается следующая тенденция – дженерики используются все шире, причем как врачами, так и при возмещении расходов на лекарственное обеспечение со стороны государства в лице страховых медицинских компаний. В некоторых исследованиях было показано, что два из трех рецептов, выписанных врачами общей практики, включали дженерики. Тем не менее довольно широко распространено мнение о том, что практикующие врачи по разным причинам предпочитают применять оригинальные лекарственные средства. Так, согласно данным литературных источников, большая часть врачей считают, что дженерики уступают по эффективности оригинальным препаратам. Это было подтверждено еще одним исследованием, в котором только 40% врачей, принявших участие в опросе, верили, что по своей терапевтической эффективности дженерики эквивалентны оригинальным препаратам. 36% врачей первичного звена здравоохранения согласились с утверждением о том, что отсутствие терапевтического эффекта является серьезной проблемой воспроизведенных препаратов [9]. Одной из причин этих сомнений может быть то, что фармацевтическая индустрия затрачивает около 7 млрд долларов США в год на продвижение брендов.
На импортируемые в Россию дженерики приходится около половины продающихся в стране лекарств и до 90% новых регистрируемых наименований препаратов [10]. Таким образом, доля дженерических препаратов на российском фармацевтическом рынке, по различным данным, может составлять от 78 до 95% (рис.). Вместе с тем рынок стран большой семерки сформировался следующим образом: в США – 12% дженериков, в Японии – 30%, в Германии – 35%, во Франции – 50%, в Англии – 55%, в Италии – 60%, в Канаде – 64% [11]. Подчеркнем: система здравоохранения требует замены дорогостоящих препаратов на более дешевые, при этом предполагается, что эффективность дженериков соответствует брендовым препаратам.
Различия между оригинальными и дженериковыми бисфосфонатами
В последние годы ситуация в сегменте средств для лечения остеопороза существенно изменилась. Во многом это связано с появлением дженериков алендроната, что повлияло на соотношение «стоимость – эффективность лечения», поскольку произошло снижение цены на препарат. В 2004 г. было проведено исследование, в котором изучалось соотношение «стоимость – эффективность» алендроната в 9 европейских странах [12]. Применение оригинального алендроната у пациенток с постменопаузальным ОП оказалось выгодным по сравнению с группой больных, не получавших лечения вообще. Причем анализ проводился как среди пациенток, имевших в анамнезе вертебральные переломы (группа высокого риска остеопоротических переломов), так и в группе без предшествующих переломов. Поскольку стоимость дженерика алендроната стала значительно ниже, то расчет параметра «стоимость – эффективность» следует провести по-новому. Однако при проведении подобных расчетов требуются данные не только о стоимости лечения, но и эффективности и переносимости того или иного препарата при его длительном применении.
Реалии сегодняшнего дня заключаются в том, что на фармацевтическом рынке многих стран Европы, а также России стали доминировать дженерики алендроната.
Как только дженерики алендроната оказались доступны для применения (с 2006 г.), в литературе начали появляться сообщения о том, что приверженность этим препаратам хуже в сравнении с оригинальными средствами. При этом нужно учитывать, что, по данным применения оригинальных препаратов, в целом приверженность пациентов с ОП к антиостеопоротическим препаратам снижается в течение первого года терапии, достигая лишь 50–66%. В настоящее время выявлен ряд причин низкой приверженности пациентов с ОП медикаментозной терапии. К ведущим факторам относят возраст пациентов, стоимость препарата, сложность дозирования и плохую переносимость. Побочные эффекты являются независимым фактором низкой приверженности лечению [13]. По результатам исследований, наиболее частым побочным эффектом антирезорбтивных препаратов являлось поражение желудочно-кишечного тракта (ЖКТ) в виде эзофагита, эрозий, гастрита, язвенной болезни (в 40,0–42,8% случаев) [14]. Мышечные боли наблюдались у 4,8% пациентов. Частота побочных эффектов при приеме алендроната колебалась в пределах 10–16%, в единичных исследованиях достигала 47,6% [15].
Таким образом, низкая приверженность пациентов лечению приводит к тому, что в реальной клинической практике эффективность лекарственных препаратов не достигает уровня, продемонстрированного в клинических исследованиях. Так, у пациентов с ОП, не соблюдавших рекомендации по приему лекарственного препарата, отмечался более высокий риск переломов, что сопровождалось бóльшими затратами на их лечение.
Аналогичные результаты были получены в канадском исследовании на основании анализа большой базы данных. Пациенты, которые начали принимать дженерик алендроната в еженедельном режиме, в 2 раза чаще отказывались от его использования в связи с развитием побочных явлений по сравнению с пациентами, получавшими оригинальный препарат [16].
В другой работе из Канады, представленной D.T. Grima и соавт. (2008), анализировалась ситуация, когда примерно 80% пациентов в июле 2005 г. без их оповещения были автоматически переведены с оригинального на воспроизведенный алендронат. В результате оказалось, что число пациентов/месяцев, получавших терапию оригинальным алендронатом 70 мг в неделю в 2003–2005 гг., было значительно выше, чем в 2006–2007 гг., когда пациенты стали получать в основном дженерики алендроната (20 492 против 9929). Всего был зарегистрирован 301 случай прекращения лечения из-за развития побочных реакций. Основной причиной прекращения антиостеопоротической терапии было развитие побочных эффектов со стороны ЖКТ. Чаще всего встречались гастралгии, расстройство пищеварения, тошнота, рефлюкс, изжога, вздутие живота, запоры. Вместе с тем были обнаружены различия в эффективности оригинального и воспроизведенного алендроната по показателю МПК. 7% пациентов (23 из 301) прекратили прием дженерика алендроната вследствие значительного снижения МПК, хотя во время приема оригинального препарата показатели МПК были стабильными [17].
В исследовании, выполненном J. Ringe и G. Moller (2009), показано, что при применении дженериков алендроната в течение 12 месяцев регистрировалась более низкая приверженность пациентов, темпы нарастания МПК были меньше, а частота побочных эффектов выше, чем при применении оригинальных препаратов алендроната и ризедроната [18].
Еще одним аргументом в пользу более высокой эффективности и лучшей переносимости оригинальных антиостеопоротических препаратов по сравнению с дженериками являются клинические исследования с продленной фазой. Длительные наблюдения за пациентами с ОП, получавшими алендронат внутрь в течение 10 лет [19], ризедронат в течение 7 лет [20], золедроновую кислоту внутривенно в течение 6 лет [21], показали, что оригинальные бисфосфонаты сохраняли свой антипереломный эффект при хорошей переносимости.
Аналогичные результаты были получены при оценке эффективности и безопасности длительного приема ибандроната в дозе 150 мг один раз в месяц. Основное двухлетнее исследование MOBILE (Monthly Oral iBandronate In LadiEs – Ежемесячный пероральный прием ибандроната у женщин) было продлено на 3 года – MOBILE LTE (long-term extension – долгосрочное продление) [22]. В исследование было включено 719 женщин (358 пациенток получали препарат в дозе 100 мг в месяц, 361 пациентка – 150 мг в месяц). В результате проведенного анализа динамики параметра МПК на фоне лечения были получены следующие данные: через 60 месяцев терапии отмечено достоверное повышение массы кости в поясничных позвонках (при использовании дозы 100 мг – на 8,2% (95% ДИ 7,2–9,2), 150 мг – на 8,4% (95% ДИ 7,5–9,4)). Повышение МПК в общем показателе бедренной кости наблюдалось через 12, 24 и 36 месяцев, после чего достигнуто плато, и показатели устойчиво сохранялись до 5-го года наблюдения. Через 60 месяцев повышение МПК составило соответственно 3,0% (95% ДИ 2,3–3,7) и 3,5% (95% ДИ 2,8–4,1). В обеих группах терапии динамика МПК в шейке бедра и большом вертеле имела те же тенденции, что и в общем показателе бедренной кости.
В текущем году опубликованы данные исследования DIVA LTE (Dosing IntraVenous Administration – long-term extension – Применение различных доз внутривенного введения ибандроната – продленная фаза) [23]. DIVA LTE является открытой фазой 2-летнего рандомизированного двойного слепого исследования III фазы. В него включались пациентки в постменопаузе, завершившие участие в исследовании DIVA, в котором проводилась сравнительная оценка эффективности ежедневного таблетированного и внутривенного ибандроната в дозе 2 и 3 мг (приверженность лечению ибандронатом в дозе 3 мг 1 раз в 3 месяца, вводимом внутривенно, за первые два года составила 75% и выше). Объединенный 5-летний анализ включил 497 пациенток. Анализ данных МПК позвоночника выявил продолжающееся увеличение показателей при использовании обеих доз ибандроната. К концу исследования было выявлено увеличение МПК данной локализации на 8,4% (95% ДИ 7,5–9,3) и 8,1% (95% ДИ 7,2–8,9) в группах лечения внутривенным ибандронатом с дозированием 2 и 3 мг соответственно. Увеличение общего показателя МПК в бедренной кости составилo 3,0% (95% ДИ 2,4–3,5) и 2,8% (95% ДИ 2,1–3,5) по сравнению с исходным уровнем исследования DIVA.
Таким образом, по всем оригинальным бисфосфонатам вне зависимости от способа назначения были завершены продленные исследования, доказавшие возможность их безопасного длительного применения при ОП.
Заключение
В связи с тем что внедрение дженериков в клиническую практику является объективным процессом, обусловленным желанием сократить государственные расходы на лекарственное обеспечение больных, требуется проведение проспективных сравнительных исследований, которые могли бы ответить на вопрос об их терапевтической эквивалентности оригинальным препаратам. Если по всем представленным на фармацевтическом рынке оригинальным бисфосфонатам проведены клинические исследования, показавшие их эффективность и безопасность при длительном применении, то аналогичные данные по дженерикам бисфосфонатов отсутствуют и вряд ли в ближайшие годы появятся. Руководствуясь статьей 74 Федерального закона Российской Федерации от 21.11.2011 № 323-ФЗ «Об основах охраны здоровья граждан в РФ», «медицинские работники и руководители медицинских организаций не вправе предоставлять при назначении курса лечения пациенту недостоверную, неполную или искаженную информацию об используемых лекарственных препаратах, о медицинских изделиях, в том числе скрывать сведения о наличии в обращении аналогичных лекарственных препаратов, медицинских изделий». Иными словами, данное положение обязывает лечащих врачей давать объективную информацию о назначаемом лекарственном препарате, основанную на результатах клинических исследований, которые легли в основу национальных клинических рекомендаций.
1. Melton L.J. 3rd. Who has osteoporosis? A conflict between clinical and public health perspectives // J. Bone Miner. Res. 2000. Vol. 15. No 12. P. 2309–2314.
2. Lips P. Epidemiology and predictors of fractures associated with osteo- porosis // Am. J. Med. 1997. Vol. 103. No 2A. P. 3S–8S.
3. Kanis J.A., Johnell O. Requirements for DXA for the management of os- teoporosis in Europe // Osteoporos. Int. 2005. Vol. 16. No 3. P. 229–238.
4. Руководство по остеопорозу / Под ред. Л.и. Беневоленской. М.: Бином. Лаборатория знаний, 2003. 524 с.
5. убкова И.И. Медико-социальные последствия остеопоротических переломов лучевой кости в типичном месте // Актуальные проблемы ревматологии: Материалы IX Северо-Западной научно- практической конференции по ревматологии. СПб., 2009. С. 37.
6. Delmas P.D. Treatment of postmenopausal osteoporosis // Lancet. 2002. Vol. 359. No 9322. P. 2018–2026.
7. Compston J., Cooper A., Cooper C. et al. Guidelines for the diagnosis and management of osteoporosis in postmenopausal women and men from the age of 50 years in the UK // Maturitas. 2009. Vol. 62. No 2. P. 105–108.
8. Haas J.S., Phillips K.A., Gerstenberger E.P. et al. Potential savings from sub- stituting generic drugs for brand-name drugs: medical expenditure panel survey, 1997–2000 // Ann. Intern. Med. 2005. Vol. 142. No 11. P. 891–897.
9. arrett L. Physicians’ attitudes and practices regarding generic drugs // AARP Knowledge Management, 2005. www.aarp.org/research.
10. Щербаков В. ВОЗ вмешивается в производство дженериков // Ремедиум. 2000. No 3. С. 57–60.
11. Perry G. The European generic pharmaceutical market review: 2006 and beyond // J. Generic Med. 2006. Vol. 4. P. 4–14.
12. Ström O., Borgström F., Sen S.S. et al. Cost-effectiveness of alendronate in the treatment of postmenopausal women in 9 European countries – an economic evaluation based on the fracture intervention trial // Os- teoporos. Int. 2007. Vol. 18. No 8. P. 1047–1061.
13. Badamgarav E., Fitzpatrick L.A. A new look at osteoporosis outcomes: the influence of treatment, compliance, persistence, and adherence // Mayo Clin. Proc. 2006. Vol. 81. No 8. P. 1009–1012.
14. Lanza F., Sahba B., Schwartz H. et al. The upper GI safety and tolerability of oral alendronate at a dose of 70 milligrams once weekly: a placebo-con- trolled endoscopy study // Am. J. Gastroenterol. 2002. Vol. 97. No 1. P. 58–64.
15. Liberman U.A., Weiss S.R., Bröll J. et al. Effect of oral alendronate on bone mineral density and the incidence of fractures in postmenopausal osteoporosis. The Alendronate Phase III Osteoporosis Treatment Study Group // N. Engl. J. Med. 1995. Vol. 333. No 22. P. 1437–1443.
16. Halkin H., Dushenat M., Silverman B. et al. Brand versus generic alen- dronate: gastrointestinal effects measured by resource utilization // Ann. Pharmacother. 2007. Vol. 41. No 1. P. 29–34.
17. Grima D.T., Papaioannou A., Thompson M.F. et al. Greater first year effectiveness drives favorable cost-effectiveness of brand risedronate versus generic or brand alendronate: modeled Canadian analysis // Osteoporos. Int. 2008. Vol. 19. No 5. P. 687–697.
18. Ringe J.D., Möller G. Differences in persistence, safety and efficacy of generic and original branded once weekly bisphosphonates in patients with postmenopausal osteoporosis: 1-year results of a retrospective patient chart review analysis // Rheumatol. Int. 2009. Vol. 30. No 2. P. 213–221.
19. Bone H.G., Hosking D., Devogelaer J.P. et al. Ten years' experience with alendronate for osteoporosis in postmenopausal women // N. Engl. J. Med. 2004. Vol. 350. No 12. P. 1189–1199.
20. Mellström D.D., Sörensen O.H., Goemaere S. et al. Seven years of treat- ment with risedronate in women with postmenopausal osteoporosis // Calcif. Tissue Int. 2004. Vol. 75. No 6. P. 462–468.
21. Black D.M., Reid I.R., Boonen S. et al. The effect of 3 versus 6 years of zoledronic acid treatment of osteoporosis: a randomized extension to the HORIZON-Pivotal Fracture Trial (PFT) // J. Bone Miner. Res. 2012. Vol. 27. No 2. P. 243–254
22. Miller P.D., Recker R.R., Reginster J.Y. et al. Efficacy of monthly oral ibandronate is sustained over 5 years: the MOBILE long-term exten- sion study // Osteoporos. Int. 2012. Vol. 23. No 6. P. 1747–1756
23. Bianchi G., Czerwinski E., Kenwright A. et al. Long-term administration of quarterly IV ibandronate is effective and well tolerated in postmeno- pausal osteoporosis: 5-year data from the DIVA study long-term exten- sion // Osteoporos. Int. 2012. Vol. 23. No 6. P. 1769–1778.
Новости на тему
27.07.2022 14:00:00
21.02.2022
Отправить статью по электронной почте
Ваш адрес электронной почты:
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.