Программа реабилитации иммунной системы пациентов с круглогодичным аллергическим ринитом, ассоциированным с повторными острыми респираторными и хроническими герпесвирусными инфекциями
- Аннотация
- Статья
- Ссылки
- English
В группу наблюдения отобраны 32 пациента в возрасте 18–60 лет, девять мужчин и 23 женщины, с различными фенотипами АР, повторными острыми респираторно-вирусными заболеваниями (ОРВИ) и ХГВИ. В ходе комплексного аллергологического и иммунологического обследования выявлены нарушения в иммунной системе и системе ИФН. Разработана программа комбинированной интерфероно- и иммунотерапии. В дополнение к стандартной базисной терапии АР (антигистаминные препараты второго поколения и топические глюкокортикостероиды интраназально) пациенты получали локальную и системную интерферонотерапию рекомбинантным ИФН-α2β в комплексе с антиоксидантами (гель для локальной и суппозитории для системной терапии ИФН) и иммуномодулирующую терапию глюкозаминилмурамилдипептидом, действие которой было направлено на нормализацию регуляторного дисбаланса иммунной системы. Разработанная программа комбинированной интерфероно- и иммунотерапии имела подтвержденную позитивную клиническую эффективность.
В группу наблюдения отобраны 32 пациента в возрасте 18–60 лет, девять мужчин и 23 женщины, с различными фенотипами АР, повторными острыми респираторно-вирусными заболеваниями (ОРВИ) и ХГВИ. В ходе комплексного аллергологического и иммунологического обследования выявлены нарушения в иммунной системе и системе ИФН. Разработана программа комбинированной интерфероно- и иммунотерапии. В дополнение к стандартной базисной терапии АР (антигистаминные препараты второго поколения и топические глюкокортикостероиды интраназально) пациенты получали локальную и системную интерферонотерапию рекомбинантным ИФН-α2β в комплексе с антиоксидантами (гель для локальной и суппозитории для системной терапии ИФН) и иммуномодулирующую терапию глюкозаминилмурамилдипептидом, действие которой было направлено на нормализацию регуляторного дисбаланса иммунной системы. Разработанная программа комбинированной интерфероно- и иммунотерапии имела подтвержденную позитивную клиническую эффективность.

Введение
Аллергический ринит (АР) не является жизнеугрожающей патологией, но в то же время имеет огромное социальное значение, связанное с его высокой распространенностью среди населения различных стран мира – от 35 до 55%. АР ухудшает качество жизни пациентов, нарушает их привычную активность, качество сна, требует ежегодно больших экономических затрат в системе здравоохранения во всем мире [1]. Кроме того, регистрируются ежегодный рост заболеваемости АР, утяжеление его течения, отмечено значительное расширение спектра сенсибилизации. Подтверждена тесная связь с развитием других аллергических заболеваний, в частности бронхиальной астмы, наблюдается частое присоединение инфекционных осложнений со стороны ЛОР-органов (хронические риносинуситы, евстахииты, отиты и др.) [2–5].
В физиологических условиях благодаря тесному взаимодействию неспецифических и специфических механизмов иммунной защиты обеспечивается поддержание мукозального иммунитета. У пациентов с АР развивается неспецифическая тканевая гиперреактивность вследствие сосудистых и рефлекторных нарушений, снижения чувствительности рецепторов к различным триггерам и медиаторам, изменениям тканевой микроциркуляции. При этом на фоне развития преимущественного Th2-иммунного ответа происходит повышение продукции различных противовоспалительных цитокинов (интерлейкина-4 (ИЛ-4), ИЛ-13, ИЛ-5, ИЛ-10), что впоследствии приводит к индукции синтеза антител-реагинов класса IgE и гиперпродукции IgE, привлечению эозинофилов в зону аллергического воспаления, снижению количества Т-регуляторных клеток. На этом фоне нарушаются индуцированная продукция интерферона (ИФН) первого и второго типов, выработка секреторного IgA, что приводит к снижению противовирусной иммунной защиты организма [2, 6, 7].
Благодаря современной классификации АР, основанной на выделении его различных фенотипов и эндотипов с учетом временных паттернов, тяжести и длительности заболевания, преобладающих симптомов, возможности контроля заболевания, а также выявления пускового фактора и определения наличия коморбидной патологии стало возможным применение персонифицированного подхода к лечению АР [6, 8, 9].
В диагностике АР ведущую роль играет сбор анамнеза с установлением фенотипа/эндотипа ринита, оценкой тяжести течения заболевания, использованием анкет и шкал. Лабораторное исследование включает цитологическое исследование назального секрета, определение уровня общего IgE, уровня эозинофилов периферической крови и назального секрета, уточнение уровня причинно-значимых специфических IgE-антител, проведение кожных скарификационных тестов. В основе прецизионной терапии с учетом гетерогенности фенотипов АР лежит необходимость индивидуального подхода с разработкой плана лечения на основе доминирующего симптома, наличия сопутствующих заболеваний, эндотипа воспаления. Алгоритм терапии зависит от тяжести симптомов [2, 3, 8, 9]. Лечение АР требует назначения антигистаминных препаратов второго поколения, топических глюкокортикостероидов (ГКС), также применяются препараты кромоглициевой кислоты, антагонисты лейкотриеновых рецепторов, назальные деконгестанты. При тяжелом неконтролируемом течении АР рекомендовано проведение биологической терапии моноклональными антителами. При достижении ремиссии заболевания необходимо рассмотреть возможность проведения аллергенспецифической иммунотерапии (АСИТ). Антигистаминные препараты второго поколения могут применяться как для системного, так и для топического лечения, возможно применение ингаляционных форм комбинированных препаратов Н1-блокаторов и топических ГКС [2, 4, 6]. Особенности патогенеза АР способствуют более быстрому проникновению патогена и снижению эффективности проводимой противоинфекционной терапии. Также известно, что респираторные вирусы обладают тропностью к клеткам слизистых оболочек респираторного тракта, что у пациентов с круглогодичным аллергическим ринитом (КАР) приводит к усугублению уже имеющихся нарушений мукозального иммунитета, снижению функции цилиарного эпителия, нарушению естественного дренажа слизи из околоносовых пазух носа и увеличению количества обострений АР [10, 11]. Наряду с этим ускоряется дифференцировка В-клеток в плазматические IgE-продуцирующие клетки, это приводит к дальнейшему обострению аллергического ринита, прогрессированию нарушений в иммунной системе, в том числе функционирования нейтрофильных гранулоцитов, фагоцитоза [7, 10–13]. Установлено, что сами вирусы способны оказывать негативное воздействие на иммунную систему, обладают способностью ускользать от внимания иммунной системы посредством возможности смены иммунодоминантных мишеней в вирусных белках, смены антигена, а также повреждать и приводить к истощению системы ИФН. Благодаря этому некоторые вирусы способны к длительной персистенции в организме [14, 15]. Герпесвирусы, блокируя активацию Toll-подобных рецепторов (TLR3), приводят к нарушению продукции ИФН-α, ИФН-γ. С учетом уже имеющихся нарушений в работе иммунной системы под ингибирующим действием персистирующих вирусных инфекций прогрессирует нарушение неспецифической и специфической иммунной защиты [3, 12–14]. Вследствие выявления комбинированных нарушений в работе системы ИФН и иммунной системы у пациентов с КАР, страдающих повторными острыми респираторно-вирусными заболеваниями (ОРВИ), частыми обострениями герпесвирусных инфекций, становится очевидной необходимость разработки программ комплексного лечения таких пациентов с иммунопатогенетически обоснованной ИФН- и иммунотерапией, что, с нашей точки зрения, является весьма актуальной проблемой.
Цель исследования – на базе проведения клинико-иммунологического исследования разработать и оценить клиническую эффективность программы комплексного лечения, включающего иммунопатогенетически обоснованную интерфероно- и иммунотерапию, для пациентов с КАР и коморбидными заболеваниями: повторные ОРВИ и хронические герпесвирусные инфекции.
Материал и методы
Под нашим наблюдением находились 32 пациента в возрасте от 18 до 60 лет, из них девять мужчин и 23 женщины, страдающие КАР, часто повторяющимися ОРВИ и хроническими герпесвирусными инфекциями (ХГВИ). Проведено клинико-анамнестическое исследование: выполнены анализ амбулаторных карт, сбор анамнеза и жалоб, физикальное обследование. При лабораторном аллергологическом исследовании методом иммуноферментного анализа уточнили уровень сывороточного общего IgE, методами ELISA или Immunocap – спектр специфических причинно-значимых аллергенов, уровень эозинофильного катионного белка. Для детекции вируса Эпштейна – Барр (ВЭБ), вируса простого герпеса первого типа (ВПГ1), ВПГ второго типа (ВПГ2), вируса герпеса человека шестого типа (ВГЧ6), цитомегаловируса (ЦМВ) использованы методы серодиагностики – иммуноферментный анализ, метод полимеразной цепной реакции в реальном времени для диагностики герпесвирусных инфекций в различных биоматериалах (кровь, соскоб с миндалин, слюна и т.д.). Для оценки особенностей функционирования иммунной системы методом проточной цитометрии исследовали: CD3+, CD3+CD4+, CD3+CD8+ T-лимфоциты, естественные киллерные клетки (ЕКК) CD3-CD16+CD56+, количество нейтрофилов, выполнено исследование ИФН-статуса с оценкой индуцированной продукции ИФН-α и ИФН-γ. Оценивали клинические критерии, характеризующие особенности вирусных инфекций: количество повторных ОРВИ в год, количество обострений ВПГ1- и ВПГ2-инфекций в год, особенности репликативной активности ВЭБ, ВГЧ6, ЦМВ. Оценку выраженности симптомов КАР проводили по 10-балльной визуальной аналоговой шкале (ВАШ). Ранее все пациенты с КАР получали стандартную противоаллергическую терапию системными антигистаминными препаратами второго поколения, топическими ГКС, при этом полного контроля с достижением клинической эффективности достичь не удавалось, а проведение АСИТ было невозможным из-за частых повторных ОРВИ и/или обострений ХГВИ.
Статистическую обработку результатов исследования проводили с использованием компьютерных программ StatPlus (версия 17.0 для Windows). В ходе анализа полученных данных оценивали правильность распределения выборки. Использовали методы непараметрической статистики: результаты представляли в виде медианы (Ме) и интерквартильного размаха (Q1; Q3). Для установления значимости различий между количественными показателями независимых групп (исследуемые группы, группа сравнения) использовали непараметрический U-критерий Манна – Уитни. Различия определяли статистически значимыми при p < 0,05.
Результаты и обсуждение
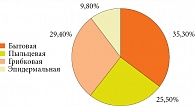
Установлено, что в 81,25% случаев у наблюдаемых пациентов преобладал фенотип КАР, при этом лишь в 18,75% КАР сочетался с сезонным АР. Выполнен анализ тяжести АР по 10-балльной ВАШ с оценкой таких симптомов, как заложенность носа, зуд в носу, насморк, чихание, ринорея и т.д. Оценка по ВАШ составила 4,0 (4,0; 6,5). Длительность заболевания КАР составляла более трех лет. У всех пациентов группы наблюдения подтверждена сенсибилизация к бытовым, и/или грибковым, и/или эпидермальным аллергенам методами ELISA, Immunocap. В структуре установленной сенсибилизации бытовая группа аллергенов составила 35,3%, грибковая – 29,4%, пыльцевая – 25,5%, к эпидермальным аллергенам – 9,8% (рис. 1).
У 37,5% пациентов группы исследования имела место упорно рецидивирующая ХГВИ, вызываемая ВПГ1 и/или ВПГ2, 25% пациентов страдали упорно рецидивирующими ХГВИ, вызванными ВПГ1 и/или ВПГ2, в сочетании с повторными ОРВИ, у 37,5% пациентов наблюдались повторные ОРВИ, ассоциированные с ВЭБ и ВГЧ6 в стадии репликативной активности. Частота эпизодов обострения упорно рецидивирующх ХГВИ, вызываемых ВПГ1 и/или ВПГ2, составляла 14,5 (Q1 9,75; Q3 19,25) раз в год, частота повторных ОРВИ – 8,0 (Q1 6,00; Q3 10,00) в год.
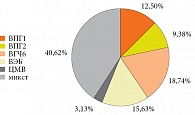
Частота встречаемости различных герпесвирусных инфекций у пациентов с КАР была следующей: ВПГ1 встречался в 12,5% случаев, ВПГ2 – в 9,38%, ВГЧ6 – в 18,74%, ВЭБ – в 15,68%, ЦМВ – в 3,13%, при этом лидирующую позицию занимали микст-ХГВИ, достигая 40,62% (рис. 2).
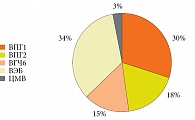
В структуре микст-герпесвирусных инфекций у пациентов с КАР в 33,3% случаев обнаружена ВЭБ-инфекция, в 30,3% – ВПГ1, 18,2% – ВПГ2, в 15,2% – ВГЧ6, в 3,0% – ЦМВ (рис. 3).
Исследование состояния интерферонового статуса у пациентов с КАР и различными вирусными инфекциями выявило нарушение индуцированной продукции ИФН-α второй-третьей степени у 57,88% пациентов в числе моно- и комбинированных иммунодефицитов (ИД). В 57,9% случаев выявлена относительная нейтропения, количество нейтрофильных гранулоцитов было снижено до 40,75 (Q1 37,22; Q3 42,67), у 42,09% пациентов выявлено снижение относительного количества Т-цитотоксических лимфоцитов CD3+CD8+ до 15,10 (Q1 14,20; Q3 16,30), дефицит ЕКК CD3-CD16+CD56+ – 0,099 (Q1 0,068; Q3 0,127) в 21,04% случаев, в числе моно- и комбинированных нарушений. Моно-ИД выявлены у 47,39% пациентов, при этом нейтропении имели место в 31,6% случаев, а нарушение индуцированной продукции ИФН-α – в 15,79% случаев от общего числа нарушений иммунной системы.
Комбинированные ИД выявлены у 51,62% пациентов, при этом были систематизированы разные комбинации нарушений иммунной системы:
- дефицит CD3+CD8+ Т-лимфоцитов + дефицит индуцированной продукции ИФН-α имели место у 15,79% пациентов;
- нейтропения + дефицит индуцированной продукции ИФН-α – у 10,52% пациентов;
- нейтропения + дефицит CD3+CD8+ Т-лимфоцитов + дефицит ЕКК + дефицит ИФН-α – у 10,52% пациентов;
- дефицит CD3+CD8+ Т-лимфоцитов + дефицит ЕКК + дефицит ИФН-α – у 5,26% пациентов;
- дефицит CD3+CD8+ Т-лимфоцитов + дефицит ЕКК – у 5,26% пациентов;
- дефицит CD3+CD8+ Т-лимфоцитов + нейтропения – у 5,26% пациентов.
Все пациенты, страдающие КАР, повторными ОРВИ и ХГВИ, до включения в группу исследования были консультированы отоларингологом и инфекционистом, прошли комплексное оториноларингологическое обследование, включающее риноскопию, исследование соскоба со слизистых носа и зева на бактериальную флору, при необходимости им была проведена санация очагов хронической бактериальной инфекции ЛОР-органов. Во время лечения упорно рецидивирующих хронических герпесвирусных инфекций пациенты получали короткие и пролонгированные курсы синтетических противовирусных препаратов (ацикловир, валацикловир или фамцикловир) в соответствии со стандартами лечения. Однако проведенная терапия не способствовала снижению частоты повторных ОРВИ и обострений упорно рецидивирующих хронических герпесвирусных инфекций, при этом не было достигнуто и позитивной клинической эффективности в лечении КАР.
С учетом сохраняющихся симптомов КАР у пациентов группы исследования, получавших классическую противоаллергическую терапию, которые часто усугублялись на фоне повторных эпизодов ОРВИ и обострений ХГВИ, с учетом выявленных при проведении иммунологического исследования дефектов функционирования основных механизмов противовирусной защиты нами разработана комплексная программа комбинированной локальной и системной интерфероно- и иммунотерапии с целью достижения лучшего контроля за течением КАР, снижения частоты повторных ОРВИ и рецидивирующих обострений ХГВИ. Всем пациентам было продолжено проведение стандартной терапии КАР с использованием антигистаминных препаратов и топических ГКС, при этом во время проведения программы интерфероно- и иммунотерапии коррекцию противоаллергической терапии КАР не проводили. При обострении ВПГ1 или ВПГ2 назначали короткий курс синтетических противовирусных препаратов (валацикловир) 1000 мг в сутки в течение 10 дней.
Разработанная программа интерфероно- и иммунотерапии включала: с целью коррекции интерферонового статуса пролонгированную локальную (гель) и системную (суппозитории) терапию рекомбинантным ИФН-α2b в комплексе с антиоксидантами и иммунотерапию глюкозаминилмурамилдипептидом (ГМДП), действие которого было направлено на восстановление уровня нейтрофильных гранулоцитов, цитотоксических Т-лимфоцитов и ЕКК. Рекомбинантный ИФН-α2b в комплексе с антиоксидантами назначался в дозе 3 млн МЕ ежедневно в течение одного месяца, далее дозы препарата градуированно снижали каждые три недели вплоть до полной отмены, курс интерферонотерапии составил 3,5 месяца. Суточная доза ГМДП составляла 3 мг в сутки, сублингвально, три приема в день равными дозами, проведено три 10-дневных курса один раз в месяц в течение трех месяцев.
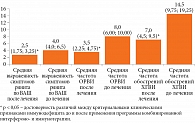
По завершении курса программной интерфероно- и иммунотерапии нами проведена оценка выраженности клинических симптомов КАР, частоты повторных ОРВИ в год и частоты рецидивирования ВПГ1 и ВПГ2 герпесвирусных инфекций в год. В соответствии с используемыми нами клиническими критериями установлено, что выраженность симптомов ринита по ВАШ достоверно снизилась после проведения комбинированной интерфероно- и иммунотерапии с 4,0 (4,0; 6,5) до 2,5 (1,75; 3,25) (р < 0,05), частота повторных ОРВИ в год достоверно уменьшилась с 8,0 (6,00; 10,00) до 3,5 (2,25; 4,75) (р < 0,05), кроме того, отмечено статистически значимое снижение частоты обострений упорно рецидивирующих ВПГ1 и ВПГ2 ХГВИ в год с 14,5 (9,75; 19,25) до 7,0 (4,5; 9,5) (р < 0,05) (рис. 4, таблица).
Обсуждение
Полученные нами данные позволяют прийти к заключению, что частые повторные ОРВИ и упорно рецидивирующие ХГВИ у пациентов, страдающих АР, ассоциированы с моно- и комбинированными нарушениями в иммунной системе. Эти нарушения способствуют возникновению частых повторных ОРВИ, ХГВИ, а их острые эпизоды отягощают течение АР. Так, у всех пациентов были выявлены или моно-, или комбинированные нарушения различных клеток врожденного и/или адаптивного иммунитета, участвующих в противовирусной защите, а также нарушение первой, очень важной линии противовирусной защиты – интерферонового статуса, поскольку был выявлен дефицит индуцированной продукции ИФН-α у преобладающего числа пациентов. В той или иной степени в числе моно- и комбинированных ИД выявлено нарушение индуцированной продукции ИФН-α второй-третьей степени у 57,88% пациентов, нейтропения – в 57,9% случаев, дефицит количества CD3+CD8+ Т-лимфоцитов с выраженными специфическими цитотоксическими свойствами – у 42,09% пациентов, дефицит клеток врожденного иммунитета ЕКК CD3-CD16+CD56+, обладающих неспецифическими цитотоксическими возможностями по уничтожению клеток инфицированных любыми вирусами, – в 21,04% случаев.
Разработанная программа интерфероно- и иммунотерапии, включающая пролонгированную локальную (гель) и системную (суппозитории) терапию рекомбинантным ИФН-α2b в комплексе с антиоксидантами (Виферон), а также иммунотерапию ГМДП (Ликопид), действие которых было направлено на восстановление системы интерферонов, количества и функциональной активности клеток иммунной системы, обладающих выраженными противовирусными цитотоксическими свойствами, продемонстрировала позитивные клинические эффекты. Так, в 1,6 раза достоверно снизилась выраженность симптомов КАР по шкале ВАШ на фоне значительного уменьшения количества эпизодов повторных ОРВИ в год – в 2,3 раза, статистически значимого (более чем в 2 раза) снижения частоты обострений упорно рецидивирующих ВПГ1 и ВПГ2 ХГВИ в год. Таким образом, уменьшение вирусной нагрузки на слизистую носовых ходов и снижение агрессивного влияния респираторных и герпетических вирусов на иммунную систему, произошедшее за счет восстановления иммунной противовирусной защиты, способствовали выраженной регрессии симптомов КАР, о чем свидетельствовало снижение баллов по шкале ВАШ.
В целом полученные данные свидетельствуют о выраженной клинической эффективности разработанной нами программы интерфероно- и иммунотерапии в комплексном лечении пациентов с КАР, ассоциированным с частыми эпизодами повторных ОРВИ, упорно рецидивирующими ВПГ1 и ВПГ2 герпесвирусными инфекциями и хроническими активными ВЭБ, ЦМВ, ВГЧ6 герпесвирусными инфекциями в стадии репликации вируса. Проведение комбинированной интерфероно- и иммунотерапии позволило достичь контроля над симптомами КАР, значительно снизить частоту повторных ОРВИ и уменьшить количество рецидивов ХГВИ, вызванных ВПГ1 и ВПГ. Результаты данного исследования демонстрируют необходимость совершенствования тактики персонифицированных подходов к лечению сложных коморбидных пациентов с КАР и сопутствующими респираторными и герпесвирусными инфекциями с дальнейшим совершенствованием индивидуализированных программ реабилитации иммунной системы.
Выводы
- Сопутствующие повторные эпизоды ОРВИ, упорно рецидивирующие ХГВИ, вызванные ВПГ1 и ВПГ, активные ВЭБ, ВГЧ6, ЦМВ герпесвирусные инфекции в стадии репликации вируса отягощают течение КАР.
- Сложные коморбидные пациенты с КАР и сопутствующими частыми повторными эпизодами ОРВИ, упорно рецидивирующими ХГВИ, вызванными ВПГ1 и ВПГ2 и активными ВЭБ, ВГЧ6, ЦМВ герпесвирусными инфекциями, имеют моно- или комбинированный иммунодефицит: дефект индуцированной продукции ИФН-α, и/или дефицит цитотоксических Т-лимфоцитов CD3+CD8+ и/или естественных киллерных клеток CD3-CD16+CD56+, и/или нейтропению – активных участников противовирусной иммунной защиты.
- Разработанная программа комбинированной интерфероно- и иммунотерапии с использованием рекомбинантного ИФН-α2b в комбинации с антиоксидантами (препарат Виферон) и ГМДП (препарат Ликопид), направленная на восстановление системы интерферонов и противовирусной иммунной защиты, продемонстрировала высокую клиническую эффективность: достигнуто улучшение контроля за течением КАР на фоне достоверного снижения количества повторных эпизодов ОРВИ в год, частоты упорно рецидивирующих ХГВИ, вызванных ВПГ1 и ВПГ2, и регрессии репликативной активности ВЭБ, ВГЧ6, ЦМВ герпесвирусных инфекций.
N.V. Garskova, E.O. Khalturina, PhD, T.P. Markova, PhD, Prof.
Academy of Postgraduate Education, Moscow
I.M. Sechenov First Moscow State Medical University
The MEDSI Academy, Department of Clinical Immunology and Allergology. Clinical and diagnostic center MEDSI on Belorusskaya, Moscow
Contact person: Natalya V. Garskova, garskova@bk.ru
Currently, allergic rhinitis (AR) is one of the most commonly detected allergic diseases with an annual increase in the number of patients, a heavier current, and a decrease in drug control. Allergic rhinitis – IgE-dependent chronic inflammation of the nasal mucosa, arising in response to contact with an allergen, against the background of disruption of the balance of T-helper cells of type 1 and 2 of activation of the Th2-dependent immune response, decrease in T-regulatory cell activity, change in cytokine profile, decrease in the production of IFN type I and II, secretory IgA and subsequent violation in the work of mucosal immunity of the mucous membranes of the respiratory tract. All these factors lead to an increased risk of recurrent respiratory diseases and exacerbations of chronic herpes viral infections (ChHVI). In this regard, the problem remains relevant: the development of a comprehensive program for the treatment of such patients, which served as the aim of our study.
The study group included 32 patients, aged 18–60 years, 9 men, 23 women, with different phenotypes of AR, recurrent ARVI and chronic herpes virus infections. Disorders in the immune system (IC) and interferon system (IFN) were detected on the basis of a comprehensive allergological and immunological study. A program of combined interferon and immunotherapy has been developed. In addition to standard base therapy for AR (2nd generation antihistamines and topical GCS intranasally), patients received local and systemic interferon therapy with recombinant IFN-α2β in complex with antioxidants (local and suppository gel for systemic IFN therapy) and immunomodulatory glucosaminylmuramyldipeptide (GMDP) therapy. The developed program of combined interferono- and immunotherapy had confirmed positive clinical efficacy.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.