Радиоизотопная визуализация медиастинальных форм B-клеточной лимфомы и дифференциальная диагностика патологически измененных участков прилежащей легочной паренхимы методами ПЭТ/КТ с 18F-ФДГ и ОФЭКТ/КТ с 99mТс-MIBI
- Аннотация
- Статья
- Ссылки
- English
Цель исследования – сравнить диагностические возможности визуализации медиастинальных форм лимфом по данным позитронно-эмиссионной и компьютерной томографии (ПЭТ/КТ) с применением 18F-фтордезоксиглюкозы (18F-ФДГ) и однофотонной эмиссионной компьютерной томографии, совмещенной с рентгеновской компьютерной томографией (ОФЭКТ/КТ), с 99mТс-MIBI, их роль в дифференциальной диагностике патологически измененных участков прилежащей легочной паренхимы.
Материал и методы. Проведен ретроспективный анализ радионуклидных исследований четырех пациентов с медиастинальной формой диффузной В-клеточной лимфомы высокой степени злокачественности с наличием зон легочной консолидации в прикорневых областях легких. Всем пациентам проводились ПЭТ/КТ с 18F-ФДГ и ОФЭКТ/КТ с 99mТс-MIBI.
Результаты. При проведении настоящего исследования выявлено, что ОФЭКТ/КТ с 99mТс-MIBI и ПЭТ/КТ с 18F-ФДГ имеют сопоставимую чувствительность в диагностической оценке пациентов с медиастинальными лимфомами. Однако поглощение 18F-ФДГ опухолевыми лимфоидными тканями было значительно выше по сравнению с накоплением 99mТс-MIBI, а выявленные очаги отчетливо дифференцировались от прилежащих тканей средостения и легких.
Заключение. ОФЭКТ с 99mТс-MIBI может быть полезна в обнаружении, дифференциальной диагностике медиастинальных лимфом, а также может рассматриваться как альтернатива, когда проведение ПЭТ невозможно. Однако лучшая визуализация метаболической активности образования имеет большее прогностическое значение, например, в оценке динамики химиотерапевтического лечения.
Цель исследования – сравнить диагностические возможности визуализации медиастинальных форм лимфом по данным позитронно-эмиссионной и компьютерной томографии (ПЭТ/КТ) с применением 18F-фтордезоксиглюкозы (18F-ФДГ) и однофотонной эмиссионной компьютерной томографии, совмещенной с рентгеновской компьютерной томографией (ОФЭКТ/КТ), с 99mТс-MIBI, их роль в дифференциальной диагностике патологически измененных участков прилежащей легочной паренхимы.
Материал и методы. Проведен ретроспективный анализ радионуклидных исследований четырех пациентов с медиастинальной формой диффузной В-клеточной лимфомы высокой степени злокачественности с наличием зон легочной консолидации в прикорневых областях легких. Всем пациентам проводились ПЭТ/КТ с 18F-ФДГ и ОФЭКТ/КТ с 99mТс-MIBI.
Результаты. При проведении настоящего исследования выявлено, что ОФЭКТ/КТ с 99mТс-MIBI и ПЭТ/КТ с 18F-ФДГ имеют сопоставимую чувствительность в диагностической оценке пациентов с медиастинальными лимфомами. Однако поглощение 18F-ФДГ опухолевыми лимфоидными тканями было значительно выше по сравнению с накоплением 99mТс-MIBI, а выявленные очаги отчетливо дифференцировались от прилежащих тканей средостения и легких.
Заключение. ОФЭКТ с 99mТс-MIBI может быть полезна в обнаружении, дифференциальной диагностике медиастинальных лимфом, а также может рассматриваться как альтернатива, когда проведение ПЭТ невозможно. Однако лучшая визуализация метаболической активности образования имеет большее прогностическое значение, например, в оценке динамики химиотерапевтического лечения.

Введение
В 2020 г. в мире было зарегистрировано 545 000 новых случаев и 260 000 смертей от неходжкинской лимфомы [1]. Неходжинские лимфомы занимают 11-е место среди наиболее часто диагностируемых видов рака и 11-е место по смертности от онкологических заболеваний в 2020 г. [2]. В последние десятилетия темпы роста заболеваемости и смертности ускорились. По прогнозам, к 2040 г. число случаев заболевания неходжкинскими лимфомами возрастет примерно до 778 000 [3]. В Российской Федерации с 2012 по 2020 г. смертность от всех злокачественных новообразований лимфатической и кроветворной ткани выросла на 16%. На их долю приходится 5% регистрируемых в течение года опухолей у мужчин и 4,6% – у женщин. Эти заболевания являются причиной около 5% случаев смерти от злокачественных новообразований [4–7]. На долю неходжкинских лимфом приходится 60% от всех лимфом, самыми частыми ее вариантами являются крупноклеточная В лимфома и В-клеточная фолликулярная лимфома, встречающиеся в этой группе в 33 и 22% случаев соответственно [8]. До внедрения в широкую практику радиоизотопных методов диагностики стадирование лимфом, как правило, осуществлялось на основании результатов клинического исследования, данных компьютерной томографии и пункционной биопсии. При этом диагностические возможности компьютерной томографии ограничены при визуализации лимфатических узлов нормальных размеров. Более того, при увеличении лимфатических узлов до 2 см вероятность специфического поражения составляет всего 50%, а увеличение более 3 см почти в 25% случаев связано с их доброкачественной гиперплазией [9]. Экстранодальные формы лимфом с поражением легочной ткани могут имитировать такие лучевые признаки воспалительных состояний легкого, как изменения по типу «матового стекла», зоны консолидации, перибронхиальные наложения, выпот в плевральной полости, возникающий либо в результате прямого поражения, либо в результате лимфатической обструкции, исходящей из лимфатических узлов, что в свою очередь также затрудняет диагностику. Появление в повседневной клинической практике современных неинвазивных радионуклидных методов диагностики, таких как однофотонная эмиссионная компьютерная томография, совмещенная с рентгеновской компьютерной томографией (ОФЭКТ), и позитронно-эмиссионная томография (ПЭТ), позволяющих одновременно выявить как патофизиологические, так и рентгеноморфологические нарушения, привело к существенному увеличению выявляемости и повышению точности стадирования неопластических процессов у большинства онкологических пациентов, а многочисленные исследования указывают на целесообразность использования методов ядерной медицины для определения степени распространенности лимфопролиферативных заболеваний, оценки эффективности проводимого лечения, определения показаний к лучевой терапии и подтверждают прогностическое значение их применения [8, 10–13]. Однако повсеместное использование позитронно-эмиссионной и компьютерной томографии (ПЭТ/КТ) ограничено высокой стоимостью исследования и недостаточным количеством ПЭТ-центров. Вместе с тем возможности использования ОФЭКТ/КТ в клинической онкологии, в отличие от ПЭТ/КТ, изучены значительно хуже, и это при том, что в целом оснащенность аппаратами ОФЭКТ и ОФЭКТ/КТ существенно выше. Так, на 2015 г. в Российской Федерации находилось 54 ПЭТ-сканера, тогда как количество гамма-камер ОФЭКТ, ОФЭКТ/КТ составляло 282 [14, 15].
Материал и методы
В данной работе были проанализированы исследования четырех пациентов медиастинальной формой диффузной В-клеточной лимфомы высокой степени злокачественности. Всем пациентам проводились исследования в режиме позитронно-эмиссионной томографии с использованием радиофармпрепарата (РФП) 18F-ФДГ и ОФЭКТ/КТ с применением 99mТс-MIBI. ПЭТ/КТ-сканирование с 18F-ФДГ проводилось в режиме Whole Body спустя 60–90 минут после введения РФП в дозе 370–480 МБк. При анализе полученных изображений визуально оценивалась интенсивность накопления РФП по цветовым шкалам, а также осуществлялся полуколичественный подсчет стандартизированного уровня накопления РФП – SUVmax. Зоной интереса являлась сферическая область диаметром 1,0 см, расположенная в наиболее активной части образования. При проведении ОФЭКТ/КТ с 99mТс-MIBI радиофармпрепарат вводился в количестве 700 МБк. Спустя 20 минут после введения пациентам проводилось исследование в режиме однофотонной эмиссионной компьютерной томографии на гибридном аппарате по циркулярной орбите в 128 проекциях с экспозицией 30 секунд в матрице 128 × 128 с последующей бесконтрастной мультиспиральной компьютерной томографией грудной клетки. Для полуколичественной оценки уровня накопления РФП в патологическом очаге выбирались две зоны интереса сферической формы диаметром 1,0 см. Первая зона интереса соответствовала наиболее активной части объемного образования, а вторая отмечалась на симметричном участке неизмененной паренхимы легкого. Измеряли число зарегистрированных фотонов в зонах интереса (counts) и рассчитывали количественный показатель аккумуляции РФП в патологическом очаге, выраженный в процентах. Компьютерная томография проводилась с использованием 16-срезового компьютерного томографа. Параметры сканирования органов грудной клетки: напряжение на трубке 120 кВ, ток в трубке 200 мА, толщина среза 1,25 мм. Исследования выполнялись при положении пациента лежа на спине с запрокинутыми кверху руками. Полученные данные радиоизотопных исследований и компьютерной томографии совмещались и анализировались в аксиальных, коронарных и сагиттальных проекциях. На полученных срезах визуально оценивались характер накопления и распределения РФП, локализация и размеры очагов гиперфиксации при их наличии.
Результаты и обсуждение
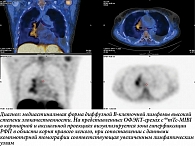
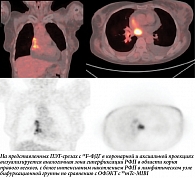
ОФЭКТ/КТ с 99mТс-MIBI активно используется в кардиологии, эндокринологии, но ее роль в ядерной онкологии точно не установлена. В этом исследовании мы сравнили результаты ОФЭКТ/КТ с 99mТс-MIBI и ПЭТ/КТ с 18F-ФДГ у четырех пациентов с гистологически верифицированной медиастинальной формой диффузной В-клеточной лимфомы. Был произведен количественный анализ ОФЭКТ- и ПЭТ-изображений в областях интереса (рис. 1, 2). Количественную оценку степени накопления радиофармпрепарата проводили путем расчета соотношения аккумуляции в патологическом очаге и здоровой ткани, их значения представлены в таблице.
Исходя из полученных данных, диагностическая чувствительность визуализации обоих методик в представленных случаях составила 100%. Однако количественный анализ аккумуляции 99mТс-MIBI и 18F-ФДГ в зонах интереса показал, что поглощение 18F-ФДГ было значительно (р < 0,001) выше по сравнению с поглощением 99mТс-MIBI (2,2 против 13,3), что указывает на высокий метаболизм глюкозы в пораженных лимфатических узлах. Кроме того, совмещение ПЭТ- и ОФЭКТ-изображений с данными компьютерной томографии одинаково позволяет визуально разграничить пораженные лимфатические узлы средостения от соседних анатомических структур и патологически измененных участков прилежащей легочной паренхимы – ателектазов или постобструктивной пневмонии вследствие обструкции дыхательных путей увеличенными лимфатическими узлами.
Заключение
Таким образом, ОФЭКТ с 99mTc-MIBI может позволить осуществить дифференциальную диагностику медиастинальных форм В-клеточной лимфомы, обладая большей доступностью, относительной легкостью проведения и существенно меньшими затратами на исследование по сравнению с ПЭТ с 18F-ФДГ, при сопоставимой с ней чувствительности. Отсюда появляются основания рекомендовать ОФЭКТ с 99mTc-MIBI пациентам с целью выявления, проведения дифференциальной диагностики при подозрении на медиастинальную лимфому, в случаях, когда ПЭТ недоступна. Однако существенно меньшее в сравнении c 18F-ФДГ поглощение 99mТс-MIBI опухолевыми лимфоидными тканями может явиться некоторым ограничением в дифференциальной диагностике заболеваний методом ОФЭКТ. Для уточнения диагностического и прогностического значения ОФЭКТ с 99mTc-MIBI необходимы дальнейшие исследования на более многочисленных группах пациентов.
M.M. Khafizov, D.E. Baikov, PhD, L.R. Akhmadeeva
Clinic of Bashkir State Medical University Federation
Bashkir State Medical University
Contact person: Munavis M. Khafizov, munavis.khafizov@gmail.com
Non-Hodgkin's lymphomas account for 3% of all cancers and rank sixth in frequency among women and seventh among men. The existing difficulties in the timely and high-quality detection of these diseases, their differential diagnosis according to the methods of radiation diagnostics, necessitate the use of radioisotope research methods.
Purpose of the study – to compare the diagnostic possibilities of visualization of mediastinal forms of lymphomas according to positron emission and computed tomography (PET/CT) using 18F-fluorodeoxyglucose (18F-FDG) and single-photon emission computed tomography combined with X-ray computed tomography (SPECT/CT) with 99mTc-MIBI, their role in the differential diagnosis of pathologically altered areas of the adjacent lung parenchyma.
Material and methods. A retrospective analysis of radionuclide studies of 4 patients with a mediastinal form of diffuse B-cell lymphoma of a high degree of malignancy with the presence of zones of pulmonary consolidation in the hilar areas of the lungs was carried out. All patients underwent PET/CT with 18F-FDG and SPECT/CT with 99mTc-MIBI.
Results. The present study found that SPECT/CT with 99mTc-MIBI and PET/CT with 18F-FDG have comparable sensitivity in the diagnostic evaluation of patients with mediastinal lymphomas. However, the uptake of 18F-FDG by tumor lymphoid tissues was significantly higher compared to the accumulation of 99mTc-MIBI, and the detected foci were clearly differentiated from the adjacent tissues of the mediastinum and lungs.
Conclusions. The present study found that SPECT/CT with 99mTc-MIBI and PET/CT with 18F-FDG have comparable sensitivity in the diagnostic evaluation of patients with mediastinal lymphomas. However, the uptake of 18F-FDG by tumor lymphoid tissues was significantly higher compared to the accumulation of 99mTc-MIBI, and the detected foci were clearly differentiated from the adjacent tissues of the mediastinum and lungs.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.