Боли в спине могут возникать по разным причинам. В ряде случаев формированию болевых синдромов могут способствовать дизрафические состояния, сопровождающиеся изменениями статики и динамики позвоночника с перераспределением нагрузки и уменьшением амортизационной способности при ходьбе (например, разная длина ног, сколиозы, плоскостопие, люмбализация, сакрализация и т.д.). Боли в спине могут быть связаны с инфекциями позвонков и межпозвонковых дисков (туберкулез, бруцеллез, эпидуральный абсцесс), неинфекционными воспалительными заболеваниями (анкилозирующий спондилит, ревматоидный артрит), метаболическими поражениями костей (остеопороз, остеомаляция), новообразованиями позвоночника и спинного мозга, травмами или последствиями повреждений позвоночника и мягких тканей, заболеваниями внутренних органов (отраженные боли). В ряде случаев, когда органических причин для болей нет, можно говорить о психогенном характере боли [1, 2].
Однако основная масса случаев болей в спине обусловлена дегенеративно-дистрофическими изменениями позвоночника: остеохондрозом (протрузия или пролапс межпозвонкового диска, дистрофическое поражение межпозвонкового диска и тел позвонков), спондилоартрозом (артроз дугоотростчатых или фасеточных суставов), спондилезом, проявляющимся костеобразованием под передней продольной связкой. Следствием могут быть дистрофический спондилолистез и вторичный люмбальный стеноз. Непосредственными причинами болей в спине в этом случае являются повреждение межпозвонковых суставов (спондилоартрит, остеохондроз) и раздражение и/или компрессия спинномозгового корешка (остеофиты, грыжа диска). Развитию дегенеративно-дистрофических процессов в позвоночнике способствуют: микротравматизация структур опорно-двигательного аппарата вследствие неадекватных нагрузок, возраст, аномалии развития, хроническая ишемизация, эндокринно-гормональные расстройства и наследственные факторы [2, 3].
Остеохондроз – самая распространенная форма дегенеративно-дистрофических изменений позвоночника. В основе его развития лежит дегенерация дисков с реакцией костной ткани в виде субхондрального остеосклероза и краевых разрастаний с формированием остеофитов. Остеохондроз близок по патогенезу с остеоартрозом, эти состояния часто сочетаются. Дегенерация межпозвонковых дисков при остеохондрозе начинается с пульпозного ядра. Оно постепенно обезвоживается, теряет тургор и утрачивает способность служить амортизатором. Изменения пульпозного ядра приводят к повышению и неравномерному распределению давления на фиброзное кольцо, что влечет за собой дегенеративно-дистрофические изменения в периферической зоне дисков. Происходит их уплощение, увеличивается нагрузка на позвонки. Далее формируется реакция костной ткани в виде остеосклероза в подхрящевом слое тел позвонков и образования по их переднебоковой поверхности горизонтальных или клювовидных выступов – остеофитов. Уплощение диска приводит к сближению расположенных сзади отростков дуг (фасеточных суставов), их перегрузка ведет к сопутствующему межпозвонковому артрозу [1, 4]. Артроз позвоночных суставов может развиваться и самостоятельно из-за усиленного лордоза, когда нагрузки падают больше не на диски, а на суставы, расположенные кзади (усилению лордоза может способствовать ношение обуви на высоком каблуке).
Источником формирования болевых ощущений при дегенеративно-дистрофических изменениях в позвоночнике являются мягкие ткани позвоночных двигательных сегментов вследствие ирритации при дегенеративных процессах дисков, капсульно-связочного и миофасциального аппарата. Формируются участки ноцицепции с местной неспецифической воспалительной реакцией, синтезом и высвобождением алгогенов (серотонина, гистамина, кининов, простагландинов, лейкотриенов, цитокинов). В формировании длительно существующего болевого ощущения помимо раздражения периферических рецепторов имеет значение состояние чувствительных нейронов задних рогов спинного мозга и нейронов желатинозной субстанции, а также активность и состоятельность антиноцицептивной системы [4, 5].
Клинические проявления болей в спине в классическом варианте можно разделить на две неравные группы: в 10–15% случаев встречаются компрессионно-ишемические синдромы в виде радикулопатий и значительно чаще (85–90%) – мышечно-тонические рефлекторные синдромы. Более всего распространены боли в нижней части спины – до 60% случаев, в грудном отделе – в 10%, в шее и надплечье – по 15%. Важно помнить, что мышечно-тонические синдромы могут возникать и без значимых вертеброгенных причин (например, при быстром растяжении мышцы при выполнении «неподготовленного» движения или перегрузке нетренированных мышц) [6].
Анамнез и тщательное обследование позволяют исключить более редкие причины болей в спине. Внезапное появление интенсивных болей, не зависящих от положения тела, без предшествующего анамнеза, очень молодой возраст, онкологическое заболевание или травма позвоночника, лихорадка или снижение массы тела без веских причин заставляют искать причину болезни вне дегенеративно-дистрофических изменений позвоночника. Особое значение имеет неврологический осмотр, позволяющий выявить признаки мышечно-тонического синдрома, страдания корешка или даже миотома (симптомы выпадения функции корешка или миотомный парез могут послужить поводом для обращения к нейрохирургу). Рентгенологические и нейровизуализационные методы являются серьезным подспорьем диагносту [7], однако стоит помнить, что часто присутствует диссоциация между изображением и клинической картиной: наличие большой грыжи может не сопровождаться болями и, наоборот, выраженный болевой синдром с признаками вовлечения корешка может быть при минимальных изменениях в позвоночнике.
Рентгенологическими признаками дегенеративно-дистрофических изменений позвоночника являются уменьшение высоты диска, уплотнение пульпозного ядра и кальцификация фиброзного кольца, субхондральный склероз, наличие остеофитов, артроз фасеточных суставов, изменение формы позвонков, листезы. При магнитно-резонансной томографии (МРТ) можно выявить снижение сигнала от межпозвонкового диска, его выбухание и влияние на нервные структуры (корешок или даже спинной мозг, последнее может быть актуально для шейных или, реже, грудных локализаций). При компьютерной томографии или МРТ можно также выявить признаки стеноза позвоночного канала (врожденного или вторичного). Важную дополнительную информацию может предоставить электронейромиография.
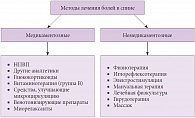
Основополагающими принципами лечения болевых синдромов, в том числе и с локализацией в спине, являются раннее начало лечения, адекватная терапия, предупреждение хронизации и комплексный подход (рис. 1). Общие подходы в терапии болей в спине заключаются в устранении источника болей и восстановлении поврежденных тканей (самая сложная позиция), воздействии на периферические компоненты боли (прием нестероидных противовоспалительных препаратов – НПВП), торможение проведения боли (блокады), воздействии на процессы в задних рогах спинного мозга (прием опиатов, противосудорожных препаратов, флупиртина, проведение физиотерапии), влиянии на состояние антиноцицептивной системы (использование антидепрессантов) [8–10]. При выборе лечебной тактики и комбинации препаратов и немедикаментозных методов важно учитывать клиническую форму, стадию заболевания, сопутствующую патологию, возможное взаимодействие препаратов, их побочные действия и влияние на основной субстрат, ответственный за формирование болей (например, влияние на хрящевую ткань или спазмированные мышцы).
Ядром медикаментозного лечения болей в спине остаются НПВП [11]. НПВП относят к числу самых распространенных лекарственных средств, применяемых в мировой клинической практике, – в мире зарегистрировано более 560 НПВП. Эти средства незаменимы при заболеваниях, сопровождающихся болью, воспалением и лихорадкой [12]. По химической структуре НПВП представляют собой слабые органические кислоты (салициловая, индоловая, пропионовая, эноликовая и др.). Механизм действия НПВП обусловлен подавлением фермента циклооксигеназы (ЦОГ). Существуют две изоформы фермента – констуциональная (ЦОГ-1) и индуцибельная (ЦОГ-2). С подавлением ЦОГ-1 связывают побочные действия НПВП, подавление активности ЦОГ-2 оказывает противовоспалительное и обезболивающее действие. Все НПВП обладают той или иной избирательностью в подавлении ЦОГ-1 или ЦОГ-2 [13].
Нимесулид (Нимесил®) – нестероидное противовоспалительное средство из класса сульфонамидов, которое оказывает противовоспалительное, обезболивающее и жаропонижающее действие. Нимесулид воздействует как ингибитор фермента циклооксигеназы, отвечающего за синтез простагландинов, и ингибирует, главным образом, ЦОГ-2. Нимесулид подавляет синтез основных провоспалительных цитокинов (интерлейкин-6, фактор некроза опухоли-альфа); снижает активность металлопротеиназ (ферменты, разрушающие хрящевую ткань при остеоартрозе); обладает антигистаминным действием; подавляет активность фермента фосфодиэстеразы IV, стимулирующей макрофаги и нейтрофилы, оказывая противовоспалительный эффект. Препарат хорошо всасывается из ЖКТ, быстро достигая максимальной концентрации в плазме, хорошо связывается с белками плазмы и обладает коротким периодом полувыведения. Легко проходит гистогематические барьеры. Нимесил® показан для лечения острых болей в спине и симптоматического лечения остеоартроза с болевым синдромом. Суточная доза нимесулида составляет 200 мг (по 100 мг 2 раза в сутки после еды).
Максимальная рекомендованная длительность лечения нимесулидом – 15 дней. Для уменьшения риска возникновения нежелательных побочных эффектов следует использовать минимальную эффективную дозу минимально коротким курсом. Побочные эффекты препарат вызывает нечасто, самые значимые из них – аллергические реакции, нежелательные явления со стороны органов кроветворения и гепатотоксические реакции. Для уменьшения возможности возникновения побочных эффектов следует учитывать лекарственные взаимодействия, избегая нежелательных сочетаний, а также сопутствующую патологию [14].
В заключение следует подчеркнуть, что главным принципом лечения болей в спине продолжает оставаться рациональная фармакотерапия с применением комплекса препаратов и использованием эффективных средств разных механизмов действия. В подборе таких средств и их дозировок необходимо руководствоваться оптимальным соотношением «риск/польза».