Разработка методологических подходов к управлению онкоэпидемиологическими показателями на модели ранней диагностики гепатоцеллюлярной карциномы в Красноярском крае
- Аннотация
- Статья
- Ссылки
- English





По данным Международного агентства по исследования рака в 2022 г. первичные злокачественные новообразования (ЗНО) печени занимали шестое место в структуре заболеваемости и третье место в структуре смертности в мире среди всех злокачественных новообразований. В 2022 г. было зарегистрировано почти 870 000 впервые выявленных случаев ЗНО печени и 759 000 смертельных исходов от данной группы онкологических заболеваний [1]. Злокачественные опухоли печени в 46 странах входят в число трех основных причин смерти от злокачественных новообразований. Предполагается увеличение количества больных ЗНО печени и умирающих от данного заболевания к 2040 г. более чем на 55,0% при сохранении текущей тенденции.
В структуре заболеваемости и смертности ЗНО рак печени и внутрипеченочных желчных протоков оцениваются совместно (МКБ – С22) [2]. При этом самая частая первичная злокачественная опухоль печени – гепатоцеллюлярная карцинома (ГЦК), на ее долю приходится 85,0% всех случаев. Еще 10,0% приходится на холангиоцеллюлярную карциному (ХЦК) и < 5% на сочетание ГЦК-ХЦК [3]. За пятилетний период в Российской Федерации (РФ), Сибирском федеральном округе (СФО) и Красноярском крае наблюдается тенденция к увеличению числа впервые выявленных случаев рака печени. Абсолютный показатель новых случаев злокачественных опухолей печени и внутрипеченочных протоков на территории РФ увеличился на 11,7% (с 9 324 в 2019 г. до 10 412 случаев в 2023 г.), в СФО показатель увеличился на 13,7% (с 1 442 в 2019 г. до 1 639 случаев в 2023 г.), в Красноярском крае прирост показателя оказался самым большим из сравниваемых территорий и составил 20,1% (с 288 случаев в 2019 г. до 346 случаев в 2023 г.) [4–8].
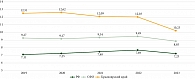
«Грубый» показатель заболеваемости злокачественными новообразованиями печени и внутрипеченочных протоков, рассчитываемый на 100 тысяч населения, в РФ вырос с 6,35 до 7,12, на 12,1%. На территории СФО за аналогичный период данный показатель вырос на 17,4% (с 8,41 в 2019 г. до 9,87 в 2023 г.). В Красноярском крае «грубый» показатель заболеваемости показал самый большой прирост с 10,03 до 12,16 на 100 тысяч населения, что составило 21,2% (рис. 1).
Важное значение при лечении злокачественных новообразований имеет стадия заболевания. Благоприятный прогноз характерен для ранних стадий. При этом выявление рака печени и внутрипеченочных желчных протоков на I–II стадиях, несмотря на рост показателя, остается низким. Так, наблюдается тенденция к увеличению показателя в целом по РФ – прирост на 33,6% (с 14,9% в 2019 г. до 19,9% в 2023 г.). По СФО выявление на I–II стадиях увеличилось на 53,3% (12,2% в 2019 г., 18,7% в 2023 г.). В Красноярском крае данный показатель вырос еще существеннее – на 72,6%, но при этом остается ниже, чем в среднем по РФ и СФО (10,6% в 2019 г., 18,3% в 2023 г.), что делает проблему ранней диагностики наиболее актуальной для населения Красноярского края.
Кроме того, для всех территорий за пять лет доля диагностики на запущенной IV стадии не снижалась менее 50,0% [4–8] (рис. 2, 3).
В Красноярском крае доля лиц, умерших в течение первого года с момента установления диагноза ЗНО печени, на протяжении всего анализируемого периода остается высокой и по итогам 2023 г. составляет 62,1% (67,0% в РФ; 61,5% в СФО). При этом по Красноярскому краю отмечается отрицательная динамика данного показателя – прирост составил 4,1% (58,9% в 2019 г.) (рис. 4).
Доля лиц с ЗНО печени и внутрипеченочных желчных протоков, состоящих на учете пять лет и более, по Красноярскому краю в 2023 г. составляла 31,7% (в 2019 г. – 28,5%; прирост – на 11,2%), что выше, чем в среднем по СФО – 29,0%, и ниже, чем в РФ – 34,7%. При этом в субъектах СФО данный показатель в 2023 г. варьировал от 14,8% в Республике Тыва до 44,4% в Республике Алтай. Индекс накопления контингента в Красноярском крае вырос по сравнению с 2019 годом с 1,0 до 1,3.
Еще один показатель, тесно связанный с низким процентом выявления злокачественных патологий печени на ранних стадиях и большой летальностью на первом году жизни, – абсолютное число умерших от данного заболевания. За период с 2019 по 2023 г. число зарегистрированных случаев смерти от злокачественных опухолей печени и внутрипеченочных протоков в Красноярском крае уменьшилось на 18,9% (с 359 в 2019 г. до 291 случая в 2023 г.). Динамика в сторону уменьшения числа умерших отмечается и на территории СФО (снижение показателя на 8,16%). В РФ, наоборот, произошло увеличение абсолютного числа умерших от ЗНО печени на 1,4% (с 10 430 случаев в 2019 г. до 10 571 в 2023 г.).
«Грубый» показатель смертности от злокачественных опухолей печени и внутрипеченочных протоков на 100 тысяч населения в Красноярском крае в 2023 г. по сравнению с 2019 г. уменьшился на 18,2% (с 12,51 до 10,23). Схожая ситуация с данным показателем отмечается и на территории СФО, где произошло снижение показателя на 4,5% (2019 г. – 9,27 на 100 тыс. населения, 2023 г. – 8,85 на 100 тыс. населения). В РФ «грубый» показатель смертности на протяжении пяти лет был существенно ниже, чем в СФО и Красноярском крае – в 2023 г. – 7,23 на 100 тыс. населения (рис. 5).
Проведенный анализ онкоэпидемиологических показателей свидетельствует о необходимости применения комплекса организационно-методических мероприятий, направленных на эффективную диагностику рака печени и внутрипеченочных протоков, в том числе на выделение из общей популяции пациентов группы высокого риска развития заболевания и поиск наиболее оптимальных подходов к ее обследованию.
Для стратификации пациентов на группы риска развития заболевания проведен обширный преаналитический этап. Известно, что гепатоцеллюлярная карцинома развивается чаще всего на фоне цирроза печени (около 80% случаев) или хронического воспаления любой этиологии: вирусных гепатитов B и C, алкогольного и неалкогольного стеатогепатита, первичного склерозирующего и аутоиммунного гепатита, вследствие экзогенных токсических повреждений печени и нарушениях состояния иммунной системы, при которых происходит повреждение печени с исходом в хронический гепатит и цирроз. Вирусные гепатиты B и C – самый частый фактор риска, являющийся причиной ГЦК в 50% и 15% случаев соответственно [9–13]. Для Красноярского края проблема хронического вирусного гепатита (ХВГ) является наиболее актуальной, поскольку уровень заболеваемости ХВГ в регионе на 84,9% выше показателя заболеваемости по РФ (Красноярский край – 55,3 случая, РФ – 29,9 на 100 тыс. населения в 2022 г.). На долю хронического гепатита С приходится 81,0% от всех случаев ХВГ. Распределение по генотипам следующее: первый генотип – 47,0% случаев, второй генотип – 8,0%, третий генотип – 45,0% [14]. Наибольшая распространенность заболевания наблюдается среди лиц трудоспособного возраста. На долю пациентов в возрасте 30–49 лет приходится 64,0% случаев. Одним из факторов, способствующих большому показателю заболеваемости ХВГ, является низкий защитный титр антител. В 2023 г. в рамках серологического мониторинга напряженности иммунитета выявлена значительная доля серонегативных лиц среди привитых против гепатита В – 50,6%, в том числе в возрасте 3–4 лет – 16,6%, 16–17 лет – 28,5%, 20–29 лет – 6,3%, 30 лет и старше – 48,6%, при нормативном показателе не более 10,0%, что свидетельствует о низком фактическом состоянии иммунитета к вирусному гепатиту В у взрослых и детей [15].
В подавляющем большинстве случаев, когда диагноз рак печени ставится на поздних стадиях, речь идет о пациентах, которые не проходили регулярные медицинские осмотры и диспансеризацию. У этих людей есть множество факторов риска, которые могут привести к развитию гепатоцеллюлярной карциномы. Данный факт обусловлен низким уровнем осведомленности населения в вопросах здоровья, порядка оказания онкологической помощи, функционирования смотровых кабинетов, проведения диспансеризации и скрининга злокачественных новообразований.
Также существует проблема недостаточной онкологической настороженности среди врачей первичного звена. Они не всегда следуют установленному алгоритму действий при подозрении на ЗНО. Это может привести к увеличению времени, затрачиваемого на диагностику, или к потере пациента из-под наблюдения. Организация информированного обмена между различными специалистами повышает преемственность в ведении пациентов.
С целью сохранения здоровья населения в Красноярском крае, начиная с июня 2024 г., была запущена программа по информированию населения и специалистов первичного звена о проблеме гепатоцеллюлярной карциномы. В отношении пациентов – это привлечение средств массовой информации: запись четырех интервью со специалистами, занимающимися патологиями печени на базе различных медицинских учреждений (КГБУЗ «Красноярский краевой клинический онкологический диспансер им. А.И. Крыжановского» (КККОД), КГБУЗ ККБ и ФСНКЦ ФМБА России); запуск двух информационных роликов с участием главных внештатных специалистов Министерства здравоохранения Красноярского края по онкологии и инфекционным болезням в медицинских организациях, имеющих прикрепленное население и занимающихся проведением диспансеризации и профилактических медицинских осмотров. Информирование было направлено на освещение причин развития ГЦК, способах предупреждения этого процесса и вариантах лечения. Интервью и видеоролики демонстрировались во всех медицинских организациях г. Красноярска и Красноярского края.
С целью информирования специалистов медицинских организаций на территории края были организованы ежемесячные видеоселекторные совещания (ВКС) по вопросам стратификации групп риска, направления первичных пациентов в КККОД и вопросам динамического наблюдения за пациентами либо в организациях прикрепления, либо в КККОД – всего более 12 ВКС за 6 месяцев. На ВКС приглашались врачи-онкологи, терапевты, инфекционисты, гастроэнтерологи и другие узкие специалисты, отвечающие за вопросы маршрутизации и оказания помощи пациентам с подозрением и диагнозом ГЦК.
С целью своевременного обнаружения патологических изменений у пациентов с ХВГ в рамках Приказа Министерства здравоохранения Российской Федерации № 168н от 15.03.2022 г. «Об утверждении порядка проведения диспансерного наблюдения за взрослыми» закреплен перечень обследований: определение уровня альфа-фетопротеина (АФП) в сыворотке крови и ультразвуковое исследование (УЗИ) органов брюшной полости. Кратность проведения динамического наблюдения зависит от наличия у пациентов тяжелого фиброза или цирроза печени. Раз в год наблюдаются пациенты без цирроза, два раза в год на динамическое наблюдение приглашаются пациенты с циррозом печени [16].
В ряде стран в основе скрининга/ранней диагностики лежит использование УЗИ совместно с определением уровня АФП или без него. Особое внимание стоит уделить рекомендациям JSH-HCC (Японское Общество Гепатологов), в которых для диагностики, помимо стандартных методик, призывают проводить предварительную стратификацию пациентов по уровню риска (высокий или очень высокий) и в зависимости от этого принимать решение об использовании более специфичных комбинаций биомаркеров и методов лучевой диагностики [17–22]. Сравнение перечня обследований, одобренных и утвержденных в различных ассоциациях, представлено в табл. 1.
Несмотря на одобрение комбинации АФП + УЗИ, которая обладает чувствительностью 63,0%, и охват диспансерным наблюдением пациентов со степенью фиброза F3–F4 на территории Красноярского края, эпидемиологические показатели остаются на низком уровне [23], что влияет на выбор метода лечения и дальнейший прогноз пациента [8].
Важным элементом своевременной диагностики является использование современных доказанных методов диагностики/выявления ГЦК. Особенно в зоне повышенного внимания должны находится пациенты с высоким риском возникновения ГЦК, для которых необходимо выбирать более эффективный комплекс обследования (т.е. обладающий большей чувствительностью). Поэтому следующим этапом организации междисциплинарного подхода было определение группы высокого риска возникновения ГЦК и создание алгоритма маршрутизации пациентов по «зеленому коридору» до врача-онколога. Обсуждение было вынесено на рабочую группу Министерства здравоохранения Красноярского края, куда вошли специалисты первичного звена и узкие специалисты, занимающиеся патологиями печени. Критерии для отбора были заданы следующие: возраст 40–70 лет, степень фиброза печени F3–F4, длительность цирроза 5 и более лет.
Стоит отметить, что в настоящее время в регионе осуществляется учет пациентов, страдающих вирусными гепатитами. В регистре помимо основных сведений о больных фиксируется степень фиброза печени, определенная с помощью эластографии. Это позволило выделить группу лиц, находящихся в группе высокого риска, этиологией развития цирроза у которых является вирусный гепатит, для участия в проекте по скринингу и ранней диагностике гепатоцеллюлярной карциномы.
На сегодняшний день маршрут пациента, независимо от принадлежности к группе высокого или умеренного риска с подозрением на ГЦК, составляет до 63–69 дней. Пациент до момента верификации диагноза и назначения соответствующих терапевтических опций проходит консультацию у врачей разных специальностей (инфекциониста, терапевта, гастроэнтеролога, хирурга и других). Разобщенность действий специалистов, отсутствие преемственности и единых стандартов ведения данной группы пациентов усугубляют проблему смертности от ГЦК. Также большая продолжительность маршрута пациента не укладывается в сроки программы государственных гарантий, в которой временной интервал от подозрения на злокачественное новообразование до постановки диагноза не должен превышать 14 дней [24].
Данные о факторах риска развития ГЦК позволяют определить пациентов, относящихся к группе высокого риска, для формирования модели наблюдения специалистами из междисциплинарной команды. В свою очередь, своевременная диагностика рака печени для пациентов из группы высокого риска позволяет сократить время с момента подозрения ЗНО до начала специализированного лечения [25].
Междисциплинарный подход к диагностике и лечению ГЦК улучшает систему направления пациентов, сокращая время до получения медицинской помощи. Одно из первых крупных исследований по формированию такого подхода было проведено в Дании в 2009 г. Правительство учредило программу ускоренного алгоритма оказания медицинской помощи (Fast Track Clinical Pathways — FTCP), чтобы ускорить процесс диагностики и лечения злокачественных новообразований, в том числе ГЦК. В нее были включены подряд 309 пациентов с подозрением на ГЦК, 79 из них получили направления к узким специалистам в 2007–2008 гг. (до учреждения FTCP), а 230 пациентов — в 2009–2011 гг. Из них у 271 пациента (88,0%) была диагностирована ГЦК, а у 161 пациента (60,0%) — цирроз, в большинстве случаев вызванный употреблением алкоголя [26].
Алгоритм маршрутизации пациентов на территории края начинался со стратификации пациентов высокого риска развития ГЦК инфекционистами, гастроэнтерологами и терапевтами – специалистами первого звена междисциплинарной команды. Пациенты этой группы отбирались во время приема в рамках динамического наблюдения согласно Приказу 168н в поликлиниках прикрепления и направлялись в КККОД для заполнения анкеты на определение риска развития ГЦК у пациентов с циррозом печени. Еженедельно специалистами первичного звена медицинских организаций г. Красноярска в КККОД направлялось около 30–50 человек из группы риска. Анкета включала в себя вопросы об этиологии цирроза печени, наличии вирусного гепатита и его лечении, наличии cопутствующих патологий, таких как варикозное расширение вен пищевода или желудка, сахарный диабет. Ряд вопросов о семейном анамнезе онкологических заболеваний, в частности анамнеза по ГЦК, и блок вопросов, посвященный лабораторным и инструментальным обследованиям пациента. Сбор данных по вопросам, отображенным в анкете, помог параллельно с приемом первичных пациентов сформировать пилотный регистр пациентов с циррозом различной этиологии, входящих в группу высокого риска возникновения рака печени. Формирование регистра также было направлено на планирование объемов динамического наблюдения и определение персонифицированного подхода в маршрутизации пациентов высокой группы риска с целью своевременной диагностики ГЦК на ранней стадии.
Для пациентов, относящихся к группе высокого риска, на территории Красноярского края в качестве пилотного проекта было выбрано определение онкомаркеров АФП в сочетании с PIVKA-II (протеин, индуцируемый отсутствием витамина К2) с последующим применением калькулятора GAAD для расчета риска ГЦК. Чувствительность данного метода составляет 73,1%, что выше чувствительности АФП + УЗИ (63,0%) [27, 28]. Вторым этапом после применения калькулятора GAAD было направление пациента на магнитно-резонансную томографию (МРТ) с применением гепатоспецифичного контраста. Стоит отметить, что частота выявления ГЦК у пациентов высокой группы риска на ранних стадиях при использовании УЗИ составляет 28,0%, в то время как частота выявления ГЦК при использовании МРТ с контрастным усилением составляет 86,0% [29]. Забор крови на два специфичных онкомаркера проходил на базе КККОД с одновременным заполнением анкеты на определение риска развития ГЦК.
С целью оптимизации маршрутизации пациентов с ГЦК в Красноярском крае была сформирована многопрофильная комиссия, включающая различных специалистов на всех этапах курации пациента. На этапе диагностики в монопрофильную комиссию включались рентгенолог, инфекционист, гастроэнтеролог и патоморфолог. Специалисты отвечали за интерпретацию МРТ-исследований с гепатотропным контрастом и гистологических исследований, определение стадии поражения печени по Барселонской системе BCLC и выявление портальной гипертензии. Стоит отметить, что с целью повышения доступности МРТ-исследований на территории края был разработан и утвержден тариф на проведение МРТ с гепатотропным контрастом, оплачиваемый за счет средств ОМС.
На следующем этапе междисциплинарный консилиум определял план лечения пациента на основании стадии заболевания и особенностей пациента. В многопрофильную комиссию включались: хирург, трансплантолог и онколог (специалист по противоопухолевой лекарственной терапии). Основной задачей являлось определение дальнейшей тактики ведения пациента и выбор метода лечения.
Работа многопрофильной комиссии проводилась не реже одного раза в неделю, с формированием тактики диагностики, лечения, динамического наблюдения за каждым пациентом.
Междисциплинарный подход для пациентов повышенного риска необходимо расширять дальше, чтобы охватить все этапы: от подозрения на ГЦК до лечения и динамического наблюдения за пациентами. В журнале «Актуальные проблемы хирургии» была опубликована работа, авторы которой взаимозаменяемо используют понятия скрининг, ранняя диагностика и динамическое наблюдение за пациентами из группы риска по ГЦК. Большую роль в междисциплинарной команде они отводят врачам-рентгенологам, которые занимаются визуализацией при неинвазивной диагностике ГЦК. От их работы зависит, к каким специалистам из большой команды, занимающейся лечением, пациент попадет на первом этапе лечения патологии [30].
Формирование регистра пациентов с повышенным риском развития ГЦК поможет не только в планировании объемов динамического наблюдения, но и, возможно, позволит выявить факторы риска, которые будут характерны именно для Красноярского края. Такую работу ретроспективно удалось провести коллективу авторов из Хьюстона, штат Техас, которые включили в общей сложности 130 медицинских учреждений и статистически значимо доказали влияние неалкогольной жировой болезни печени (НАЖБП) на риск развития ГЦК [30].
Разработка и внедрение в Красноярском крае междисциплинарного подхода к ранней диагностике пациентов высокого риска развития ГЦК показало свою актуальность и необходимость. Ожидаемо произошло не только увеличение общего количества впервые выявленных случаев ГЦК (с 346 случаев в 2023 г. до 457 случаев в 2024 г. – прирост показателя на 32,1%), но и увеличение доли новых случаев, обнаруженных на ранних стадиях, с 18,3% до 24,5% (прирост показателя на 33,9%).
Работа в многопрофильной команде способствовала увеличению количества хирургических методов лечения ГЦК на 16,5% (2023 г. – 97 случаев, 2024 г. – 113 случаев) и количества биопсий печени на 33,2% (2023 г. – 407 биопсий, 2024 г. – 542 биопсии). Отмечается увеличение доли противоопухолевого лечения, в т.ч. иммунотерапии (атезолизумабом + бевацизумабом) на 85,0% (2023 г. – 20 пациентов, 2024 г. – 37 пациентов).
Таким образом, проведенный в регионе комплекс организационно-методических мероприятий позволил повысить осведомленность пациентов и их родственников о важности скрининга ГЦК. Закономерно наметилась тенденция роста общей заболеваемости ГЦК со снижением количества случаев, обнаруженных на III–IV стадиях, что носит для региона положительный социально-экономический эффект.
R.A. Zukov, PhD, I.P. Safontsev, PhD, V.A. Komissarova, D.A. Stoyan
A.I. Kryzhanovsky Krasnoyarsk Regional Clinical Oncology Dispensary
V.F. Voino-Yasenetsky Krasnoyarsk State Medical University
Contact person: Ruslan A. Zukov, zukov_rus@mail.ru
Organizational and methodological work aimed at public awareness, stratification of risk groups, development of a screening program for hepatocellular carcinoma for high-risk groups, formation of an interdisciplinary team at the regional level, monitoring patient routing and meeting deadlines at various stages can have a positive impact on oncoepidemiological indicators. An increase in the proportion of newly diagnosed cases in the early stages, in turn, allows the use of modern approaches and technologies for the treatment of patients: surgical treatment, transarterial chemoembolization, new antitumor therapy regimens.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.