Роль структуры витреоретинального интерфейса в патогенезе отслойки сетчатки при эндофтальмите
- Аннотация
- Статья
- Ссылки
- English
Введение
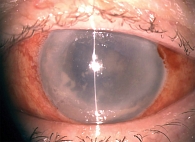
Эндофтальмит, представляющий собой тотальное воспаление внутренних структур глазного яблока, остается одной из самых драматичных патологий в офтальмохирургии из-за высокого риска необратимой потери зрительных функций [1]. Ключевым и наиболее прогностически неблагоприятным осложнением тяжелого эндофтальмита является тракционная и регматогенная отслойка сетчатки (ОС), значительно усложняющая хирургическую тактику и ухудшающая функциональные исходы. Традиционно патогенез ОС при эндофтальмите обусловлен массивной экссудацией, образованием фибринозно-гнойных мембран и прямым цитопатическим воздействием инфекционных агентов и медиаторов воспаления на нейросенсорный эпителий [2] (рис. 1).
Цель – проанализировать на основании имеющихся данных этиологию и патогенез эндофтальмита, его диагностику в зависимости от основных клинических проявлений, а также основные принципы лечения, профилактики и прогноза заболевания.
Материал и методы
В проспективном когортном исследовании участвовало 45 пациентов (45 глаз) с тотальным эндофтальмитом бактериальной этиологии, развившимся в послеоперационном периоде (после факоэмульсификации катаракты) или в результате проникающего ранения глазного яблока (основная группа). Контрольную группу составили 15 пациентов (15 глаз) с идиопатическим макулярным отверстием, у которых во время запланированной витрэктомии были получены интактные образцы стекловидного тела и внутренней пограничной мембраны (ВПМ).
Все пациенты основной группы были разделены на две подгруппы в зависимости от исхода. Первую подгруппу представляли 28 пациентов с эндофтальмитом, у которых не произошло ОС, вторую – 17 пациентов с эндофтальмитом, осложненным тракционно-регматогенной ОС.
Клинические и визуализационные методы обследования
Всем пациентам помимо стандартного офтальмологического обследования (визометрия, тонометрия, биомикроскопия) проводилась комплексная визуализация структур витреоретинального интерфейса (ВРИ):
- оптическая когерентная томография (ОКТ) по стандартному протоколу макулярного и перипапиллярного сканирования. Особое внимание уделялось оценке состояния задней гиалоидной мембраны, наличию и характеру витреомакулярных тракций, структуре ВПМ;
- ультразвуковое В-сканирование в режиме реального времени для определения состояния стекловидного тела, выявления швартообразования, фибринозных тяжей и признаков начальной или манифестной ОС в условиях непрозрачных оптических сред.
Хирургические методики и забор биологического материала
Всем пациентам основной группы выполняли трехпортовую трансконъюнктивальную микроинвазивную витрэктомию 25G. В ходе оперативного вмешательства проводили забор биологических проб для последующего анализа:
- аспират стекловидного тела (1,0–1,5 мл) до начала инфузии сбалансированного солевого раствора;
- эпиретинальные мембраны и образцы ВПМ, полученные в ходе витрэктомии и пилинга ВПМ (вторая подгруппа).
Лабораторные методы исследования
В ходе исследования выполнялся микробиологический анализ. Аспираты стекловидного тела подвергались посеву на жидкие и плотные питательные среды с последующей идентификацией микроорганизмов и определением их чувствительности к антибиотикам.
Статистический анализ
Статистическая обработка данных осуществлялась с использованием программного пакета SPSS Statistics 26.0. Для межгруппового сравнения количественных показателей применялся t-критерий Стьюдента для независимых выборок или непараметрический U-критерий Манна – Уитни (в зависимости от нормальности распределения, проверяемой с помощью критерия Шапиро – Уилка). Для оценки корреляций использовался коэффициент корреляции Спирмена. Различия считались статистически значимыми при p < 0,05.
Результаты
Микробиологический спектр возбудителей эндофтальмита
Микробиологический анализ аспиратов стекловидного тела позволил идентифицировать возбудителя в 41 (91%) случае из 45. Распределение микроорганизмов имело следующие особенности. Грамположительные кокки обнаружены в 28 (68%) случаях из 41, в частности Staphylococcus epidermidis – в 11 (39%), Staphylococcus aureus – в 8 (29%), прочие (энтерококки, стрептококки) – в 9 (32%). Грамотрицательная флора выявлена в 9 (22%) случаях из 41, в частности Pseudomonas aeruginosa – в 4 случаях, Klebsiella pneumoniae – в 3 случаях, прочие – в 2 случаях. В 4 (10%) случаях из 41 идентифицирована полимикробная ассоциация.
Статистически значимой корреляции между видом микроорганизма и частотой развития ОС не выявлено (p = 0,45). Это говорит о том, что дальнейшая патология ВРИ в большей степени обусловлена результатом общего воспалительного ответа, а не спецификой возбудителя.
Ультразвуковое В-сканирование
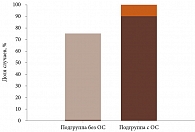
Качественный анализ эхограмм выявил различие между подгруппами (рис. 2).
В первой подгруппе (эндофтальмит без ОС) в 21 (75%) случае из 28 определялась средне- и крупнодисперсная взвесь в полости стекловидного тела без признаков грубого швартообразования. Тракционный синдром отсутствовал.
Во второй подгруппе (эндофтальмит с ОС) в 17 (100%) случаев визуализировались плотные, фибринозно-геморрагические шварты, фиксированные к диску зрительного нерва и/или зубчатой линии. В 15 (88%) случаях из 17 данные шварты формировали звездчатые конфигурации с выраженной витреоретинальной тракцией, приводившей к подъему и складчатости сетчатки.
ОКТ
В условиях помутнения оптических сред получить информативные ОКТ-сканы удалось у 22 пациентов (12 из первой подгруппы и 10 из второй).
У пациентов первой подгруппы структура ВРИ была относительно сохранена. Наблюдались диффузная гиперрефлективность слоя нервных волокон и незначительное утолщение ВПМ вследствие отека. Задняя гиалоидная мембрана, как правило, была не дифференцирована.
У всех пациентов второй подгруппы зафиксированы патогномоничные изменения:
- локальные тракционные разрывы ВПМ – 70%;
- фокальные или диффузные эпиретинальные мембраны с коэффициентом рефлективности > 90 dB, плотно адгезированные к поверхности сетчатки;
- кистовидные изменения внутренних слоев сетчатки и субретинальный фиброз в зонах максимальной тракции – 80%.
Обсуждение
Проведенное исследование указывает на ключевые патофизиологические механизмы, лежащие в основе одного из наиболее тяжелых осложнений бактериального эндофтальмита – отслойки сетчатки. Полученные данные позволяют утверждать, что ОС является не случайным или исключительно механическим следствием воспаления, а закономерным итогом активного и диcрегулируемого процесса фибропролиферативного ремоделирования ВРИ, инициируемого специфическим цитокиновым каскадом.
Диcрегуляция профибротических цитокинов как центральное патогенетическое звено
Наиболее значимым открытием нашего исследования стало выявление резкого дисбаланса в системе профибротических цитокинов между пациентами с принципиально разными исходами. Одинаково высокие в обеих подгруппах уровни провоспалительных цитокинов – интерлейкина 6 и фактора некроза опухоли альфа – указывают на то, что общая тяжесть инфекционно-воспалительного процесса не является предиктором развития ОС. Ключевым фактором риска служит избыточная и длительная продукция именно трансформирующего фактора роста (ТФР) бета-2 и тромбоцитарного фактора роста (PDGF-AA).
Как известно, ТФР-бета-2 – один из наиболее мощных стимуляторов фиброза в глазу [3]. Он индуцирует экспрессию альфа-гладкомышечного актина (альфа-SMA) в фибробластах и глиальных клетках, способствуя их трансдифференцировке в миофибробласты, и стимулирует синтез компонентов внеклеточного матрикса [4]. PDGF-AA в свою очередь выступает основным митогеном для этих клеток [5]. Обнаруженная нами сильная положительная корреляция между уровнем ТФР-бета-2 и долей альфа-SMA-позитивных клеток в эпиретинальных мембранах служит прямым доказательством этой причинно-следственной связи. Таким образом, именно специфический профибротический фон создает условия для неконтролируемой пролиферации и приобретения клетками контрактильных свойств [6, 7].
Клеточные источники пролиферации и роль повреждения внутренней пограничной мембраны
Иммуногистохимический анализ выявил тройной клеточный источник эпиретинальных мембран: миофибробласты, глиальные клетки и клетки пигментного эпителия сетчатки. Высокое содержание глиальных клеток (GFAP+) подтверждает теорию об их миграции из внутренних слоев сетчатки через поврежденную ВПМ. Данные ОКТ, продемонстрировавшие локальные разрывы ВПМ в подгруппе с ОС, морфологически подтверждают этот путь.
Обнаружение клеток пигментного эпителия сетчатки (ПЭС) в 70% образцов мембран крайне важно, поскольку свидетельствует о том, что воспалительный процесс приводит к потере не только внутренней, но и внешней целостности гематоретинального барьера. Миграция ПЭС в полость стекловидного тела и их последующая трансдифференцировка под действием ТФР-бета-2 является ключевым драйвером агрессивного фиброза, так как эти клетки обладают высоким пролиферативным и синтетическим потенциалом [8].
Патогенетическая модель развития отслойки сетчатки при эндофтальмите
На основании полученных данных мы предлагаем следующую двухфазную модель патогенеза:
фаза I: инициация и повреждение. Массивное бактериальное воспаление приводит к лизису стекловидного тела, высвобождению провоспалительных медиаторов и структурному повреждению ВРИ. Происходят активация резидентных клеток (гиалоцитов, глиальных клеток) и нарушение целостности ВПМ;
фаза II: пролиферация и тракция. У отдельных пациентов в силу индивидуальных особенностей иммунного ответа или специфики инфекционного агента формируется доминирующий профибротический цитокиновый профиль (ТФР-бета-2/PDGF-AA). Это запускает неконтролируемую пролиферацию миофибробластов, миграцию глиальных клеток и ПЭС, что приводит к формированию контрактильных эпиретинальных мембран. Генерируемые ими тракционные силы, действующие на ослабленную и отечную сетчатку, в конечном итоге приводят к ее отслойке.
Клинические импликации и перспективы
Полученные результаты имеют не только теоретическое, но и практическое значение. Определение уровня ТФР-бета-2 и PDGF-AA в аспирате стекловидного тела на ранней стадии эндофтальмита может служить прогностическим биомаркером высокого риска развития ОС. Это позволит идентифицировать группу пациентов, нуждающихся не просто в санационной витрэктомии, а в более агрессивной хирургической тактике, направленной на максимально полное удаление кортикального слоя стекловидного тела и пилинг ВПМ для профилактики последующей пролиферации. В долгосрочной перспективе появится возможность для разработки адъювантной антифибротической терапии, например с применением ингибиторов ТФР-бета, для подавления пролиферативного каскада и улучшения функциональных исходов лечения.
Заключение
Проведенное комплексное исследование позволило установить, что развитие ОС при бактериальном эндофтальмите – закономерный исход каскада патологических процессов, инициируемых специфическим дисбалансом регуляторных молекул и структурным ремоделированием ВРИ.
Основные выводы сводятся к следующему.
- Ключевым патогенетическим фактором, определяющим развитие ОС, является не общая тяжесть воспаления, а избыточная активация профибротических сигнальных путей, о чем свидетельствует резкое повышение концентраций ТФР-бета-2 и PDGF-AA в стекловидном теле у пациентов с данным осложнением.
- Морфологическим субстратом ОС служат контрактильные эпиретинальные мембраны гетерогенного клеточного состава, сформированные преимущественно миофибробластами (альфа-SMA+), глиальными клетками (GFAP+) и клетками пигментного эпителия (панцитокератин+). Данный состав подтверждает гипотезу о множественных клеточных источниках пролиферации при повреждении ВПМ.
- Определение уровня ТФР-бета-2 и PDGF-AA может быть использовано в качестве прогностического биомаркера для стратификации риска развития ОС. Это открывает возможности для персонализации хирургической тактики, предусматривающей более раннее и радикальное витреоретинальное вмешательство у пациентов с неблагоприятным прогнозом, а также для разработки новых адъювантных стратегий терапии, направленных на селективное подавление фиброза.
Прозрачность финансовой деятельности. Никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
S.A. Abakarov, PhD, I.A. Loskutov, PhD
Moscow Regional Research and Clinical Institute
Contact person: Sapiyulla A. Abakarov, Boss@limesmedia.ru
Endophthalmitis, a total inflammation of the internal structures of the eyeball, remains one of the most dramatic pathologies in ophthalmic surgery due to the high risk of irreversible visual loss. The key and most prognostically unfavorable complication of severe endophthalmitis is tractional and rhegmatogenous retinal detachment, the development of which significantly complicates surgical tactics and worsens functional outcomes. Traditionally, the pathogenesis of retinal detachment in endophthalmitis is associated with massive exudation, the formation of fibrinous-purulent membranes, and the direct cytopathic effect of infectious agents and inflammatory mediators on the neurosensory epithelium.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.