История появления и применения инсулинов началась в 1921 г., когда ученым Университета в Торонто Фредерику Бантингу и Чарльзу Бесту впервые удалось выделить из поджелудочной железы экстракт, снижающий уровень глюкозы в крови у собак с экспериментальным сахарным диабетом. Первому пациенту экспериментальный препарат был введен в январе 1922 г. С тех пор в терапии СД применяли естественные препараты инсулинов, которые получали из поджелудочной железы крупного рогатого скота и свиней. «Первые» препараты инсулина позволяли продлить жизнь пациентов, страдающих СД, но имели достаточно много побочных эффектов. В 1953 г. Фредериком Сангером была расшифрована химическая структура инсулина, что позволило улучшить качество применяемых препаратов инсулина. Но по-настоящему эра фармакологической «гонки» за лучший препарат инсулина началась только в 1977 г. с открытия структуры ДНК и внедрения рекомбинантных технологий.
Это позволило определить индивидуальные последовательности аминокислот в белках, изменять их и оценивать биологические эффекты полученных продуктов, что привело к возникновению в фармакологии целого направления, занимающегося синтезом новых молекул с улучшением свойств ранее изученных веществ, лекарственных препаратов. Таким образом, начиная с прошлого столетия, фармакологический рынок препаратов инсулина значительно изменился – от бычьих и свиных через генно-инженерные к аналоговым инсулинам. Препараты инсулина, применяемые в настоящее время, различаются в основном по четырем признакам: происхождению, скорости наступления действия и его продолжительности, способу очистки и степени чистоты препаратов, а также концентрации инсулина. В середине 1990-х гг. в лекарственную терапию сахарного диабета вошли аналоги инсулина.
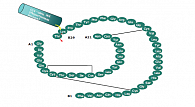
Одним из препаратов инсулина, рекомендованных к применению для достижения компенсации углеводного обмена у пациентов, страдающих СД 2 типа, является детемир (Левемир®, компания «Ново Нордиск»). Это первый ацилированный аналог человеческого инсулина длительного действия (рис. 1). Его получают в процессе экспрессии рекомбинантой ДНК Saccharomyces cerevisiae с последующей химической модификацией. При этом происходит удаление аминокислоты треонин из положения B30 и прикрепление к аминокислоте лизин в положении B29 жирно-кислотного остатка, состоящего из 14 атомов углерода – C14 (миристиновая кислота), боковые цепи которых связываются между собой с образованием дигексамеров, а также с тканевым альбумином [3]. Самооассоциация инсулина и связывание с альбумином определяет способность к пролонгированию абсорбции инсулина из депо в подкожно-жировой клетчатке в месте инъекции [4].
После подкожного введения благодаря активному связыванию с альбумином (более 98%) в месте инъекции сывороточная концентрация инсулина детемир в крови повышается медленнее. Максимальная сывороточная концентрация достигается между 6 и 8 ч, при этом инсулин не имеет выраженных пиков действия. Еще одной отличительной чертой действия данного инсулина является минимальная вариабельность абсорбции, которая позволяет избежать значимых колебаний уровня гликемии и развития гипогликемических состояний, что, в свою очередь, формирует приверженность пациентов к применению данного препарата для лечения.
Инсулин детемир представляет собой стерильный, прозрачный нейтральный раствор с pH = 7,4, который не образует преципитатов в месте инъекции, создавая жидкостное депо дигексамеров в подкожно-жировой клетчатке [5]. Кроме того, формируются обратимые связи с альбумином, что также способствует пролонгированию действия. После абсорбции в систему кровотока происходит быстрая диссоциация с образованием мономеров. В циркуляции также отмечается определенная пролонгация действия детемира за счет связывания с альбумином. Но это играет меньшую роль, чем связывание препарата с альбумином в подкожном депо.
Еще одним важным аспектом является минимальное влияния инсулина детемир на вес пациентов. Этот факт представляется особенно значимым, учитывая выраженный жиромобилизующий эффект гормона и частое наличие избыточного веса или ожирения у пациентов с СД 2 типа. Терапия инсулином детемир сопровождалась меньшей динамикой массы тела по сравнению с нейтральным протамином Хагедорна (инсулин НПХ), а также низкой интраиндивидуальной вариабельностью показателей гликемии натощак [9]. Edith M. Heintjes и соавт. провели ретроспективную оценку веса у пациентов, находившихся на терапии аналогами инсулина пролонгированного действия (гларгин и детемир) и пероральными сахароснижающими препаратами (ПССП) в течение 3 лет (ретроспективный анализ регистра PHARMO 2004–2008, Нидерланды). Были проанализированы истории болезни 720 пациентов, страдающих СД 2 типа, из которых 252 человека находились на терапии инсулином детемир и ПССП, а 460 человек получали терапию инсулином гларгин и ПССП. Через два года лечения прибавка веса у пациентов первой группы составила 0,2 кг, а у пациентов второй группы – 1,2 кг [10].
Аналогичные результаты были получены при оценке веса и у пациентов с СД 1 типа. Philippe Vague c соавт. провели 6-месячное сравнительное исследовании с параллельными группами, включавшими 448 человек с СД 1 типа. Пациенты были рандомизированны на две группы: получавшие терапию инсулином детемир и НПХ в сочетании с быстродействующим аналогом инсулина аспарт (НовоРапид®) препрандиально. К концу исследования масса тела была достоверно ниже у пациентов в группе инсулина детемир [11]. Отметим также отсутствие прибавки массы тела при использовании инсулина детемир два раза в день, согласно данным 16-недельного исследования, проведенного с участием пациентов с СД 1 типа (n = 408). Они были рандомизированы в группы, получавшие инсулин детемир дважды в день в двух разных режимах: перед завтраком и перед сном или с 12-часовым интервалом, и инсулин НПХ, который вводился перед завтраком и перед сном. В качестве болюсного инсулина назначался ультракороткий инсулиновый аналог аспарт (НовоРапид®). В группе терапии инсулином НПХ у пациентов отмечалось увеличение массы тела. В группах терапии инсулином детемир изменения массы тела не зафиксировано. Таким образом, общий гликемический контроль на фоне терапии инсулином детемир оказался лучше в сравнении с терапией инсулином НПХ независимо от режима введения [12].
Для сравнения инсулина детемир и инсулина гларгин при СД 2 типа Julio Rosenstock и соавт. провели 52-недельное международное рандомизированное открытое исследование в параллельных группах. Сорок пять процентов пациентов получали аналог инсулина детемир 1 раз в сутки и 55% – 2 раза в сутки в зависимости от уровня глюкозы в крови перед обедом. Инсулин гларгин назначался 1 раз в сутки. По влиянию на гликемический контроль и частоте гипогликемий существенных различий между препаратами не наблюдалось. В группе пациентов, получавших инсулин детемир, отмечена существенно меньшая прибавка массы тела по сравнению с группой пациентов, находившихся на аналоге инсулина гларгин, – 3,0 и 3,9 кг соответственно. Авторы сделали вывод: оба препарата улучшают контроль уровня глюкозы крови, однако инсулин детемир имеет некоторое преимущество относительно динамики массы тела [13].
Louis Monnier и соавт. обнаружили, что у больных СД 2 типа при прогрессирующем ухудшении контроля уровня глюкозы нарушается в большей степени постпрандиальный контроль [14]. Многие пациенты имеют не-адекватный контроль гликемии из-за боязни возникновения гипогликемических состояний и/или на фоне их развития. Инсулиновые аналоги являются инсулинами беспикового действия, что значительно снижает риск развития данных состояний. Во всех исследованиях при сравнении инсулина НПХ и инсулиновых аналогов отмечается меньше гипогликемических состояний на фоне терапии инсулиновыми аналогами (Philippe Vague и соавт. [11], David Russell-Jones и соавт. [22], Philip Home и соавт. [12] и др.). Проведен ряд сравнительных исследований по оценке частоты и степени тяжести гипогликемий при применении инсулиновых аналогов пролонгированного действия.
Thomas R. Pieber и соавт. провели многоцентровое открытое исследование в параллельных группах, в котором приняли участие 320 пациентов с СД 1 типа, получавших инсулин короткого действия во время приема пищи и инсулин детемир 2 раза в сутки или аналог инсулин гларгин 1 раз в сутки. Пациенты проводили самоконтроль гликемии. Было отмечено, что уровни глюкозы в крови были ниже в группе, находящейся на аналоге инсулина гларгин, чем в группе, применявшей аналог инсулина детемир (7,0 ммоль/л и 7,7 ммоль/л соответственно; p < 0,001), однако различий в показателях глюкозы, измеренных в 9 точках в течение суток, не было. Колебания уровня глюкозы в крови в группе инсулина детемир были ниже перед ужином (p < 0,05). Общая частота гипогликемии между группами не различалась, но в группе инсулина детемир частота тяжелой гипогликемии была на 72% ниже, а ночной гипогликемии – на 32% ниже, чем в группе инсулина гларгин (p < 0,05). Это подтверждает, что аналог инсулина детемир обеспечивает плоский и пролонгированный фармакодинамический профиль с высокой межиндивидуальной предсказуемостью действия. В группе инсулина гларгин отмечена большая прибавка массы тела (0,96 кг), чем в группе инсулина детемир (0,52 кг), но разница не была статистически значимой (p = 0,193) [15].
В 2007–2008 гг. были опубликованы результаты международного открытого проспективного исследования PREDICTIVETM, которое проводилось с целью оценки безопасности и эффективности инсулина детемир в рутинной клинической практике [16–18]. В исследовании приняли участие более 30 тыс. больных СД 1 и 2 типа, начавших лечение инсулином детемир. В когорте, включавшей 20 531 пациента из 11 стран мира, в начале лечения инсулином детемир зафиксировано 214 серьезных нежелательных явлений, среди которых была и выраженная гипогликемия [18]. Однако при сравнении с предыдущей терапией лечение инсулином детемир сопровождалось статистически значимым снижением частоты серьезной гипогликемии с 3 до 0,7 эпизодов у пациента в год, а также существенным снижением уровня HbA1c, глюкозы натощак, массы тела и колебаний уровня глюкозы крови. При этом 49% пациентов СД 1 типа и 77% пациентов СД 2 типа получали аналог инсулина детемир 1 раз в сутки, а 50 и 23% больных соответственно – 2 раза в сутки. Отмечено 9 случаев общих нежелательных явлений, из которых 6 были местными кожными реакциями. У больных с сахарным диабетом 2 типа, ранее получавших инсулин гларгин [17], инсулин детемир существенно снижал уровень HbA1c, вариабельность уровня глюкозы крови и массу тела. У больных диабетом 1 типа, входивших в европейскую когорту [17], замена инсулина гларгин на инсулин детемир также приводила к существенному снижению уровня HbA1c, глюкозы натощак и колебаний уровня глюкозы, но различий в массе тела выявлено не было.
Безусловный интерес представляет приведенная в работе Allen B. King [23] сводная таблица, включающая результаты различных исследований, посвященных оценке и сравнению инсулина НПХ и аналоговых инсулинов гларгин и детемир (табл. 1). Таким образом, основными отличительными особенностями инсулина детемир являются значимо меньшее влияние на прибавку массы тела, меньшая вариабельность уровня глюкозы и меньшая частота гипогликемии.
Когда и кому мы можем уверенно рекомендовать терапию аналогом инсулина детемир? Прежде всего пациентам с сахарным диабетом 2 типа, нуждающимся в начале инсулинотерапии с последующей возможной интенсификацией, которые ориентированы на измерение уровня гликемии натощак, а также имеющим избыточную массу тела. Необходимость соблюдения режима питания и физических нагрузок очевидна для пациентов с СД и является первым этапом в лечении данного заболевания. Однако достигнуть компенсации углеводного обмена только при соблюдении данных условий практически не удается. Частично это связано с поведением пациентов («знать не означает соблюдать»), но чаще, особенно при СД 2 типа, – с поздней диагностикой данного заболевания.
Критерии компенсации отличаются в разных странах мира. Так, по рекомендации Американской диабетологической ассоциации (ADA) целевой уровень глюкозы плазмы натощак должен составлять 5,0–7,2 ммоль/л, уровень глюкозы плазмы после еды (в любое время!) должен быть менее 10,0 ммоль/л. Американская ассоциация клинических эндокринологов (AACE) рекомендует достигать уровня глюкозы плазмы натощак (ГПН) менее 6,1 ммоль/л, уровня глюкозы плазмы после еды (через 2 часа) менее 7,8 ммоль/л. Международная диабетологическая федерация (IDF) предписывает уровень глюкозы плазмы натощак менее 5,5 ммоль/л, уровень глюкозы плазмы после еды (через 2 часа) менее 7,8 ммоль/л. Значимо отличаются и целевые значения НbА1с: ADA – 7%, AACE – 6,5%, IDF – 6,5%.
Для Российской Федерации критериями компенсации углеводного обмена являются уровень НbА1c менее 7%, ГПН менее 6,5 ммоль/л в капиллярной крови [19]. Первым этапом в лечении СД является диетотерапия, нормализация веса и увеличение физических нагрузок. При отсутствии достаточного эффекта на втором этапе добавляют ПССП разных групп. Необходимо отметить, что большинство препаратов стимулируют глюкозонезависимую секрецию инсулина и могут «приводить» к истощению β-клеток. Кроме того, многие из них имеют длительный период действия (более 12 часов), что, в свою очередь, приводит к увеличению аппетита, прибавке веса и усилению инсулинорезистентности. Формируется «порочный» круг декомпенсации СД. В 2010 г. на базе ЭНЦ РАМН под руководством И.И. Дедова был проведен скрининг пациентов, страдающих СД. При оценке НbА1с отмечено, что большинство пациентов имеют уровень данного показателя выше 8% (рис. 2, 3).
Большинство пациентов находились на терапии ПССП и только 14,2% были на терапии с применением инсулина. Достоверно известно, что инсулин обладает протективным воздействием на β-клетки и при рациональном подборе дозы приводит к компенсации углеводного обмена при относительно сохранной массе тела. Своевременное назначение инсулина способствует улучшению гликемического профиля, как тощакового, так и постпрандиального. При развитии СД 2 типа нарушается не только 1 фаза секреции инсулина, но и базальная продукция. Для данных пациентов часто бывает достаточным восстановить нормальный базальный уровень инсулина для возможной коррекции постпрандиальной гликемии. Целесообразным является начало инсулинотерапии при уровне HbA1c более 7,5% или при гликемии натощак более 7,5–8,0 ммоль/л (на фоне предшествующей терапии максимальными дозами или комбинации ПССП) [19]. Начальная доза терапии инсулином детемир определяется фармакологическими свойствами. По рекомендации фирмы производителя («Ново Нордиск») она составляет 0,2 ЕД/кг массы тела [24].
Были проведены несколько исследований по определению оптимальных доз при начале терапии аналогом инсулина детемир. Исходя из полученных данных и нашего опыта можно рекомендовать начинать терапию аналогом инсулина детемир с 10–12 ЕД один раз в день или с перерасчетом на массу тела 0,2–0,4 ЕД на килограмм реального веса, но не более 15 ЕД при стартовой терапии в одну инъекцию. Титрация дозы должна проводиться раз в неделю (± 2–4 Ед) до достижения целевых значений (гликемия натощак от 5,0 до 6,5 ммоль/л). Наши данные согласуются с данными Lawrence Blonde и соавт., которые указывают, что 64% пациентов достигли уровня НbА1c ниже 7% при титрации дозы аналогового инсулина детемир, вводимого один раз в день [21]. В ряде случаев можно рекомендовать проведение коррекции (снижение доз) принимаемых ПССП и/или смену группы данных препаратов. Учитывая минимальный риск развития гипогликемических состояний, детемир оптимально подходит пожилым пациентам, а также пациентам любого возраста, ведущим активный образ жизни.
Заключение
- Аналог инсулина пролонгированного действия детемир является оптимальным для коррекции гликемического профиля у пациентов СД 2 типа.
- Назначение данной терапии оптимально при отсутствии компенсации углеводного обмена на фоне соблюдения режима питания и физических нагрузок и использования ПССП.
- Применение инсулина детемир в оптимальных дозах, при правильной титрации практически не вызывает развития гипогликемических состояний.
- Данный препарат не способствует увеличению массы тела.
- Достижение компенсации углеводного обмена возможно при назначении инсулина детемир один раз в день.
NB
Терапию аналогом инсулина детемир можно рекомендовать пациентам с сахарным диабетом 2 типа, нуждающимся в начале инсулинотерапии с последующей возможной интенсификацией, которые ориентированы на измерение уровня гликемии натощак, а также имеющим избыточную массу тела. Одним из препаратов инсулина, рекомендованных к применению для достижения компенсации углеводного обмена у пациентов, страдающих СД 2 типа, является детемир (Левемир®, компания «Ново Нордиск»).

![Табл. 1. Сравнение инсулина детемир с инсулином НПХ и инсулином гларгин [23]*.](/upload/resize_cache/iblock/7b2/195_350_1/7b2b39b10076785c01437641dda41a1b.png)
![Рис. 2. Структура лечения больных с СД 2 типа [20].](/upload/resize_cache/iblock/67e/195_350_1/67e7f39b38b4d75051afa1e69db35138.png)
![Рис. 3. Соотношение больных с СД 2 типа с различным уровнем HbA1c [20].](/upload/resize_cache/iblock/761/195_350_1/761d86b1740589d05ceb2bb2fa2cac48.png)