Сахарный диабет типа 2: возможно ли повернуть течение вспять?
- Аннотация
- Статья
- Ссылки


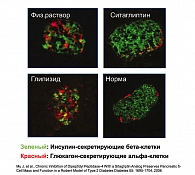


Функция бета-клеток и прогрессирование сахарного диабета типа 2
Сахарный диабет (СД) является глобальной проблемой современной медицины. Увеличение числа больных СД происходит в основном за счет пациентов с СД второго типа (СД типа 2). К 2025 г. ожидается удвоение числа больных по сравнению с концом прошлого века. Это приведет к колоссальному возрастанию расходов на ведение этой категории больных. Пациенты, с которыми мы сталкиваемся каждый день, – это больные с впервые выявленным СД, уже имеющие терминальные осложнения СД. К сожалению, это реалии.
Более чем в 90% случаев СД типа 2 связан с увеличением массы тела. Две трети больных СД типа 2 имеют ИМТ ³ 27 кг/м2. Существует зависимость между ИМТ и относительным риском развития СД типа 2: риск возрастает при увеличении ИМТ с 27 до 29 кг/м2 в 7-28 раз у женщин и 7 раз у мужчин. В настоящее время известно, что окружность талии – тот параметр, который более, нежели ИМТ, сопряжен с развитием инсулинорезистентности.
Как мы знаем благодаря исследованию UKPDS, хрестоматийному для всех диабетологов, контроль диабета может быть связан с прогнозом развития сосудистых осложнений СД. Снижение гликированного гемоглобина (HbA1с) на 1% сопровождается значительным уменьшением риска развития микрососудистых осложнений (на 37%). Тот пациент, у которого хороший контроль диабета, проживет дольше примерно на 20 лет, и что самое главное – он проживет большую часть своей жизни без осложнений СД. Расходы на ведение этого больного на каком-то этапе возрастут за счет интенсификации лечения, но в конечном итоге будут значительно ниже за счет уменьшения вероятности развития осложнений.
Алгоритм лечения больных СД типа 2 предполагает интенсификацию лечения при определенной цифре HbA1с, составляющей 7%. По данным исследования UKPDS, эта традиционная терапия, которую мы интенсифицируем, к сожалению, не позволяет достичь стабильного гликемического контроля, т.е. с течением времени большинство больных оказываются далеко от цели лечения СД типа 2, которая декларирована Американской диабетической ассоциацией (7%) или Европейской диабетической ассоциацией (6,5% по уровню HbA1с). Больные, имеющие HbA1с > 8% (это выраженная декомпенсация заболевания), составляют больше половины российской популяции.
Инсулинорезистентность лежит в основе развития тех состояний, которые в дальнейшем приводят к СД, но ключевым моментом в развитии и прогрессировании заболевания является нарушение функции островковых клеток. Утрата функции бета-клеток происходит значительно раньше, чем мы диагностируем заболевание. При этом потери и снижение функции бета-клеток продолжаются во времени развития заболевания и в целом составляют около 6% в год.
У кавказоидов и лиц других этнических групп с высоким риском СД проводилось исследование, где в условиях повышенного уровня гликемии оценивалась секреторная активность инсулярного аппарата. И в отличие от здоровых лиц, у которых был нормальный инсулиновый ответ, у больных с СД и даже у больных с нарушенной толерантностью к глюкозе в ответ на гипергликемию практически отсутствовала реакция со стороны бета-клеток, т.е. функциональная реакция, связанная с повышением секреции инсулина. Таким образом, прогрессирование заболевания связано в основном со снижением функциональной активности бета-клеток, о чем также свидетельствует и исследование UKPDS.
В подходах к лечению больных СД традиционно очень много внимания уделяется вопросам восстановления инсулярного ответа на биохимические колебания, однако ключевую роль, как в развитии заболевания, так и в его прогрессировании, играет прогрессивное снижение функции и массы бета-клеток.
Масса бета-клеток – состояние островкового инсулярного аппарата, которое подвержено определенной динамике в зависимости от активности процессов апоптоза и репликации, неогенеза – образования бета-клеток из клеток-предшественников (в основном это клетки эндокринной части протоков поджелудочной железы).
В 2003 г. на аутопсийном материале 124 больных и здоровых людей обследовался относительный объем бета-клеток по отношению к общему объему ткани поджелудочной железы. Это больные, наблюдающиеся в одной клинике в течение определенного промежутка времени. Естественно, было ожидаемо и получено, что у больных СД имеет место значительное уменьшение массы бета-клеток по сравнению с лицами без ожирения, без избыточной массы тела и без СД. Однако было показано, что снижение массы бета-клеток происходит не только у больных с СД, но и у лиц с нарушенной толерантностью к глюкозе, что подчеркивает значимость данного процесса на ранних этапах развития заболевания.
В этом исследовании пришли к следующему заключению: у лиц с СД и с ожирением, и с нормальной массой тела вне зависимости от лечения наблюдается значительное снижение массы бета-клеток. В основе снижения массы бета-клеток лежит повышенная активность процесса апоптоза, и соответственно усилия по угнетению повышенного апоптоза могли бы послужить основой для восстановления или сохранения массы бета-клеток.
Говоря о том, каков у нас терапевтический потенциал, а речь пойдет о инкретиннаправленной терапии, надо отметить, что в этой области сейчас очень много исследований. На мой взгляд, очень важно не упустить возможность раннего воздействия на фактор снижения функции бета-клеток как определяющий дальнейшее развитие и прогрессирование СД типа 2.
Янувия: улучшение функции бета-клеток и эффективное снижение гликемии
Основное место Янувии в терапии сахарного диабета 2 типа – это комбинация с метформином, для которой доказана высокая эффективность. У пациентов, получавших стартовую комбинированную терапию Янувией в дозе 100 мг и метформином в дозе 2000 мг в сутки к 54-й неделе на фоне комбинированной терапии было достигнуто снижение HbА1c в среднем на 1,8% (исходный уровень HbА1c 8,7%). При этом в подгруппе с высоким исходным уровнем HbА1c (среднее 10,4%) было достигнуто снижение на 3,1%. Впечатляющий показатель эффективности лечения: целевых значений HbА1c < 7% достигали 77% пациентов (рисунок 1).
Все это говорит о том, что настало время более раннего старта комбинированной терапии.
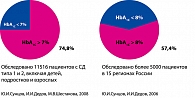
В официальных данных, опубликованных академиком И.И. Дедовым и профессором Ю.И. Сунцовым, касающихся компенсации больных СД типа 2 в России, говорится, что только 25% взрослых пациентов с СД типа 2 достигают целевых значений HbA1C, следовательно, большинство пациентов не компенсированы или компенсированы не так хорошо, как нам бы того хотелось (рисунок 2). Необходимо подчеркнуть, что в мировой практике также отмечается, что на самом деле менее 50% взрослых пациентов СД типа 2 в США достигает целевых значений HbA1C, и это при том, что берется цифра целевых значений HbA1C, равная 7%.
Говоря о тактике лечения, надо отметить, что цели терапевтического вмешательства могли бы быть сформулированы следующим образом: 1) уменьшение инсулинорезистентности; 2) улучшение функции бета-клеток поджелудочной железы; 3) подавление продукции глюкозы печенью (хотя контролируют три основных параметра: гликемия натощак, гликемия после еды и гликированный гемоглобин).
Наряду с патологией бета-клеток необходимо обязательно учитывать и патологию альфа-клеток поджелудочной железы. И если на уровне бета-клеток происходит деструкция, то на уровне альфа-клеток – усиление секреции глюкагона, что дает в практическом смысле чрезвычайно важную информацию. Повышенный уровень глюкагона приводит к повышению продукции глюкозы в печени, что и является фактором повышения уровня гликемии натощак. Далее – дефицит инсулина, который должен подавлять гиперпродукцию глюкозы печенью. Таким образом, у наших пациентов наблюдается ухудшение условий утилизации глюкозы на уровне периферической ткани. И это все формирует состояние хронической гипергликемии, иначе – глюкозотоксичности. Хроническая глюкозотоксичность поддерживается и еще одним источником – постпрандиальной гипергликемией.
Еще 7-10 лет тому назад после установления диагноза обозначились цели терапии – считалось, что монотерапия должна нас устроить. Назначался хороший препарат глибенкламид (золотой стандарт 5 мг), и таким образом продвигались к достижению цели. Если не удавалось достичь целевых значений HbA1C – увеличивали дозу глибенкламида до 10 мг, затем до 20 мг, затем добавляли метформин, к 15 году терапии добавляли инсулин. Таким образом, проходили 15 лет жизни пациентов. Эта тактика лечения сахарного диабета долгие и долгие годы использовалась во всем мире и отражала традиционную точку зрения – терапия пероральными препаратами так долго, как только возможно. Использовался даже такой термин – лечение до неудачи. Не до цели, а до неудачи, потому что такая тактика не может привести к хорошему результату. Подобная тактика терапии способствует стабильно высокому уровню гликированного гемоглобина, и это не может нас никоим образом устраивать. С прогрессированием заболевания становится все труднее достичь целей лечения.
При этом функция бета-клеток поджелудочной железы прогрессирующим образом уменьшается, несмотря на то, что назначается сначала монотерапия, потом два препарата, потом комбинация с инсулином, потом просто инсулинотерапия. В итоге эти 15 лет – потерянное время.
Всего 6 лет тому назад один из величайших диабетологов и популярнейших специалистов в мире профессор Ralph De Fronzo опубликовал алгоритм терапии применительно к контролю гликемии, решив вопрос неадекватной секреции глюкагона и снижения функции бета-клеток.
Теперь это решение у нас есть – инкретины, которые очень активно входят в практику эндокринологов. Теперь фактически возможности терапии сахарного диабета расширяются, и ингибиторы ДПП-4 отвечают как минимум двум целям терапевтического вмешательства из трех. Недалек тот день, когда определять уровень гликированного гемоглобина у наших пациентов мы будем не менее 4 раз в год и понимать, что надо делать, а именно на ранних этапах назначать комбинированную терапию.
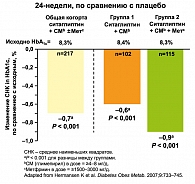
Механизм действия ситаглиптина (Янувия), ингибитора ДПП-4 позволяет осуществлять гликемический контроль. Наиболее популярная комбинация – сочетание с метформином. Комбинация ситаглиптина и метформина комплементарно действует уже на все три терапевтические цели при СД типа 2, а действие метформина как инсулинового сенситайзера напрямую значительно снижает избыточную продукцию глюкозы печенью. Метформин повышает чувствительность к инсулину на уровне мышечной ткани у пациентов СД типа 2. Ситаглиптин оказывает положительное действие на массу и функцию бета-клеток поджелудочной железы, позволяя замедлить прогрессию заболевания. Комбинация сильнее, чем метформин и ситаглиптин в отдельности – совместный прием приводит к более высоким уровням ГПП-1. Комбинация ситаглиптина и метформина ничуть не хуже, чем известная нам комбинация сульфонилмочевина + метформин: данные исследования вполне сопоставимы. Важно, что комбинация ситаглиптин + метформин вызывает снижение веса и меньшую частоту гипогликемий, здесь разница между группами испытуемых уже ощутимая, а это вопрос эффективности и безопасности терапии. В стартовой терапии комбинацией ситаглиптин + метформин доказано взаимодополняющее влияние на снижение уровня гликированного гемоглобина (Goldstein B. et al., 2007) (рисунок 3), значительное снижение постпрандиальной гликемии и гликемии натощак, улучшение функции бета-клеток (индекс HOMA-b) на сочетание метформин 1000 мг и ситаглиптин 100 мг/сут. (Williams–Herman D. et al., 2007). В исследовании Farilla et al. приводятся данные о том, что тройная комбинация с глимепиридом показывает еще большую эффективность. Хроническое воздействие ситаглиптина восстанавливает почти до нормы баланс бета- и альфа-клеток. Янувия (ситаглиптин) предоставляет гибкие возможности для широкого круга пациентов с СД типа 2.
В настоящее время можно рекомендовать как добавление Янувии к метформину всем пациентам с уровнем HbA1C более 7% (или гликемии натощак более 6,5 ммоль/л), так и стартовую комбинированную терапию Янувией и метформином пациентам с впервые выявленным сахарным диабетом 2 типа. При таком раннем назначении терапии врач может быть уверен, что пациент проведет большее время жизни с приемлемым уровнем гликемии.
Фраза, которой я люблю заканчивать свои выступления, звучит так: «Долой клиническую инерцию – ранняя интенсификация лечения, лечение до цели, пожизненное обучение пациентов и членов их семей!» От того, как мы сможем использовать предоставляемые сегодня возможности, зависят продолжительность и качество жизни наших пациентов.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.