Современные аспекты патофизиологии и лечения эректильной дисфункции после вмешательства на органах малого таза
- Аннотация
- Статья
- Ссылки

Рак предстательной железы (РПЖ) является одной из наиболее распространенных злокачественных опухолей у пожилых мужчин. После внедрения в рутинную практику определения уровня простатспецифического антигена (ПСА) увеличилась доля локализованных форм РПЖ. Излечение данных пациентов возможно при выполнении операции радикальной простатэктомии (РПЭ). Эректильная дисфункция (ЭД) является наиболее частым осложнением после РПЭ и встречается у 29-100% мужчин после данной операции (1). ЭД значительно усугубляет качество жизни пациентов с сохраненной потенцией перед операцией.
Патогенез эректильной дисфункции после рпэ и рцэ
Согласно определению, предложенному Национальным институтом здоровья США, эректильная дисфункция определяется как неспособность достигать или поддерживать эрекцию, достаточную для совершения удовлетворительного сексуального действия (2).
Радикальная прост- и цистатэктомия подразумевает под собой полное удаление предстательной железы, семенных пузырьков и регионарных лимфатических узлов.
Основной причиной возникновения ЭД после РПЭ является денервация пещеристых тел полового члена, вследствие повреждения во время операции кавернозных нервов, входящих в состав сосудистонервных пучков. Последние проходят по заднебоковой поверхности предстательной железы и удаляются с целью достижения радикальности операции. Сохранение одного или двух кавернозных нервов возможно при применении нервосберегающей техники РПЭ (НСРПЭ), но данная операция возможна лишь у ограниченной части пациентов и противопоказана при обширном поражении предстательной железы злокачественной опухолью. Но даже при выполнении НСРПЭ у большинства пациентов в раннем послеоперационном периоде спонтанные эрекции отсутствуют. Восстановление нормальной эректильной функции может происходить на протяжении двух лет. Данный феномен связан с возникновением нейропраксии, возникающей вследствие травмирования кавернозных нервов, несмотря на выполнение нервосберегающей техники РПЭ. Отсутствие спонтанных эрекций приводит к развитию кавернозного фиброза, который, в свою очередь, приводит к нарушению функционального состояния кавернозных тел и тем самым к удлинению периода восстановления, снижению или отсутствию эрекции. По мнению ряда авторов, основной причиной развития фиброза кавернозных тел является гипоксия кавернозной ткани, развивающаяся из-за снижения притока оксигенированной крови вследствие отсутствия спонтанных эрекций (3-5). Развивающийся фиброз кавернозной ткани приводит к поддерживанию гипоксии. Таким образом, образуется так называемый порочный круг.
Ориентируясь на механизм развития изменений кавернозной ткани, с профилактической целью для более раннего восстановления эрекции, применяются интракавернозные инъекции вазоактивных веществ. Одним из таких препаратов явился простагландин Е (альпростадил), который продемонстрировал свою эффективность в уменьшении периода восстановления эрекций (6). Так же свою эффективность продемонстрировали ингибиторы фосфодиэстеразы 5 типа (иФДЭ-5). Эффект данных препаратов (силденафил, варденафил, тадалафил) связан с блокированием изоэнзима ФДЭ-5 и тем самым сохранением на высоком уровне цГМФ. Все три препарата продемонстрировали так же свою эффективность в раннем возвращении спонтанных эрекций после НСРПЭ (7, 8, 9) и профилактике кавернозного фиброза (10). Но эффект иФДЭ-5 типа на торможение фиброза не может быть объяснен улучшением оксигенации кавернозной ткани, как при применении вазоактивных препаратов. Это позволило нам выдвинуть гипотезу, что на фоне развития нейропраксии кавернозных нервов после РПЭ основной причиной развития кавернозного фиброза является стресс-реакция всех клеточных элементов пещеристой ткани, как универсальный механизм в ответ на их денервацию. Соответственно, применение препаратов, возмещающих дефицит оксида азота в кавернозных телах пениса, может предотвратить развитие в них фиброза и ускорить восстановление спонтанных эрекций после НСРПЭ. Таким препаратом может быть синтезированный эндогенный донатор NO – динитрозильный комплекс железа (ДНКЖ).
Материалы и методы
Материалом для исследований явились экспериментальные животные – крысы самцы линии Wistar, исходным весом от 250 до 300 г, возрастом 3-4 месяца.
Все животные были разделены на три группы. Первую группу составили 10 животных, которым выполнялась операция по пересечению кавернозных нервов. Вторую группу составили 10 животных, которым выполнялось пересечение кавернозных нервов с интра- и последующим послеоперационным (2 раза в неделю) интракавернозным введением донатора оксида азота – динитрозильного комплекса железа. Контрольную группу составили 6 животных, которым выполнялся доступ до задней поверхности предстательной железы, но пересечение кавернозных нервов не производилось. Забор биологического материала осуществляли через 3 и 6 месяцев от начала эксперимента (таблица 1).
Обезболивание для операции проводили внутрибрюшинным введением препарата хлоралгидрат из расчета 300 мг на 1 кг массы крысы. Соблюдая правила асептики и антисептики, нижнесрединным разрезом послойно выполнялся доступ до мочевого пузыря. Мочевой пузырь и семенные пузырьки смещались книзу и обнажалась задняя поверхность предстательной железы. Кавернозные нервы располагались по заднелатеральным поверхностям простаты. Далее выполнялось пересечение последних холодным ножом на протяжении 5 мм. Рана послойно ушивалась. После ушивания в группе 2 выполнялась интракавернозная инъекция раствора ДНКЖ 0,5 ммоль/л – 0,1 мл. В последующем интракавернозное введение производилось 2 раза в неделю. Продолжительность операции составляла около 20-30 минут.
С целью определения изменений кавернозной ткани, вследствие ее денервации и их профилактики препаратом ДНКЖ, мы использовали электронно-микроскопические, иммуногистохимические и морфометрические методы исследования.
Результаты
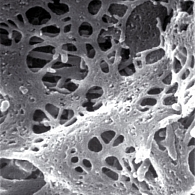
Пещеристые тела полового члена крысы, так же как и человека, имеют лакунарное строение (рисунок 1). Стенка лакун кавернозной ткани представлена содружеством нескольких видов тканей, а именно, эндотелия, который принадлежит к эпителиальной ткани, а также гладкомышечных клеток, фибробластов и перицитов (адвентициальных клеток), составляющих наружный контур. Указанные выше образования относятся к тканям внутренней среды.
Монослой эндотелия пещеристых тел полового члена экспериментальных животных представлен веретенообразными клетками, которые вытянуты по длиннику пещеристых тел и имеют выраженную гексагональную симметрию, т.е. каждая клетка имеет, как правило, шесть плотных контактов (гексагон). Характерной особенностью данной сосудистой организации является обилие перемычек, которые образуют лабиринт, что имеет важное функциональное значение в момент эрекции.
Опорная структура стенки пещеристых тел имеет циркулярно расположенные гладкомышечные клетки.
В адвентициальной оболочке расположены фибробласты, малодифференцированные клетки и перициты (адвентициальные клетки).
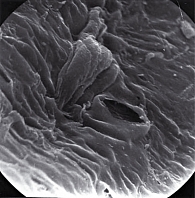
Через 3 и 6 месяцев от начала опыта в группе 1 мы обнаружили повышенную потенцию эндотелиальных клеток к пролиферации. У интактных животных в поле зрения мы обнаруживали потенцированные к делению клетки, меченные моноклональными антителами, в количестве 1,07 ± 0,01 в поле зрения стандартного увеличения (масляная имерсия). Через 3 месяца количество клеток, потенцированных к делению, в группе 1 увеличилось в 3 раза (3,14 ± 0,07), а через 6 месяцев в 5 раз и составило 5,17 ± 0,11 (р < 0,05). Визуально при анализе сканограмм группы 1 выявлено нарушение контактного торможения клеточного пласта, появление щелей между эндотелоцитами, что создает возможности для их повышенной пролиферации, «заползания и нахлестывания» эндотелиальных клеток друг на друга (рисунок 2).
При исследовании гладких миоцитов у интактных животных в поле зрения обнаружено потенцирование к делению у 2,01 ± 0,06 клеток. У экспериментальных животных в группе 1 через 3 месяца от начала опыта и тем более через 6 месяцев пролиферативная активность снизилась соответственно 1,79 ± 0,04 и 1,14 ± 0,03, т.е. мы наблюдали снижение митотической активности гладких миоцитов после денервации почти в два раза (р < 0,05).
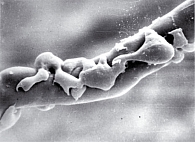
Большой интерес представило исследование синтетической активности коллагеназы в гладких миоцитах. Так, в группе 1 через 3 и особенно через 6 месяцев с помощью моноклональных антител была выявлена коллагеназа в гладких мышечных клетках, что с морфофункциональной точки зрения возможно только в клетках фибробластического ряда. В количественном отношении через 3 месяца количество гладкомышечных клеток с синтетической активностью коллагеназы составило 5,18 ± 0,64 в поле зрения, а через 6 месяцев – 6,81 ± 1,19. Визуально при исследовании сканограмм первой группы мы наблюдали изменение формы гладких мышечных клеток, отдельные из которых имели звездчатую или округлую структуру, более характерную для клеток фибробластного ряда – перицитов (рисунок 3).
С помощью методов иммуногистохимии у животных группы 1 была выявлена выраженная митотическая активность фибробластов, особенно через 6 месяцев от начала эксперимента. Так, если у интактных животных в поле зрения обнаруживали фибробласты, содержащие циклин в количестве 4,18 ± 0,23, то в группе 1 через 3 месяца – 6,19 ± 0,97, а через 6 месяцев – 8,21 ± 1,13. Таким образом, денервация кавернозных тел в группе 1 привела к существенному увеличению потенции фибробластов к делению, синтезу межклеточных веществ, коллагена по сравнению с контрольной группой. Данные изменения свидетельствуют о развитии облитерации стенок пещеристых тел, что отрицательно сказывается на их кровенаполнении.
В серии экспериментов с интракавернозным введением препарата ДНКЖ животным из группы 2 спустя 3 месяца мы обнаружили определенные закономерности в сравнении с группой прооперированных животных, не получавших данный препарат. Так, нами не отмечено усиленной пролиферации эндотелиоцитов пещеристых тел, не обнаружено «наползания» эндотелиальных клеток друг на друга с образованием холмиков. Также не отмечено снижение митотической активности гладких миоцитов и повышенной пролиферативной активности фибробластов адвентициальной оболочки. Что самое главное, в гладких миоцитах мы не обнаружили синтетической активности коллагеназы, только в отдельных трехмесячных препаратах можно отметить ее обнаружение в количестве 0,47 ± 0,01. В цифровом выражении пролиферативная активность эндотелиоцитов выражалась цифрами 1,97 ± 007; в гладкомышечных клетках 2,56 + 0,09, а фибробластов 3,97 + 0,11 клеток в поле зрения. Сравнение результатов показывает близость цифровых данных группы интактных животных.
При оценке пещеристой ткани полового члена экспериментального животного после денервации и леченного препаратом ДНКЖ (группа 2) в течение 6 месяцев пролиферативная активность эндотелия составила 1,74 + 0,05 клеток в поле зрения стандартизированного увеличения. Соответственно, митотическая активность в гладкомышечных клетках находилась в норме (2,34 ± 0,12) и фибробласты адвентициальной оболочки имели пролиферативную активность, близкую к норме (4,01 ± 0,17). В гладкомышечных клетках мы не обнаружили синтетической активности коллагеназы.
Обсуждение
Радикальная простат- и цистэктомия на сегодняшний день является доминирующим методом лечения локализованной формы рака предстательной железы и мышечноинвазивного рака мочевого пузыря. Эректильная дисфункция является наиболее частым осложнением данной операции вследствие иссечения кавернозных нервов. Применение нервосберегающей техники не приводит к сохранению потенции в послеоперационном периоде у всех пациентов. Проблема развития фиброза кавернозных тел у данной категории больных активно изучается на протяжении последних двух десятков лет. Основные изменения кавернозной ткани, возникающие после РПЭ, изучены на экспериментальных животных. На сегодняшний день известно, что пересечение кавернозных нервов крысы приводит к достоверному уменьшению NOS-позитивных нервных волокон (11), снижению соотношения гладкомышечных клеток к коллагеновым волокнам, увеличению экспрессии трансформирующего фактора роста – β1 (12), увеличению гипокси-индуцибильного фактора-1α, синтеза коллагена III (4), снижению веса пениса крысы, уменьшению содержания ДНК, активации апоптоза (13), уменьшению NOS-I, отсутствию изменений NOS-II и NOS-III (14), увеличению мРНК, экспрессии сульфида гликопротеида-2, внутриядерной дефрагментации ДНК, появлению апоптозных ядер (15).
В нашем эксперименте мы наблюдали достоверное как количественное, так и качественное изменение всех пулов клеток кавернозной ткани. Так, денервация полового члена приводит к нарушению монослоя эндотелия, образованию несвойственных эндотелиальных структур, что, бесспорно, приводит к нарушению кровотока в синусоидах. Пересечение кавернозных нервов привело к снижению эластичности стенки кавернозных тел вследствие изменений количества, нарушения функции и трансформации гладкомышечных клеток. Все это бесспорно приводит к снижению сократимости и способности к расслаблению стенок кавернозных синусоидов и, соответственно, к нарушению выполнения ими нормальной функции.
Рядом авторов было продемонстрировано, что основной причиной данных изменений является развивающаяся гипоксия кавернозной ткани. Но данным фактом нельзя объяснить положительное влияние препаратов иФДЭ-5 на предотвращение патологических изменений кавернозной ткани. Данный факт позволил нам выдвинуть гипотезу, что дополнительной, а возможно, и главной причиной кавернозного фиброза является патологическая реакция клеток кавернозной ткани в ответ на их денервацию. Следовательно, применение NO-заместительной терапии привело бы к профилактике кавернозного фиброза и более раннему возвращению эректильной функции после операции.
В нашем эксперименте интракавернозное введение донатора оксида азота препарата ДНКЖ в группе 2 привело к стабилизации клеточной ситуации. Отсутствие синтетической активности коллагеназы в гладкомышечных клетках, по сравнению с группой 1, свидетельствует о торможении трансформации гладкомышечной ткани в соединительную и о нарушении функциональной особенности полового члена. Схожие результаты получены при биопсии кавернозных тел мужчин, перенесших РПЭ и принимавших иФДЭ-5 в послеоперационном периоде [10]. Преимущество донаторов NO перед иФДЭ-5 заключается в том, что последние поддерживают уровень вырабатываемого оксида азота, а ДНКЖ может компенсировать недостаток или полное отсутствие последнего при полном пересечении кавернозных нервов.
Выводы
Травма или полное пересечение кавернозных нервов во время операции на органах малого таза является основной причиной ЭД после операции, а соответственно, и снижения качества жизни пациентов. Данное исследование продемонстрировало, что развитие кавернозного фиброза происходит вследствие денервации пещеристых тел, и следовательно, отсутствия в кавернозной ткани главного медиатора эрекции – оксида азота. Результаты применения динитрозильного комплекс железа, являющегося синтезированным аналогом эндогенного донатора NO, продемонстрировало очередные биологические свойства оксида азота. Восстановление уровня последнего в кавернозной ткани является основной целью при желании восстановить эректильную функцию после РПЭ. Проведение заместительной терапии оксидом азота, посредством интракавернозного введения донора NO (ДНКЖ), приводит к предотвращению кавернозного фиброза и, следовательно, к профилактике ЭД и ускоряет возвращение достойного качества жизни пациентов после РПЭ.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.