Современные подходы к хирургическому лечению объемных образований придатков матки у детей и подростков
- Аннотация
- Статья
- Ссылки
- English
Материал и методы. Проведен анализ публикаций, представленных в базах данных PubMed, Scopus, Embase и eLibrary за период 2015–2025 гг. В обзор включены систематические обзоры, проспективные и ретроспективные исследования, клинические рекомендации и описания серий клинических случаев.
Результаты. Новообразования придатков матки у пациенток детского и подросткового возраста регистрируются относительно редко (в среднем 2,6 случая на 100 тыс. девочек в год), однако обладают высокой клинической значимостью из-за риска малигнизации и потенциального влияния на репродуктивное здоровье. По данным литературы, злокачественные опухоли выявляются в 3–8% случаев, но у девочек до менархе доля злокачественных образований может достигать 30–40%. В большинстве случаев образования имеют доброкачественный или функциональный характер. Ключевым этапом при выборе лечебной тактики является точная предоперационная оценка риска малигнизации. Современные подходы к лечению объемных образований придатков матки у детей и подростков ориентированы на органосохраняющие и минимально инвазивные хирургические вмешательства. Обязательная оценка онкологического риска на предоперационном этапе позволяет снизить травматичность оперативного лечения, повысить его безопасность и максимально сохранить овариальный резерв пациенток.
Заключение. Персонализированный подход к хирургическому лечению объемных образований придатков матки у несовершеннолетних должен сочетать высокую точность предоперационной диагностики, онкологическую настороженность и стремление к максимальному сохранению репродуктивного потенциала.
Материал и методы. Проведен анализ публикаций, представленных в базах данных PubMed, Scopus, Embase и eLibrary за период 2015–2025 гг. В обзор включены систематические обзоры, проспективные и ретроспективные исследования, клинические рекомендации и описания серий клинических случаев.
Результаты. Новообразования придатков матки у пациенток детского и подросткового возраста регистрируются относительно редко (в среднем 2,6 случая на 100 тыс. девочек в год), однако обладают высокой клинической значимостью из-за риска малигнизации и потенциального влияния на репродуктивное здоровье. По данным литературы, злокачественные опухоли выявляются в 3–8% случаев, но у девочек до менархе доля злокачественных образований может достигать 30–40%. В большинстве случаев образования имеют доброкачественный или функциональный характер. Ключевым этапом при выборе лечебной тактики является точная предоперационная оценка риска малигнизации. Современные подходы к лечению объемных образований придатков матки у детей и подростков ориентированы на органосохраняющие и минимально инвазивные хирургические вмешательства. Обязательная оценка онкологического риска на предоперационном этапе позволяет снизить травматичность оперативного лечения, повысить его безопасность и максимально сохранить овариальный резерв пациенток.
Заключение. Персонализированный подход к хирургическому лечению объемных образований придатков матки у несовершеннолетних должен сочетать высокую точность предоперационной диагностики, онкологическую настороженность и стремление к максимальному сохранению репродуктивного потенциала.
Введение
Объемные образования придатков у детей и подростков представляют сложную и актуальную клиническую проблему в силу возрастающей частоты их выявления в педиатрической и подростковой гинекологической практике. Среди всех новообразований придатков матки у детей и подростков наиболее распространены опухоли и кисты яичников.
По данным разных авторов, доля опухолевых и опухолеподобных образований яичников составляет от 1,0 до 4,6% всех гинекологических заболеваний у пациенток в возрасте до 18 лет [1, 2]. Несмотря на сравнительно низкую распространенность (в среднем около 2,6 случая на 100 тыс. девочек в год), объемные образования придатков матки у пациенток детского и подросткового возраста ассоциируются с серьезными последствиями из-за риска малигнизации и потенциального неблагоприятного влияния на репродуктивное здоровье [3, 4].
Согласно данным современных систематических обзоров, злокачественные опухоли диагностируются в 3–8% случаев у несовершеннолетних и составляют около 1–2% всех онкологических заболеваний в педиатрической популяции [5]. При этом у девочек до наступления менархе доля злокачественных новообразований достоверно выше: до 30–40% опухолей яичников, выявляемых в этой возрастной группе, носят злокачественный характер. При своевременном начале лечения опухоли яичников у детей, включая злокачественные формы, характеризуются высоким уровнем благоприятного исхода: 5–10-летняя выживаемость достигает 80–90% [6]. Опухолевидные образования яичников у детей чаще всего обнаруживаются в пубертатном периоде, что обусловлено активацией гипоталамо-гипофизарно-гонадной оси и становлением овариально-менструальной функции, сопровождающимся циклическими гормональными колебаниями [7].
Новообразования яичников у пациенток детского и подросткового возраста в большинстве своем доброкачественные или функциональные. Диагностический этап играет решающую роль в выборе лечебной тактики, поскольку подходы к ведению пациенток с доброкачественными и злокачественными новообразованиями принципиально различаются и определяют как объем хирургического вмешательства, так и последующее сохранение репродуктивной функции [8, 9].
Классификация объемных образований придатков матки у детей
Классификация опухолей яичников у детей и подростков принципиально отличается от таковой у взрослых. В репродуктивной и перименопаузальной возрастных группах преобладают эпителиальные новообразования. В то же время у пациенток детского и подросткового возраста чаще выявляются функциональные кисты: фолликулярная киста, киста желтого тела, а также эндометриоидные кисты яичников и параовариальные кисты. Согласно классификации Всемирной организации здравоохранения (ВОЗ) (2020), такие кисты относятся к опухолевидным образованиям и составляют 39,5–70% всех иных новообразований [1, 5, 10]. Однако до менархе диагностика объемного образования требует повышенного внимания: хотя доброкачественные функциональные кисты встречаются даже в этом возрасте, наличие объемного образования и особенности клинико-инструментальной картины могут указывать на риск герминогенной или иной опухоли. Это определяет необходимость тщательной предоперационной оценки и онконастороженности [11–13].
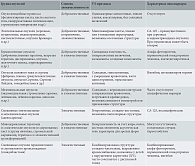
В таблице представлена современная гистологическая классификация опухолей и опухолеподобных образований придатков матки у детей и подростков, основанная на классификации ВОЗ (2020) и клинических рекомендациях Российского общества акушеров-гинекологов (2024) [10, 14]. В нее включены ультразвуковые признаки, характерные для различных нозологических групп, а также типичные онкомаркеры, которые имеют особую значимость на предоперационном этапе оценки [15, 16]. Такая систематизация способствует совершенствованию диагностики, поддерживает онкопрофилактическую настороженность и формирует базу для разработки персонализированных хирургических подходов у юных пациенток.
Клинические проявления и особенности диагностики
Клинические проявления и диагностика объемных образований яичников у детей и подростков не обладают патогномоничностью и часто характеризуются неспецифичностью симптоматики. Наиболее распространенным считается абдоминальный болевой синдром. Он регистрируется почти в 80% случаев и нередко обусловлен развитием осложнений, например перекрутом кисты [17, 18]. К менее распространенным проявлениям относят пальпируемое образование в брюшной полости, увеличение окружности живота, диспепсические проявления (тошнота, рвота), нарушения менструального цикла, а также признаки эндокринной дисфункции, включая преждевременное половое созревание при гормонально активных опухолях. Рост частоты обнаружения объемных образований яичников у девочек указывает на клиническую значимость проблемы дифференциальной диагностики опухолей данной локализации в детском и подростковом возрасте [19]. Диагностический алгоритм при подозрении на объемные образования яичников у данной категории пациенток базируется на сочетании визуализирующих методик и определения серологических онкомаркеров. Первым и наиболее доступным методом визуализации считается ультразвуковое исследование (УЗИ) органов малого таза, выполняемое трансабдоминальным доступом. Такой метод рекомендуется даже самым маленьким пациенткам. Трансвагинальное исследование допустимо лишь у подростков, ведущих половую жизнь.
УЗ-картина достаточно информативна для первичной оценки природы опухоли: простые кистозные образования небольших размеров и однородной структуры чаще свидетельствуют о доброкачественности. В то же время крупные образования (более 8–10 см), наличие солидных компонентов, перегородок и гетерогенность структуры требуют исключения злокачественной природы.
В ретроспективном исследовании (2023) анализировали диагностическую эффективность классификации O-RADS при УЗИ 163 опухолевых образований яичников у 159 пациенток в возрасте до 18 лет. Доброкачественные образования составили 89% (преобладали зрелые тератомы), злокачественные – 11% (в основном герминогенные опухоли). Размер злокачественных опухолей был статистически значимо больше (p = 0,012). Система O-RADS продемонстрировала высокую диагностическую точность (AUC = 0,944), чувствительность – 94,4%, специфичность – 86,2%. Малигнизация наблюдалась в 0% случаев при O-RADS 2, в 4,8% – при O-RADS 3, в 34,6% – при O-RADS 4 и в 72,7% случаев – при O-RADS 5. Анализ показал, что классификация O-RADS – надежный инструмент стратификации риска злокачественности у детей с опухолями яичников.
В сложных диагностических ситуациях или при наличии неоднозначных данных УЗИ выполняется магнитно-резонансная либо компьютерная томография, характеризующаяся высокой точностью в дифференциальной диагностике за счет детальной оценки структуры образования, наличия характерных жировых включений (например, при дермоидных кистах), а также признаков инвазии и метастазирования.
Важным дополнительным компонентом обследования является определение серологических онкомаркеров, таких как альфа-фетопротеин (АФП), лактатдегидрогеназа (ЛДГ), бета-субъединица хорионического гонадотропина человека (бета-ХГЧ), СА-125 и ингибин [20]. Повышение уровня АФП характерно для опухолей желточного мешка и встречается примерно у половины пациенток с незрелыми тератомами [11]. Повышенный уровень бета-ХГЧ наблюдается при хориокарциномах; имеет место примерно у 5% пациенток с дисгерминомой. СА-125 повышен чаще при эндометриоидных кистах. ЛДГ служит маркером дисгермином. Ее повышенный уровень регистрируется почти у 95% таких больных. Вместе с тем нормальные значения онкомаркеров не исключают наличия злокачественной опухоли, а их повышение не является абсолютным подтверждением малигнизации [13].
A.E. Lawrence и соавт. (2020) провели крупнейшее многоцентровое ретроспективное исследование с участием 819 пациенток в возрасте от двух до 21 года, перенесших хирургическое лечение по поводу опухолей яичников в десяти педиатрических центрах США за период 2010–2016 гг. В анализ вошли данные 401 пациентки с признаками высокого риска злокачественности образования на УЗИ (размер > 8 см, солидные компоненты, папиллярные разрастания, асцит и др.) и проведенной предоперационной оценкой опухолевых маркеров. У 78 (19,5%) из них, по данным гистологии, выявлены злокачественные опухоли (в том числе герминогенные – 50%, стромальные – 28%, эпителиальные – 15%). Средний размер злокачественных образований был достоверно выше, чем доброкачественных: 15,1 против 10,0 см (p < 0,001). Наиболее часто используемыми маркерами были АФП (94% пациенток), бета-ХГЧ (78%), CA-125 (54%) и ЛДГ (39%). Высокой чувствительностью обладала только ЛДГ – 98% у больных с подтвержденной злокачественной опухолью. Чувствительность остальных маркеров не превышала 60%. При этом маркеры AФП, раково-эмбриональный антиген, ингибины A и B имели высокую специфичность (до 100%) и положительную прогностическую ценность (86–100%). Следует отметить, что у 46% пациенток с гистологически подтвержденными злокачественными опухолями яичников все рутинно используемые серологические опухолевые маркеры (AФП, бета-ХГЧ, ЛДГ и др.) оставались в пределах нормы [4]. Окончательная верификация диагноза возможна исключительно после хирургического удаления опухоли и гистологического исследования материала, полученного интраоперационно.
Современные принципы хирургического лечения
Современная стратегия лечения опухолей яичников у детей и подростков направлена на достижение онкологического излечения при обязательном сохранении овариальной функции и репродуктивного потенциала. С учетом юного возраста пациенток приоритетным становится выбор щадящей хирургической тактики, нацеленной на сохранение гормональной активности яичников и поддержание фертильности в будущем. В случае доброкачественного характера образования стандартом хирургического лечения у пациенток детского и подросткового возраста является органосохраняющее вмешательство – кистэктомия или резекция яичника с сохранением функционирующей ткани [14]. Широкое внедрение малоинвазивных технологий сделало возможным выполнение подобных операций лапароскопическим доступом. Это обеспечивает более быстрое восстановление, меньшую выраженность болевого синдрома, лучший косметический результат и снижает риск формирования спаек по сравнению с лапаротомией.
По данным ретроспективных исследований, при доброкачественных опухолях лапароскопическая цистэктомия характеризуется низким уровнем рецидивов и повторных операций при сохранении функции яичника [21].
Несмотря на активное внедрение лапароскопических методов в практику лечения детей и подростков с доброкачественными опухолями яичников, данные международных исследований демонстрируют сохраняющуюся вариативность в выборе хирургической тактики.
В одном из клинических центров за период 2005–2018 гг. лапароскопический доступ был применен в 87% случаев оперативного лечения пациенток детского и подросткового возраста с опухолями яичников. При этом всем пациенткам удалось сохранить орган. Ни в одном случае не потребовалась конверсия в лапаротомию [3].
В ретроспективном исследовании H.B. Kim и соавт. (2015) были проанализированы данные 106 пациенток младше 20 лет, оперированных лапароскопически по поводу доброкачественных опухолей яичников [22]. Средний возраст составил 17,1 года (от восьми лет). В 65,1% случаев выполнены органосохраняющие вмешательства: кистэктомия (48,1%), аспирация содержимого (5,7%), коагуляция капсулы (4,7%) и деторсия (3,8%). У всех пациенток удалось сохранить яичниковую ткань. Ни в одном случае не потребовалась конверсия в лапаротомию. Интра- и послеоперационные осложнения не зарегистрированы.
Напротив, в исследовании R. Kapoor и соавт. (2024) с участием 30 пациенток в возрасте от 15 дней до 18 лет с опухолями яичников лапаротомия оставалась основным хирургическим доступом, особенно при подозрении на злокачественный процесс или при размере опухоли более 6 см [23]. Лапароскопические вмешательства были выполнены лишь 20% пациенток с доброкачественными образованиями небольших размеров. По данным авторов, выбор лапаротомии был обусловлен необходимостью соблюдения онкологических принципов хирургии, возможностью адекватной ревизии брюшной полости и предотвращения интраоперационной диссеминации при потенциально злокачественных новообразованиях.
X. Chen и соавт. (2025) провели ретроспективный анализ данных пациенток детского возраста с доброкачественными опухолями яичников, находившихся на лечении с 2014 по 2021 г. [24]. Средний возраст пациенток составил 9,1 ± 3,1 года. Всего выполнено 423 оперативных вмешательства, из них 362 с сохранением яичниковой ткани (органосохраняющее вмешательство) и 61 в объеме овариоэктомии. В послеоперационном периоде 337 пациенток находились под динамическим наблюдением от трех месяцев до девяти лет (в среднем 1,6 ± 1,8 года). Сохранение функции яичника после первичной органосохраняющей операции достигнуто в 94,4% случаев. Общая частота рецидива составила 3,9% (13 из 337). При этом в большинстве случаев (84,6%) рецидив выявлен в течение первых трех лет. У десяти пациенток рецидив диагностирован при плановом УЗ-контроле без клинической симптоматики, а у трех пациенток – после нерегулярного наблюдения и повторного обращения по поводу симптомов. Авторы подчеркивают необходимость регулярного ультразвукового мониторинга в течение не менее трех лет после органосохраняющего вмешательства для своевременного выявления возможного рецидива.
K.J. Childress и соавт. (2017) выполнили ретроспективное когортное исследование с участием 144 пациенток в возрасте 1–21 года, перенесших овариальную цистэктомию по поводу зрелых тератом в Texas Children's Hospital в 2007–2015 гг. [25]. Авторы установили, что лапароскопические вмешательства сопровождались достоверно более высокой частотой интраоперационного разрыва кисты с проливом содержимого (63,2 против 15,8% при лапаротомии; p < 0,001). Однако развитие перитонита не наблюдалось ни в одном случае, что подтверждает клиническую безопасность и оправданность применения малоинвазивной органосохраняющей тактики у детей и подростков с дермоидными кистами яичников.
В ретроспективном исследовании O. Dural и соавт. (2017), включавшем 69 пациенток в возрасте 9–19 лет, продемонстрированы высокая эффективность и безопасность лапароскопического лечения заболеваний придатков матки [26]. Во всех случаях проводились органосохраняющие вмешательства. Наиболее частой морфологической находкой была зрелая тератома (30,2%). Частота интра- и послеоперационных осложнений, длительность госпитализации и объем вмешательств не имели статистически значимых различий между возрастными подгруппами. В то же время тактика при подозрении на злокачественную опухоль отличалась: требовалось полноценное хирургическое стадирование и удаление опухоли единым блоком, что традиционно выполнялось методом лапаротомии (удаление пораженного яичника с придатком).
Врожденные кисты яичников являются наиболее распространенной формой абдоминальных кистозных образований у плода женского пола с частотой выявления около одного случая на 2,5 тыс. беременностей, преимущественно в третьем триместре [27]. Их развитие связывают с повышенной секрецией хорионического гонадотропина плаценты, фетальных гонадотропинов и эстрогенов матери, оказывающих стимулирующее воздействие на незрелую яичниковую ткань.
Согласно современным данным, кисты диаметром менее 20 мм рассматриваются как физиологические, соответствующие развивающимся фолликулам. В то же время кисты более 20 мм считаются патологическими и классифицируются на простые (однокамерные, тонкостенные, анэхогенные) и сложные (с толстыми стенками, неоднородным содержимым, септами, участками взвеси или кровоизлияния) [27].
Важным этапом дородовой оценки является дифференциальная диагностика с другими аномалиями, например мультикистозной дисплазией почек, гидронефрозом, кистами урахуса, энтерогенными дупликационными кистами, псевдокистами мекония и лимфатической мальформацией [28, 29].
Согласно консенсусному заявлению Европейской ассоциации детских хирургов (2022), при выявлении у новорожденных кист яичника диаметром более 4 см рекомендовано хирургическое вмешательство в течение первых двух недель жизни [30]. Предпочтительна лапароскопическая аспирация с частичным иссечением стенки кисты с использованием биполярной энергии. Такой подход направлен на снижение риска перекрута и ишемического повреждения яичниковой ткани, что крайне актуально в аспекте органосохраняющей тактики у пациенток раннего возраста.
Спонтанный регресс антенатально диагностированных кист яичников чаще всего происходит в течение первых шести месяцев жизни. Частота регресса обратно пропорциональна начальному диаметру кисты: при размере ≤ 2,9 см спонтанный регресс наблюдается примерно в 90% случаев, тогда как при диаметре ≥ 6 см – менее чем в 20% [31–33].
В допубертатном возрасте развитие кист яичников встречается сравнительно редко, что объясняется физиологическим угасанием гонадотропной стимуляции после завершения неонатального периода и ее стойким снижением вплоть до начала пубертата. Исключение составляют случаи, ассоциированные с эндокринными и наследственными нарушениями, предрасполагающими к кистозной трансформации яичников. У девочек допубертатного возраста важным этапом диагностики является ультразвуковая дифференциация истинных кист яичников от параовариальных, мезотелиальных кист, а также кист широкой связки матки [31, 32, 34]. При бессимптомном течении предпочтительна выжидательная тактика с обязательным информированием родителей о возможных признаках перекрута яичника.
Согласно данным литературы, образования до 9 см обычно подвергаются спонтанному регрессу. Однако при диаметре ≥ 9 см, наличии солидных включений, перегородок, кальцинатов, признаков перекрута или разрыва с гемоперитонеумом показано хирургическое вмешательство [8, 35, 36]. Ввиду гетерогенности опухолевых и опухолеподобных образований яичников у детей и подростков, современная клиническая практика требует дифференцированного подхода к лечению каждой нозологической формы с учетом гистогенеза, клинического течения и риска малигнизации.
Особенности ведения пациенток с наиболее распространенной патологией
Функциональные кисты яичников, представляющие собой фолликулярные образования и кисты желтого тела, являются наиболее распространенной патологией у девочек и подростков, особенно в первые годы после менархе. Функциональные кисты яичников, особенно размером до 3–4 см, в большинстве случаев склонны к спонтанной регрессии в течение двух-трех месяцев. Образования ≥ 6 см регрессируют реже и требуют динамического наблюдения из-за повышенного риска осложнений, включая перекрут [12].
Согласно данным клинической практики, функциональные кисты составляют до 60% всех хирургически подтвержденных образований придатков матки у пациенток в возрасте до 21 года, что подчеркивает необходимость четкой интерпретации ультразвуковых характеристик с целью оптимизации тактики ведения и избежания необоснованных хирургических вмешательств [37].
В соответствии с международными клиническими рекомендациями и результатами исследований, кистозные образования придатков матки, сохраняющиеся более 3–6 месяцев и/или достигающие диаметра ≥ 6 см, в отсутствие признаков регресса и эффекта от консервативной терапии подлежат плановому хирургическому лечению [38]. Показания к экстренному хирургическому вмешательству у детей и подростков с образованиями придатков матки обусловлены развитием острых осложнений, таких как разрыв кисты с внутрибрюшным кровотечением и признаками гемодинамической нестабильности, а также перекрут яичника.
По данным клинических наблюдений, своевременная деторсия позволяет сохранить орган и избежать овариоэктомии более чем в 90% случаев, что обусловлено высокой способностью яичниковой ткани к восстановлению даже при выраженных ишемических изменениях [35, 39].
C. Defert и соавт. (2025) провели ретроспективное многоцентровое исследование с участием 502 девочек с перекрутом яичника в допубертатном возрасте, оперированных в 30 педиатрических хирургических центрах Франции в 2000–2022 гг. [40]. Средний возраст пациенток составил 7,9 ± 2,8 года. Наиболее частыми симптомами при перекруте яичника были тошнота или рвота (71%) и повышение температуры тела (23%), особенно при обращении более чем через 24 часа от начала болевого синдрома (p < 0,0001). Повторный перекрут зарегистрирован у 14,7% пациенток, которым при первом эпизоде не выполнялась овариопексия. В большинстве таких случаев (55%) перекрут происходил на фоне увеличенного яичника. Несмотря на выявленное увеличение яичника более 97-го перцентиля у 142 пациенток, только 30% из них были направлены на гинекологическое дообследование.
В соответствии с клиническими рекомендациями «Доброкачественные новообразования яичников» (2024), хирургическое лечение доброкачественных опухолей яичников у пациенток репродуктивного возраста предпочтительно проводить с использованием лапароскопического доступа при наличии технической возможности и отсутствии противопоказаний [14]. Такой доступ обеспечивает меньшую травматичность, более быстрое восстановление, сокращение сроков госпитализации и уменьшение выраженности болевого синдрома и интраоперационной кровопотери по сравнению с лапаротомией. Основная цель органосохраняющего хирургического вмешательства заключается в полном удалении новообразования при максимально возможном сохранении овариального резерва. Рекомендуется выполнение резекции яичника путем энуклеации капсулы кисты с минимальной травматизацией коркового слоя. При удалении кистозных образований яичника важно соблюдать меры, направленные на предотвращение интраоперационного распространения содержимого. Капсула кисты подлежит удалению в герметичном эндоконтейнере, особенно когда образование носит потенциально сложный или неясный характер. Это позволяет снизить риск имплантационного распространения клеток в брюшную полость и обеспечивает безопасность послеоперационного восстановления.
Эпителиальные опухоли яичников у детей и подростков встречаются относительно редко – менее 2% всех опухолей детского возраста; общая частота – около 2,6 на 100 тыс. девочек младше 15 лет [41–43]. Эпителиальные новообразования составляют 10–17%, а подавляющее большинство – цистаденомы, из которых около 75% – серозные и 25% – муцинозные формы. Несмотря на доброкачественную природу, цистаденомы у девочек и подростков в отдельных случаях могут достигать гигантских размеров, имитируя злокачественное образование и требуя индивидуального подхода к выбору хирургической тактики [44]. В большинстве случаев у детей и подростков с доброкачественными цистаденомами операцией выбора считается органосохраняющая лапароскопическая цистэктомия с максимальным сохранением овариальной ткани. При наличии гигантских образований, сопровождающихся выраженной деформацией, сдавлением или истончением ткани яичника, возможно выполнение сальпинго-оофорэктомии. Прежде всего это касается ситуации, когда сохранить функциональную паренхиму не представляется возможным.
Согласно данным литературы, у детей и подростков герминогенные опухоли яичников составляют около 35–45% всех неоплазий [12]. Среди них доброкачественные формы (преимущественно зрелые и незрелые тератомы) встречаются примерно в 80% случаев, злокачественные герминогенные опухоли (ЗГО) – в 20% [45]. Наиболее частой злокачественной формой в детском возрасте является опухоль желточного мешка, в подростковом возрасте – дисгерминома, которая в 10% случаев может быть двусторонней [46]. Гонадобластомы, напротив, встречаются крайне редко и, как правило, ассоциированы с дисгенезией гонад [47]. Возникновение герминогенных неоплазий обусловлено нарушениями в процессе дифференцировки зародышевых клеток.
Согласно результатам эпидемиологического исследования P. Kaatsch и соавт. (2015), охватившего 1366 случаев ЗГО у детей в возрасте 0–14 лет, зарегистрированных в национальном реестре Германии за период 1987–2011 гг., заболеваемость ЗГО у девочек составляет 5,3 на 1 млн. При этом наиболее частой локализацией являются яичники – 4,5 на 1 млн лиц в возрасте 10–14 лет [48]. Авторы отметили статистически значимое увеличение заболеваемости ЗГО яичников. Пятилетняя и двадцатилетняя выживаемость – 92 и 90% соответственно, что свидетельствует об исключительно благоприятном прогнозе при своевременной диагностике и адекватной терапии.
В соответствии с клиническими рекомендациями «Неэпителиальные опухоли яичников» (2020), при герминогенных образованиях у пациенток, заинтересованных в сохранении фертильности, независимо от стадии заболевания рекомендуется выполнение односторонней сальпингоовариоэктомии (уровень убедительности рекомендаций – А, уровень достоверности доказательств – 3) [49]. В случаях, когда сохранение репродуктивной функции не требуется, показана экстирпация матки с придатками. Лапароскопический доступ возможен при ранней стадии и небольшом размере опухоли. Хирургическое стадирование включает срочное гистологическое исследование, забор смывов, биопсию подозрительных участков и при показаниях лимфодиссекцию. Хотя традиционно при злокачественных герминогенных опухолях яичников у взрослых проводится расширенное хирургическое стадирование для оценки распространенности процесса, в детской и подростковой практике такой подход применяется значительно реже. Как показывают клинические наблюдения, ограничение объема хирургического стадирования у этой группы пациенток не ухудшает прогноз и не снижает показатели выживаемости [50, 51].
В обзоре Е.В. Сибирской и соавт. (2018) подчеркивается, что частота встречаемости опухолей стромы полового тяжа у детей и подростков варьируется в широких пределах – от 2,1 до 21,8% всех опухолей яичников. Это может быть связано с разным числом наблюдений и неоднородностью выборок в представленных исследованиях [52].
Наиболее часто встречающиеся гистологические варианты включают гранулезоклеточные опухоли, опухоли клеток Сертоли – Лейдига и их смешанные формы. Эти новообразования нередко выявляются у девочек с нарушениями развития гонад, а также у пациенток с клиническими признаками преждевременного полового созревания.
Современная хирургическая тактика при опухолях стромы полового тяжа яичников у пациенток подросткового возраста ориентирована на выполнение органосохраняющих вмешательств с использованием лапароскопического доступа [53]. У пациенток с локализованной стадией заболевания и односторонним поражением стандартом является односторонняя сальпингоовариоэктомия с сохранением интактного контралатерального яичника и матки. Биопсия противоположного яичника выполняется только при наличии визуально подозрительных изменений. Абсолютное противопоказание к органосохраняющему лечению – дисгенезия гонад с кариотипом XY, требующая двусторонней аднексэктомии ввиду высокого онкологического риска. Распространенные стадии опухолевого процесса, двустороннее поражение яичников или вовлечение матки также являются показанием к выполнению более радикальных хирургических вмешательств.
J. Zhao и соавт. (2024) провели ретроспективный анализ данных 34 пациенток в возрасте до 20 лет с пограничными опухолями яичников, перенесших органосохраняющие хирургические вмешательства [54]. Преобладали муцинозные опухоли (82,4%), серозные выявлены у 14,7% пациенток, серомуцинозные – у 2,9%. Все случаи соответствовали стадии I FIGO. В 41,2% случаев выполнялась односторонняя цистэктомия, в 52,9% – односторонняя сальпингоовариоэктомия. При медиане наблюдения 65 месяцев рецидивы зарегистрированы у 29,4% пациенток. В одном случае отмечалось прогрессирование в низкодифференцированную карциному. Пятилетняя безрецидивная выживаемость составила 67,1%, общая – 100%. Это говорит о безопасности и эффективности органосохраняющего подхода.
Эндометриальная стромальная саркома (ЭСС) составляет менее 0,2% всех злокачественных новообразований матки и около 10–15% всех злокачественных мезенхимальных опухолей [55].
Описан редкий клинический случай высокозлокачественной ЭСС у 17-летней пациентки с внематочной локализацией в шейке матки и влагалище. Это указывает на необходимость включения данной патологии в дифференциальную диагностику аномальных маточных кровотечений у подростков и молодых женщин [56].
С учетом агрессивного характера опухоли и ее склонности к метастазированию ключевое значение имеют ранняя диагностика и индивидуализированный подход к лечению.
Эндометриоз считается ведущей причиной вторичной дисменореи у подростков и выявляется лапароскопически у 62–75% пациенток с хронической тазовой болью и/или дисменореей, особенно при неэффективности нестероидных противовоспалительных препаратов и комбинированных оральных контрацептивов [57]. При эндометриоидных кистах яичников у подростков лапароскопическое вмешательство показано при выраженной клинической симптоматике, увеличении размеров образования (особенно свыше 4 см) или наличии сомнительных УЗ-признаков.
Европейское общество репродукции и эмбриологии (ESHRE, 2022) рекомендует овариальную цистэктомию вместо простого дренирования или электрокоагуляции, поскольку такой подход снижает риск рецидива эндометриом и связанных симптомов при одновременном учете возможного снижения овариального резерва [58].
В соответствии с руководством ESHRE, после хирургического удаления эндометриом у девушек, не планирующих беременность в ближайшем будущем, рекомендуется назначение гормональной терапии на срок минимум 18–24 месяца с целью профилактики рецидива эндометриоза и уменьшения болевого синдрома и дисменореи. Рецидив эндометриоза после лапароскопического вмешательства наблюдается в среднем у 21,5% пациенток в течение первых двух лет и достигает 40–50% при более длительном наблюдении (пять лет) [59].
Заключение
Современные подходы к хирургическому лечению объемных образований придатков матки у детей и подростков предполагают обязательное применение индивидуализированной тактики, основанной на точной предоперационной диагностике, оценке риска малигнизации и стремлении к максимальному сохранению овариального резерва. Несмотря на относительную редкость данной патологии, риск злокачественного течения и потенциального негативного влияния на репродуктивную функцию требует особой онкологической настороженности и стандартизации диагностических и лечебных алгоритмов.
Активное внедрение малоинвазивных и органосохраняющих хирургических методов способствует улучшению клинических исходов за счет снижения частоты осложнений, уменьшения травматичности вмешательств и сокращения сроков реабилитации. Вместе с тем остаются актуальными вопросы повышения диагностической точности с использованием современных классификаций ультразвуковых данных (O-RADS), а также интеграции серологических и генетических маркеров в клиническую практику.
Дальнейшие исследования должны быть направлены на разработку персонализированных лечебных алгоритмов, уточнение критериев стратификации риска и совершенствование послеоперационного наблюдения. Это позволит не только обеспечить высокую безопасность и эффективность лечения, но и максимально сохранить репродуктивное здоровье и качество жизни пациенток детского и подросткового возраста.
S.A. Korotkova, L.V. Adamyan, PhD, Prof., Academician of RAS, Е.V. Sibirskaya, PhD, Prof., G.T. Osipova, A.Yu. Kurmangaleeva
Morozovskaya Children's City Clinical Hospital of the Moscow City Health Department
Russian University of Medicine
V.I. Kulakov National Medical Research Center for Obstetrics, Gynecology and Perinatology
Russian Children’s Clinical Hospital – a Branch of N.I. Pirogov Russian National Research Medical University
N.I. Pirogov Russian National Research Medical University
Contact person: Aliya Yu. Kurmangaleeva, askarova-aliya@yandex.ru
The aim is to systematize modern data on the clinical signs, diagnosis and surgical treatment of bulky formations of the uterine appendages in children and adolescents.
Material and methods. A literature review was conducted using PubMed, Scopus, Embase, and eLibrary databases covering the period from 2015 to 2025. The analysis included systematic reviews, prospective and retrospective studies, clinical guidelines, and case series.
Results. Adnexal masses in girls are relatively rare (2.6 cases per 100,000 per year), but they are clinically significant due to the risk of malignancy and their potential impact on reproductive health. Malignant tumors are found in 3–8% of cases; however, among girls before menarche, the proportion may reach 30–40%. Most lesions are benign or functional. Accurate preoperative malignancy risk assessment is essential for treatment planning. Current approaches prioritize organ-preserving and minimally invasive techniques with obligatory oncological vigilance to reduce surgical trauma and preserve ovarian reserve.
Conclusion. Surgical treatment of adnexal masses in pediatric patients requires a personalized approach based on precise preoperative diagnostics, oncological alertness, and reproductive preservation.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.