Влияние хирургического лечения глаукомы на количество применяемых пациентом гипотензивных препаратов
- Аннотация
- Статья
- Ссылки
- English
Введение
Основным направлением терапии глаукомы считается уменьшение внутриглазного давления (ВГД), а соответственно риска прогрессирования снижения зрительных функций [1]. Одним из главных компонентов для достижения данной цели является консервативная терапия [2]. Группу препаратов первого выбора составляют аналоги простагландинов: латанопрост 0,005%, биматопрост 3,0%, тафлупрост 0,0015%. Цель терапии достигается за счет высоких показателей эффективности, безопасности и удобства режима применения препаратов [3].
Еще одну категорию препаратов, назначаемых при глаукоме, представляют ингибиторы карбоангидразы, в частности бринзоламид 1,0% и дорзоламид 2,0% [4, 5]. Указанные лекарственные средства, способные снижать ВГД на 20–25% от исходного уровня, показаны к применению при остром приступе закрытоугольной глаукомы, а также перед хирургическим лечением [6].
Бримонидин 0,1, 0,15 и 0,2%, относящийся к группе селективных агонистов альфа-2-адренорецепторов, назначается не только для снижения ВГД. За счет улучшения кровотока он применяется с нейропротективной целью [7].
Еще одной важной группой препаратов являются бета-адреноблокаторы, среди которых широкое распространение получили тимолол 0,5% и бетаксолол 0,5% [8]. Эти лекарственные средства за счет воздействия на бета-2-рецепторы сокращают продукцию водянистой влаги, что приводит к снижению уровня ВГД. Указанные препараты, введенные в схемы терапии лекарственными средствами других групп, применяют в фиксированных комбинациях для усиления общего эффекта [9, 10].
Следует отметить, что на фоне консервативной терапии не всегда удается полностью компенсировать ВГД. Тогда выполняют хирургическое вмешательство. Основными применяемыми операциями считаются синустрабекулэктомия, вмешательства с применением шунтов Ex-Press, бесклапанных (Molteno) и клапанных дренажных устройств (Ahmed, Baerveldt) [11–13]. Данные методики высокоэффективны в достижении целевых значений ВГД и предотвращении развития глаукомы, но ассоциируются с высоким риском развития послеоперационных осложнений [11, 12].
В 1980 г. С.Н. Федоровым и соавт. была предложена непроникающая глубокая склерэктомия (НГСЭ) как более безопасное альтернативное хирургическое вмешательство [14].
Согласно результатам ряда исследований, подобная операция характеризуется меньшей эффективностью из-за того, что не происходит вскрытия передней камеры глаза [15–17].
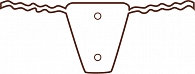
Для достижения более высоких результатов хирургического лечения Е.Х. Тахчиди предложил микроинвазивную НГСЭ, позволяющую уменьшить разрез конъюнктивы и лоскут склеры [18]. Однако даже в этом случае не исключено послеоперационное рубцевание. При выполнении НГСЭ могут быть использованы антиглаукомные имплантаты, которые также дополнительно усиливают гипотензивный эффект [19]. Одним из таких устройств является Репер-НН А2. Имплантат представляет собой трапециевидную пластину длиной 3 мм в осевой части и 1 и 2 мм в основаниях. На расстоянии 0,25 мм от широкого основания трапеции отходят два ответвления, предназначенные для имплантации в просвет шлеммова канала, шириной 0,25 мм и длиной 2,1 мм. За счет их неправильной формы поддерживается просвет в открытом состоянии, а также происходит фиксация данного устройства. В области широкого основания имплантата имеется отверстие, улучшающее эффективность возможной десцеметогониопунктуры. Еще одно отверстие ближе к короткому основанию служит для дополнительной шовной фиксации при необходимости. Имплантат изготовлен из биосовместимого пространственно-сшитого полимера на основе лапрола, монометакрилового эфира этиленгликоля и метакриловой кислоты (рис. 1).
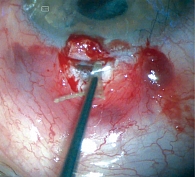
Для дополнительного уменьшения зоны хирургического вмешательства было предложено изменить параметры имплантата. У короткого основания ширину устройства уменьшили до 0,5 мм, убрали дополнительное фиксационное отверстие, размер длинного основания уменьшили до 1,0 мм. Отверстие в области широкого основания имплантата оставили. Сохранилось также одно извитое ответвление, фиксирующее имплантат в шлеммовом канале и дополнительно поддерживающее его просвет. За счет таких изменений достигается уменьшение зоны проводимой операции, увеличивается гипотензивный эффект и снижается выраженность рубцевания в области фильтрационной подушки (рис. 2).
В связи с этим особый интерес представляет исследование, которое проводится на базе Московского областного научно-исследовательского клинического института им. М.Ф. Владимирского.
Цель – изучить эффективность и безопасность модифицированного антиглаукомного имплантата.
Материал и методы
В исследовании участвует 61 пациент с диагнозом первичной открытоугольной глаукомы разной степени выраженности глаукомного процесса. Пациенты разделены на три группы. Первую представляют 23 пациента, которым проведена непроникающая глубокая склерэктомия с имплантацией антиглаукомного устройства Репер-НН А2, вторую – 18 пациентов, которым в ходе хирургического лечения глаукомы имплантировано дренажное устройство Ex-Press, третью – 20 пациентов, которым проведена модифицированная синустрабекулэктомия. Средний возраст пациентов – 68,8 года (53–85). Среднее значение ВГД у пациентов первой группы – 35,8 мм рт. ст., второй – 36,8 мм рт. ст., третьей – 35,8 мм рт. ст. Среднее количество гипотензивных препаратов, назначенных до хирургического вмешательства, в первой группе – 2,5 (1–4), во второй – 1,68 (1–4), в третьей – 2,15 (1–4). Срок наблюдения составляет один год с шестью визитами: две недели, один, два, три, шесть и 12 месяцев после хирургического вмешательства. Всем пациентам в пред- и послеоперационном периоде, а также на всех осмотрах выполнялись визометрия, тонометрия, оптическая когерентная томография переднего и заднего отрезка глаза.
Результаты
Во всех группах удалось достигнуть снижения количества применяемых препаратов. У 13 пациентов первой группы уровень ВГД снизился в отсутствие дополнительной консервативной терапии, шести пациентам потребовалось ее назначение в объеме 1,17 (1–2) препарата. Одиннадцати пациентам второй группы не потребовалась дополнительная гипотензивная терапия, четырем пациентам назначили 1,75 (1–2) препарата. Пять пациентов третьей группы получают антиглаукомную терапию в объеме 1,6 (1–2) препарата.
Заключение
Хирургическое лечение глаукомы позволяет улучшить качество жизни пациентов и прогноз, а также уменьшить количество применяемых с гипотензивной целью лекарственных средств. Необходимо отметить, что использование модифицированного антиглаукомного устройства Репер-НН А2 в ходе операции способствует большему сокращению количества применяемых пациентами препаратов для контроля ВГД.
S.S. Khaldeev, I.A. Loskutov, PhD, O.М. Andryukhina
M.F. Vladimirsky Moscow Regional Research Clinical Institute
Contact person: Igor A. Loskutov, loskoutigor@mail.ru
The main direction in the treatment of glaucoma is to reduce intraocular pressure (IOP), which reduces the risk of progression of visual function decline. One of the main components to achieve this goal is conservative therapy. However, it does not always allow for complete compensation of intraocular pressure, which leads to the need for surgical intervention. Non-penetrating deep sclerectomy is one of the methods of surgical treatment of glaucoma; in order to improve the prognosis after the intervention, this operation can be supplemented by the use of a modified anti-glaucoma implant.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.