количество статей
7415
Загрузка...
Пожалуйста, авторизуйтесь:
Обзоры
Современные принципы лечения ревматоидного артрита: акцент на раннюю агрессивную терапию
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Ревматология. Травматология. Ортопедия" №1
- Аннотация
- Статья
- Ссылки
Представлены данные, говорящие об особой роли генно-инженерных биологических препаратов для достижения ремиссии, на примере этанерцепта и других препаратов из группы ингибиторов ФНО-альфа.
Обсуждаются современные рекомендации по лечению ревматоидного артрита, принципы лечения до достижения цели (treat to target), дается обоснование ранней агрессивной терапии.
Представлены данные, говорящие об особой роли генно-инженерных биологических препаратов для достижения ремиссии, на примере этанерцепта и других препаратов из группы ингибиторов ФНО-альфа.
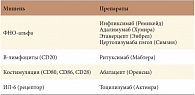
Таблица 1. Зарегистрированные в России для лечения РА биологические генно-инженерные препараты (ГИБП)
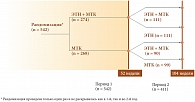
Рис. 1. Схема исследования COMET
У больных РА наблюдаются ранняя инвалидизация и уменьшение продолжительности жизни по сравнению с общей популяцией на 3–7 лет [1–3]. Распространенность и тяжесть этой патологии, сложность патогенетических механизмов, гетерогенность клинических форм и течения заболевания делают его терапию серьезной задачей [4]. Кроме того, длительные когортные исследования и клинические наблюдения, анализ многолетней динамики активности и прогрессирования болезни, оценка исходов РА приводят к следующим основным выводам в отношении возможностей контроля над болезнью [4–12]:
- РА – гетерогенное заболевание по клинико-иммунологическим характеристикам, воспалительной активности и скорости прогрессирования деструктивных изменений;
- основными факторами, определяющими исходы РА, являются выраженность и персистенция воспалительной активности;
- существует ранняя стадия болезни, когда лечение максимально эффективно;
- рано назначенная патогенетическая терапия позволяет в той или иной степени контролировать активность РА, включая возможность развития стойко низкой активности болезни и клинической ремиссии;
- различные методы патогенетической терапии могут обладать неодинаковым потенциалом в отношении торможения структурных нарушений.
- немедленное начало активной терапии после установления диагноза;
- активное ведение больного, тщательный контроль его состояния;
- подбор терапии при недостаточной эффективности.
В программе Т2Т не указываются конкретные методы лечения, но обозначены общие принципы и рекомендации по оптимальному ведению больных. Достигнутый консенсус основывается на данных, полученных при системном анализе литературы, описывающей стратегические терапевтические подходы, обеспечивающие наилучшие результаты. Последние положения были приняты в марте 2009 г., в их разработке участвовали 60 экспертов из 25 стран Европы, Северной и Латинской Америки, Японии и Австралии, а также представители пациентов. В рекомендациях не упоминается никаких конкретных препаратов либо классов препаратов; первостепенное значение здесь придается терапевтическим стратегиям, нацеленным на улучшение помощи пациентам с РА.
Общие принципы Т2Т сформулированы следующим образом.
А. Лечение ревматоидного артрита следует проводить на основании совместного решения пациента и врача-ревматолога.
А. Лечение ревматоидного артрита следует проводить на основании совместного решения пациента и врача-ревматолога.
B. Основная цель при лечении больного ревматоидным артритом – обеспечить максимально продолжительное сохранение высокого качества жизни, связанного с состоянием здоровья, путем контроля над симптоматикой, предотвращения структурного поражения суставов, нормализации функции и социальных возможностей пациента.
C. Подавление воспаления – важнейший способ достижения этой цели.
D. Лечение до достижения цели с помощью оценки активности заболевания и соответствующего подбора терапии способствует оптимизации исходов при РА.
На основании общих принципов международным комитетом разработаны 10 рекомендаций Т2Т по лечению ревматоидного артрита до достижения цели, базирующихся на научных доказательствах и мнении экспертов.
Рекомендации EULAR по лечению РА в краткой форме представлены ниже.
Возможность индукции клинической ремиссии изучалась в многоцентровом международном исследовании COMET (COmbination of Methotrexate and ETanercept) [25, 26], которое было проведено на большой группе больных ранним РА. В это рандомизированное исследование было включено 542 больных ранним (до 2 лет) активным РА, ранее не получавших метотрексат. Исследование проводилось в 2 этапа. На первом этапе пациенты были рандомизированы на 2 группы: 1-я группа – 274 больных получали комбинацию метотрексат (в дозе до 20 мг/нед) и ЭТН 50 мг/нед; 2-я группа – 268 больных получали метотрексат (до 20 мг/нед) и плацебо. Продолжительность первого этапа лечения составила 52 недели. Основной конечной точкой исследования было достижение клинической ремиссии по критериям EULAR (то есть индекс активности DAS28 ? 2,6 балла). До начала исследования 21% больных получали БПВП (но не метотрексат и не ГИБП), 49% – глюкокортикоиды и 74% – нестероидные противовоспалительные препараты.
К 52-й неделе лечения стойко низкая активность РА была достигнута у 41% больных на метотрексате и у 64% – на комбинации ЭТН и метотрексата, клиническая ремиссия (DAS28 ? 2,6 балла) развилась у 28 и 50% пациентов соответственно. Нормализация функционального состояния (значение функционального индекса HAQ < 0,5 балла – так называемая функциональная ремиссия) наблюдалась у 39% больных на метотрексате и у 55% – на комбинированной терапии. Отсутствие рентгенологического прогрессирования (так называемая рентгенологическая ремиссия) в течение 52 недель наблюдения было отмечено у 80% пациентов, получавших ЭТН и метотрексат, и только у 59% больных, получавших метотрексат и плацебо. Все различия были статистически достоверны. У значительной группы больных ранним РА оказалось возможным достижение «полной ремиссии» (сочетание клинической ремиссии, нормализации функции и отсутствия прогрессирования). Полная ремиссия наблюдалась к концу 1-го года исследования у 35% больных на комбинированной терапии ЭТН и метотрексатом (против 20% на плацебо и метотрексате).
C. Подавление воспаления – важнейший способ достижения этой цели.
D. Лечение до достижения цели с помощью оценки активности заболевания и соответствующего подбора терапии способствует оптимизации исходов при РА.
На основании общих принципов международным комитетом разработаны 10 рекомендаций Т2Т по лечению ревматоидного артрита до достижения цели, базирующихся на научных доказательствах и мнении экспертов.
- Первичная цель лечения ревматоидного артрита – достижение состояния клинической ремиссии.
- Клиническая ремиссия определяется как отсутствие признаков значимой воспалительной активности.
- Хотя основной целью остается достижение ремиссии, на основании имеющихся научных данных допустимо считать приемлемой альтернативной целью лечения достижение низкой активности заболевания, особенно при стабильном состоянии и длительно протекающем заболевании.
- До тех пор, пока не будет достигнута цель лечения, пересмотр лекарственной терапии необходимо осуществлять не реже 1 раза в 3 месяца.
- Необходимо регулярно оценивать и документировать данные об активности заболевания: стоянии ремиссии – реже (1 раз в 3–6 месяцев).
- В каждодневной клинической практике для принятия решений о лечении необходимо использовать валидированные комплексные показатели активности заболевания, включающие оценку состояния суставов.
- Помимо использования комплексных показателей активности заболевания, при принятии клинических решений необходимо учитывать структурные изменения и нарушения функции.
- Желаемая цель лечения должна поддерживаться в течение всего течения заболевания.
- На выбор (комплексного) показателя активности заболевания и целевых параметров могут повлиять сопутствующие заболевания, индивидуальные особенности пациента и риски, связанные с приемом лекарственных препаратов.
- Пациент должен быть в достаточной степени информирован о цели лечения и запланированной стратегии для достижения этой цели под наблюдением ревматолога.
- нацеленность на сохранение качества жизни и социальной активности (в противовес зачастую имеющей место практике быстрого определения инвалидности);
- необходимость тщательногоконтроля над процессом лечения с использованием современных интегральных показателей активности болезни и, соответственно, повышение роли специалиста-ревматолога в системе оказания медицинской помощи;
- подтверждена необходимость как можно более активного подавления воспалительного процесса с целью достижения ремиссии, что стало возможным с внедрением генно-инженерных биологических препаратов;
- поддержание достигнутого улучшения при помощи целенаправленной терапии на протяжении всего заболевания (фактически – всей жизни больного), что диктует необходимость улучшения медикаментозного снабжения.
- метотрексат среди всех синтетических БПВП наиболее эффективен в отношении активности РА и структурных повреждений;
- лефлуномид близок к метотрексату по эффективности;
- сульфасалазин и соли золота (инъекционные) эффективны в отношении симптоматики и структурных повреждений;
- циклоспорин, гидроксихлорохин, миноциклин, такролимус ставного синдрома;
- ауранофин и Д-пеницилламин не имеют строго доказанного превосходства над плацебо;
- циклофосфамид и азатиоприн повышают риск опухолей и инфекций.
- глюкокортикоиды эффективны в качестве бридж-терапии (то есть при относительно кратковременном назначении в низких и средних дозах на период до наступления терапевтического эффекта от действия БПВП либо при смене базисных препаратов);
- при раннем РА низкие дозы глюкокортикоидов (? 7,5 мг/сут в пересчете на преднизолон) могут уменьшать рентгенологическое прогрессирование;
- при развернутом и позднем РА дозы глюкокортикоидов ? 15 мг/сут способствуют снижению активности болезни;
- доза глюкокортикоидов может медленно снижаться по достижении успеха.
- эффективны при первичном назначении у больных, не получавших ранее метотрексат: инфликсимаб, адалимумаб, этанерцепт, абатацепт;
- эффективны у больных с недостаточной эффективностью метотрексата: инфликсимаб, адалимумаб, этанерцепт, ритуксимаб, тоцилизумаб, абатацепт;
- при недостаточном ответе на ингибиторы ФНО эффективен переход на ритуксимаб, тоцилизумаб, абатацепт;
- переключение на другой антиФНО при недостаточном эффекте первого препарата из этой группы возможно, но менее подтверждено фактами;
- ингибиторы ФНО повышают вероятность инфекций.
- ревматологи – специалисты, которые первично занимаются больными РА;
- лечение больных РА должно быть направлено на наилучшие результаты и базироваться на совместном решении врача и пациента;
- РА – дорогое заболевание в отношении медицинских расходов и затрат, связанных со снижением производительности, оба обстоятельства должны рассматриваться лечащим ревматологом.
Рекомендации EULAR по лечению РА в краткой форме представлены ниже.
- Как только больному устанавливается диагноз РА, ему сразу должно быть назначено лечение синтетическим БПВП.
- Цель лечения – как можно более быстрое достижение ремиссии или низкой активности болезни у каждого пациента, если эта цель не достигается, необходим подбор терапии путем частого и непосредственного мониторинга (каждые 1–3 мес.).
- Метотрексат должен быть частью первой стратегической схемы лечения у больных активным РА.
- В случае противопоказаний к назначению метотрексата (или его непереносимости), следующие БПВП должны обсуждаться в качестве (первой) стратегии лечения: сульфасалазин, лефлуномид и соли золота (инъекции).
- Для больных, ранее не получавших БПВП, рекомендуется монотерапия, а не комбинированная терапия синтетическими БПВП.
- Глюкокортикоиды могут быть полезны в качестве первоначального метода терапии (кратковременного) в комбинации с синтетическим БПВП.
- Если после первоначального назначения БПВП цель терапии не достигнута, при наличии факторов неблагоприятного прогноза (положительные тесты на ревматоидный фактор и антицитруллиновые антитела, раннее появление эрозий, быстрое прогрессирование, высокая активность болезни), должно быть обсуждено добавление ГИБП. При отсутствии факторов неблагоприятного прогноза должно быть обсуждено переключение на другой синтетический БПВП.
- Больным, недостаточно отвечающим на метотрексат и/или другие синтетические БПВП, должны быть назначены ГИБП. Текущая практика состоит в назначении ингибитора ФНО-альфа, который должен комбинироваться с метотрексатом.
- При неудаче (неэффективности или непереносимости) тера-пии первым ингибитором ФНО пациенту должен быть назначен либо второй ингибитор ФНО, либо препараты других классов – абатацепт, ритуксимаб или тоцилизумаб.
- При рефрактерном тяжелом РА либо при наличии противопоказаний к ГИБП или указанным ранее синтетическим БПВП может обсуждаться назначение следующих препаратов в монотерапии или комбинации с вышеуказанными средствами: азатиоприн, циклоспорин А, циклофосфамид.
- Стратегии интенсивного лечения должны применяться у каждого пациента, в первую очередь у больных с неблагоприятными прогностическими факторами.
- Если больной находится в стойкой ремиссии, доза ГК должна быть снижена, возможно обсуждение снижения дозы ГИБП, особенно если эта терапия комбинируется с синтетическим БПВП.
- В случае длительной устойчивой ремиссии может быть обсуждено осторожное титрование дозы БПВП, как общее решение врача и пациента.
- У пациентов, имеющих факторы неблагоприятного прогноза и ранее не получавших БПВП, может быть обсуждено назначение метотрексата в комбинации с ГИБП (в качестве первой схемы лечения).
- При подборе терапии, кроме активности болезни, должны учитываться такие факторы, как прогрессирование рентгенологических изменений, сопутствующие заболевания и соображения безопасности лечения. Таким образом, можно видеть, что в клинических рекомендациях по лечению РА делается акцент на максимально раннее начало терапии сильнодействующими медикаментозными средствами, такими как метотрексат и ГИБП. При этом для пациентов, имеющих серьезный прогноз, признается возможным использование комбинации метотрексата и ГИБП в качестве первой схемы патогенетической терапии.
Возможность индукции клинической ремиссии изучалась в многоцентровом международном исследовании COMET (COmbination of Methotrexate and ETanercept) [25, 26], которое было проведено на большой группе больных ранним РА. В это рандомизированное исследование было включено 542 больных ранним (до 2 лет) активным РА, ранее не получавших метотрексат. Исследование проводилось в 2 этапа. На первом этапе пациенты были рандомизированы на 2 группы: 1-я группа – 274 больных получали комбинацию метотрексат (в дозе до 20 мг/нед) и ЭТН 50 мг/нед; 2-я группа – 268 больных получали метотрексат (до 20 мг/нед) и плацебо. Продолжительность первого этапа лечения составила 52 недели. Основной конечной точкой исследования было достижение клинической ремиссии по критериям EULAR (то есть индекс активности DAS28 ? 2,6 балла). До начала исследования 21% больных получали БПВП (но не метотрексат и не ГИБП), 49% – глюкокортикоиды и 74% – нестероидные противовоспалительные препараты.
К 52-й неделе лечения стойко низкая активность РА была достигнута у 41% больных на метотрексате и у 64% – на комбинации ЭТН и метотрексата, клиническая ремиссия (DAS28 ? 2,6 балла) развилась у 28 и 50% пациентов соответственно. Нормализация функционального состояния (значение функционального индекса HAQ < 0,5 балла – так называемая функциональная ремиссия) наблюдалась у 39% больных на метотрексате и у 55% – на комбинированной терапии. Отсутствие рентгенологического прогрессирования (так называемая рентгенологическая ремиссия) в течение 52 недель наблюдения было отмечено у 80% пациентов, получавших ЭТН и метотрексат, и только у 59% больных, получавших метотрексат и плацебо. Все различия были статистически достоверны. У значительной группы больных ранним РА оказалось возможным достижение «полной ремиссии» (сочетание клинической ремиссии, нормализации функции и отсутствия прогрессирования). Полная ремиссия наблюдалась к концу 1-го года исследования у 35% больных на комбинированной терапии ЭТН и метотрексатом (против 20% на плацебо и метотрексате).
Частота серьезных нежелательных явлений (НЯ), частота отмен препаратов из-за НЯ и неэффективности, а также общая частота отмен препаратов были выше у пациентов, получавших метотрексат и плацебо, чем у больных, получавших активную терапию ЭТН. Не наблюдалось ни одного случая туберкулеза. Это подчеркивает ранее продемонстрированную во многих исследованиях высокую безопасность и хорошую переносимость ЭТН. Таким образом, при назначении ранней агрессивной терапии комбинацией ЭТН и метотрексата (МТ) клиническая ремиссия была достигнута у 50% больных, функциональная ремиссия у 55% и рентгенологическая ремиссия у 80% больных, включая состояние полной ремиссии у 35% пациентов. Дополнительно проведенный анализ данных исследования COMET показал, что лечение комбинацией ЭТН + МТ достоверно уменьшало нетрудоспособность у работающих больных РА. Даже при пессимистической оценке больные, получающие ЭТН, теряют на 22 рабочих дня в год меньше, чем больные, получающие только МТ [26].
На втором этапе исследования COMET (второй год от начала терапии) пациенты были разбиты на 4 подгруппы (рис. 1): 1-я подгруппа – продолжившие терапию комбинацией ЭТН и метотрексата; 2-я подгруппа – перешедшие на монотерапию ЭТН; 3-я подгруппа – получавшие ранее метотрексат и плацебо и перешедшие на комбинацию ЭТН и метотрексата; 4-я подгруппа – продолжившие монотерапию метотрексатом. В 1-й подгруппе (продолживших лечение комбинацией ЭТН и метотрексата) к концу двухлетнего наблюдения частота клинической ремиссии составила 57%, среди продолживших лечение монотерапией метотрексатом (4-я подгруппа) – 35%. Среди больных, отменивших метотрексат и перешедших на монотерапию ЭТН (2-я подгруппа), частота клинической ремиссии осталась прежней (как на 1-м году лечения) – 50%.
На втором этапе исследования COMET (второй год от начала терапии) пациенты были разбиты на 4 подгруппы (рис. 1): 1-я подгруппа – продолжившие терапию комбинацией ЭТН и метотрексата; 2-я подгруппа – перешедшие на монотерапию ЭТН; 3-я подгруппа – получавшие ранее метотрексат и плацебо и перешедшие на комбинацию ЭТН и метотрексата; 4-я подгруппа – продолжившие монотерапию метотрексатом. В 1-й подгруппе (продолживших лечение комбинацией ЭТН и метотрексата) к концу двухлетнего наблюдения частота клинической ремиссии составила 57%, среди продолживших лечение монотерапией метотрексатом (4-я подгруппа) – 35%. Среди больных, отменивших метотрексат и перешедших на монотерапию ЭТН (2-я подгруппа), частота клинической ремиссии осталась прежней (как на 1-м году лечения) – 50%.
У больных 3-й подгруппы, перешедших с монотерапии метотрексатом на комбинацию метотрексата и ЭТН, наблюдался значительный рост доли пациентов, достигших клинической ремиссии – с 28% на 1-м году до 58% на 2-м году лечения. Таким образом, исследование COMET чрезвычайно важно тем, что оно демонстрирует большие возможности терапии ГИБП (в частности, ЭТН) на ранней стадии болезни и превосходство комбинированной схемы лечения ЭТН и метотрексатом над монотерапией метотрексатом как на 1-м, так и на 2-м году наблюдения. Исследование COMET поддерживает концепцию ранней агрессивной терапии как важнейшего метода достижения клинической ремиссии у больных РА. Необходимы большие регистровые и регулярные фармакоэкономические исследования для обоснования введения этой концепции в широкую клиническую практику.
1. Ревматология: клинические рекомендации / Под ред. Е.Л. Насонова. М.: ГЭОТАР-Медиа, 2006. 288 с.
2. Ревматология: национальное руководство / Под ред. Е.Л. Насонова, В.А. Насоновой. М.: ГЭОТАР-Медиа, 2008. 720 с.
3. Насонов Е.Л. Ревматоидный артрит как общемедицинская проблема // Терапевтич. архив. Т. 76. 2004. № 5. С. 5–7.
4. Насонов Е.Л. Почему необходима ранняя диагностика и лечение ревматоидного артрита? // РМЖ. 2002. Т. 10. № 22. С. 1009–1101.
5. Emery P. Therapeutic approaches for early rheumatoid arthritis. How early? How aggressive? // Br. J. Rheumatol. Vol. 34. 1995. № 2. P. 87–90.
6. Каратеев Д.Е., Иванова М.М., Балабанова Р.М., Акимова Т.Ф. Анализ летальных исходов ревматоидного артрита при длительном наблюдении // Росс. ревматол. 1998. № 1. С. 17–28.
7. Emery P., Breedveld F.C., Dougados M., Kalden J.R., Schiff M.H., Smolen J.S. Early referral recommendation for newly diagnosed rheumatoid arthritis: evidence based development of a clinical guide // Ann. Rheum. Dis. Vol. 61. 2002. № 4. P. 290–297.
8. Насонов Е.Л. Фармакотерапия ревматоидного артрита с позиций доказательной медицины: новые рекомендации // РМЖ. Т. 10. 2002. № 6. С. 294–302.
9. Каратеев Д.Е. Ретроспективная оценка многолетней базисной терапии у больных ревматоидным артритом // Научно-практич. ревматол. 2003. № 3. С. 32–36.
10. Каратеев Д.Е. Основные тенденции и вариабельность эволюции ревматоидного артрита: результаты многолетнего наблюдения // Научно-практич. ревматол. 2004. № 1. С. 8–14.
11. Насонов Е.Л., Каратеев Д.Е., Чичасова Н.В., Чемерис Н.А. Современные стандарты фармакотерапии ревматоидного арт-рита // Клин. фармакол. тер. 2005. № 1. С. 72–75.
12. Каратеев Д.Е., Лучихина Е.Л., Тогизбаев Г. Современные принципы ведения больных ранним артритом // РМЖ. Т. 16. 2008. № 24. С. 1610–1614.
13. Smolen J.S., Aletaha D., Machold K.P. Therapeutic strategies in early rheumatoid arthritis // Best Pract. Res. Clin. Rheumatol. Vol. 19. 2005. № 1. P. 163–177.
14. Каратеев Д.Е. Низкая активность и ремиссия при ревматоидном артрите: клинические, иммунологические и морфологические аспекты // Научно-практич. ревматол. 2009. № 5. С. 4–12.
15. Knevel R., Schoels M., Huizinga T.W., Aletaha D., Burmester G.R., Combe B., Landewé R.B., Smolen J.S., Sokka T., van der Heijde D.M. Current evidence for a strategic approach to the management of rheumatoid arthritis with disease-modifying antirheumatic drugs: a systematic literature review informing the EULAR recommendations for the management of rheumatoid arthritis // Ann. Rheum. Dis. Vol. 69. 2010. № 6. P. 987–994.
16. Smolen J.S., Aletaha D., Bijlsma J.W., Breedveld F.C., Boumpas D., Burmester G., Combe B., Cutolo M., de Wit M., Dougados M., Emery P., Gibofsky A., Gomez-Reino J.J., Haraoui B., Kalden J., Keystone E.C., Kvien T.K., McInnes I., Martin-Mola E., Montecucco C., Schoels M., van der Heijde D. Treating rheumatoid arthritis to target: recommendations of an international task force // Ann. Rheum. Dis. Vol. 69. 2010. № 4. P. 631–637.
17. Каратеев Д.Е. Академия ревматологии на российской земле // Consilium medicum. 2010. Экстравыпуск. С. 3–14.
18. Gaujoux-Viala C., Smolen J.S., Landewé R., Dougados M., Kvien T.K., Mola E.M., Scholte-Voshaar M., van Riel P., Gossec L. Current evidence for the management of rheumatoid arthritis with synthetic disease-modifying antirheumatic drugs: a systematic literature review informing the EULAR recommendations for the management of rheumatoid arthritis // Ann. Rheum. Dis. Vol. 69. 2010. № 6. P. 1004–1009.
19. Gorter S.L., Bijlsma J.W., Cutolo M., Gomez-Reino J., Kouloumas M., Smolen J.S., Landewé R. Current evidence for the management of rheumatoid arthritis with glucocorticoids: a systematic literature review informing the EULAR recommendations for the management of rheumatoid arthritis // Ann. Rheum. Dis. Vol. 69. 2010. № 6. P. 1010–1014.
20. Nam J.L., Winthrop K.L., van Vollenhoven R.F., Pavelka K., Valesini G., Hensor E.M., Worthy G., Landewé R., Smolen J.S., Emery P., Buch M.H. Current evidence for the management of rheumatoid arthritis with biological disease-modifying antirheumatic drugs: a systematic literature review informing the EULAR recommendations for the management of RA // Ann. Rheum. Dis. Vol. 69. 2010. № 6. P. 976–986.
21. Smolen J.S., Landewé R., Breedveld F.C., Dougados M., Emery P., Gaujoux-Viala C., Gorter S., Knevel R., Nam J., Schoels M., Aletaha D., Buch M., Gossec L., Huizinga T., Bijlsma J.W., Burmester G., Combe B., Cutolo M., Gabay C., Gomez-Reino J., Kouloumas M., Kvien T.K., Martin-Mola E., McInnes I., Pavelka K., van Riel P., Scholte M., Scott D.L., Sokka T., Valesini G., van Vollenhoven R., Winthrop K.L., Wong J., Zink A., van der Heijde D. EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs // Ann. Rheum. Dis. Vol. 69. 2010. № 6. P. 964–975.
22. Roundtree A.K., Kallen M.A., Lopez-Olivo M.A., Kimmel B., Skidmore B., Ortiz Z., Cox V., Suarez-Almazor M.E. Poor reporting of search strategy and conflict of interest in over 250 narrative and systematic reviews of two biologic agents in arthritis: a systematic review // J. Clin. Epidemiol. Vol. 62. 2009. № 2. P. 128–137.
23. Furst D.E., Keystone E.C., Kirkham B., Fleischmann R., Mease P., Breedveld F.C., Smolen J.S., Kalden J.R., Burmester G.R., Braun J., Emery P., Winthrop K., Bresnihan B., De Benedetti F., Dörner T., Gibofsky A., Schiff M.H., Sieper J., Singer N., Van Riel P.L.C.M., Weinblatt M.E., Weisman M.H. Updated consensus statement on biological agents for the treatment of rheumatic diseases, 2008 // Ann. Rheum. Dis. Vol. 67. 2008. Suppl. 3. P. iii2–iii25.
24. Каратеев Д.Е. Этанерцепт при ревматоидном артрите // Научно-практич. ревматол. 2009. № 5. С. 53–57.
25. Emery P., Breedveld F.C., Hall S., Durez P., Chang D.J., Robertson D., Singh A., Pedersen R.D., Koenig A.S., Freundlich B. Comparison of methotrexate monotherapy with a combination of methotrexate and etanercept in active, early, moderate to severe rheumatoid arthritis (COMET): a randomised, double-blind, parallel treatment trial // Lancet. Vol. 372. 2008. № 9636. P. 375–382.
26. Anis A., Zhang W., Emery P., Sun H., Sato R., Singh A. et al. Work-related outcomes in early active rheumatoid arthritis: results from the COMET trial // Ann. Rheum. Dis. Vol. 67. 2008. Suppl. 2. P. 79.
Новости на тему
25.02.2025
14.09.2023
11.08.2023
07.11.2022
Отправить статью по электронной почте
Ваш адрес электронной почты:
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.