количество статей
7415
Загрузка...
Пожалуйста, авторизуйтесь:
Возможно ли предотвратить прогрессирование ревматоидного артрита у впервые заболевших?
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Ревматология. Травматология. Ортопедия" №1
- Аннотация
- Статья
- Ссылки
Приведены данные российских и международных исследований, посвященных предотвращению развития ревматоидного артрита у пациентов с недифференцированным артритом. Показано, что эффективными в этом отношении препаратами могут считаться метотрексат и абатацепт.
В статье представлена современная концепция раннего недифференцированного артрита. Дана характеристика клинической картины и прогноза при этом состоянии, изложены международные рекомендации по ведению пациентов.
Приведены данные российских и международных исследований, посвященных предотвращению развития ревматоидного артрита у пациентов с недифференцированным артритом. Показано, что эффективными в этом отношении препаратами могут считаться метотрексат и абатацепт.
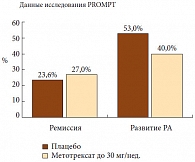
Рис. 1. Ранняя терапия метотрексатом снижает частоту развития ревматоидного артрита* у больных недифференцированным артритом / вероятным ревматоидным артритом
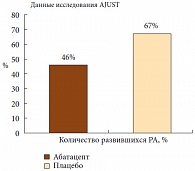
Рис. 2. Ранняя терапия абатацептом снижает частоту развития ревматоидного артрита* у больных недифференцированным артритом
Американской коллегией ревматологов (АCR) [4] или в 2010 г. Американской коллегией ревматологов совместно с Европейской лигой по борьбе с ревматизмом (ACR/EULAR) [5], как, впрочем, и критериям других заболеваний (аниклозирующий спондилит, псориатический артрит и др.). В данной связи состояние, характеризующееся воспалительным поражением (артритом) одного или более суставов, которое на момент обследования не может быть отнесено к определенной нозологической форме, обычно обозначается как так называемый недифференцированный артрит (НДА).
По оценке различных авторов [6–11], НДА встречается в среднем у каждого третьего пациента с впервые возникшим артритом. Различия между когортами больных объясняются отсутствием стандартизованного подхода к критериям отбора пациентов, длительностью заболевания к моменту первичного обследования и другими факторами. С теоретической точки зрения, обосновано утверждение Annette H.M. van der Helm-van Mil и соавт. [12], что в ревматологической практике большинство первичных пациентов (при достаточно раннем обследовании) могут быть отнесены к группе с НДА. НДА может иметь множество клинических вариантов, среди которых в качестве основных описаны следующие [13]:
Поскольку клиническую картину хронического артрита нельзя охарактеризовать как сформировавшуюся, что, очевидно, является отражением неполного включения характерных для развернутой стадии РА иммунопатологических механизмов, ряд авторов отмечали склонность НДА к развитию спонтанных ремиссий [6, 11]. Однако в целом это не означает, что у большинства больных НДА прогноз благоприятен. Другие авторы [7–10] особо подчеркивают: НДА является достаточно серьезным состоянием, которое в течение 1 года выливается в достоверный РА в среднем у одной трети больных.
Российские исследователи, основываясь на данных наблюдения за большой когортой больных [9] в рамках программы «Ранний артрит: диагностика, исход, критерии, активное лечение» (РАДИКАЛ), продемонстрировали: из 366 больных с воспалительным поражением суставов и давностью болезни до 1 года только у 57,9% мог быть сразу установлен диагноз РА, 36,3% были классифицированы как имеющие НДА, и только 5,7% при первичном обследовании были поставлены другие диагнозы. Через 12 месяцев диагноз РА был установлен у 33,1% больных с НДА, что подтверждает данные зарубежных исследователей, засвидетельствовавших серьезность прогноза при НДА.
Больные с НДА требуют активного наблюдения. Зачастую для уточнения нозологической формы необходимо многомесячное наблюдение и многократные повторные обследования в динамике, поскольку верификация диагноза по современным представлениям является основой для грамотного обоснования патогенетической терапии. Важнейшим моментом при НДА является определение антицитруллиновых антител, в частности антител к циклическому цитруллинированному пептиду (АЦЦП) преимущественно у больных, серонегативных по РФ. На ранней стадии заболевания данный тест чувствительнее и специфичнее РФ и может использоваться для прогнозирования развития персистирующего артрита у больных НДА [16–19]. Наличие антицитруллиновых антител, особенно при их высоком уровне в сыворотке крови, считается одним из важнейших факторов, определяющих тяжесть и неблагоприятный прогноз у больных НДА.
В то же время ни один отдельно взятый показатель не дает возможность точно предсказать развитие РА у больных НДА [8, 9, 15]. Предложены специальные критерии (prediction rule – «решающее правило»), позволяющие предсказать развитие при НДА «настоящего» РА путем подсчета суммы баллов [12]. Эта методика успешно апробирована за рубежом [20] и в нашей стране [21], опыт ее применения использован при создании последней версии классификационных критериев РА [5]. Наблюдения за пациентами с НДА привели специальный комитет Европейской лиги по борьбе с ревматизмом (EULAR) к необходимости постулировать: в случае выявления у пациента признаков (факторов риска) формирования персистирующего воспалительного заболевания суставов с тенденцией к деструктивному поражению, даже если больной не соответствует классификационным критериям РА, ревматолог должен рассмотреть вопрос о назначении базисных противовоспалительных препаратов (БПВП) [22]. Таким образом, больных НДА с признаками хронизации и структурных нарушений фактически предлагается вести как больных с ранним РА.
Это положение обосновано клиническими наблюдениями и теоретическими соображениями, позволяющими считать возможным развитие лекарственно индуцированной ремиссии у больных НДА, что будет равнозначно отсрочке или даже предотвращению развития типичного РА. Поиск оптимальной схемы лечения пациентов с НДА ведется в течение нескольких последних лет. Как правило, лечение впервые возникшего артрита начинают с назначения симптоматической терапии нестероидными противовоспалительными препаратами (НПВП). В России осуществлено многоцентровое открытое исследование в условиях поликлинической практики [23] с участием более чем 200 пациентов с впервые возникшим артритом. В рамках данной работы проводилась четырехнедельная терапия средними и высокими дозами НПВП (диклофенак и нимесулид) с целью исследовать возможности контроля над симптоматикой и индукции ремиссии. Несмотря на вполне удовлетворительный симптоматический эффект, полное купирование симптоматики наблюдалось лишь в единичных случаях и скорее может быть объяснено хорошо известным фактом развития спонтанной ремиссии у больных НДА. Таким образом, наше исследование доказало, что НПВП не обладают индуцирующим ремиссию эффектом при НДА (так же как при РА).
Применение высоких доз глюкокортикоидов (ГК) при раннем РА всегда вызывало значительный интерес, поскольку хорошо известен мощный противовоспалительный эффект и возможность определенного базисного действия ГК. Международное рандомизированное плацебо-контролируемое исследование SAVE (Stop Arthritis Very Early), в котором также принимали участие российские ревматологи (НИИР РАМН), было посвящено предотвращению развития РА у больных НДА с длительностью симптоматики до 12 недель с помощью болюсного введения высокой дозы пролонгированного глюкокортикоидного препарата (метилпреднизолон-депо 120 мг). В исследование было включено 383 больных из 40 исследовательских центров [24]. В отношении достижения клинической ремиссии, развития РА (по критериям АCR (1987)), потребности в назначении БПВП группы, получавшие активный препарат и плацебо, достоверно не различались. Исследование SAVE показало, что монотерапия ГК при однократном введении высокой дозы не дает возможности контролировать развитие симптоматики хронического артрита при НДА.
В настоящее время все национальные и международные организации ревматологов в качестве «золотого стандарта» лечения РА признают метотрексат (MTX) [25]. Однако в случае неуточненного диагноза (НДА) врачи нередко избегают назначать этот серьезный иммуносупрессивный препарат из-за опасения, что это будет сложно обосновать. В то же время, как уже говорилось выше, существуют рекомендации EULAR [22], согласно которым возможно назначение БПВП пациентам, симптоматика которых еще не соответствует классификационным критериям РА. Кроме того, согласно современной отечественной классификации РА (2007), больные НДА с наличием факторов риска развития РА могут рассматриваться как пациенты с «вероятным РА» [26].
Серьезным аргументом в пользу назначения МТ на самых ранних стадиях развития заболевания стало исследование PROMPT (Th e PRObable rheumatoid arthritis: Methotrexate versus Placebo Treatment) [27]. В этом рандомизированном исследовании 110 больным с «вероятным» РА с длительностью болезни с момента появления симптоматики не более 2 лет назначались: MTX (в начальной дозе 15 мг в неделю с постепенным повышением до 30 мг в неделю(n = 55) или плацебо (n = 55). Длительность лечения составляла 12 месяцев, после чего MTX (либо плацебо) отменялись, и пациенты наблюдались до 30 месяцев. В исследовании PROMPT было показано (рис. 1), что среди получавших MTX развили РА 22 из 55 больных (40%), в то время как среди получавших плацебо – 29 из 55 (53%). При этом в группе MTX появление типичной для РА симптоматики происходило позже (р = 0,04), и у меньшего количества пациентов было отмечено рентгенологическое ухудшение (р = 0,046). Таким образом, раннее назначение метотрексата в дозе 15–30 мг в неделю может замедлять развитие РА, включая рентгенологическое прогрессирование.
Генно-инженерные биологические препараты (ГИБП) весьма привлекательны в отношении индукции ремиссии и абортивного течения РА на ранней стадии, поскольку вызывают быстрое и стойкое клиническое улучшение. В маленькой группе пациентов (n = 17) была проведена попытка применения инфликсимаба при НДА [28]. Результаты показали отчетливое кратковременное улучшение, однако наблюдение в течение 52 недель не продемонстрировало достоверного снижения числа больных, развивших РА, по сравнению с плацебо. Препарат абатацепт (ABA) обладает уникальным механизмом действия, являясь ингибитором костимуляции Т-лимфоцитов, то есть потенциально может обрывать начальный этап развития иммуновоспалительного процесса.
По оценке различных авторов [6–11], НДА встречается в среднем у каждого третьего пациента с впервые возникшим артритом. Различия между когортами больных объясняются отсутствием стандартизованного подхода к критериям отбора пациентов, длительностью заболевания к моменту первичного обследования и другими факторами. С теоретической точки зрения, обосновано утверждение Annette H.M. van der Helm-van Mil и соавт. [12], что в ревматологической практике большинство первичных пациентов (при достаточно раннем обследовании) могут быть отнесены к группе с НДА. НДА может иметь множество клинических вариантов, среди которых в качестве основных описаны следующие [13]:
- олигоартрит крупных суставов;
- асимметричный артрит суставов кисти;
- серонегативный по ревматоидному фактору (РФ) олигоартрит суставов кистей;
- нестойкий полиартрит.
Поскольку клиническую картину хронического артрита нельзя охарактеризовать как сформировавшуюся, что, очевидно, является отражением неполного включения характерных для развернутой стадии РА иммунопатологических механизмов, ряд авторов отмечали склонность НДА к развитию спонтанных ремиссий [6, 11]. Однако в целом это не означает, что у большинства больных НДА прогноз благоприятен. Другие авторы [7–10] особо подчеркивают: НДА является достаточно серьезным состоянием, которое в течение 1 года выливается в достоверный РА в среднем у одной трети больных.
Российские исследователи, основываясь на данных наблюдения за большой когортой больных [9] в рамках программы «Ранний артрит: диагностика, исход, критерии, активное лечение» (РАДИКАЛ), продемонстрировали: из 366 больных с воспалительным поражением суставов и давностью болезни до 1 года только у 57,9% мог быть сразу установлен диагноз РА, 36,3% были классифицированы как имеющие НДА, и только 5,7% при первичном обследовании были поставлены другие диагнозы. Через 12 месяцев диагноз РА был установлен у 33,1% больных с НДА, что подтверждает данные зарубежных исследователей, засвидетельствовавших серьезность прогноза при НДА.
Больные с НДА требуют активного наблюдения. Зачастую для уточнения нозологической формы необходимо многомесячное наблюдение и многократные повторные обследования в динамике, поскольку верификация диагноза по современным представлениям является основой для грамотного обоснования патогенетической терапии. Важнейшим моментом при НДА является определение антицитруллиновых антител, в частности антител к циклическому цитруллинированному пептиду (АЦЦП) преимущественно у больных, серонегативных по РФ. На ранней стадии заболевания данный тест чувствительнее и специфичнее РФ и может использоваться для прогнозирования развития персистирующего артрита у больных НДА [16–19]. Наличие антицитруллиновых антител, особенно при их высоком уровне в сыворотке крови, считается одним из важнейших факторов, определяющих тяжесть и неблагоприятный прогноз у больных НДА.
В то же время ни один отдельно взятый показатель не дает возможность точно предсказать развитие РА у больных НДА [8, 9, 15]. Предложены специальные критерии (prediction rule – «решающее правило»), позволяющие предсказать развитие при НДА «настоящего» РА путем подсчета суммы баллов [12]. Эта методика успешно апробирована за рубежом [20] и в нашей стране [21], опыт ее применения использован при создании последней версии классификационных критериев РА [5]. Наблюдения за пациентами с НДА привели специальный комитет Европейской лиги по борьбе с ревматизмом (EULAR) к необходимости постулировать: в случае выявления у пациента признаков (факторов риска) формирования персистирующего воспалительного заболевания суставов с тенденцией к деструктивному поражению, даже если больной не соответствует классификационным критериям РА, ревматолог должен рассмотреть вопрос о назначении базисных противовоспалительных препаратов (БПВП) [22]. Таким образом, больных НДА с признаками хронизации и структурных нарушений фактически предлагается вести как больных с ранним РА.
Это положение обосновано клиническими наблюдениями и теоретическими соображениями, позволяющими считать возможным развитие лекарственно индуцированной ремиссии у больных НДА, что будет равнозначно отсрочке или даже предотвращению развития типичного РА. Поиск оптимальной схемы лечения пациентов с НДА ведется в течение нескольких последних лет. Как правило, лечение впервые возникшего артрита начинают с назначения симптоматической терапии нестероидными противовоспалительными препаратами (НПВП). В России осуществлено многоцентровое открытое исследование в условиях поликлинической практики [23] с участием более чем 200 пациентов с впервые возникшим артритом. В рамках данной работы проводилась четырехнедельная терапия средними и высокими дозами НПВП (диклофенак и нимесулид) с целью исследовать возможности контроля над симптоматикой и индукции ремиссии. Несмотря на вполне удовлетворительный симптоматический эффект, полное купирование симптоматики наблюдалось лишь в единичных случаях и скорее может быть объяснено хорошо известным фактом развития спонтанной ремиссии у больных НДА. Таким образом, наше исследование доказало, что НПВП не обладают индуцирующим ремиссию эффектом при НДА (так же как при РА).
Применение высоких доз глюкокортикоидов (ГК) при раннем РА всегда вызывало значительный интерес, поскольку хорошо известен мощный противовоспалительный эффект и возможность определенного базисного действия ГК. Международное рандомизированное плацебо-контролируемое исследование SAVE (Stop Arthritis Very Early), в котором также принимали участие российские ревматологи (НИИР РАМН), было посвящено предотвращению развития РА у больных НДА с длительностью симптоматики до 12 недель с помощью болюсного введения высокой дозы пролонгированного глюкокортикоидного препарата (метилпреднизолон-депо 120 мг). В исследование было включено 383 больных из 40 исследовательских центров [24]. В отношении достижения клинической ремиссии, развития РА (по критериям АCR (1987)), потребности в назначении БПВП группы, получавшие активный препарат и плацебо, достоверно не различались. Исследование SAVE показало, что монотерапия ГК при однократном введении высокой дозы не дает возможности контролировать развитие симптоматики хронического артрита при НДА.
В настоящее время все национальные и международные организации ревматологов в качестве «золотого стандарта» лечения РА признают метотрексат (MTX) [25]. Однако в случае неуточненного диагноза (НДА) врачи нередко избегают назначать этот серьезный иммуносупрессивный препарат из-за опасения, что это будет сложно обосновать. В то же время, как уже говорилось выше, существуют рекомендации EULAR [22], согласно которым возможно назначение БПВП пациентам, симптоматика которых еще не соответствует классификационным критериям РА. Кроме того, согласно современной отечественной классификации РА (2007), больные НДА с наличием факторов риска развития РА могут рассматриваться как пациенты с «вероятным РА» [26].
Серьезным аргументом в пользу назначения МТ на самых ранних стадиях развития заболевания стало исследование PROMPT (Th e PRObable rheumatoid arthritis: Methotrexate versus Placebo Treatment) [27]. В этом рандомизированном исследовании 110 больным с «вероятным» РА с длительностью болезни с момента появления симптоматики не более 2 лет назначались: MTX (в начальной дозе 15 мг в неделю с постепенным повышением до 30 мг в неделю(n = 55) или плацебо (n = 55). Длительность лечения составляла 12 месяцев, после чего MTX (либо плацебо) отменялись, и пациенты наблюдались до 30 месяцев. В исследовании PROMPT было показано (рис. 1), что среди получавших MTX развили РА 22 из 55 больных (40%), в то время как среди получавших плацебо – 29 из 55 (53%). При этом в группе MTX появление типичной для РА симптоматики происходило позже (р = 0,04), и у меньшего количества пациентов было отмечено рентгенологическое ухудшение (р = 0,046). Таким образом, раннее назначение метотрексата в дозе 15–30 мг в неделю может замедлять развитие РА, включая рентгенологическое прогрессирование.
Генно-инженерные биологические препараты (ГИБП) весьма привлекательны в отношении индукции ремиссии и абортивного течения РА на ранней стадии, поскольку вызывают быстрое и стойкое клиническое улучшение. В маленькой группе пациентов (n = 17) была проведена попытка применения инфликсимаба при НДА [28]. Результаты показали отчетливое кратковременное улучшение, однако наблюдение в течение 52 недель не продемонстрировало достоверного снижения числа больных, развивших РА, по сравнению с плацебо. Препарат абатацепт (ABA) обладает уникальным механизмом действия, являясь ингибитором костимуляции Т-лимфоцитов, то есть потенциально может обрывать начальный этап развития иммуновоспалительного процесса.
В связи с этим очевиден большой интерес к ABA, который продемонстрировал высокую эффективность при РА у пациентов с ранним артритом. Интересные результаты были продемонстрированы при использовании ABA у больных НДА в рандомизированном исследовании ADJUST [29], куда было включено 56 больных с синовиитом ? 2 сустава, длительностью менее 18 месяцев и положительным тестом на АЦЦП (то есть с высоким риском развития РА). Больным проводился шестимесячный курс ABA или плацебо, после чего пациенты наблюдались до двух лет. К 12 месяцам наблюдения частота развития симптоматики РА (по критериям АCR (1987)) была более чем на 20% ниже (46,2%), чем у получавших плацебо (66,7%) (рис. 2), а рентгенологическое прогрессирование было существенно менее выраженным.
Назначение ABA ассоциировалось с развитием клинической ремиссии: через 6 мес. 71,4% больных, получавших ABA, против 35% на плацебо достигли состояния клинической ремиссии. Через 12 месяцев (после отмены АБА) в ремиссии оставались 47,4% пациентов, получавших активный препарат, против 38,5% на плацебо. Что касается клинической картины, через 6 месяцев 62,5% больных, получавших АБА, не имели припухших и болезненных суставов против 14,3% на плацебо; через 12 месяцев (после отмены ABA) соотношение изменилось до 30% без припухших и болезненных суставов на BA против 14,3% на плацебо.
Рано начатая адекватная терапия метотрексатом и абатацептом продемонстрировала, что лечение может способствовать замедлению развития симптоматики хронического артрита, предотвращая у ряда пациентов прогрессирование из недифференцированного артрита в достоверный ревматоидный артрит. Эти результаты являются весьма многообещающими, поскольку потенциально открывают дорогу для развития нового направления – медикаментозной профилактики хронических воспалительных ревматических заболеваний.
Рано начатая адекватная терапия метотрексатом и абатацептом продемонстрировала, что лечение может способствовать замедлению развития симптоматики хронического артрита, предотвращая у ряда пациентов прогрессирование из недифференцированного артрита в достоверный ревматоидный артрит. Эти результаты являются весьма многообещающими, поскольку потенциально открывают дорогу для развития нового направления – медикаментозной профилактики хронических воспалительных ревматических заболеваний.
1. Насонов Е.Л. Почему необходима ранняя диагностика и лечение ревматоидного артрита? // РМЖ. 2002. Т. 10. № 22. С. 1009–1101.
2. Насонов Е.Л. Ревматоидный артрит как общемедицинская проблема // Терапевтич. архив. 2004. Т. 76. № 5. С. 5–7.
3. Каратеев Д.Е., Лучихина Е.Л., Тогизбаев Г. Современные принципы ведения больных ранним артритом // РМЖ. 2008. Т. 16. № 24. С. 1610–1614.
4. Arnett F.C., Edworthy S.M., Bloch D.A. et al. The american rheumatism association 1987 revised criteria for the classification of rheumatoid arthritis // Arthritis Rheum. Vol. 31. 1988. № 3. P. 315–324.
5. Aletaha D., Neogi T., Silman A.J. et al. 2010 Rheumatoid arthritis classification criteria: an American College of Rheumatology/European League Against Rheumatism collaborative initiative // Ann. Rheum. Dis. Vol. 69. 2010. № 9. P. 1580–1588.
6. Hülsemann J.L., Zeidler H. Undifferentiated arthritis in an early synovitis out-patient clinic // Clin. Exp. Rheumatol. Vol. 13. 1995. № 1. P. 37–43.
7. Machold K.P., Stamm T.A., Eberl G.J.M., Nell V.K.P., Dunky A., Uffmann M., Smolen J.S. Very recent onset arthritis – clinical, laboratory, and radiological findings during the first year of disease // J. Rheumatol. Vol. 29. 2002. № 11. P. 2278–2287.
8. Jansen L.M.A., van Schaardenburg D., van der Horst-Bruinsma I.E., Dijkmans B.A.C. One year outcome of undifferentiated polyarthritis // Ann. Rheum. Dis. Vol. 61. 2002. № 8. P. 700–703.
9. Каратеев Д.Е., Лучихина Е.Л., Тюрина Л.Н. и др. Возможности ранней диагностики ревматоидного артрита в клинической практике на современном этапе (результаты наблюдений за московской когортой больных ранним артритом в рамках программы РАДИКАЛ) // Терапевтич. архив. 2008. Т. 80. № 5. С. 8–13.
10. Quinn M.A., Green M.J., Marzo-Ortega H., Proudman S., Karim Z., Wakefield R.J., Conaghan P.G., Emery P. Prognostic factors in a large cohort of patients with early undifferentiated inflammatory arthritis after application of a structured management protocol // Arthritis Rheum. Vol. 48. 2003. № 11. P. 3039–3045.
11. Van Aken J., van Bilsen J.H.M., Allaart C.F., Huizinga T.W.J., Breedveld F.C. The Leiden Early Arthritis Clinic // Clin. Exp. Rheumatol. 2003. Vol. 21. № 5. Suppl. 31. P. 100–105.
12. Van der Helm-van Mil A.H., le Cessie S., van Dongen H., Breedveld F.C., Toes R.E.M., Huizinga T.W.J. A prediction rule for disease outcome in patients with recent-onset undifferentiated arthritis: how to guide individual treatment decisions // Arthritis Rheum. Vol. 56. 2007. № 2. P. 433–440.
13. Каратеев Д.Е., Лучихина Е.Л. Ранняя диагностика ревматоидного артрита: проблемы и решения // Росс. мед. вести. 2007. № 4. С. 24–27.
14. Firestein G.S. Evolving concepts of rheumatoid arthritis // Nature. 2003. Vol. 423. № 6937. P. 356–361.
15. Dixon W.G., Symmons D.P.M. Does early rheumatoid arthritis exist? // Best Pract. Res. Clin. Rheumatol. Vol. 19. 2005. № 1. P. 37–53.
16. Александрова Е.Н., Чемерис Н.А., Каратеев Д.Е. и др. Антитела к циклическому цитруллинированному пептиду при ревматоидном артрите // Терапевтич. архив. 2004. Т. 76. № 12. С. 64–68.
17. Avouac J., Gossec L., Dougados M. Diagnostic and predictive value of anti-cyclic citrullinated protein antibodies in rheumatoid arthritis: a systematic literature review // Ann. Rheum. Dis. Vol. 65. 2006. № 7. P. 845–851.
18. Svärd A., Kastbom A., Reckner-Olsson A., Skogh T. Presence and utility of IgA-class antibodies to cyclic citrullinated peptides in early rheumatoid arthritis: the Swedish TIRA project // Arthritis Res. Ther. Vol. 10. 2008. № 4. R75.
19. Каратеев Д.Е., Александрова Е.Н., Демидова Н.В. и др. Антицитруллиновые антитела и данные магнито-резонансной томографии суставов кисти у больных ранним артритом // Терапевтич. архив. 2008. Т. 80. № 10. С. 72–77.
20. Van der Helm-van Mil A.H., Detert J., le Cessie S., Filer A., Bastian H., Burmester G.R., Huizinga T.W.J., Raza K. Validation of a prediction rule for disease outcome in patients with recent-onset undifferentiated arthritis: moving toward individualized treatment decision-making // Arthritis Rheum. Vol. 58. 2008. № 8. P. 2241–2247.
21. Лучихина Е.Л., Каратеев Д.Е., Новиков А.А., Насонов Е.Л. Прогнозирование развития ревматоидного артрита у больных с ранним недифференцированным артритом // Научно-практич. ревматол. 2009. № 2. С. 31–37.
22. Combe B., Landewe R., Lukas C., Bolosiu H.D., Breedveld F., Dougados M., Emery P., Ferraccioli G., Hazes J.M.W., Klareskog L., Machold K., Martin-Mola E., Nielsen H., Silman A., Smolen J., Yazici H. EULAR recommendations for the management of early arthritis: report of a task force of the European Standing Committee for International Clinical Studies Including Therapeutics (ESCISIT) // Ann. Rheum. Dis. Vol. 66. 2007. № 1. P. 34–45.
23. Каратеев А.Е., Каратеев Д.Е., Лучихина Е.Л. и др. Эффективность и безопасность монотерапии высокими дозами НПВП при раннем артрите (открытое рандомизированное контролируемое 4-недельное исследование эффективности высоких и среднетерапевтических доз нимесулида и диклофенака при раннем артрите) // РМЖ. 2006. Т. 14. № 25. С. 1805–1809.
24. Machold K.P., Landewé R., Smolen J.S., Stamm T.A., van der Heijde D.M., Verpoort K.N., Brickmann K., Vázquez-Mellado J., Karateev D.E., Breedveld F.C., Emery P., Huizinga T.W.J. Extended report: The Stop Arthritis Very Early (SAVE) trial, an international multicentre, randomised, double-blind, placebo-controlled trial on glucocorticoids in very early arthritis // Ann. Rheum. Dis. Vol. 69. 2010. № 3. P. 495–502.
25. Ревматология. Клинические рекомендации / Под ред. Е.Л. Насонова. М.: ГЭОТАР-Медиа, 2006.
26. Каратеев Д.Е., Олюнин Ю.А. О классификации ревматоидного артрита // Научно-практич. ревматол. 2008. № 1. С. 5–16.
27. Van Dongen H., van Aken J., Lard L.R., Visser K., Ronday H.K., Hulsmans H.M.J., Speyer I., Westedt M.-L., Peeters A.J., Allaart C.F., Toes R.E.M., Breedveld F.C., Huizinga T.W.J. Efficacy of methotrexate treatment in patients with probable rheumatoid arthritis: a double-blind, randomized, placebo-controlled trial // Arthritis Rheum. Vol. 56. 2007. № 5. P. 1424–1432.
28. Saleem B., Mackie S., Quinn M., S Nizam, Hensor E., Jarrett S., Conaghan P.G., Emery P. Does the use of tumour necrosis factor antagonist therapy in poor prognosis, undifferentiated arthritis prevent progression to rheumatoid arthritis? // Ann. Rheum. Dis. Vol. 67. 2008. № 8. P. 1178–1180.
29. Emery P., Durez P., Dougados M., Legerton C.W., Becker J.-C., Vratsanos G., Genant H.K., Peterfy C., Mitra P., Overfield S., Qi K., Westhovens R. Extended report: Impact of T-cell costimulation modulation in patients with undifferentiated inflammatory arthritis or very early rheumatoid arthritis: a clinical and imaging study of abatacept (the ADJUST trial) // Ann. Rheum. Dis. Vol. 69. 2010. № 3. P. 510–516.
Новости на тему
25.02.2025
14.09.2023
11.08.2023
07.11.2022
Отправить статью по электронной почте
Ваш адрес электронной почты:
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.