Спектральная оптическая когерентная томография в режиме enhanced depth imaging в диагностике начальных новообразований хориоидеи
- Аннотация
- Статья
- Ссылки
Методическое пособие, подготовленное В.В. Нероевым, д.м.н., профессором, директором Московского НИИ глазных болезней им. Гельмгольца, С.В. Саакян, д.м.н., профессором кафедры глазных болезней Медицинского государственного медико-стоматологического университета, Е.Б. Мякошиной, к.м.н., научным сотрудником отдела офтальмоонкологии и радиологии Московского НИИ глазных болезней им. Гельмгольца, предназначено для врачей-офтальмологов поликлиник, специализированных офтальмологических стационаров и консультативных центров.
Методическое пособие, подготовленное В.В. Нероевым, д.м.н., профессором, директором Московского НИИ глазных болезней им. Гельмгольца, С.В. Саакян, д.м.н., профессором кафедры глазных болезней Медицинского государственного медико-стоматологического университета, Е.Б. Мякошиной, к.м.н., научным сотрудником отдела офтальмоонкологии и радиологии Московского НИИ глазных болезней им. Гельмгольца, предназначено для врачей-офтальмологов поликлиник, специализированных офтальмологических стационаров и консультативных центров.
Введение
Последние годы наблюдается рост распространенности новообразований органа зрения – 11–12 случаев на 100 000 населения. У большинства пациентов, обратившихся за медицинской помощью, регистрируется далеко зашедшая стадия заболевания, что требует хирургического вмешательства, приводит к инвалидизации и снижению качества жизни. Утрата зрительных функций, метастазирование, неблагоприятный жизненный прогноз при первичных злокачественных опухолях определяют медицинскую и социальную значимость своевременной адекватной терапии, особенно органосохраняющего характера. Проведение подобных мероприятий возможно только при раннем выявлении внутриглазных опухолей хориоидеи.
Несмотря на многообразие современных высокотехнологичных инструментальных методов исследования, часто диагноз злокачественной опухоли при детальном обследовании не подтверждается. Вместе с тем выявление меланомы хориоидеи на начальной стадии связано с некоторыми сложностями из-за полиморфизма клинической картины.
Золотым стандартом ранней диагностики патологии заднего полюса глаза остается флуоресцентная ангиография (ФАГ). Последние десятилетия активно применяется метод аутофлуоресценции. Однако на основании только ФАГ провести дифференциальную диагностику злокачественной опухоли с другими заболеваниями, симулирующими ее, не всегда удается.
Опухоли хориоидеи подразделяют на доброкачественные (стационарный и прогрессирующий невус, отграниченная гемангиома, меланоцитома) и злокачественные (меланома, метастаз).
Клинически стационарные невусы хориоидеи характеризуются плоским пигментированным или беспигментным очагом с ровными четкими границами, гладкой поверхностью.
Прогрессирующие невусы проявляются проминирующим фокусом в постэкваториальной зоне аспидного или светло-серого цвета с зеленоватым оттенком, диаметром 0,5–4,5 мм, четкими или нечеткими перистыми очертаниями, неровной поверхностью. Зачастую выявляют экссудативные изменения в прилежащей сетчатке, поражение ретинального пигментного эпителия (РПЭ) (компрессию, дегенерацию, облитерацию хориокапилляров с формированием друз, серозную отслойку РПЭ), снижающие остроту зрения и провоцирующие появление дефектов в поле зрения. Сходство клинической картины можно объяснить общим происхождением от клетки-родоначальника – меланоцита при невусе хориоидеи и увеальной меланоме.
Офтальмоскопически отграниченная гемангиома хориоидеи представляет собой очаг постэкваториальной локализации розового, желтовато-серого или оранжевого цвета округлой или овальной формы с неровными нечеткими границами, наличием бледных или пигментированных очагов в прилежащем РПЭ и микрокист или крупных полостей в нейроэпителии, обильной васкуляризацией.
Меланоцитому отличает густопигментированный темно-коричневый или черный проминирующий фокус, расположенный папиллярно, юкстапапиллярно, реже на средней периферии, с неровными нечеткими перистыми границами, неровной поверхностью.
Клинически начальная меланома хориоидеи визуализируется как проминирующий, чаще солитарный очаг, цвет которого варьируется от желтого до темно-аспидного, округлой или овальной формы, с неровными нечеткими границами, гладкой или неровной поверхностью, оранжевым пигментом и наличием субретинальной жидкости, преимущественно постэкваториальной локализации.
При метастазировании рака молочной железы в хориоидею на глазном дне выявляют диффузный, быстро разрастающийся, проминирующий очаг кремового или бледно-желтого цвета, c пигментированными гранулами на поверхности, преобладанием диаметра над проминенцией. Часто наблюдается вторичная распространенная отслойка сетчатки с транссудатом над опухолью и в отдаленных зонах глазного дна, сопровождающаяся отеком диска зрительного нерва.
При метастазах меланомы кожи имеет место очаг темно-серого или коричневого оттенка, при метастазах почечно-клеточной карциномы и рака щитовидной железы – очаг оранжево-красного цвета. При раке легкого, кишечника метастаз имеет двугорбую или трехгорбую форму, наблюдаются кровоизлияния на поверхности опухоли и гемофтальм. Однако в ряде случаев офтальмоскопическая картина исследуемых опухолей может быть сходной, в связи с чем требуются дополнительные обследования, позволяющие провести дифференциальную диагностику злокачественных и доброкачественных опухолей, а следовательно, назначить своевременное адекватное лечение.
Метод оптической когерентной томографии (ОКТ), разработанный в конце прошлого века и в настоящее время модифицированный для изучения не только сетчатки, но и хориоидеи в режиме enhanced depth imaging, все чаще применяется в ранней диагностике заболеваний глазного дна [1–15]. Однако единая интерпретация дифференциально-диагностических томографических признаков начальных внутриглазных опухолей хориоидеи до сих пор не разработана.
Показания и противопоказания
Оптическая когерентная томография показана в целях диагностики и дифференциальной диагностики начальных опухолей хориоидеи: невуса (стационарного и прогрессирующего), отграниченной гемангиомы, меланоцитомы, меланомы и метастаза.
Противопоказаниями являются:
- психические заболевания в анамнезе;
- недостаточная прозрачность преломляющих сред глаза;
- проминенция опухоли более 3,5 мм.
Материально-техническое обеспечение
- Спектральный оптический когерентный томограф SOCT Copernicus HR (Optopol, Польша).
- Ретиноангиотомограф HRA + OCT в режиме enchanced depth imaging (Heidelberg, Германия).
Описание медицинской технологии
Обследовано 677 больных, рандомизированных на шесть групп:
- 1-я группа: 77 больных (56 женщин, 21 мужчина, возраст 63,02 ± 2,6 года), 154 глаза – стационарные невусы хориоидеи;
- 2-я группа: 103 больных (72 женщины, 31 мужчина, возраст 60,9 ± 1,88 года), 206 глаз – прогрессирующие невусы хориоидеи;
- 3-я группа: 17 больных (6 женщин, 11 мужчин, возраст 49,6 ± 0,77 года), 34 глаза – меланоцитома;
- 4-я группа: 92 больных (35 женщин, 57 мужчин, возраст 50,7 ± 0,24 года), 184 глаза – отграниченная гемангиома хориоидеи;
- 5-я группа: 344 больных (226 женщин, 118 мужчин, возраст 59,1 ± 0,09 года), 688 глаз – начальная меланома хориоидеи;
- 6-я группа: 44 больных (32 женщины, 12 мужчин, возраст 58,3 ± 1,95 года), 88 глаза – метастаз в хориоидею.
Манифестацию начальных опухолей хориоидеи наблюдали чаще у женщин в возрасте 51–70 лет.
Показанием для офтальмоскопии служили снижение зрения, метаморфопсия, искажение формы предметов. После двукратной инстилляции раствором алкаина на переднюю поверхность роговицы устанавливали трехзеркальную линзу Гольдмана. На глазном дне выявляли патологический очаг. Затем проводили ультразвуковое исследование (УЗИ). По данным эхографии, проминенция очага составила от 1,0 до 3,0 мм (в среднем 2,1 ± 0,15 мм), диаметр основания – 3,0 до 10,0 мм (в среднем 7,95 ± 0,17 мм). После офтальмоскопии и УЗИ выполняли ОКТ.
Технически ОКТ осуществляется следующим образом. Пациент размещает подбородок на подставке и фиксирует взгляд на мигающем объекте в линзе фундус-камеры. Камера приближается к глазу до тех пор, пока изображение сетчатки не отобразится на мониторе. После этого камера закрепляется нажатием кнопки фиксатора и регулируется четкость изображения. Если острота зрения низкая и пациент не видит мигающий объект, используется внешняя подсветка. Пациент должен смотреть прямо перед собой не мигая. Оптимальное расстояние между глазом и линзой камеры – 9 мм. Исследовали зону очага, макулу и сопредельные с опухолью зоны.
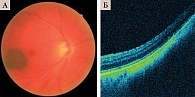
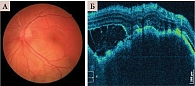
При стационарном невусе хориоидеи у 77 больных (77 глаз) во всех случаях диагностирован ровный хориоидальный профиль. В хориоидее – компрессия хориокапилляров с узким ровным «поясом» с эффектом тени (рис. 1).
При прогрессирующем невусе хориоидеи у 103 больных (103 глаза) отмечалось незначительное веретенообразное изменение хориоидального профиля. Томографически диагностированы потеря, ретракция, нерегулярность светочувствительных клеток. В случае прогрессирующих невусов хориоидеи имело место скопление интра- и субретинальной жидкости, проявлявшееся кистовидным отеком, локальной отслойкой нейроэпителия. Изменения в РПЭ характеризовались отслойкой с гиперрефлективным содержимым (друзой).
В хориоидее выявлена компрессия хориокапилляров с узким ровным «поясом» с эффектом тени во всех случаях, что затрудняло визуализацию увеальных сосудов (рис. 2).
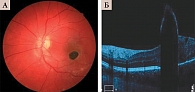
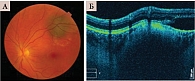
Томографически меланоцитома у 17 больных (17 глаз) характеризовалась резко приподнятым, гиперрефлективным, истонченным слоем ткани над очагом (возможно, пролиферация глиальных элементов с пигментной абсорбцией в случае папиллярной локализации) с оптическим затемнением под ним, соответствующим расположению очага. Зафиксированы резкое истончение и полная дезорганизация ретинальных слоев с отсутствием визуализации каждого слоя в отдельности (рис. 3).
Кроме того, выявлены атрофически-деструктивные изменения в прилежащей к образованию сетчатке (гиперрефлективность), что позволило дифференцировать меланоцитому от начальной меланомы хориоидеи.
Визуализация хориоидеи и ее сосудов оказалась затруднительной из-за эффекта тени. Меланоцитома характеризовалась отсутствием интра- и субретинальной жидкости.
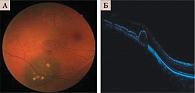
Томографически при отграниченной гемангиоме хориоидеи у 92 больных (92 глаза) отмечалось дугообразное изменение хориоидального профиля с гладким контуром (рис. 4).
У пациентов с отграниченной гемангиомой хориоидеи выявлены нерегулярность фоторецепторов, интра- и субретинальное скопление жидкости. Вместе с тем отмечались томографические особенности скопления экссудата, характерные для отграниченной гемангиомы хориоидеи: сегментарные отслойки нейроэпителия, кистовидные полости больших размеров, диффузный отек.
При отграниченной гемангиоме хориоидеи обнаружена отслойка РПЭ с гипорефлективным содержимым.
Дезорганизация пигмента в РПЭ характеризовалась формированием пигментных фокусов преимущественно на уровне РПЭ.
Дефекты РПЭ при отграниченной гемангиоме хориоидеи имели место в 87% случаев. При гемангиоме хориоидеи хориокапилляры визуализировались во всех случаях. В зоне локализации опухоли определялась оптическая тень с нечеткими контурами опухоли.
У пациентов с метастатической карциномой хориоидеи наблюдалось мелкобугристое изменение хориоидального профиля (рис. 5).
Томографической особенностью слоя нейроэпителия при метастатической карциноме хориоидеи оказалась потеря фоторецепторов во всех случаях.
Интра- и субретинальное скопление жидкости проявлялось расслоением сетчатки на уровне средних и внутренних слоев, отслойками РПЭ с гипорефлективным содержимым, отслойкой нейроэпителия, кистовидным отеком.
Дезорганизация РПЭ в случае метастатической карциномы хориоидеи характеризовалась наличием пигментных фокусов на уровне средних и внутренних слоев сетчатки.
На уровне хориоидеи отмечалась частичная компрессия хориокапилляров с узким ровным «поясом», визуализацией склеры и хориокапилляров.
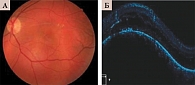
Томографически при начальной меланоме хориоидеи у всех 344 обследуемых больных наблюдалось формирование дугообразного изменения хориоидального профиля вследствие объемного опухолевого процесса в сосудистой оболочке. Регистрировалась дольчатость фоторецепторов (рис. 6).
У пациентов с начальной меланомой хориоидеи диагностировано появление интра- и субретинальной жидкости в виде диффузного кистовидного отека и отслойки нейроэпителия.
При начальной меланоме хориоидеи слой РПЭ видоизменяется. Томография показывает отслойку РПЭ с гиперрефлективным содержимым, дезорганизацией пигмента РПЭ с формированием пигментных фокусов, локализующихся на разных уровнях сетчатки, и дефекты пигментного эпителия.
Отслойка пигментного эпителия при начальной меланоме хориоидеи проявляется его приподнятостью вместе со всей сетчаткой над слоем хориокапилляров и имеет вид холма, верхние контуры которого окаймлены высокорефлективной полосой РПЭ.
Для начальной меланомы хориоидеи характерно гиперрефлективное содержимое отслойки, морфологически связанное с друзами.
При дезорганизации пигмента в РПЭ формируются пигментные фокусы в виде скопления пигмента, высвободившегося из клеток РПЭ.
Локализация пигментных фокусов выявлена на уровне РПЭ, средних и внутренних слоев сетчатки.
Нарушение структуры сетчатки проявлялось также окончатыми дефектами РПЭ, диагностируемыми на томограмме оптически гипорефлективными зонами на уровне пигментного эпителия.
При начальной меланоме хориоидеи выявлена компрессия хориокапилляров с узким ровным «поясом» с эффектом тени во всех случаях, вследствие чего измерить калибр увеальных сосудов не удалось.
Осложнения при использовании медицинской технологии
Использование медицинской технологии осложнениями не сопровождалось.
Эффективность медицинской технологии
У 677 больных изучены томографические признаки новообразований хориоидеи:
- стационарные невусы хориоидеи (n = 77);
- прогрессирующие невусы (n = 103);
- меланоцитома (n = 17);
- отграниченная гемангиома (n = 92);
- начальная меланома (n = 344);
- метастазы в хориоидею (n = 44).
Показаны особенности каждой нозологии. Благодаря расширению диагностических возможностей за счет внедрения спектральных оптических томографов процент установления правильного диагноза увеличился. В свою очередь своевременное выявление злокачественных опухолей (начальной меланомы хориоидеи и метастазов в хориоидее) позволяет проводить раннее адекватное органосохраняющее лечение, способствующее снижению инвалидизации и улучшению жизненного прогноза пациентов.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.