Сравнительная оценка эффективности антибактериальной терапии острых кишечных инфекций у беременных и ее безопасности для новорожденных
- Аннотация
- Статья
- Ссылки
- English
Количество работ, посвященных антибактериальной терапии ОКИ у беременных, ограниченно. Описано применение цефтриаксона, амоксициллина с клавулановой кислотой, секнидазола и офлоксацина для лечения шигеллеза у беременных. Однако не рассматривается вопрос влияния данных антибактериальных препаратов на состояние новорожденных.
Цель – оценить эффективность этиотропной терапии ОКИ у беременных на доношенном сроке гестации и небеременных и ее влияние на состояние новорожденных.
Материал и методы. Проведен сравнительный анализ течения ОКИ и состояния новорожденных по шкале Апгар в трех группах. Основную группу составили 60 беременных с ОКИ, родоразрешенных на доношенном сроке, группу сравнения 1 – 60 здоровых беременных, родоразрешенных на доношенном сроке, группу сравнения 2 – 30 небеременных с ОКИ.
Выводы. Результаты исследования показали, что антибактериальная терапия, проводимая у рожениц с ОКИ с доношенным сроком беременности, безопасна для новорожденных. Эффективность лечения ОКИ у беременных препаратами цефалоспоринов третьего поколения и производными нитрофурана сопоставима.
Количество работ, посвященных антибактериальной терапии ОКИ у беременных, ограниченно. Описано применение цефтриаксона, амоксициллина с клавулановой кислотой, секнидазола и офлоксацина для лечения шигеллеза у беременных. Однако не рассматривается вопрос влияния данных антибактериальных препаратов на состояние новорожденных.
Цель – оценить эффективность этиотропной терапии ОКИ у беременных на доношенном сроке гестации и небеременных и ее влияние на состояние новорожденных.
Материал и методы. Проведен сравнительный анализ течения ОКИ и состояния новорожденных по шкале Апгар в трех группах. Основную группу составили 60 беременных с ОКИ, родоразрешенных на доношенном сроке, группу сравнения 1 – 60 здоровых беременных, родоразрешенных на доношенном сроке, группу сравнения 2 – 30 небеременных с ОКИ.
Выводы. Результаты исследования показали, что антибактериальная терапия, проводимая у рожениц с ОКИ с доношенным сроком беременности, безопасна для новорожденных. Эффективность лечения ОКИ у беременных препаратами цефалоспоринов третьего поколения и производными нитрофурана сопоставима.
Введение
Применение этиотропной терапии при острых кишечных инфекциях (ОКИ) во время беременности имеет ряд ограничений. Значительное число антибактериальных препаратов, которые применяют при ОКИ, не разрешены для использования во время гестации из-за потенциального влияния на организм женщины и плода.
Работы, посвященные антибактериальной терапии ОКИ у беременных, немногочисленны. Описано применение цефтриаксона, амоксициллина с клавулановой кислотой, секнидазола и офлоксацина для лечения беременных с шигеллезом [1].
Терапия фторхинолонами, аминогликозидами и сульфаниламидными препаратами, широко используемыми при ОКИ, противопоказана во время беременности. В актуальных клинических рекомендациях, касающихся ведения взрослых с шигеллезом и сальмонеллезом, не говорится об особенностях оказания медицинской помощи и антибактериальной терапии при беременности. В то же время в документе рассматривается применение цефалоспоринов третьего поколения, разрешенных во время беременности и лактации. В утвержденных в 2024 г. клинических рекомендациях по лечению взрослых с ОКИ для этиотропной терапии во время беременности рекомендованы цефалоспорины третьего поколения и бактериофаги [2–4].
Нами не найдены отечественные работы по оценке безопасности и эффективности антибактериальных препаратов при лечении ОКИ во время беременности и по их влиянию на новорожденных.
Цель – оценить эффективность этиотропной терапии ОКИ у беременных и небеременных и ее влияние на состояние новорожденных.
Материал и методы
В исследовании участвовало 150 женщин, получавших лечение по поводу ОКИ и родоразрешенных в акушерском отделении Клинической инфекционной больницы им. С.П. Боткина Санкт-Петербурга в 2017–2019 гг. Женщин разделили на три группы. Основную группу составили 60 беременных с ОКИ, родоразрешенных на доношенном сроке, группу сравнения 1 – 60 здоровых беременных, родоразрешенных на доношенном сроке, группу сравнения 2 – 30 небеременных репродуктивного возраста с ОКИ.
Этиотропные препараты назначали эмпирически, принимая во внимание клинические проявления заболевания и эпидемиологический анамнез.
Эффективность антибактериальной терапии оценивали на основании изменений показателей температуры тела, частоты рвоты и дефекации в течение первых трех дней госпитализации. Состояние новорожденных анализировали по шкале Апгар через одну и пять минут после рождения.
Протокол исследования и форма информированного согласия одобрены этическим комитетом ФГБОУ ВО «ПСПбГМУ им. И.П. Павлова» Минздрава России. Все женщины, принявшие участие в исследовании, дали письменное добровольное согласие.
Статистическую обработку результатов проводили с использованием IBM SPSS Statistics 24.
Результаты и обсуждение
Средний возраст женщин основной группы составил 27,4 ± 4,2 года и значимо не отличался от возраста женщин групп сравнения (28,9 ± 4,5 и 28,5 ± 6,2 соответственно).
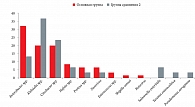
Этиологическая расшифровка возбудителей ОКИ не выявила статистически достоверных различий у беременных (n = 60) и небеременных (n = 30). У беременных ОКИ были вызваны преимущественно условно-патогенной флорой. Так, Enterobacter spp. выявлена в 19 (32%) случаях, Klebsiella spp. – в 12 (20%) и Citrobacter spp. – в 12 (20%) случаях. Реже ОКИ были вызваны Hafnia spp., Proteus spp. и Enterococcus spp. Лишь в одном случае установлена дизентерия Зонне. ОКИ вирусной этиологии ассоциировались с Norovirus в 4 (6,5%) и с Rotavirus в 1 (1,6%) случае.
У небеременных ОКИ чаще были связаны с Klebsiella spp. – 11 (36,6%), Citrobacter spp. – 7 (23,3%) и Enterobacter spp. – 4 (13,3%) случая. Реже выявляли Salmonella enteritidis и Hafnia spp., а также Proteus spp., Yersinia enterocolitica и Pseudomonas aeruginosa. ОКИ вирусной этиологии зарегистрирована у одной больной (рисунок).
ОКИ у небеременных достоверно чаще сопровождались лихорадкой по сравнению с беременными (85,7 и 43,3% соответственно; р = 0,001). Менее выраженная лихорадочная реакция у женщин во время беременности, вероятно, связана с выработкой плацентой кортикостероидов [5], которые способствуют уменьшению продукции медиаторов воспаления и арахидоновой кислоты, приводя к снижению образования простагландинов и эндогенных пирогенов [6].
Диарея зарегистрирована у всех беременных и небеременных с ОКИ. Рвота отмечалась у 36 (60%) больных основной группы и 13 (46,4%) – группы сравнения 2.
Этиотропное лечение назначали эмпирически, принимая во внимание клинические проявления ОКИ и эпидемиологический анамнез. Антибиотики назначали с момента поступления в стационар 30 (50%) беременным и 28 (93%) небеременным с ОКИ. Цефалоспорины третьего поколения получали 17 (56,6%) беременных, производные нитрофурана – 11 (36,6%), антибиотики пенициллинового ряда – 2 (6,8%). Необходимо отметить, что в период проведения исследования беременность не являлась противопоказанием к назначению нифуроксазида согласно инструкции к его применению. В настоящее время использование данного препарата при беременности противопоказано.
Небеременным цефалоспорины третьего поколения назначали в 16 (57,1%) случаях, производные нитрофурана – в 5 (17,9%), фторхинолоны – в 7 (25%) случаях.
Сравнительный анализ терапевтического эффекта цефалоспоринов третьего поколения и производных нитрофурана на течение ОКИ у беременных и небеременных не выявил различий в динамике показателей температуры тела, частоты рвоты и дефекации. Не установлено и различий в частоте диареи и рвоты, динамике их купирования у больных, получавших антибиотики.
Срок родоразрешения на момент поступления в стационар у беременных с ОКИ составил 39,3 ± 1,1 недели, а у здоровых беременных – 39,2 ± 1,0 недели. Различий в оценке новорожденных по шкале Апгар через одну и пять минут после родов у матерей с ОКИ и без ОКИ не выявлено (7,8 ± 0,4 и 7,9 ± 0,1, 8,7 ± 0,4 и 8,9 ± 0,2 соответственно). Не установлена также связь между антибактериальной терапией ОКИ у рожениц и показателями по шкале Апгар при сравнении состояния детей, рожденных женщинами, получавшими и не получавшими антибиотики (группа сравнения 1). Дети, рожденные от женщин обеих групп, не потребовали перевода в детские стационары города и были выписаны в удовлетворительном состоянии (как и матери). Однако пребывание после родов в стационаре новорожденных и родильниц основной группы было более продолжительным (5,1 ± 1,2 дня; F = 25,634; p < 0,001), чем здоровых родильниц и их детей (4,0 ± 1,0 дня). Это обусловлено ожиданием результата посева кала у женщин основной группы.
Выводы
Эффективность лечения беременных с ОКИ препаратами цефалоспоринов третьего поколения и производными нитрофурана сопоставима. Показано, что их применение у рожениц с доношенным сроком беременности безопасно для новорожденных. Однако в связи с небольшой выборкой пациенток, получавших производные нитрофурана, необходимы дальнейшие исследования влияния указанных препаратов на состояние новорожденных.
В целях повышения качества оказания медицинской помощи беременным с сопутствующими ОКИ требуется разработка рекомендаций по ведению таких пациенток и тактике этиотропной и патогенетической терапии инфекционного процесса.
Финансирование. Работа проведена на личные средства авторского коллектива.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
A.S. Kovalchuk, D.A. Lioznov, PhD, Prof., A.V. Samarina, PhD, Prof., A.N. Kucheryavenko, PhD
Clinical Infectious Diseases Hospital named after S.P. Botkin, Saint Petersburg
Academician I.P. Pavlov First St. Petersburg State Medical University
Smorodintsev Research Institute of Influenza, Saint Petersburg
Center for the Prevention and Control of AIDS and Infectious Diseases, Saint Petersburg
Contact person: Aleksey S. Kovalchuk, Babai_Jo@bk.ru
Relevance. The use of antibacterial drugs for acute intestinal infections (AII) during pregnancy has a number of limitations. Drugs used for acute kidney injury outside of pregnancy are not allowed for use during gestation due to the potential effect not only on the woman's body, but also on the fetus. The number of papers devoted to the antibacterial therapy of AII in pregnant women is limited. The use of ceftriaxone, amoxicillin with clavulanic acid, secnidazole and ofloxacin for the treatment of shigellosis in pregnant women is described. However, the issue of the effect of these antibacterial drugs on the condition of newborns is not being considered.
The aim is to evaluate the effectiveness of etiotropic therapy of AII in pregnant women at full term gestation and non-pregnant women and its effect on the condition of newborns.
Material and methods. A comparative analysis of the course of AII and the condition of newborns on the Apgar scale in three groups was carried out. The main group consisted of 60 pregnant women with AII who were delivered at full term, the comparison group 1 consisted of 60 healthy pregnant women who were delivered at full term, and the comparison group 2 consisted of 30 non-pregnant women with AII.
Results. The results of the study showed that antibacterial therapy performed in women with full term AII is safe for newborns. The effectiveness of treatment of AII in pregnant women with third-generation cephalosporins and nitrofuran derivatives is comparable.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.