V Российский конгресс по остеопорозу и другим метаболическим заболеваниям скелета. Нерешенные задачи в лечении остеопороза. Ключевые факторы успеха
- Аннотация
- Статья
- Ссылки






Ключевые факторы успеха в лечении остеопороза. Двойное действие деносумаба на кортикальную и трабекулярную костную ткань
Остеопороз – заболевание скелета, характеризующееся снижением плотности кости и предрасполагающее к повышенному риску переломов. Профессор Колумбийского университета (США) Джон БИЛЕЗИКЯН (John BILEZIKIAN) посвятил свой доклад анализу эффективности препарата деносумаб (Пролиа) в предотвращении риска остеопоротических переломов за счет улучшения качества кортикальной и трабекулярной костной ткани. «Благодаря научным открытиям в области ремоделирования кости мы очень быстро смогли получить инновационные препараты с уникальным механизмом действия, ярким представителем которых является препарат деносумаб», – отметил докладчик.
Кортикальная костная ткань составляет около 80% общей массы скелета. Количественное распределение кортикальной и трабекулярной костной ткани варьирует в зависимости от участка скелета. Так, кортикальная кость преобладает в диафизах длинных трубчатых костей. Даже позвонки, преимущественно представленные трабекулярной костью, содержат значительную часть кортикальной костной ткани. В ходе многочисленных исследований была установлена значимая корреляция между истончением кортикальной кости и риском переломов. Именно поэтому терапевтическая цель должна состоять в увеличении кортикальной и трабекулярной костной массы.
Костное ремоделирование зависит от активности остеокластов, разрушающих кальцинированный костный матрикс, и остеобластов, синтезирующих новое основное вещество кости. Ключевая роль в развитии остеопороза принадлежит цитокиновой системе RANK/RANKL/OPG (Receptor activator of nuclear factor kappa-B – рецептор активатора ядерного фактора каппа-В, Receptor activator of nuclear factor kappa-B ligand – лиганд RANK, osteoprotegerin – остеопротегерин). RANKL, соединяясь с RANK, запускает процесс дифференцировки активного остеокласта. Активный остеокласт формирует кислую среду, выделяет катепсин К – фермент, способствующий расщеплению белка. Катепсин K играет ключевую роль в тканевой деструкции, ремоделировании и деградации хряща. Он способен разрушить самую крепкую костную ткань в организме. OPG, связывая RANKL, останавливает миграцию остеокластов. В результате запускается процесс синтеза костного матрикса. Доказано, что лиганд RANK – один из самых мощных стимуляторов резорбции костной ткани, способствующий снижению минеральной плотности костной ткани (МПКТ), ее объема и прочности, а OPG – своеобразная антирезорбтивная молекула1. Нарушение соотношения RANKL/OPG может привести к ускоренной потере костной массы.
Деносумаб является полностью человеческим моноклональным антителом к лиганду RANK, он способен контролировать систему RANKL/RANK. Это изотип иммуноглобулина G₂ с высокой аффинностью и специфичностью к RANKL, который подобно OPG предотвращает доступ лиганда RANK к его рецептору, контролируя активацию и выживаемость остеокласта. Связывая RANKL подобно OPG, деносумаб предотвращает взаимодействие между RANK и RANKL, снижает дифференцировку, активность и жизнеспособность остеокласта, подавляя костную резорбцию. Будучи биологическим препаратом, деносумаб не накапливается в костной ткани. Средний период полувыведения – 34 дня.
Эффективность препарата деносумаб (Пролиа) в отношении снижения риска переломов доказана в ходе исследований. В настоящее время имеются данные исследований III фазы, посвященных оценке эффективности препарата у женщин в постменопаузальном периоде.
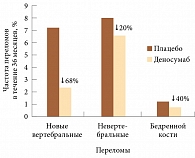
В базовом международном плацебоконтролируемом исследовании III фазы FREEDOM (The fracture reduction evaluation of denosumab in osteoporosis every 6 months – оценка снижения частоты переломов при применении деносумаба каждые 6 месяцев у больных остеопорозом) участвовали 7868 женщин с постменопаузальным остеопорозом (средний возраст 72,3 года). 23% женщин имели переломы позвонков до начала исследования. Пациентки были в равном соотношении распределены на 2 группы: группу плацебо и группу деносумаба (60 мг каждые 6 месяцев в течение 3 лет)2. В целом за 3 года применения деносумаба снизился относительный риск вертебральных переломов на 68%, невертебральных – на 20%, переломов бедренной кости – на 40% по сравнению с группой плацебо (рис. 1). Снижение частоты переломов также было отмечено в группах с повышенным риском переломов.
«Деносумаб прекрасно работает и у пациентов с более высоким риском переломов, и у пациентов с более низким риском. Таким образом, мы получили высокоэффективный препарат универсального действия», – отметил профессор Д. Билезикян.
В июне 2010 г. препарат деносумаб был одобрен FDA (Food and Drug Administration – Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США) для лечения пациентов с высоким риском переломов, множественными низкоэнергетическими переломами, а также пациентов, у которых предшествующая терапия оказалась неэффективной или непереносимой.
На сегодняшний день имеются данные об эффективности и безопасности длительного непрерывного применения деносумаба в течение 8 лет (расширенная фаза исследования FREEDOM). Эти данные демонстрируют продолжающийся на фоне применения препарата прирост МПКТ позвоночника (+18,5%) и бедра (+8,2%) по сравнению с плацебо. Достоверное повышение МПКТ в дистальном отделе лучевой кости свидетельствовало о влиянии деносумаба на кортикальную кость, что не отмечалось ранее при лечении другими антиостеопоротическими препаратами3, 4.
Деносумаб, ингибируя RANKL, подавляет формирование и активность остеокластов без связывания с костным матриксом, поэтому у деносумаба воздействие на кортикальную кость более выражено, чем у бисфосфонатов. Результаты сравнительного многоцентрового двойного слепого исследования с активным контролем по оценке влияния деносумаба и алендроната на микроархитектонику костной ткани продемонстрировали, что лечение деносумабом приводит к более выраженному повышению МПКТ. Эффективность деносумаба в отношении уменьшения порозности трабекулярной и кортикальной костной ткани изначально была показана в исследованиях у животных. В дальнейшем эффективность препарата была подтверждена в исследовании с участием женщин в постменопаузе: прием деносумаба в отличие от алендроната способствовал снижению порозности кортикальной костной ткани5–7. Опубликованные в октябре 2013 г. результаты исследования R.M. Zebaze и соавт. продемонстрировали благоприятное воздействие деносумаба на снижение кортикальной порозности бедренной кости8. Доказано, что деносумаб значимо и прогрессивно по сравнению с плацебо увеличивает массу кортикальной кости (р < 0,0001) в проксимальном отделе бедренной кости, причем изменения именно в этом отделе обычно приводят к переломам шейки бедра9.
«Деносумаб благодаря снижению кортикальной порозности прогрессивно и значимо увеличивает кортикальную массу проксимального отдела бедренной кости, увеличивает минеральную плотность кортикальной и трабекулярной кости», – констатировал профессор Д. Билезикян.
В ходе исследований FREEDOM, STAND (The study of transitioning from Alendronate to Denosumab – исследование перехода с алендроната на деносумаб), DEFEND (The Denosumab Fortifies Bone Density – повышение плотности кости под действием деносумаба), DECIDE (The determining efficacy: comparison of initiating Denosumab versus Alendronate – определение эффективности: сравнение начальной терапии деносумабом и алендронатом) изучалась не только эффективность, но и безопасность терапии деносумабом10. Анализ развития возможных нежелательных явлений (НЯ) в первые 3 года исследования FREEDOM сначала показал более высокую частоту кожных реакций в группе деносумаба по сравнению с группой плацебо. Однако спустя 6 лет, в период расширенной фазы исследования FREEDOM, анализ НЯ показал отсутствие статистически достоверных различий между группами в отношении побочных эффектов, в том числе со стороны кожных покровов. Данные исследования DEFEND подтвердили, что деносумаб не накапливается в костной ткани и имеет обратимый эффект после отмены.
«Благодаря исследованию DEFEND мы узнали, что деносумаб повышает МПКТ в сценарии раннего постменопаузального синдрома. В исследовании DECIDE было показано, что терапия деносумабом характеризуется более выраженным повышением МПКТ бедра по сравнению с алендронатом. В исследовании STAND у пациентов, которых переводили с алендроната на деносумаб, наблюдался более активный рост МПКТ на фоне деносумаба по сравнению с теми, кто продолжал принимать алендронат. Этот эффективный, безопасный и удобный в использовании препарат занимает особое место в схеме лечения у женщин в постменопаузальном периоде с высоким риском переломов», – подчеркнул профессор Д. Билезикян, завершая выступление.
Результаты клинических исследований и опыт длительного применения деносумаба (Пролиа)
Заведующая отделением нейроэндокринологии и остеопатий ФГБУ «Эндокринологический научный центр» Минздрава России, д.м.н., профессор Людмила Яковлевна РОЖИНСКАЯ более детально остановилась на анализе результатов трех исследований эффективности и безопасности деносумаба.
Многоцентровое двойное слепое рандомизированное исследование III фазы DEFEND относится к профилактическому исследованию, поскольку в нем приняли участие 322 здоровые женщины в постменопаузе, но с низкой костной массой (значения Т-критерия поясничных позвонков от -1,0 до -2,5). Пациентки в равном соотношении были рандомизированы в группу терапии деносумабом 60 мг 1 раз в 6 месяцев в течение 24 месяцев и группу плацебо11.
Результаты исследования продемонстрировали высокую антирезорбтивную эффективность деносумаба: применение препарата привело к достоверно значимому по сравнению с плацебо повышению МПКТ в позвоночнике, бедре, лучевой кости, в костях в целом (р = 0,0001). Данные изучения влияния прекращения терапии деносумабом после непрерывного двухлетнего лечения на костные маркеры подтвердили уникальную особенность препарата: он не накапливается в костной ткани и имеет обратимый эффект после отмены лечения. Профиль безопасности препарата оставался неизменным на протяжении всего исследования. Частота НЯ в основном была сопоставимой с таковой плацебо, за исключением некоторого увеличения частоты кожной сыпи и инфекций дыхательных путей. Инфекции были преимущественно внебольничными и хорошо отвечали на стандартную терапию.
В многоцентровом двойном слепом исследовании III фазы DECIDE сравнивали эффективность деносумаба и алендроната в отношении их влияния на МПКТ и биомаркеры костной резорбции у женщин в постменопаузе с низкой костной массой, а также оценивали безопасность препаратов12. В исследовании приняли участие 1189 женщин (2 группы – 594 и 595 пациенток соответственно) с величиной Т-критерия для бедренной кости и поясничного отдела позвоночника ≤ -2,0. Пациентки одной группы получали 1 мл раствора деносумаба (60 мг) каждые 6 месяцев и таблетку плацебо перорально еженедельно, пациентки другой группы – 1 раз в полгода инъекции 1 мл плацебо и 1 раз в неделю таблетку алендроната (70 мг).
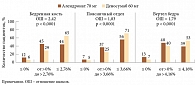
Терапия деносумабом сопровождалась большим по сравнению с алендронатом увеличением МПКТ: в области вертела бедренной кости на 3,5% (2,6% для алендроната), лучевой кости – на 1,1% (0,6% для алендроната), шейки бедра – на 2,4% (1,8% для алендроната), поясничных позвонков – на 5,3% (4,2% для алендроната) (р ≤ 0,0001). В исследовании DECIDE также показано быстрое снижение уровня маркеров костной резорбции на фоне приема деносумаба. Таким образом, полученные данные подтвердили способность деносумаба быстро и выраженно тормозить костную резорбцию, а также более значимо повышать МПКТ во всех отделах скелета по сравнению с алендронатом (рис. 2 и 3). Переносимость обоих препаратов была хорошей. Существенных различий в частоте и характере НЯ между двумя препаратами не отмечено.
В многоцентровом рандомизированном двойном слепом исследовании III фазы STAND изучали влияние изменения терапии (замена алендроната деносумабом) на МПКТ. В исследование были включены 504 женщины в постменопаузе со значениями Т-критерия от -2,0 до -4,0, все пациентки ранее принимали алендронат в течение 6 месяцев и более. Кроме того, все пациентки получали 1000 мг кальция и не менее 400 МЕ витамина D (в сутки). Пациенток разделили на 2 сопоставимые группы: 251 пациентке назначили алендронат в дозе 70 мг, 253 – деносумаб в дозе 60 мг подкожно.
У пациенток, перешедших на деносумаб через 12 месяцев терапии, наблюдалось увеличение МПКТ в поясничном отделе позвоночника, общем показателе бедренной кости и дистальном отделе лучевой кости, а также снижение маркеров костной резорбции в большей степени, чем у тех, кто продолжал терапию алендронатом. Оценка влияния деносумаба на динамику МПКТ в зависимости от длительности предварительного лечения алендронатом показала, что назначение деносумаба после терапии алендронатом приводит к дальнейшему повышению МПКТ. Деносумаб и алендронат имели сходные профили безопасности. Случаев гипокальциемии не выявлено13.
На основании результатов рандомизированных клинических исследований были сделаны следующие выводы:
- деносумаб эффективен для профилактики остеопороза у женщин с низкой МПКТ;
- деносумаб повышает минеральную плотность и общее содержание минеральных веществ как в трабекулярной, так и в кортикальной кости и увеличивает прочность кости;
- действие деносумаба на костную ткань обратимо и прекращается сразу после отмены лечения;
- деносумаб в большей степени, чем алендронат, снижает уровни маркеров костного метаболизма и повышает МПКТ;
- применение деносумаба после алендроната в большей степени, чем продолжающаяся терапия алендронатом, повышает МПКТ и снижает уровни маркеров костного метаболизма;
- деносумаб обладает хорошим профилем безопасности.
ASMBR-2013: новые данные
FREEDOM – одно из важнейших исследований, послуживших основанием для регистрации деносумаба в качестве препарата, предназначенного для лечения остеопороза у женщин в постменопаузе. Медицинский директор компании «Амджен» (Швейцария) доктор Карим ЭЛЬ-ХАШИМИ (Karim EL-HASCHIMI) акцентировал внимание участников симпозиума на данных расширенного исследования FREEDOM продолжительностью 8 лет по оценке эффективности и безопасности деносумаба.
Согласно результатам исследования, применение деносумаба в течение 8 лет сопровождалось прогрессивным увеличением МПКТ как в позвоночнике, так и в бедре соответственно на 18,4 и 8,3% от начального уровня. Аналогичная ситуация наблюдалась у пациенток, начавших прием деносумаба после 3 лет лечения плацебо. В этой группе за 5 лет терапии показано достоверное повышение МПКТ поясничного отдела позвоночника и бедренной кости на 13,7 и 4,9% соответственно. При этом в течение всех 8 лет терапии уровни маркеров костной резорбции имели минимальные значения. Частота новых переломов за 8 лет терапии деносумабом снизилась с 2,6% в основном исследовании до 0,7% в расширенном. Отмечено достоверное снижение частоты переломов и у женщин, перешедших на терапию деносумабом через 3 года, с 3,1 до 1,4%.
Частота НЯ при 8-летнем использовании деносумаба не увеличилась по сравнению с таковой при 3-летнем исследовании препарата. «На фоне длительной терапии деносумабом наблюдается постоянный прирост МПКТ и снижение частоты позвоночных и внепозвоночных переломов, в том числе переломов бедренной кости. Такова краткая оценка 8-летних данных по деносумабу, которые были представлены профессором Папапулосом в рамках конгресса Американского общества специалистов по исследованию костной ткани и минерального обмена», – констатировал доктор К. Эль-Хашими.
Согласно результатам основного исследования FREEDOM, введение деносумаба 2 раза в год в течение 3 лет достоверно снижало риск переломов во всех исследованных участках скелета2.
Насколько непрерывная терапия деносумабом спустя 3 года может быть ассоциирована с последующим дополнительным снижением частоты невертебральных переломов?
Анализ данных расширенного исследования FREEDOM показал, что пик снижения риска частоты невертебральных переломов приходится на 4-й год терапии с последующим умеренным стабильным уменьшением в течение периода с 4 до 7 лет: снижение частоты невертебральных переломов за первые 3 года составило в среднем 1,98%, за 4-й год – 1,43%, за период 4–7 лет – 1,45% (рис. 4).
Таким образом, долгосрочная терапия деносумабом обеспечивает снижение риска невертебральных переломов. По мнению докладчика, это объясняется уникальным механизмом действия деносумаба, который, обладая высокой антирезорбтивной активностью, снижает кортикальную порозность, положительно влияет на увеличение минеральной плотности кортикальной и трабекулярной костной ткани и значимо улучшает качественные характеристики прочности костей скелета в целом.
В ходе подисследований TTI и TTR сравнивали эффективность применения подкожной инъекции деносумаба и пероральных бисфосфонатов (ибандроната, ризедроната) у женщин в постменопаузе, большинство из которых имели высокий риск переломов и недостаточно эффективную терапию другими бисфосфонатами14. Согласно полученным результатам переход на терапию деносумабом сопровождается значимым повышением МПКТ во всех исследованных отделах скелета по сравнению как с ибандронатом, так и ризедронатом.
Завершая выступление, доктор К. Эль-Хашими подчеркнул, что деносумаб является прекрасной альтернативой пероральным бисфосфонатам у пациентов с высоким риском переломов и плохой приверженностью терапии.
Программа «Приоритет»: российский клинический опыт
Вице-президент Российской ассоциации по остеопорозу, д.м.н., профессор Ольга Борисовна ЕРШОВА представила предварительные результаты российского многоцентрового открытого проспективного исследования по оценке эффективности и безопасности препарата Пролиа (деносумаб) у женщин с постменопаузальным остеопорозом (ПМО).
Исследование длительностью 12 месяцев стартовало 1 марта 2013 г. Оно охватывает 8 центров из 4 российских городов (Москвы, Ярославля, Екатеринбурга, Уфы). В нем приняла участие 51 женщина в постменопаузе (средний возраст 68 лет) со значением Т-критерия поясничного отдела позвоночника или бедренной кости < -2,5. Большинство пациенток (33%) имели в анамнезе как множественные, так и единичные переломы позвоночника, бедра, лучевой кости, а также сопутствующие заболевания. Половина пациенток имела опыт лечения бисфосфонатами (алендронатом, ибандронатом, золедронатом, ризедронатом), стронция ранелатом, кальцитонином, витамином D.
Пациентки были разделены на 2 группы. 1-ю группу составили больные ПМО, ранее не получавшие терапию, 2-ю группу – получавшие терапию остеопороза. Всем участницам исследования перед началом лечения препаратом Пролиа был рекомендован прием витамина D (100 000 МЕ в течение 10 дней) с последующим переводом на прием поддерживающих доз витамина (800–1200 МЕ/день) вместе с препаратом кальция (1000 мг/день).
Были определены первичный и вторичные критерии оценки эффективности. Первичным критерием стала динамика МПКТ у пациенток с ПМО, получавших лечение препаратом Пролиа в течение 12 месяцев. Вторичные критерии оценки эффективности включали динамику маркера костной резорбции (С-телопептида) у пациенток с ПМО, получавших лечение препаратом Пролиа de novo, динамику МПКТ у больных ПМО, получавших лечение препаратом Пролиа в течение 6 месяцев.
Предварительные результаты исследования 3-месячного лечения продемонстрировали хорошую антирезорбтивную эффективность препарата Пролиа: уровень С-телопептида снизился на 89% по сравнению с исходным, и это снижение было достоверным (р = 0,0001). У некоторых пациенток показатель костной резорбции снижался до 200 раз. Наблюдалось снижение уровня кальция в крови. Это позволило сделать вывод, что во время терапии препаратом Пролиа целесообразно принимать препараты кальция и витамин D. Достоверных данных о снижении уровней щелочной фосфатазы и креатинина не было получено.
Переносимость препарата Пролиа была оценена как хорошая: НЯ отмечались лишь у 12% участниц исследования. Что касается оценки динамики МПКТ, она будет проведена через 6 и 12 месяцев терапии этим препаратом.
По мнению докладчика, многочисленные международные исследования и полученные предварительные данные российского исследования дают основание считать препарат Пролиа эффективным и безопасным средством для лечения постменопаузального остеопороза у женщин с повышенным риском переломов. Отсутствие отрицательного влияния Пролиа на уровень креатинина – существенное преимущество препарата, позволяющее назначать его при сниженной функции почек.
Заключение
Представленные докладчиками данные клинических исследований убедительно продемонстрировали:
- эффективность препарата Пролиа (деносумаб) в отношении предотвращения остеопоротических переломов основных локализаций;
- более мощный антирезорбтивный эффект по сравнению с пероральными бисфосфонатами;
- благоприятный профиль безопасности;
- хороший уровень приверженности пациенток лечению.
Показаны полная обратимость антирезорбтивных эффектов без накопления препарата в костном матриксе и обратимый характер НЯ. Потенциальная возможность применения деносумаба в качестве монотерапии у пациенток с ПМО, удобство применения (1 раз в 6 месяцев подкожно) свидетельствуют о несомненных перспективах применения препарата для лечения и профилактики системного остеопороза и предупреждения связанных с ним переломов костей.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.