Ведение пациентов с местнораспространенным раком прямой кишки с гнойно-воспалительными осложнениями и наличием свищевого хода
- Аннотация
- Статья
- Ссылки
- English
Введение
Проблема лечения рака прямой кишки актуальна во всем мире. Зачастую добиться успеха в лечении мешают ранние проявления осложнений опухоли прямой кишки.
По данным многочисленных медицинских статистических исследований, местнораспространенный колоректальный рак (МРКРР), или рак прямой кишки, является широко распространенной злокачественной патологией. Его доля в структуре злокачественных новообразований неуклонно растет [1, 2]. Ежегодно в мире этим видом рака заболевают около 1 млн человек, причем не менее 50% пациентов умирают в первый год наблюдения [3]. В России в общей структуре онкопатологии злокачественные опухоли толстой кишки занимают порядка 7,6%, прямой кишки – 5,9% [1]. Рак толстой и прямой кишки развивается быстро, практически незаметно и бессимптомно. Поэтому у большинства пациентов опухоль обнаруживается на стадии метастазирования в печень или осложнений, что существенно усугубляет течение патологического процесса.
Методология лечения
Нередко рак прямой кишки осложняется параканкрозным деструктивным нагноением [4, 5]. Одно из таких осложнений – анальный свищ. Данная патология вызывает задержку в назначении специального противоопухолевого лечения, а иногда и вовсе становится поводом для отказа от противоопухолевой лекарственной терапии.
Следует отметить, что аноректальный свищ может быть не следствием рака прямой кишки, а его причиной: у пациентов с длительно существующим (до 20 лет) анальным свищом выявляются в дальнейшем опухоли в данной области [6]. Такое осложнение может проявиться при метастатическом поражении промежности на фоне новообразования толстой кишки [7]. В ряде случаев формирование свищевого хода может повлечь за собой ухудшение состояния пациента за счет присоединения новых осложнений, таких как гангрена Фурнье, парапроктит, забрюшинная флегмона, что делает невозможным противоопухолевое лечение [8].
Кроме того, не следует забывать о совокупности ряда осложнений, затрудняющих процесс излечения. К таким неблагоприятным прогностическим факторам относят:
- локализацию опухоли в нижнеампулярном отделе прямой кишки, лишенном фасциального футляра;
- инвазию опухоли в стенки сосудов или нервную ткань;
- значительное поражение регионарных лимфатических узлов;
- распространение опухоли в ткани в сторону предполагаемого края резекции [9, 10].
Методология лечения основана на двух важнейших аспектах – неуклонном прогрессе хирургических технологий и внедрении новейших методик лучевой и лекарственной противоопухолевой терапии [11]. В настоящее время широко используется комбинированный принцип лечения. Однако многофакторность осложнений может затруднить выбор оптимального метода лечения и вероятностный прогноз. Кроме того, выбор зависит от точности и полноты диагностики и полученной на этапе дооперационного исследования информации о генезе и локализации опухоли [12].
Общепринятой тактикой лечения в таких случаях, а также в случае местнораспространенного рака прямой кишки без подобного осложнения является предоперационная химиолучевая терапия с последующим хирургическим этапом спустя 6–10 недель [13].
В исследованиях показано, что послеоперационное облучение не оказывает должного эффекта на лечение осложненного МРКРР и не влияет существенно на выживаемость пациентов [14]. В связи с этим возникла идея предоперационной химиолучевой терапии (ХЛТ), которая способствует значительной предварительной гибели опухолевых клеток, а значит, снижению вероятности распространения живых опухолевых клеток в органы и ткани во время операции. В процессе использования данного метода располагающим фактором была названа такая причина, как более высокая оксигенация и чувствительность к облучению клеток опухоли до операции. По мнению исследователей, предварительная регрессия раковой опухоли повышает возможность сфинктер-сберегающих операций и снижает глубину пагубного воздействия облучения органов малого таза [15].
На сегодняшний день доказана целесообразность и перспективность применения неоадъювантной ХЛТ с фторпиримидинами и оксалиплатином в сочетании с оперативным лечением [9]. Использование пероральных фторпиримидинов показано для профилактики инфузионных осложнений. Хорошо апробированным фторпиримидином является капецитабин, который в сочетании с оксалиплатином демонстрирует эффективность, сопоставимую с таковой типовой химиотерапии в режиме FOLFOX [16].
Предоперационная ХЛТ с 5-фторурацилом – классический прием в лечении МРКРР. По итогам примененного предоперационного лечения отмечается статистически значимое снижение количества пациентов с глубоким прорастанием опухоли в мезоректальную клетчатку и поражением регионарных лимфоузлов [9].
По мнению ряда авторов, осложнения рака прямой кишки могут быть серьезным противопоказанием к проведению неоадъювантной лучевой терапии [15, 17]. В этом случае некоторые клиницисты рекомендуют эндохирургические методы, позволяющие восстановить толстокишечный пассаж, и неоадъювантную лучевую терапию [5, 18].
Латеральный край резекции (pCRM) служит важнейшим критерием качества проведенного оперативного вмешательства и ведущим фактором, воздействующим на развитие рецидивов и метастазирование у пациентов с диагнозом МРКРР [3, 12]. Клиницистами было показано, что частота вовлечения pCRM возрастает при внедрении новообразования в мезоректальную клетчатку, фасцию, серозную оболочку прямой кишки и не зависит от локализации опухоли и поражения лимфоузлов. На безрецидивную выживаемость пролеченных больных негативно влияют стадия заболевания и радикальность операции [9].
Тактика ведения пациентов с диагнозом МРКРР остается неопределенной при инфильтрации опухолью мезоректальной фасции или внедрении за ее пределы. Осложненное течение МРКРР определяет необходимость применения нестандартных подходов и проведения комплексного лечения с применением предоперационной ХЛТ и последующей хирургической резекцией. Показан персонализированный подход к пациентам с различными осложнениями. Разработка разновекторных программ лечения с использованием новейших сенсибилизаторов является одним из актуальных направлений в области онкопроктологии [19].
Клиницисты отмечают, что больным МРКРР, которым проведены радикальные комбинированные операции, при наличии выраженного гнойного воспаления с абсцессом, формированием свищей с органами, вовлеченными в процесс, и их вскрытием во время мобилизации кишки необходимо выполнять операцию по удалению кишки. Удельный вес операций, позволяющих сохранить сфинктер, значителен – 62,2%. Осложнения после клинически радикальных операций отмечаются у 9,6% пациентов. Летальность в таком случае среди пациентов в возрасте старше 60 лет составляет 7,9% и, как правило, связана с осложнениями и вовлечением в процесс других органов. В этой связи для больных МРКРР с осложнениями выполнение подобных операций целесообразно и оправданно при дополнительной предоперационной ХЛТ [20].
В результате многолетних наблюдений установлено, что наиболее эффективным методом предупреждения постоперативных гнойно-воспалительных осложнений является адекватная антибиотическая профилактика, нацеленная на те виды микроорганизмов, которые с наибольшей вероятностью могут инфицировать зону операции и вызывать нагноение. Антибиотики пациентам с МРКРР назначаются всегда, поскольку при большом объеме операции имеет место вскрытие кишки, что создает условия для попадания бактерий в брюшную полость. Необходимо учесть, что больные МРКРР по иммунному статусу являются больными с высоким риском инфицирования. Гнойно-воспалительные и септические осложнения чаще регистрируются у пациентов с лишним весом и сопутствующими соматическими заболеваниями [21].
Клинический случай
Больная О., 58 лет, обратилась в Краснодарский клинический онкологический диспансер № 1 в ноябре 2017 г. с жалобами на патологические выделения из прямой кишки, в том числе крови. Перечисленные жалобы отмечала с 2015 г., однако за медицинской помощью в течение двух лет не обращалась.
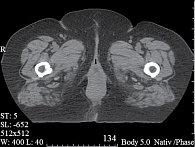
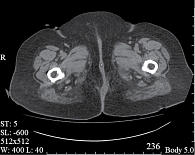
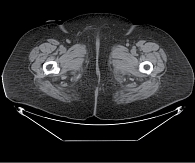
При обследовании выявлена распадающаяся опухоль нижнеампулярного отдела прямой кишки с формированием параканкрозного воспаления и свищевого хода в центре с гнойным отделяемым. По данным компьютерного рентгенологического исследования органов грудной, брюшной полостей и малого таза, визуализирована инфильтративная бластома прямой кишки с распространением на анальную область и мягкие ткани правой ягодицы, тазовая, внутренняя подвздошная, двусторонняя паховая лимфаденопатия. Метастатического поражения паренхиматозных органов не выявлено. Патоморфологически опухоль представлена высокодифференцированной аденокарциномой. При анализе соматических мутаций в гене KRAS методом полимеразной цепной реакции в режиме реального времени мутаций в кодонах 12/13 и 61 гена KRAS не обнаружено.
В качестве первого этапа лечения выполнена разгрузочная илеостомия.
С учетом клинической картины синдрома системной воспалительной реакции, локальных гнойно-некротических изменений тканей проведение предоперационной химиолучевой терапии на момент первичного лечения представлялось невозможным. Было принято решение о проведении комплекса мероприятий по санации свищевого хода и назначении антибактериальной терапии в адекватном объеме для предотвращения гнойно-септических осложнений. В ходе бактериологического исследования отделяемого свищевого хода и прямой кишки были выделены возбудители Escherichia coli, Staphylococcus aureus, Pseudomonas aeruginosa. Согласно данным антибактериальной чувствительности, назначена терапия комбинацией цефтаролина фосамила 600 мг дважды в сутки и амикацина 1,5 г один раз в сутки. По стабилизации состояния и стихании воспалительной реакции на восьмые сутки антибактериальной терапии начата химиотерапия по протоколу FOLFOX4. Реализовано четыре курса химиотерапии с выраженным клиническим эффектом в виде значительного стихания признаков локального воспаления, отсутствия отделяемого из свищевого хода, регрессии астении, нормализации температуры тела. Токсичность терапии была управляемой, отсрочек курсов не было.
Рентгенологическая картина в динамике представлена на рис. 1–3.
По решению мультидисциплинарного консилиума, 15 мая 2018 г. проведена дистанционная лучевая терапия (ДЛТ) на область опухоли и паховые области (40 Гр). Результаты контрольного обследования показали положительную динамику основной опухоли. Спустя шесть недель после ДЛТ выполнен хирургический этап лечения – брюшнопромежностная экстирпация прямой кишки с резекцией задней стенки влагалища. После удаления опухоли с ее ткани осуществлен посев, выделен возбудитель Staphylococcus epidermidis. Согласно данным антибиотикограммы, проведена антибактериальная терапия: пиперациллин + тазобактам 4,5 г трижды в сутки каждые восемь часов в течение семи дней. От проведения послеоперационной химиотерапии пациентка воздержалась.
Пациентка находится под наблюдением врача. На последнем визите в августе 2019 г. признаков прогрессирования заболевания не обнаружено.
Таким образом, удалось добиться полной ремиссии, безрецидивный период составляет 16 месяцев.
Заключение
Рассмотренный случай – успешный пример реализации мультидисциплинарного подхода к лечению распространенного рака прямой кишки (участие хирургов, химиотерапевтов, радиотерапевтов, клинических фармакологов, специалистов по паллиативной помощи и поддерживающей терапии).
Среди факторов успешного лечения необходимо отметить тщательную санацию очагов гнойных осложнений местнораспространенного процесса с выключением прямой кишки из пассажа кишечного содержимого, тщательный подбор антибактериальной терапии, согласно данным посевов из свищей, опухоли, отделяемого дренажей. Таким образом, даже у непростой категории больных можно планировать и осуществлять адекватный объем противоопухолевого лечения.
R.A. Murashko, PhD, A.V. Yashchenko, M.G. Leonov, MD, PhD, R.V. Konkov, A.Yu. Goryaynova
Clinical Oncology Center № 1, Krasnodar
Oncology Center № 3, Novorossiysk
Contact person: Mikhail G. Leonov, novonko@yandex.ru
This article provides a literary review of the features of medical methodological approaches to patients and locally advanced rectal cancer with purulent-inflammatory complications, also describes and advantages the possibility of using radiation preoperative therapy, introduced own clinical experience of the patient with purulent complications of colorectal cancer.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.