Влияние хронической инсомнии на стабилометрические показатели у больных дисциркуляторной энцефалопатией
- Аннотация
- Статья
- Ссылки
- English
В сравнительное исследование включены 38 человек (30 женщин и восемь мужчин, средний возраст 63,9 ± 4,8 года) с диагнозом дисциркуляторной энцефалопатии. После обследования их разделили на две группы – страдающие хронической инсомнией (n = 22) и без нарушений сна (n = 16). Проведено сравнение стабилометрических показателей всех пациентов.
У пациентов с хронической инсомнией в отличие от пациентов без нарушений сна выявлено достоверное увеличение длины статокинезиограммы (472,1 ± 164,7 против 325,4 ± 120,8 мм, p = 0,004), площади статокинезиограммы (392,8 ± 311,9 против 201,5 ± 130,7 мм2, p = 0,02) и скорости перемещения центра давления (15,7 ± 5,4 против 10,8 ± 4,0 мм/с, p = 0,004) в пробе с закрытыми глазами, что свидетельствует о нарушении компенсаторных механизмов поддержания равновесия. Обнаружены корреляционные связи уровня тревоги с длиной статокинезиограммы и скоростью перемещения центра давления (r = -0,4, p < 0,005 и r = -0,4, p < 0,005 соответственно). В результате подтверждены нарушения постурального контроля при хронической инсомнии. При этом нарастание тревоги приводило, наоборот, к усилению постурального контроля и уменьшению длины и площади статокинезиограммы по данным стабилографии.
В сравнительное исследование включены 38 человек (30 женщин и восемь мужчин, средний возраст 63,9 ± 4,8 года) с диагнозом дисциркуляторной энцефалопатии. После обследования их разделили на две группы – страдающие хронической инсомнией (n = 22) и без нарушений сна (n = 16). Проведено сравнение стабилометрических показателей всех пациентов.
У пациентов с хронической инсомнией в отличие от пациентов без нарушений сна выявлено достоверное увеличение длины статокинезиограммы (472,1 ± 164,7 против 325,4 ± 120,8 мм, p = 0,004), площади статокинезиограммы (392,8 ± 311,9 против 201,5 ± 130,7 мм2, p = 0,02) и скорости перемещения центра давления (15,7 ± 5,4 против 10,8 ± 4,0 мм/с, p = 0,004) в пробе с закрытыми глазами, что свидетельствует о нарушении компенсаторных механизмов поддержания равновесия. Обнаружены корреляционные связи уровня тревоги с длиной статокинезиограммы и скоростью перемещения центра давления (r = -0,4, p < 0,005 и r = -0,4, p < 0,005 соответственно). В результате подтверждены нарушения постурального контроля при хронической инсомнии. При этом нарастание тревоги приводило, наоборот, к усилению постурального контроля и уменьшению длины и площади статокинезиограммы по данным стабилографии.

Введение
Равновесие поддерживается благодаря координированной работе визуального, кинестетического и вестибулярного анализаторов. Этот механизм обеспечивает пространственную ориентацию, вертикальное положение тела и ходьбу. Контроль за всеми группами мышц, от которых зависит статика и движения тела, позволяет противодействовать влиянию веса тела и центробежных сил.
Система регуляции постуральных функций обладает высокой надежностью, хотя при ряде заболеваний и/или в процессе старения эффективность компенсаторных механизмов снижается. Самые частые последствия нарушения равновесия в пожилом и старческом возрасте – несчастные случаи на производстве и бытовые травмы в связи с падениями. Проблема падений характерна для людей старше 60–65 лет, и даже единичный эпизод в этом возрасте указывает на снижение эффективности контроля постуральных функций. Чаще всего падения случаются во время ходьбы [1]. Помимо медицинских последствий также важно отметить значительные экономические затраты, связанные с падениями в пожилом возрасте, которые, например, в США составляют около 19 млрд долларов в год [2].
Среди множества причин нарушения равновесия в пожилом возрасте лидирует патология вестибулярного аппарата и центральных механизмов обеспечения равновесия на фоне сосудистых заболеваний головного мозга. К нарушению равновесия в этой возрастной группе могут также приводить снижение когнитивных функций, нарушение восприятия и походки, замедление реакции, а также употребление алкоголя и прием некоторых лекарственных средств.
Процесс старения сам по себе не приводит к нарушению сна, но различные заболевания, связанные со старением, могут быть факторами риска развития чаще всего хронической инсомнии. По результатам эпидемиологических исследований, отдельные симптомы инсомнии встречаются в популяции в 33–50% случаев. У пожилых людей после 75 лет по сравнению с лицами среднего возраста частота инсомнии удваивается. При коморбидных расстройствах, психических заболеваниях или хронических болевых синдромах сон нарушается в 50–75% случаев [3].
В литературе приводится мало данных о влиянии расстройств сна на показатели равновесия. В основном обсуждалось значение депривации (лишения) сна для постуральных функций. N. Avni и соавт. (2006) изучали возможности применения метода постурографии как индикатора усталости. Результаты постурографии коррелировали с показателями, оценивавшими степень усталости: когнитивными тестами и тестом психомоторной бдительности. Усталость после лишения сна негативно сказывалась и на постурографических показателях, и на когнитивных функциях [4]. M. Patel и соавт. (2008) оценивали эффективность постурального контроля и адаптации после депривации сна в зависимости от субъективной оценки сонливости. Авторы продемонстрировали, что постуральный контроль и адаптация после 36-часовой депривации сна значительно ухудшились на фоне усиления сонливости [5]. S. Aguiar и соавт. (2015) изучали воздействие визуальной информации на показатели стабилометрии у молодых людей после лишения сна. По данным ученых, депривация сна стала причиной ухудшения показателей постуральных функций при предъявлении визуальной информации [6].
Таким образом, эксперименты на здоровых молодых добровольцах демонстрируют, что кратковременная депривация сна приводит к снижению постуральных функций. Можно ожидать, что сокращение времени сна при некоторых его расстройствах, в частности хронической инсомнии, у пожилых людей будет сопровождаться ухудшением функции равновесия. Поскольку распространенность инсомнии и риск падений наиболее велики в этой возрастной группе, целью нашего исследования стало изучение этого вопроса.
Материал и методы
Характеристика групп и критерии отбора. На первом этапе было проведено пилотное исследование для определения распространенности нарушений сна среди пожилых пациентов с дисциркуляторной энцефалопатией и влияния этих нарушений на показатели равновесия по шкалам Тинетти и оценки тяжести головокружения. Всего обследовано 100 больных (37 мужчин, 63 женщины) в возрасте от 52 до 75 лет. Средний возраст пациентов с диагнозом дисциркуляторной энцефалопатии составил 64,7 ± 6,0 года. В зависимости от ответа на вопрос «считаете ли Вы, что у вас имеется нарушение сна», больные были разделены на две группы: с нарушением сна (n = 68) и без нарушений сна (n = 32). Количественная оценка сна проводилась с помощью Питтсбургского опросника для определения индекса качества сна [7].
На втором этапе изучалось влияние хронической инсомнии на показатели равновесия у пациентов с дисциркуляторной энцефалопатией. Равновесие оценивалось при помощи объективного метода исследования – стабилометрической платформы. Всего обследовано 38 пациентов (восемь мужчин, 30 женщин) в возрасте от 58 до 75 лет (средний возраст 63,9 ± 4,8 года). Диагноз дисциркуляторной энцефалопатии ставился на основании жалоб, данных нейропсихологического обследования, магнитно-резонансной томографии головного мозга (первая и вторая стадии по шкале Фазекас) [8]. Эти больные также были разделены на две группы: с хронической инсомнией (n = 22) и без нее (n = 16). Диагноз хронической инсомнии ставился согласно критериям третьей версии Международной классификации расстройств сна 2014 г. [9].
Набор и обследование пациентов осуществлялись на базе клиники нервных болезней Университетской клинической больницы № 3 Первого Московского государственного медицинского университета им. И.М. Сеченова и больницы Российской академии наук в городе Троицке.
Критерии исключения из исследования:
- прием влияющих на сон препаратов, отказ или отсутствие возможности прекратить прием этих препаратов как минимум за три дня до начала и на весь период исследования;
- злоупотребление лекарственными средствами, алкоголем, наркотическими веществами в анамнезе;
- патология центрального и периферического вестибулярного аппарата;
- заболевания, вызывающие поражение периферической нервной системы;
- эндогенные психические заболевания;
- деменция;
- работа по сменному графику;
- иные заболевания, влияющие на глубину и продолжительность сна: синдром обструктивного апноэ сна средней и тяжелой степени, синдром беспокойных ног;
- выраженный болевой синдром;
- тяжелые хронические заболевания, а также соматические заболевания в стадии обострения или декомпенсации, не позволяющие принимать участие в исследовании.
Пациенты подписывали информированное согласие на участие в клиническом исследовании согласно форме, установленной локальным комитетом по этике при Первом Московском государственном медицинском университете им. И.М. Сеченова. Протокол № 05-18.
Схема проведения исследования. Дизайн исследования – сравнительный (контролируемый).
На первом этапе в качестве целевой группы были набраны пациенты с дисциркуляторной энцефалопатией и нарушениями сна, а в качестве группы сравнения – пациенты без этих нарушений. Продолжительность наблюдения – один день. Пациенты подписывали информированное согласие, заполняли анкеты, их клинически обследовали, после чего проводилась итоговая беседа.
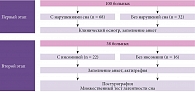
На втором этапе в качестве целевой группы выступали больные дисциркуляторной энцефалопатией с хронической инсомнией, а в качестве группы сравнения – больные дисциркуляторной энцефалопатией без хронической инсомнии. Продолжительность наблюдения – четыре дня. Дизайн исследования подразумевал три визита, в ходе которых пациенты подписывали информированное согласие, заполняли анкеты, им выполнялись актиграфия, множественный тест латентности сна и постурография. После завершения обследования по его результатам с пациентами проводилась беседа (рис. 1).
Три пациента, подписавших согласие на участие в исследовании, выбыли на втором этапе: один в связи с обострением хронического заболевания и двое в самом начале решили не участвовать без объяснения причин.
Анкетирование. После клинического осмотра в рамках первого визита пациенты самостоятельно заполняли следующие анкеты: Эпвортскую шкалу сонливости [10], индекс тяжести инсомнии [11], Питтсбургский опросник для определения индекса качества сна [7], Берлинский опросник [12], шкалу тревоги Спилбергера [13], шкалу депрессии Бека [14], шкалу оценки тяжести головокружения [15]. Для количественной оценки равновесия использовалась шкала оценки двигательной активности пожилых Тинетти [16].
Актиграфия. В рамках первого визита на запястье пациента закреплялся датчик в форме наручных часов, который регистрировал его двигательную активность. Через два дня датчик снимали. Использовался прибор SOMNOwatchtm (SOMNOmedics, Германия). При помощи программного обеспечения (DOMINO light, версия 1.4.0) определялись следующие показатели: время засыпания и время периода сна, время бодрствования в период сна и эффективность сна.
Во время второго визита с целью количественной оценки дневной сонливости выполнялся множественный тест латентности сна. В течение дня осуществлялись четыре 20-минутные попытки засыпания, разделенные между собой двухчасовыми интервалами. Данные расшифровывались по критериям Американской академии медицины сна 2007 г. [17]. Оценивались такие показатели, как среднее время засыпания и наличие эпизодов раннего начала фазы быстрого сна.
Постурография. Показатели стабилометрии оценивались во время второго визита с использованием компьютеризированной постурографической платформы с биологической обратной связью (стабилоплатформа ST-150, «Биомера», Россия). Стабилометрическое исследование включало проведение функциональной пробы Ромберга: пациент стоял на платформе по 30 секунд с открытыми, а потом с закрытыми глазами. При выполнении пробы он опирался на две ноги (пятки вместе, носки немного врозь), руки опущены. Оценивались длина и площадь статокинезиограммы, а также скорость перемещения центра давления.
Статистическая обработка. Формирование статистической матрицы и обработка данных осуществлялись при помощи программы Statistica ver. 7.0 (StatSoft Inc., США). Описательные данные для непрерывных переменных были представлены в виде средних и среднеквадратического отклонения. Сравнительный анализ проводился с использованием U-критерия Манна – Уитни. Для выявления связей между непрерывными переменными использовался корреляционный анализ Пирсона. Критический уровень значимости (p) для проверки верности статистических гипотез находился на уровне менее 0,05.
Результаты
На первом этапе исследования выполнено сравнение показателей количественной оценки двигательной функции по шкалам оценки двигательной активности пожилых Тинетти и оценки тяжести головокружения у больных с нарушениями сна и без таковых. По данным опроса, у 68% пациентов наблюдались нарушения сна различного характера (увеличение времени засыпания, частые пробуждения, ранние утренние пробуждения). У пациентов с нарушениями сна продемонстрировано статистически достоверное ухудшение двигательных функций (22,5 ± 4,0 против 24,7 ± 3,7, p = 0,01) и качества жизни вследствие головокружения (28,4 ± 25,7 против 15,8 ± 18,7, p = 0,01).
Данные равновесия и показатели дневной сонливости сопоставлялись с помощью визуальной аналоговой шкалы сонливости методом корреляционного анализа. Не было установлено достоверных корреляционных связей с характеристиками равновесия и показателями дневной сонливости.
На втором этапе исследования сравнивались показатели стабилографии у пациентов с хронической инсомнией и без нее. У пациентов с хронической инсомнией обнаружено достоверное увеличение длины статокинезиограммы (472,1 ± 164,7 против 325,4 ± 120,8 мм, p = 0,004), площади статокинезиограммы (392,8 ± 311,9 против 201,5 ± 130,7 мм2, p = 0,02) и скорости перемещения центра давления (15,7 ± 5,4 против 10,8 ± 4,0 мм/с, p = 0,004) в пробе с закрытыми глазами.
Кроме того, выявлены отрицательные корреляционные связи между уровнем тревоги по шкале Спилбергера и длиной статокинезиограммы (r = -0,4), а также скоростью перемещения центра давления (r = -0,4). Положительные корреляционные связи наблюдались между уровнем сонливости по Эпвортской шкале и площадью статокинезиограммы при открытых и закрытых глазах (r = 0,4).
После получения такой корреляции было высказано предположение о том, что высокая тревожность пациентов может влиять на результаты тестов равновесия независимо от нарушений сна. Поэтому пациенты с инсомнией были разделены на две подгруппы в зависимости от уровня личностной тревожности по шкале Спилбергера – первая с низкой и умеренной тревожностью (n = 10), а вторая – с высокой тревожностью (n = 12).
При сравнении показателей равновесия обнаружено, что у пациентов с хронической инсомнией, низкой и умеренной тревожностью и больных без нарушений сна достоверно отличаются следующие показатели: длина статокинезиограммы при открытых (318,6 ± 126,0 против 214,1 ± 52,8 мм, p = 0,02) и закрытых (584,9 ± 171,3 против 325,4 ± 120,8 мм, p = 0,001) глазах, скорость перемещения центра давления при открытых (10,6 ± 4,2 против 7,0 ± 1,8 мм/с, p = 0,02) и закрытых (19,4 ± 5,7 против 10,8 ± 4,0 мм/с, p = 0,001) глазах, площадь статокинезиограммы при закрытых глазах (573,7 ± 361,2 против 201,5 ± 130,7 мм2, p = 0,009) (табл. 1).
С помощью метода корреляционного анализа сопоставлялись показатели равновесия с характеристиками сна и бодрствования пациентов. Оценивались индекс тяжести инсомнии, результаты по Питтсбургскому опроснику для определения индекса качества сна, Эпвортской шкале сонливости и Берлинскому опроснику. Не установлено достоверных корреляционных связей с характеристиками равновесия ни по одному из этих показателей. Кроме того, не выявлялись корреляционные связи показателей равновесия с показателями сна и сонливости, по данным актиграфии и множественного теста латентности сна.
Обсуждение результатов
Результаты исследования продемонстрировали, что нарушение сна – фактор, ухудшающий постуральный контроль у пожилых людей. Такая связь уже выявлялась в экспериментальных условиях после депривации сна у молодых добровольцев. Влияние хронической инсомнии на постурографические показатели у лиц пожилого возраста с сопутствующей патологией ранее не изучалось. Представлялось актуальным определить, действительно ли нарушения сна в пожилом возрасте приводят к нарушению равновесия, поскольку, с одной стороны, в этой возрастной группе существует проблема падений, а с другой – часто встречается инсомния.
По результатам обследования, субъективное повышение уровня сонливости (по Эпвортской шкале) соответствовало нарушениям равновесия (по данным стабилографии), что проявлялось увеличением площади статокинезиограммы в пробе с открытыми и закрытыми глазами. Однако в результате изучения объективных характеристик сна и дневной сонливости методами актиграфии и множественного теста латентности сна не было обнаружено их связи с показателями равновесия. Ни степень нарушения сна, ни выраженность дневной сонливости не влияли на постурографические показатели. Нельзя сопоставить данные этого исследования с результатами других работ, поскольку они были посвящены оценке связи степени усталости с показателями равновесия [4, 5], а в настоящем исследовании акцент был сделан на оценке сна и его последствий.
Связь между расстройством сна и постуральной неустойчивостью может быть не прямой, а опосредованной такими факторами, как нарушение когнитивных функций, эмоциональные нарушения, прием лекарственных препаратов. С помощью корреляционного анализа действительно была обнаружена достоверная отрицательная связь уровня тревоги с показателями стабилометрии. По данным проведенных ранее исследований, повышение уровня тревоги у пациентов с тревожным расстройством без органического поражения центральной и периферической нервной системы приводило к изменению показателей стабилографии и проявлялось уменьшением длины и площади статокинезиограммы, особенно в пробе с закрытыми глазами. По мнению авторов, эти изменения на стабилограмме отражали избыточную напряженность постурального контроля, которая проявлялась субъективным ощущением неустойчивости, страхом падения [18].
Можно предположить, что у пациентов с дисциркуляторной энцефалопатией, хронической инсомнией и высоким уровнем тревоги паттерн стабилографических показателей тревожного расстройства наслаивается на умеренное повышение стабилографических показателей неустойчивости, которое отмечалось у других обследованных пациентов с дисциркуляторной энцефалопатией, и модифицирует их. Это удалось установить, разделив пациентов на группы в зависимости от уровня тревоги. Показатели длины и площади статокинезиограммы у больных с низким и умеренным уровнем тревожности были значительно больше, чем у пациентов без инсомнии и пациентов с инсомнией и высокой тревожностью. Вероятно, при усилении тревоги происходит избыточная активация проприоцептивного контроля, что приводит к уменьшению амплитуды колебательных движений и стабилометрических показателей.
Постуральная неустойчивость у пациентов с хронической инсомнией не была связана с повышенной дневной сонливостью или эмоциональными нарушениями. Чем тогда можно объяснить возникновение этого феномена у пожилых людей с нарушениями сна? По современным представлениям, ключевой патофизиологический механизм инсомнии – повышенная функция активирующих систем мозга (hyperarousal). Установлено, что при хронической инсомнии гиперактивация присутствует во время не только сна, но и бодрствования. Это было доказано, например, методом транскраниальной магнитной стимуляции. Однако деятельность других отделов мозга при инсомнии может изменяться разнонаправленно. По данным функциональной магнитно-резонансной томографии в состоянии покоя, при этом заболевании отмечаются снижение функциональной активности в сети управления исполнительных функций, повышение возбудимости сенсомоторных областей и различные изменения активности в других областях головного мозга. Следовательно, инсомния – неоднородное состояние с многогранной патофизиологией, которую невозможно объяснить только глобальным механизмом гиперактивности [19].
Обнаруженное нарушение постурального контроля при инсомнии может быть связано с дисбалансом активирующих и тормозных систем головного мозга, отвечающих за равновесие (ретикулярной формации, ствола мозга, гипоталамуса). Как уже упоминалось, при хронической инсомнии отмечается изменение активности систем, обеспечивающих управляющие функции, в частности дорсолатеральные и вентролатеральные префронтальные области, островковая кора, дополнительная моторная зона [20]. Кроме того, эти отделы головного мозга имеют большое значение для поддержания устойчивости, поскольку в них происходит формирование и поддержание двигательной программы, а также контроль за ее выполнением. Например, нарушение связей между дополнительной моторной корой, подкорковыми и стволовыми структурами проявляется нарушением поддержания равновесия высшего уровня по типу лобно-подкорковой дисбазии, что характерно для хронического сосудистого поражения головного мозга [21]. Изменение функциональной активности лобно-подкорково-стволовых связей при инсомнии, обусловленное дисбалансом тормозных и активирующих влияний ГАМКергических и глутаматергических систем, может усиливать обусловленные сосудистым поражением головного мозга нарушения устойчивости. Для подтверждения этой теории требуется дальнейшая оценка функционального состояния именно этих структур у пациентов с инсомнией и постуральной неустойчивостью.
S.L. Tsenteradze, L.М. Antonenko, MD, PhD, M.G. Poluektov, PhD, Assoc. Prof., B.I. Shigol, S.A. Stanislavsky
I.M. Sechenov First Moscow State Medical University, Moscow
Contact person: Sergo L. Tsenteradze, s.tsenteradze@mail.ru
In experimental studies demonstrated that sleep limitation is accompanied by the postural imbalance. Chronic insomnia is the common problem in patients with mild cognitive impairments and may contribute the postural instability.
38 patients (mean age 63.9 ± 4.8, male/female = 8/30) with mild cognitive impairments. Participants were divided in two groups: 22 patients with chronic insomnia and 16 patients without insomnia.
In patients with insomnia postural sway parameters during Romberg test with closed eyes were significantly increased comparing controls (length of statokinesiogram – 472.1 ± 164.7 mm against 325.4 ± 120.8 mm, p = 0.004, square of statokinesiogram – 392.8 ± 311.9 mm2 against 201.5 ± 130.7 mm2, p = 0.02 and center of pressure – 15.7 ± 5.4 mm/s against 10.8 ± 4.0 mm/s, p = 0.004) which indicates insufficiency of compensatory mechanisms. The correlation between anxiety level (STAI score) and increased postural sway parameters was also identified. This could reflect the influence of emotional state on balance.
Postural sway parameters worsen in patients with insomnia. These disturbances are more pronounced in patients with low anxiety.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.