вульгарный псориаз, интерлейкин 23, устекинумаб, гуселькумаб, эффективность, PASI 90, PASI 100, ускользание эффекта
- Аннотация
- Статья
- Ссылки
- English
Эффект ускользания, или вторичная неэффективность ГИБП, определяет необходимость смены тактики ведения пациентов, в том числе переключение на другой ГИБП. В клинической практике это достаточно сложная задача, которая прежде всего касается выбора следующего препарата.
Переключение на препарат той же группы считается эффективным. Несмотря на принадлежность к одному семейству, данные препараты имеют разное молекулярное строение, механизм действия, фармакодинамику и фармакокинетику.
Если предыдущее лечение было прекращено из-за развития побочных эффектов, рекомендуется переводить пациентов на препараты другой группы.
Гуселькумаб является первым представителем ингибиторов интерлейкина 23. Он имеет ряд преимуществ перед существующей на сегодняшний день терапией. Согласно данным прямых сравнительных рандомизированных клинических исследований, гуселькумаб превосходит по эффективности в краткосрочной и, что особенно важно, в долгосрочной перспективе большинство ГИБП, в том числе ингибиторы фактора некроза опухоли α секукинумаб и устекинумаб. В исследованиях фазы III VOYAGE 1 и 2, исследовании ECLIPSE показано, что уже к 16-й неделе терапии гуселькумаб позволяет достигать полного (PASI 100) и почти полного (PASI 90) очищения кожи у 37,4 и 73,3% пациентов с последующим нарастанием их числа к 24-й неделе до 44,4 и 80,2% и удержанием эффекта в течение четырех лет у 51,7 и 84,0% соответственно.
Терапия гуселькумабом характеризуется благоприятным профилем безопасности, сопоставимым с устекинумабом. В ходе рандомизированных контролируемых исследований фазы III получены данные о высокой безопасности препарата и отсутствии существенных рисков в отношении развития серьезных инфекций, сердечно-сосудистых событий, злокачественных новообразований или суицидальных наклонностей.
Препарат эффективен при недостаточном ответе на адалимумаб и устекинумаб.
В качестве примера приведены два клинических случая применения гуселькумаба у пациентов с тяжелым псориазом, коморбидной патологией, вторичной неэффективностью устекинумаба. У всех пациентов удалось достичь PASI 90/100. Нежелательные явления не отмечались.
Эффект ускользания, или вторичная неэффективность ГИБП, определяет необходимость смены тактики ведения пациентов, в том числе переключение на другой ГИБП. В клинической практике это достаточно сложная задача, которая прежде всего касается выбора следующего препарата.
Переключение на препарат той же группы считается эффективным. Несмотря на принадлежность к одному семейству, данные препараты имеют разное молекулярное строение, механизм действия, фармакодинамику и фармакокинетику.
Если предыдущее лечение было прекращено из-за развития побочных эффектов, рекомендуется переводить пациентов на препараты другой группы.
Гуселькумаб является первым представителем ингибиторов интерлейкина 23. Он имеет ряд преимуществ перед существующей на сегодняшний день терапией. Согласно данным прямых сравнительных рандомизированных клинических исследований, гуселькумаб превосходит по эффективности в краткосрочной и, что особенно важно, в долгосрочной перспективе большинство ГИБП, в том числе ингибиторы фактора некроза опухоли α секукинумаб и устекинумаб. В исследованиях фазы III VOYAGE 1 и 2, исследовании ECLIPSE показано, что уже к 16-й неделе терапии гуселькумаб позволяет достигать полного (PASI 100) и почти полного (PASI 90) очищения кожи у 37,4 и 73,3% пациентов с последующим нарастанием их числа к 24-й неделе до 44,4 и 80,2% и удержанием эффекта в течение четырех лет у 51,7 и 84,0% соответственно.
Терапия гуселькумабом характеризуется благоприятным профилем безопасности, сопоставимым с устекинумабом. В ходе рандомизированных контролируемых исследований фазы III получены данные о высокой безопасности препарата и отсутствии существенных рисков в отношении развития серьезных инфекций, сердечно-сосудистых событий, злокачественных новообразований или суицидальных наклонностей.
Препарат эффективен при недостаточном ответе на адалимумаб и устекинумаб.
В качестве примера приведены два клинических случая применения гуселькумаба у пациентов с тяжелым псориазом, коморбидной патологией, вторичной неэффективностью устекинумаба. У всех пациентов удалось достичь PASI 90/100. Нежелательные явления не отмечались.
Введение
В развитии псориаза генетический компонент составляет 60–70%, на средовые факторы приходится около 40%. Именно поэтому псориаз относится к полигенным заболеваниям, при котором один и тот же фенотип может определяться различными генами. На настоящий момент времени идентифицировано более 100 генов, расположенных на восьми различных хромосомах, ассоциированных с развитием псориаза. Эти генные локусы получили название «гены предрасположенности к псориазу» (psoriasis susceptibility genes) [1].
Псориаз является управляемым цитокинами заболеванием. Доказано, что выраженная пролиферация Т-лимфоцитов предшествует повышенной пролиферации кератиноцитов и акантозу, однако последующая миграция Т-клеток из дермы в эпидермис связана с гиперпролиферацией кератиноцитов [2, 3].
Ведущая роль отводится иммуноопосредованному воспалению, которое реализуется через сложные механизмы взаимодействия кератиноцитов с клетками системы врожденного (миелоидные и плазмоцитарные клетки, дендритные клетки, макрофаги, NK- и NK-Т-клетки) и адаптивного иммунитета (Т-лимфоциты). От степени иммунологических нарушений, дисбаланса цитокиновой регуляции межклеточных взаимодействий зависят тяжесть течения и исход заболевания [4, 5].
Кератиноциты конститутивно экспрессируют интерлейкин 18 (ИЛ-18) мРНК. Этот цитокин в небольших количествах выявляется в цитоплазме базальных кератиноцитов нормальной кожи. При псориазе его количество в кератиноцитах резко возрастает. При активации форболмиристатацетатом, липополисахаридом или контактным сенсибилизатором DNCB кератиноциты синтезируют биологически активный ИЛ-18, способный индуцировать образование в мононуклеарах крови интерферона γ (ИФН-γ) [6]. В воспаленной коже кератиноциты синтезируют практически все провоспалительные цитокины, в частности ИЛ-1β, количество которого в очагах поражения существенно выше, чем в непораженных участках [7]. В воспаленной коже кератиноциты синтезируют хемокины и цитокины СXCL8, CXCL20, ИЛ-1, ИЛ-17, ИЛ-18, ИЛ-20, ИЛ-23, ИФН-γ, привлекающие к псориатическому очагу практически все клетки иммунной системы [8, 9].
Выбор метода лечения прежде всего зависит от тяжести псориатического процесса, локализации поражения, значимых сопутствующих заболеваний (коморбидностей), эффективности предыдущих методов и предпочтений пациента [10].
Раннее начало терапии генно-инженерными биологическими препаратами (ГИБП) способно улучшить отдаленные исходы псориаза. Данные, полученные при изучении иммуноопосредованных заболеваний (включая болезнь Крона, ревматоидный артрит), свидетельствуют, что раннее начало системной терапии имеет важное значение для улучшения результатов лечения и прогноза [11, 12].
Ранний старт терапии ГИБП у пациентов с псориазом с целью достижения полного очищения кожи может рассматриваться как рациональный подход для сдерживания повреждений, связанных с системным воспалением, предотвращения будущих изменений, связанных с системным воспалением, в том числе развития коморбидных состояний, модифицирования течения заболевания, уменьшения его бремени [11–13].
Согласно действующим в Российской Федерации клиническим рекомендациям Российского общества дерматовенерологов и косметологов (РОДВК) (доступно на http://cr.rosminzdrav.ru/#!/schema/866, дата обращения 23.07.2020), ГИБП применяются:
- при среднетяжелом и тяжелом бляшечном псориазе;
- в случаях, если системные иммуносупрессоры или фототерапия оказываются недостаточно эффективными или у пациента развивается непереносимость или имеются противопоказания для их применения.
В Российской Федерации зарегистрированы четыре класса ГИБП по показанию «бляшечный (вульгарный) псориаз»: ингибиторы фактора некроза опухоли α (ФНО-α), ингибиторы ИЛ-17, ИЛ-12/23 и ИЛ-23.
В 2009 г. в РФ для лечения среднетяжелого, тяжелого псориаза и псориатического артрита был зарегистрирован устекинумаб. Это полностью гуманизированное моноклональное антитело, действующее против ИЛ-12p40, который является общей субъединицей ИЛ-12 и ИЛ-23. Данный препарат нейтрализует активность и ИЛ-12, и ИЛ-23, блокируя их взаимодействие с ИЛ-12β1, что приводит к снижению экспрессии провоспалительных цитокинов ИФН-γ, ИЛ-2, ИЛ-8, ИЛ-10, ИЛ-17A и ФНО-α [14].
Эффективность устекинумаба в лечении псориаза была изучена в двух крупных рандомизированных плацебо-контролируемых исследованиях PHOENIX 1 (n = 766) и PHOENIX 2 (n = 1230), в которых препарат назначали при среднетяжелом и тяжелом псориазе в дозе 45 или 90 мг каждые три месяца после индукционной дозы на нулевой и четвертой неделях.
В исследовании PHOENIX 1 на 12-й неделе 75, 90 и 100 баллов по индексу тяжести и распространенности псориатического процесса (Psoriasis Area and Severity Index – PASI) при дозе устекинумаба 45 мг достигли 67,1, 41,6 и 12,5% пациентов, при дозе 90 мг – 66,4, 36,7 и 10,9% соответственно. На 28-й неделе PASI 75, PASI 90 и PASI 100 зафиксированы у 71,2, 49,2 и 20,8% получавших устекинумаб в дозе 45 мг и 78,6, 55,6 и 29,2% применявших его в дозе 90 мг [15].
Исследование PHOENIX 2 проводилось на базе 70 медицинских центров Северной Америки и Европы. Его отличительной чертой стала оценка интенсификации режима введения препарата у имевших частичный ответ на терапию. Так, на 28-й неделе терапии частичный ответ (50 < PASI < 75) отмечался у 22,7% в группе устекинумаба 45 мг и у 15,8% в группе устекинумаба 90 мг. У пациентов имели место более высокая масса тела и неэффективность как минимум одного системного препарата (стандартный или ГИБП). Согласно дизайну исследования, частичные ответчики с 28-й по 52-ю неделю стали получать устекинумаб в дозе 90 мг один раз в два месяца. В результате PASI 75 у них был достигнут в гораздо большем числе случаев по сравнению с теми, кто получал устекинумаб в той же дозе, но один раз в три месяца (68,8 vs 33,3%) [16]. К 244-й неделе наблюдения PASI 75 сохранялся у 76,5% получавших устекинумаб в дозе 45 мг и 78,6% – в дозе 90 мг, PASI 90 – у 50,0 и 55,5% соответственно [17].
При первичной неэффективности ГИБП, появлении антител, развитии нежелательных явлений или других веских причинах больных переводят с одного биологического препарата на другой. Это может быть смена как группы ГИБП, так и препарата внутри одной и той же группы. Регулярное появление все более эффективных и менее затратных биологических препаратов, высокие ожидания пациентов от лечения привели к широкому распространению этого метода в повседневной практике дерматологов.
Ранее полагали, что перед назначением нового препарата необходимо выждать, пока не завершится вымывание предыдущего, что по времени должно было превышать период полувыведения препарата в четыре раза [18]. Однако в настоящее время считается, что если причиной смены ГИБП является его неэффективность, то не следует дожидаться окончания периода его вымывания из организма. Вместе с тем в случае, когда причиной смены препарата послужили развившиеся побочные эффекты, выжидательную тактику следует соблюсти [19].
Эффективность переключения между препаратами внутри группы обусловлена тем, что, несмотря на принадлежность к одному семейству, они имеют совершенно разное молекулярное строение, механизм действия, фармакодинамику и фармакокинетику.
Если предыдущее лечение было прекращено из-за развития побочных эффектов, рекомендуется перевод больных на препараты другой группы.
Развитие первичной неэффективности, обусловленной генетическими особенностями реципиента, преодолевается с помощью изменения дозы или режима дозирования ГИБП, комбинации с низкими дозами метотрексата, смены одного ГИБП на другой. Возможно также развитие вторичной неэффективности, или эффекта ускользания, главной причиной которого является выработка нейтрализующих антител к препарату, что в большей степени касается ингибиторов ФНО-α, особенно в долгосрочной перспективе [20, 21].
Согласно результатам многочисленных наблюдений, почти у трети получавших инфликсимаб в течение одного года эффективность терапии снижалась на 30%. Иная картина отмечалась при применении устекинумаба, эффект которого сохранялся на протяжении пяти лет [22].
Представитель нового класса ГИБП гуселькумаб – моноклональное человеческое антитело типа иммуноглобулин 1λ, которое селективно связывается с белком ИЛ-23 с высокой специфичностью и аффинностью. ИЛ-23 – регуляторный цитокин, который влияет на дифференцировку, миграцию и жизнеспособность субпопуляций Т-клеток, например Тh17 и Тc17, и незрелых субпопуляций иммунных клеток, являющихся источником эффекторных цитокинов, включая ИЛ-17А, ИЛ-17F и ИЛ-22, участвующих в воспалительном каскаде. В исследованиях in vivo показано, что селективная блокада ИЛ-23 нормализует выработку этих цитокинов. В присутствии ИЛ-23 повышается выживаемость Th17-лимфоцитов, продуцирующих ИЛ-17 и родственные ему цитокины. Кроме того, ИЛ-23 вызывает фенотипические и функциональные изменения Т-регуляторных клеток, способствующих повышению продукции воспалительных цитокинов, таких как ИФН-γ, ФНО-α, ИЛ-17A и ИЛ-22 [23, 24]. Именно поэтому ИЛ-23 считается ключевым цитокином в патогенезе псориаза. Это подтверждается его высоким содержанием как в сыворотке крови, так и в коже, взятой из псориатических очагов [25, 26].
Гуселькумаб позволял достигать PASI 100, PASI 90, а также PASI 75 уже к 16-й неделе терапии у 37,4, 73,3 и 91,2% пациентов с последующим возрастанием доли последних к 24-й неделе до 44,4, 80,2 и 71,2% и удержанием достигнутых показателей в течение четырех лет у 55,7% (49,1% на 52-й неделе), 82,2% (79,7%) и 94,1% (93,8%) соответственно [27, 28]. По эффективности гуселькумаб превосходил адалимумаб и устекинумаб у пациентов с тяжелым и среднетяжелым псориазом, в том числе у недостаточно ответивших на терапию данными препаратами.
В исследованиях фазы III VOYAGE 1 и 2 показано, что на 16-й и 24-й неделях гуселькумаб превосходил адалимумаб по количеству достигших PASI 75, PASI 90 и PASI 100, а также по количеству достигших полного/почти полного очищения кожи по шкале глобальной оценки (Investigator Global Assessment – IGA) – IGA 0/1 [29].
На 16-й неделе PASI 90 был достигнут у 73,3% в группе гуселькумаба по сравнению с 49,7% в группе адалимумаба в исследовании VOYAGE 1 и 70,0 по сравнению с 46,8% в группе адалимумаба в исследовании VOYAGE 2 (p < 0,001 в обоих случаях) [27, 28].
В клинической практике одним из основных показателей эффективности ГИБП является выживаемость терапии. Применение гуселькумаба обеспечивает длительный и стойкий эффект. Так, достижение PASI 90 и PASI 100 на первом, втором, третьем и четвертом году терапии составило 80,6, 83,3, 84,0, 84,3 и 49,7, 51,8, 51,8, 57,1% соответственно [30].
Эффект ускользания, или вторичная неэффективность ГИБП, обусловливает смену тактики ведения пациентов, в том числе переключение на другой генно-инженерный препарат. В клинической практике это достаточно сложная задача, которая прежде всего касается выбора следующего препарата. Решением может быть переключение на ГИБП с иным механизмом действия.
В исследованиях VOYAGE 1 и 2 у 73% пациентов, не достигших ответа на фоне 48-недельной терапии адалимумабом, отмечалось достижение PASI 90 после переключения на гуселькумаб [31].
В исследовании NAVIGATE прирост эффективности у пациентов с недостаточным ответом на устекинумаб при переводе на гуселькумаб составил 27% (р < 0,001) при оценке доли достигших PASI 90 к 52-й неделе терапии [32, 33].
Таким образом, данные клинических исследований позволяют рекомендовать гуселькумаб в качестве препарата выбора при эффекте ускользания, или недостаточной эффективности ингибиторов ФНО-α, ИЛ-17 и ИЛ 12/23.
Гуселькумаб характеризуется низкой иммуногенностью. Доля пациентов, у которых появились антитела к препарату, составила 5,5%, при этом не было отмечено влияния антител к препарату на показатели эффективности и безопасности лечения [32].
В клинических исследованиях гуселькумаб продемонстрировал хороший профиль безопасности. Так, менее 3% пациентов прекратили лечение из-за развития нежелательных явлений и менее 7% отметили возникновение серьезных нежелательных явлений. Наиболее частыми нежелательными явлениями были инфекции. При этом в клинических исследованиях не сообщалось о развитии у получавших гуселькумаб оппортунистических инфекций, реактивации туберкулеза или возникновении реакций гиперчувствительности [34].
В клинических исследованиях среднее время потери ответа по PASI 90 на терапию гуселькумабом составило 23 недели. После последней инъекции гуселькумаба у 36% пациентов сохранялся ответ по PASI 90, у 60% – по PASI 75 в течение 28 недель [28]. У 80% больных ответ по PASI 90 восстанавливался уже после трех введений гуселькумаба [35].
Клиническая практика и обсуждение ее результатов
Ниже приведены примеры конкретных клинических случаев.
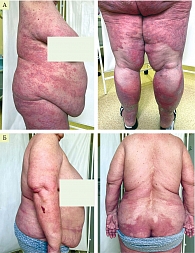
Клинический случай 1. Пациентка И., 1958 г.р., болеет псориазом с 2018 г. Именно тогда впервые отметила высыпания на коже туловища, выраженные боли в суставах. Появление высыпаний связывает с перенесенным стрессом. C 2019 г. с регулярностью один-два раза в год получала лечение в условиях стационара Краснодарского краевого клинического кожно-венерологического диспансера (ККВД).
Диагноз: псориаз вульгарный, прогрессирующая стадия.
Сопутствующие диагнозы: гипертоническая болезнь II стадии, риск 4-й, хроническая сердечная недостаточность 1-й степени, 2-го функционального класса по классификации выраженности хронической сердечной недостаточности Нью-Йоркской кардиологической ассоциации, сахарный диабет 2 типа, целевой уровень гликированного гемоглобина менее 7,5%, ожирение 3-й степени.
Осложнения основного заболевания: псориатический артрит, полиартрит умеренной степени активности с поражением коленных, голеностопных, мелких суставов стоп, с энтезитами (ахиллово сухожилие), рентгенологическая стадия требует уточнения, функциональная недостаточность суставов 2-й степени, консолидированный перелом трети диафиза малоберцовой кости, неконсолидированный перелом медиальной лодыжки с небольшим смещением отломков, выраженный посттравматический крузартроз 3-й степени, пяточная шпора, функциональная недостаточность суставов 3-й степени.
Пациентке были назначены метотрексат в дозе 20 мг, наружная терапия, фототерапия.
После приема метотрексата в дозе 20 мг еженедельно в течение трех месяцев с учетом коморбидности и незначительной динамики кожного и суставного процессов больной был назначен устекинумаб с инициацией согласно инструкции.
Через 18 месяцев от начала приема препарата пациентка отметила появление новых высыпаний, боли в области шейного отдела позвоночника.
Больная была госпитализирована в стационарное отделение ККВД.
Анализ крови: скорость оседания эритроцитов – 35 мм/ч, уровень С-реактивного белка – 40 мг/л.
При осмотре: на коже волосистой части головы (затылочная область), туловища (грудь, спина, живот), верхних конечностей (разгибательные поверхности плеч, предплечий, локтевых суставов), нижних конечностей (передние и задние поверхности бедер, голеней, разгибательные поверхности коленных суставов) множественные инфильтрированные бляшки ярко-красного цвета, покрытые частично прилегающими серебристыми чешуйками, PASI – 35 баллов.
С учетом прогрессирования кожного процесса, суставного синдрома на фоне приема устекинумаба (эффект ускользания), наличия сопутствующих соматических заболеваний пациентке был назначен гуселькумаб (Тремфея) в дозе 100 мг в виде подкожных инъекций. Вторая инъекция – через четыре недели после первой, последующие введения – один раз каждые восемь недель.
К 12-й неделе терапии гуселькумабом отмечена выраженная положительная динамика – достижение PASI 85. После четырех инъекций наблюдался полный регресс высыпаний – достижение PASI 100. В клиническом и биохимическом анализах крови отклонений не выявлено. После десяти месяцев терапии ремиссия сохранялась, жалобы на боли в суставах отсутствовали (рис. 1).
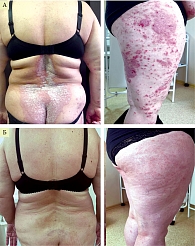
Клинический случай 2. Пациентка Р., 1981 г.р. Считает, что больна с 1987 г., когда впервые появились высыпания на коже нижних конечностей. Обратилась к дерматологу по месту жительства, где был поставлен диагноз «псориаз».
В подростковом возрасте использовала народные методы лечения (отвар ржаной соломы), отмечала улучшение.
В 15 лет высыпания распространились на кожу волосистой части головы и туловища. Обращалась к дерматологу по месту жительства. Назначенные топические наружные средства способствовали улучшению состояния.
Системную патогенетическую терапию псориаза больная не получала. Суставной синдром не беспокоил.
В 2020 г. в связи с распространением высыпаний пациентка была госпитализирована в стационарное отделение ККВД в тяжелом состоянии. Диагноз: вульгарный псориаз, прогрессирующая стадия, PASI – 20 баллов. При осмотре: на коже волосистой части головы, туловища (грудь, спина, живот), верхних конечностей (разгибательные поверхности плеч, предплечий), нижних конечностей (передние и задние поверхности бедер, голеней) множественные инфильтрированные по периферии папулы и бляшки ярко-красного цвета, покрытые частично прилегающими серебристыми чешуйками.
С учетом тяжести, торпидности, давности течения заболевания пациентке был назначен устекинумаб с инициацией согласно инструкции.
Через шесть месяцев приема препарата больная отметила появление новых высыпаний.
При осмотре: на коже волосистой части головы (затылочная область), туловища (грудь, спина, живот), верхних конечностей (разгибательные поверхности плеч, предплечий, локтевых суставов), нижних конечностей (передние и задние поверхности бедер, голеней, разгибательные поверхности коленных суставов) множественные инфильтрированные бляшки ярко-красного цвета, покрытые частично прилегающими серебристыми чешуйками, PASI – 45 баллов.
В связи с прогрессированием кожного процесса, суставного синдрома на фоне приема устекинумаба (эффект ускользания), наличием сопутствующих соматических заболеваний пациентке был назначен гуселькумаб (Тремфея) в дозе 100 мг в виде подкожных инъекций. Вторая инъекция – через четыре недели после первой. В дальнейшем препарат вводили один раз каждые восемь недель.
После 16 недель лечения отмечены регресс высыпаний, отсутствие новых высыпаний, на месте разрешившихся элементов пятна вторичной гиперпигментации, отсутствие шелушения, достижение PASI 100 (рис. 2).
Обсуждение результатов. Препарат гуселькумаб активно внедряется в практику дерматовенерологов для лечения среднетяжелого и тяжелого псориаза. Особенно актуально использование данного препарата после ускользания эффекта от ранее проведенной генно-инженерной биологической терапии.
Представленные клинические случаи демонстрируют высокую эффективность препарата гуселькумаб как у бионаивных пациентов, так и у пациентов, не ответивших на ингибитор ФНО-α.
Гуселькумаб оказался высокоэффективным в отношении достижения PASI 90 и PASI 100 у пациентов с тяжелым псориазом, в том числе в сочетании с псориатическим артритом и сопутствующей коморбидной патологией. Лечение переносилось хорошо, нежелательных явлений не зарегистрировано.
Данные клинических исследований и практический опыт применения препарата определяют выбор гуселькумаба как препарата с лучшим на текущий период времени профилем эффективности и безопасности, который возможно применять у пациентов с сочетанной коморбидной патологией.
Выводы
Гуселькумаб является первым представителем ингибиторов ИЛ-23 и имеет ряд преимуществ.
Согласно данным метаанализа, гуселькумаб превосходит по эффективности в краткосрочной и, что особенно важно, в долгосрочной перспективе большинство ГИБП, в том числе ингибиторы ФНО-α секукинумаб и устекинумаб [21, 26].
Гуселькумаб эффективен не только в отношении бляшечного псориаза, но и псориаза проблемной локализации (псориаз волосистой части головы, псориаз ладоней и подошв, псориатическая ониходистрофия) и превосходит в этом адалимумаб.
Благодаря своему механизму действия гуселькумаб практически не имеет противопоказаний и особых указаний, связанных с использованием ингибиторов ФНО-α (сердечная недостаточность, аутоиммунное или демиелинизирующее заболевание) и ингибиторов ИЛ-17 (воспалительное заболевание кишечника, кандидоз слизистых оболочек и кожи) [17].
Результаты клинических исследований гуселькумаба свидетельствуют о том, что он улучшает показатели качества жизни и трудоспособности, обладает благоприятным профилем безопасности.
Терапия гуселькумабом характеризуется удобным режимом дозирования, а также низкими показателями иммуногенности и позволяет существенно повысить эффективность и переносимость проводимой терапии, в том числе у пациентов с недостаточным ответом на адалимумаб и устекинумаб.
Гуселькумаб включен в российские клинические рекомендации РОДВК по ведению больных псориазом 2020 г. [27]. Препарат показан пациентам с бляшечным псориазом средней и тяжелой степени с непрерывно-рецидивирующим характером течения (частота госпитализаций в связи с обострением кожного процесса более трех раз в год), выраженным нарушением качества жизни, отсутствием эффекта или плохой переносимостью/наличием противопоказаний для применения системных противовоспалительных препаратов (метотрексата, ацитретина, циклоспорина или ГИБП) или угрозой утраты трудоспособности и инвалидизации.
Гуселькумаб эффективен у пациентов с псориазом ногтей, волосистой части головы, ладонно-подошвенной области.
Эффективность препарата не зависит от веса пациентов.
Опыт применения гуселькумаба в реальной клинической практике показал его высокую эффективность у пациентов с тяжелым бляшечным псориазом, проблемным псориазом, в том числе в сочетании с псориатическим артритом и другой коморбидной патологией.
Долгосрочные данные (исследование VOYAGE 1 продолжительностью 204 недели) свидетельствуют об устойчивом поддержании высокого ответа по PASI 100, PASI 90, PASI 75, IGA 0, IGA 0/1 и, что не менее важно, по показателям качества жизни пациентов, что может определять выбор препарата с учетом хронического прогрессирующего течения заболевания.
A.A. Hotko, PhD, M.Yu. Pomazanova, L.S. Kruglova, MD, PhD
Clinical Dermatovenerologic Dispensary of the Ministry of Healthcare of Krasnodar Region
Central State Medical Academy Department of Presidential Affairs
Contact person: Alkes A. Hotko, alkes@inbox.ru
The article provides the results of clinical studies of the effectiveness and safety of genetically engineered biological drugs (GEBP) ustekinumab and guselkumab.
The eluding effect, or secondary inefficiency of the GEBP, determines the need to change the tactics of patient management, including switching to another GEBP. In clinical practice, this is a rather difficult task, which primarily concerns the choice of the next drug.
Switching to a drug of the same group is considered effective. Despite belonging to the same family, these drugs have different molecular structure, mechanism of action, pharmacodynamics and pharmacokinetics.
If the previous treatment was discontinued due to the development of side effects, to transfer patients to drugs of another group is recommended.
Guselkumab appears to be the first representative of interleukin 23 inhibitors. It has a number of advantages over the current therapy. According to the data of direct comparative randomized clinical trials, guselkumab is superior in efficacy in the short term and, most importantly, in the long term to most GEBPs, including α tumor necrosis factor inhibitors secukinumab and ustekinumab. In phase III VOYAGE 1 and 2 studies, the ECLIPSE study showed that by the 16th week of therapy guselkumab allows achieving complete (PASI 100) and almost complete (PASI 90) skin cleansing in 37.4 and 73.3% of patients, followed by the increase in their number by the 24th week to 44.4 and 80.2% and retention of the effect for four years in 51.7 and 84.0%, respectively.
Guselkumab therapy is characterized by a favorable safety profile comparable to ustekinumab. In the course of randomized controlled phase III trials, data were obtained on the high safety of the drug and the absence of significant risks in relation to the development of serious infections, cardiovascular events, malignant neoplasms or suicidal tendencies.
The drug is effective in case of insufficient response to adalimumab and ustekinumab.
As an example, two clinical cases of guselkumab usage in patients with severe psoriasis, comorbid pathology, secondary inefficiency of ustekinumab are given. PASI 90/100 was achieved in all patients. Adverse events were no observed.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.