Выбор биологической терапии с позиции долгосрочной эффективности у пациента молодого возраста с болезнью Крона
- Аннотация
- Статья
- Ссылки
- English
Введение
Болезнь Крона (БК) и язвенный колит, входящие в группу воспалительных заболеваний кишечника (ВЗК), являются актуальной проблемой современной гастроэнтерологии. Этиология заболеваний не ясна. В развитии заболеваний играет роль ряд факторов: генетическая предрасположенность, нарушение регуляции иммунного ответа на кишечную микрофлору, различные факторы окружающей среды. Больные с этими заболеваниями более склонны к развитию злокачественных новообразований [1].
Предполагается, что самые высокие показатели заболеваемости ВЗК отмечаются в развитых странах, а самые низкие – в развивающихся. В регионах с более холодным климатом и городских районах частота возникновения ВЗК выше, чем в регионах с более теплым климатом и в сельской местности. В международном масштабе заболеваемость ВЗК составляет 0,5–24,5 случая на 100 тыс. населения для язвенного колита и 0,1–16 случаев на 100 тыс. населения для болезни Крона. В целом распространенность ВЗК составляет 396 случаев на 100 тыс. человек в год [2, 3]. Первый пик заболеваемости отмечается между 20 и 30 годами жизни, а второй – в возрасте 60–70 лет [1, 4].
Распространенность БК в России составляет 3,0–4,5 на 100 тыс. населения [5]. БК характеризуется поражением любого сегмента желудочно-кишечного тракта (от полости рта до ануса). В 35% случаев БК возникает в подвздошной и толстой кишке, в 32% – исключительно в толстой кишке, в 28% – в тонкой кишке и в 5% случаев – в гастродуоденальной области [6].
Основные группы лекарственных препаратов, используемых при лечении БК, утверждены отечественными клиническими рекомендациями и хорошо изучены. Основными задачами терапии БК являются индукция ремиссии, поддержание ремиссии без стероидов, профилактика осложнений. Противорецидивную терапию следует проводить даже после хирургического вмешательства, так как оперативное лечение не приводит к полному излечению пациентов с БК [1].
Наибольшие успехи в терапии ВЗК связаны с применением генно-инженерной биологической терапии (ГИБТ). По промежуточным результатам исследования INTENT [7], общая частота применения ГИБТ у среднетяжелых и тяжелых пациентов составила 66,4%. Основная часть ГИБТ приходится на препараты из группы ингибиторов фактора некроза опухоли альфа (иФНО-α), которые суммарно получают более 40% пациентов [7].
К факторам, влияющим на выбор ГИБТ, относятся: клиническая форма заболевания, наличие перекрестной иммуновоспалительной патологии, сопутствующих хронических неинфекционных заболеваний, сопутствующих вирусных и инфекционных заболеваний, режим дозирования и способ введения препарата, иммуногенность, возможность длительного применения препарата (потенциальная «выживаемость терапии»), скорость наступления терапевтического эффекта, доступность, предпочтения пациента [8].
Наличие актуальных клинических рекомендаций и зарубежных гайдлайнов во многом может обосновать правильность выбора терапии, но не всегда полностью закрыть все возникшие вопросы. Позиции доказательной медицины основываются на данных клинических исследований, имеющих достаточно репрезентативную выборку и проведенных с учетом всех требований GСP (добросовестной клинической практики) [9].
Клиническое наблюдение
Пациент К., 34 года, обратился к колопроктологу поликлиники Окружной клинической больницы г. Ханты-Мансийска в июне 2018 г. с жалобами на жидкий стул до 6–8 раз в сутки с примесью крови (со слов, до 5–15 мл при каждой дефекации), боль в области заднего прохода, повышение температуры тела до 38 °С.
Из анамнеза известно, что впервые следы крови в стуле появились в январе 2018 г. (на момент появления первых симптомов заболевания возраст пациента был 30 лет, курит с 18 лет по настоящее время). Пациент самостоятельно не обследовался и за медицинской помощью не обращался. Состояние ухудшилось в течение трех недель.
При колоноскопии (КС): эрозии в области баугиниевой заслонки и в терминальном отделе подвздошной кишки на протяжении 15 мм; слизистая толстой кишки на всем протяжении от прямой до слепой кишки ярко гиперемирована, эрозирована (от афтозных высыпаний до сливных эрозий) с поверхностными язвенными дефектами, контактно кровоточит, гаустрация сглажена. При патогистологическом исследовании: в терминальном отделе подвздошной кишки явления хронического высокоактивного выраженного энтерита с лимфофолликулярной гиперплазией без дисплазии покровного эпителия; в биоптатах толстой кишки гистологическая картина хронического активного колита с полиморфно-клеточной инфильтрацией, крипт-абсцессами, полными эрозиями без дисплазии эпителия.
У пациента также диагностирован острый ишиоректальный парапроктит. Сформулирован диагноз: «язвенный колит, тотальное поражение (с терминальным отделом подвздошной кишки), умеренная эндоскопическая активность, среднетяжелое течение».
Пациент госпитализирован в хирургическое отделение, парапроктит вскрыт. Для дальнейшей терапии переведен в круглосуточный стационар гастроэнтерологического профиля. С целью индукции ремиссии назначена терапия системными глюкокортикостероидами (ГКС) (преднизолон 60 мг в сутки перорально, по схеме снижения в течение 12 недель), месалазин 2,4 г в сутки перорально. Клинически купирование симптомов заболевания пациент отметил через 4–5 дней. Пациент продолжил поддерживающую терапию месалазином 2,4 г в сутки перорально до июня 2019 г. Затем самостоятельно отменил терапию.
В сентябре 2019 г. возник рецидив острого гнойного парапроктита (вскрыт, дренирован). В октябре 2019 г. – учащение стула до 5–8 раз в сутки с кровью, боли в животе, повышение температуры тала до фебрильных цифр. Госпитализирован для дообследования.
При КС в подвздошной кишке (до 15,0 см от баугиниевой заслонки) умеренное воспаление, две язвы до 0,5 см, под фибрином; выраженный патологический процесс от верхнеампулярного отдела до 45,0 см от ануса – множественные глубокие язвы круглой и продольной формы до 1,0 см, 2,0 × 1,2 см; в прямой кишке множественные афтозные эрозии; в слепой кишке участок рыхлой воспаленной слизистой; в ободочной кишке единичные афты. По результатам эндоскопической картины возникло предположение о наличии у пациента болезни Крона. При патогистологическом исследовании выявлено: признаки хронического илеита средней степени активности с полиморфно-клеточной инфильтрацией; хронический активный колит средней степени активности с полиморфно-клеточной инфильтрацией; гранулирующий полип толстой кишки. Основной клинический диагноз: «язвенный колит, тотальное поражение толстой кишки (с терминальным отделом подвздошной кишки), хроническое рецидивирующее течение, среднетяжелая атака; болезнь Крона (?)».
С целью индукции ремиссии назначена терапия системными стероидами (преднизолон 60 мг в сутки перорально, по схеме снижения в течение 12 недель), микроклизмы с суспензией гидрокортизона по 125 мг один раз в сутки № 10, азатиоприн 100 мг в сутки, месалазин 3 г в сутки перорально. Клинически купирование симптомов заболевания отмечено через 10 дней. Пациент продолжил поддерживающую терапию азатиоприном 100 мг в сутки и месалазином 3 г в сутки.
На фоне приема поддерживающей терапии в августе 2020 г. возникло обострение заболевания. Рецидив острого гнойного парапроктита (самостоятельное вскрытие). Появление болей в животе, неоформленный стул до пяти раз в сутки с кровью, снижение аппетита, похудение.
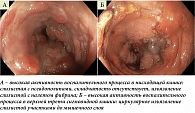
По данным лабораторных исследований, в общем анализе крови отмечено снижение уровня гемоглобина до 100 г/л, увеличение СОЭ до 40 мм/ч, повышение С-реактивного белка до 77,15 мг/л; в биохимическом анализе крови снижение уровня железа до 2,7 ммоль/л. Выполнена КС: терминальный отдел подвздошной кишки эндоскопически не изменен; слизистая передней губы баугиниевой заслонки слабо гиперемирована, пастозная, с поверхностными эрозиями; в слепой кишки псевдополипы; начиная с селезеночного изгиба до средней трети сигмовидной кишки (до уровня 28 см от ануса) циркулярное изъязвление слизистой участками до мышечного слоя, с островками сохраненной слизистой, псевдополипами, складчатость отсутствует, дистально просвет незначительно сужен (на данном участке большое количество псевдополипов), у дистального края видны два фиксированных темных сгустка, активного кровотечения на момент осмотра нет, края язвенного дефекта приподняты, слизистая в краях ярко гиперемирована, отечная, с геморрагиями (рис. 1).
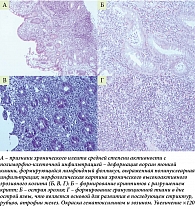
При патогистологическом исследовании: поверхностные фрагменты слизистой с признаками хронического илеита средней степени активности с полиморфно-клеточной инфильтрацией; морфологическая картина хронического высокоактивного эрозивного колита (рис. 2).
Учитывая на тот момент эпидемиологический подъем заболеваемости новой коронавирусной инфекцией COVID-19, перепрофилирование коек круглосуточного стационара гастроэнтерологического профиля в инфекционные, лечение данной атаки заболевания проводилось амбулаторно. С целью индукции ремиссии назначена терапия системными стероидами (преднизолон 50 мг в сутки перорально, по схеме снижения в течение 12 недель), продолжена терапия азатиоприном 100 мг в сутки, месалазин отменен. Клинически купирование симптомов заболевания пациент отметил через 1,5 месяца.
Учитывая особенности клинической, эндоскопической и гистологической картины, в ноябре 2020 г. диагноз изменен: «болезнь Крона, илеоколит с вовлечением слепой, поперечно-ободочной, нисходящей, сигмовидной кишки, распространенное поражение с перианальным поражением (транссфинктерный свищ прямой кишки), хроническое рецидивирующее течение, высокая активность».
По данным компьютерной томографии (КТ) органов брюшной полости с внутривенным болюсным контрастированием в октябре 2020 г., выявлены следующие изменения: стенки толстой кишки в области селезеночного угла, в нисходящем отделе диффузно утолщены, демонстрируют повышенную васкуляризацию, слоистое контрастирование. Заключение: болезнь Крона.
Пациент продолжил поддерживающую терапию азатиоприном 100 мг в сутки.
В феврале 2021 г. на фоне поддерживающей терапии иммуносупрессорами (ИС), клинической ремиссии проведена контрольная КС. При КС эндоскоп проведен в купол слепой кишки с осмотром терминального отдела подвздошной кишки. Слизистая оболочка терминального отдела подвздошной, слепой, восходящей и поперечно-ободочной кишки розовая с равномерным сосудистым рисунком. В области селезеночного изгиба видны два эрозированных участка продолговатой формы 15 × 7 и 6 × 4 мм с налетом фибрина, плоские, на фоне рубцово измененной слизистой, на всем протяжении нисходящей кишки и верхней трети сигмовидной кишки слизистая рубцово источена, сосудистый рисунок неравномерный, видны псевдополипы от 2 × 3 до 8 × 5 мм. От ректосигмоидного отдела до верхней трети сигмовидной кишки слизистая розовая с равномерным сосудистым рисунком. В ректосигмоидном отделе округлый очаг рубцово измененной слизистой с измененным сосудистым рисунком и псевдополипами. В прямой кишке слизистая розовая, с неравномерным сосудистым рисунком.
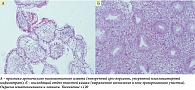
По результатам морфологического исследования биопсийного материала, взятого при КС, в терминальном отделе подвздошной кишки выявлена картина хронического низкоактивного илеита. В правых отделах толстой кишки и в поперечно-ободочной – хронический атрофический колит вне фазы активности. В зоне эндоскопических изменений – эпителизирующаяся хроническая эрозия слизистой оболочки толстой кишки в активной фазе с перифокальным высокоактивным воспалением (рис. 3).
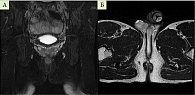
С учетом отсутствия эндоскопического заживления слизистой оболочки толстой кишки на фоне терапии иммуносупрессорами и с целью определения дальнейшей тактики ведения пациента проведена телемедицинская консультация со специалистами Национального медицинского исследовательского центра колопроктологии имени
А.Н. Рыжих, по результатам которой получено заключение: согласно предоставленной медицинской документации, пациенту можно выставить диагноз болезни Крона; принимая во внимание сохранение активного воспалительного процесса на фоне проводимой терапии иммуносупрессорами, пациенту показана ГИБТ (возможно устекинумабом); хирургическое лечение перианального поражения в настоящий момент не показано, так как определяющийся транссфинктерный свищ дренируется на кожу промежности (рис. 4).
В мае 2021 г. пациенту проведена инициация ГИБТ препаратом устекинумаб в дозе 390 мг внутривенно капельно. Дальнейший режим терапии – один раз в 12 недель по 90 мг подкожно. Поддерживающая терапия азатиоприном в дозе 100 мг в сутки продолжена.
При контрольной КС в ноябре 2021 г. определена эндоскопическая ремиссия.
По результатам патогистологического исследования биопсийного материала, взятого при КС, выявлено: нисходящая кишка – хронический умеренно-активный колит с формированием лимфоидных скоплений, очагами фиброза и очаговой гиперплазией слизистой оболочки; сигмовидная кишка – хронический атрофический колит низкой степени активности с выраженным фиброзом собственной пластинки (рубец).
В феврале 2022 г. пациент перенес новую коронавирусную инфекцию COVID-19, легкой степени тяжести; ОРВИ, легкое течение.
В настоящее время – 80-я неделя терапии. Клинически у пациента стул один раз в сутки без крови, боли в животе нет, температура тела нормальная, прибавка в весе составила 2 кг; лабораторных признаков активности заболевания не выявлено.
Контрольное эндоскопическое исследование, КТ-энтерография запланированы на январь 2023 г. (обследоваться ранее пациент не имел возможности по личным обстоятельствам).
Обсуждение
В соответствии с российскими клиническими рекомендациями, любой биологический препарат может быть выбран в качестве терапии первой линии БК [1].
При выборе терапии важно оценить наличие у пациента факторов неблагоприятного прогноза заболевания на момент установления диагноза: возраст < 40 лет, распространенное (> 100 см) поражение тонкой кишки, ранняя потребность в назначении системных стероидов, перианальная и пенетрирующая формы заболевания, вовлечение верхних отделов ЖКТ, отсутствие заживления слизистой оболочки при достижении клинической ремиссии, статус курильщика, наличие эпителиоидных гранулем, наличие сопутствующих аутоиммунных заболеваний [1, 8].
Согласно эпидемиологическим данным о заболеваемости ВЗК в Российской Федерации, полученным Е.А. Белоусовой и соавт. [4], дебют БК приходится на возрастную группу 21–30 лет. У наблюдаемого пациента заболевание было диагностировано в 30 лет.
Курение считается важным неблагоприятным фактором в развитии и прогрессировании БК. Факт курения с возраста 18 лет у курируемого пациента, вероятно, способствовал увеличению риска возникновения заболевания, а продолжение курения до настоящего времени является фактором неблагоприятного прогноза по развитию осложнений [3, 4].
За период болезни в течение трех лет у пациента трижды возникала потребность в назначении системных ГКС. У пациента наблюдался ответ в виде достижения клинической ремиссии на терапию ГКС. Проявлений стероидорезистентности и стероидозависимости не зафиксировано. При этом обращает на себя внимание снижение скорости достижения ответа при повторных курсах индукции ремиссии с использованием ГКС. Потребность в двух и более курсах ГКС является одним из критериев целесообразности назначения ГИБТ [7].
По данным эпидемиологического исследования ESCApe, проведенного в Российской Федерации, иммуносупрессоры при БК были назначены всего 26,8% пациентов. Результаты ESCApe-2 показали, что через три года статистически значимо выросла доля больных, получавших ИС при БК, – до 55% [4]. Несмотря на терапию иммуносупрессорами, у данного пациента сохранялся активный воспалительный процесс, в связи с чем ему была назначена ГИБТ.
Таким образом, у пациента К. имеется пять факторов неблагоприятного прогноза заболевания (возраст < 40 лет, ранняя потребность в назначении системных стероидов, перианальная форма заболевания, отсутствие заживления слизистой оболочки при достижении клинической ремиссии, статус курильщика), что является веским аргументом в пользу выбора системного биологического препарата с благоприятным профилем безопасности – ингибитора интерлейкинов (ИЛ) 12 и 23 (устекинумаба).
Молекула устекинумаб блокирует ключевые регуляторные цитокины, ингибирует путь активации Th1-, Th2-, Th17-лимфоцитов, блокирует передачу сигналов ИЛ-12 и ИЛ-23, обеспечивая эффективность как на ранней, так и на поздней стадии БК [10–14].
Не менее важное значение имеет и переносимость терапии. В данном аспекте устекинумаб продемонстрировал преимущества перед другими системными биологическими препаратами. Устекинумаб характеризуется достаточно быстрым механизмом действия, низкой иммуногенностью и высоким профилем безопасности, что позволяет применять его в случае клинической активности заболевания для обеспечения быстрого терапевтического эффекта [15].
Следует отметить, что наиболее высокие результаты долгосрочной эффективности устекинумаб демонстрирует в группе бионаивных пациентов. По данным A. Johnson и соавт. [16], кумулятивная частота клинической и эндоскопической ремиссии на фоне терапии устекинумабом у бионаивных пациентов через год терапии составила 63 и 55% соответственно, в том случае, если устекинумаб применяли во второй линии биологической терапии, – 43 и 37% соответственно.
По данным австралийского регистра, устекинумаб обладает самой высокой «выживаемостью терапии» у пациентов с БК по сравнению с инфликсимабом, адалимумабом, ведолизумабом: через год 80% пациентов с БК продолжили терапию устекинумабом [17].
По данным продолженной фазы исследования UNITI LTE, доля пациентов с БК с достижением клинической ремиссии через пять лет терапии устекинумабом составила 55% (устекинумаб 90 мг подкожно один раз в восемь недель) и 46,7% (устекинумаб 90 мг подкожно один раз в 12 недель) в группе бионаивных пациентов, 36,3 и 35,3% в группе пациентов с неэффективностью/непереносимостью иФНО-α [12].
Следовательно, выбор препарата устекинумаб представляется наиболее предпочтительным в данной клинической ситуации.
Заключение
Таким образом, приведенное клиническое наблюдение демонстрирует возникновение и течение болезни Крона с поражением толстой и тонкой кишки у пациента молодого возраста. Необходимо помнить, что специфического маркера ВЗК не существует – диагноз устанавливается на основании анализа совокупности данных (клинических, эндоскопических, рентгенологических и морфологических). При выборе терапии важно оценить наличие у пациента факторов неблагоприятного прогноза заболевания. Своевременный выбор биологического препарата с быстрым механизмом действия, низкой иммуногенностью, высоким профилем безопасности, долгосрочной эффективностью способствует снижению риска развития осложнений, прогрессирования заболевания, а также обеспечению благоприятного прогноза.
E.V. Sosnovskaya, PhD, B.R. Saytadzhiev, T.L. Mogil'nickaya, D.A. Marchenko, E.D. Khadieva, PhD, L.F. Nekrasova
District Clinical Hospital, Khanty-Mansiysk Autonomous Okrug – Yugra, Khanty-Mansiysk
Khanty-Mansiysk State Medical Academy
Contact person: Evgenia V. Sosnovskaya, evg-sosnovskaya@yandex.ru
A clinical case of observation of a young patient with Crohn's disease is presented. The article reflects the features of the clinical course of the disease, the formulation of a clinical diagnosis, the tactics of conservative treatment and the choice of a biological preparation.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.