Железодефицитные состояния в практике врача: новости и междисциплинарный подход. XXII Всероссийский научно-образовательный форум «Мать и дитя – 2021». Сателлитный симпозиум компании «Эгис»
- Аннотация
- Статья
- Ссылки




Латентный дефицит железа
Симпозиум открыл профессор, д.м.н., академик РАН, заведующий кафедрой внутренних болезней № 1 лечебного факультета Московского государственного медико-стоматологического университета им. А.И. Евдокимова, президент Российского научного медицинского общества терапевтов, заслуженный деятель науки РФ, заслуженный врач РФ Анатолий Иванович МАРТЫНОВ. Он поделился с акушерами-гинекологами опытом диагностики и лечения латентного дефицита железа.
Роль железа в организме не ограничивается транспортировкой кислорода к тканям. Железо участвует в реализации метаболических процессов. В организме человека железо является составной частью многих ферментов и белков, необходимых для обменных процессов – холестеринового обмена, превращения калорий в энергию, разрушения и утилизации токсинов. Железо также помогает иммунной системе справляться с агрессорами, в частности вирусной инфекцией.
В среднем женщина должна ежедневно получать с пищей не менее 2–3 мг элементарного железа. Во время беременности и лактации потребность возрастает до 6 мг. Суточная доза железа для мужчин – 1–2 мг, детей – не менее 1 мг. Потребность в данном микроэлементе увеличивается с возрастом.
Много железа содержится в красном мясе, субпродуктах, особенно печени, устрицах, яйце, орехах, бобовых, яблоках, гранате, изюме, инжире. Чтобы поступающее в организм железо усваивалось, необходимо дополнять пищевой рацион продуктами, содержащими витамины C и В12. Для лучшего усвоения железа употребление чая, кофе и газированных напитков лучше ограничить, а алкоголь исключить совсем. Продукты, богатые кальцием, снижают всасывание железа.
В клинической практике анемия встречается у 25% пациентов, причем у 80% – так называемая железодефицитная анемия (ЖДА)1.
С дефицитом железа связывают слабость, головную боль, головокружение, сонливость, неспособность сосредоточить внимание, сложности с выполнением физических нагрузок, тахикардию (учащенное сердцебиение), сухость во рту, боль в языке, атрофию вкусовых сосочков, истончение волос, алопецию, раннее выпадение волос, синеватый оттенок белков глаз, ощущение дискомфорта в ногах в состоянии покоя. Нередко наблюдается извращение вкусовых пристрастий (желание есть глину, землю, лед, крахмал и бумагу). Кроме того, на фоне железодефицитных состояний обостряются ишемическая болезнь сердца, сердечная недостаточность и деменция.
Отсутствие своевременной профилактики ЖДА у беременных приводит к рождению маловесных детей. Установлено, что на фоне профилактики препаратами железа во время беременности масса тела детей при рождении составляет в среднем 3,5 кг, в отсутствие профилактики – около 3 кг. К основным причинам дефицита железа у женщин относятся тяжелые менструальные кровотечения, беременность и роды, травмы, гематемезис, мелена, кровохарканье и гематурия.
Для диагностики дефицита железа и ЖДА проводят клинический анализ крови с лейкоцитарной формулой для определения уровня гемоглобина и биохимический анализ крови для оценки уровня сывороточного железа и ферритина. Анемия диагностируется при уровне гемоглобина менее 120 г/л. Для постановки диагноза ЖДА имеет значение и уровень насыщения трансферрина железом. Показатель насыщения трансферрина железом менее 20% и содержание сывороточного железа менее 30 мкг/л свидетельствуют о наличии ЖДА. При этом сывороточный ферритин – наиболее точный тест для выявления дефицита железа в отсутствие воспалительных процессов2.
В настоящее время проблема недостаточной диагностики дефицита железа и ЖДА у женского населения сохраняется. Так, в Москве частота ЖДА и дефицита железа среди гинекологических больных составляет 38%, в Московской области – 27,8–48,3%.
Дефицит железа и ЖДА приводят к увеличению материнской и младенческой смертности, росту инфекционной заболеваемости, снижению качества жизни, работоспособности и производительности труда, репродуктивной функции. По разным данным, распространенность дефицита железа среди женского населения в мире достигает 70–100% в зависимости от региона3.
Выделяют три стадии железодефицитных состояний: предлатентный дефицит, латентный дефицит и ЖДА. Своевременное выявление латентного (скрытого) дефицита железа имеет большое значение. На этом этапе нередко сохраняется нормальный или слегка сниженный уровень гемоглобина, симптомы дефицита железа выражены незначительно. Определение уровня сывороточного ферритина позволяет обнаружить латентный дефицит железа и провести профилактику дальнейшего развития ЖДА.
Как показали результаты наблюдательного исследования (2020) с участием 4451 пациента старше 50 лет, общая распространенность латентного дефицита железа – 8,8%, среди женщин – 10,9%, среди мужчин – 6,3%. У пациентов с латентным дефицитом железа по сравнению с пациентами с нормальным уровнем ферритина в течение 14 лет наблюдения отмечалось увеличение летальности на 58%. Таким образом, наличие в течение длительного периода латентного дефицита железа ассоциируется с повышенным риском смерти4.
На экспертном совете «Актуальные вопросы диагностики и лечения дефицита железа в клинической практике» в июне 2020 г. гематологи, терапевты, акушеры-гинекологи, клинические фармакологи подвели итоги изучения проблемы латентного дефицита железа в России в рамках проекта SUPER IRON. По данным экспертов, латентный дефицит железа имеет место у 20–30% людей, риск развития анемии – у 50–86% женщин5.
При нелеченом железодефиците существует три сценария развития событий:
- пройдет самостоятельно – 13,4% случаев;
- останется на том же уровне – 60% случаев;
- манифестирует, перейдет в явную анемию – 26,6% случаев.
При этом в биохимическом анализе крови отмечаются гипоферритинемия, уменьшение концентрации сывороточного железа и увеличение общей железосвязывающей способности сыворотки из-за повышенного содержания трансферрина.
Дефицит железа у женщин рассматривается как негативный фактор наступления беременности, в том числе при экстракорпоральном оплодотворении. Дефицит железа отягощает течение беременности: не исключены преэклампсия, плацентарная недостаточность, слабость родовой деятельности, преждевременные роды, кровотечения. Увеличивается риск неблагоприятных исходов для плода, таких как задержка внутриутробного развития и развития плода, низкая масса тела новорожденного. Кроме того, дефицит железа провоцирует гипогалактию и сокращает период грудного вскармливания с риском развития анемии у ребенка, а также приводит к нарушению его умственного и психического развития. На фоне железодефицитного состояния возрастают частота гнойно-септических осложнений в послеродовом периоде, риск развития психоэмоциональных нарушений во время и после беременности, снижаются показатели сексуальной функции и удовлетворенности.
Симптомы латентного дефицита железа во многом совпадают с показателями и клиническими проявлениями ЖДА. Наиболее характерными симптомами латентного дефицита железа являются быстрая утомляемость, слабость, сонливость, раздражительность, сухость кожных покровов, заеды, выпадение волос и мелькание «мушек» перед глазами.
К лабораторным признакам латентного дефицита железа относят снижение уровня ферритина менее 30 мкг/л, нормальный уровень железа в крови или незначительное его снижение, нормальный уровень гемоглобина. Для дифференциальной диагностики дефицита железа определяют также MCH – среднее содержание гемоглобина в эритроците и MCV – средний объем эритроцита. При латентном дефиците железа эти показатели снижены.
По мнению экспертов, исследования на ферритин должны быть включены в программу государственных гарантий у пациентов групп риска развития дефицита железа. Определение уровня ферритина упростит алгоритм диагностики латентного дефицита в реальной врачебной практике6.
У пациентов с ЖДА широко используются внутривенные препараты железа: декстраны железа, глюконат железа, сахарат железа, карбоксимальтозат железа.
К преимуществам внутривенных препаратов относят быстрый ответ, быстрое и эффективное пополнение запасов железа, хорошую переносимость, высокую приверженность терапии. Между тем есть и недостатки: эффект и нежелательные явления зависят от формулы используемого препарата, возможны реакция гиперчувствительности и окислительный стресс. Кроме того, лечение внутривенными препаратами железа весьма дорогостоящее.
Таблетированные препараты двух- и трехвалентного железа для постоянного длительного лечения имеют ряд преимуществ. В частности, пероральный препарат двухвалентного железа пролонгированного действия Сорбифер Дурулес, содержащий 100 мг элементарного железа и аскорбиновую кислоту, предназначен для профилактики и лечения ЖДА, включая латентный дефицит железа, состояний, сопровождающихся дефицитом железа, для профилактики дефицита железа при беременности, лактации, у доноров крови.
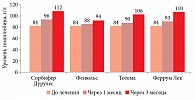
Исследователи сравнивали скорость восстановления уровня гемоглобина на фоне терапии пероральными двух- и трехвалентными препаратами железа. Сорбифер Дурулес продемонстрировал в два раза более высокий суточный прирост гемоглобина по сравнению с препаратами трехвалентного железа (рис. 1)7.
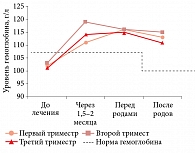
На фоне применения препарата железа Сорбифер Дурулес отмечалось наиболее выраженное восстановление уровня гемоглобина у беременных (рис. 2)8.
При использовании препарата железа Сорбифер Дурулес по одной таблетке два раза в сутки до завершения лактации отмечались полная клиническая и гематологическая ремиссия, восстановление уровня гемоглобина у многорожавших женщин с гестозом и ЖДА. Уровень гемоглобина увеличился в среднем на 23,7%. Коэффициент насыщения трансферрина железом в исследуемой группе был в два раза выше, чем в контрольной группе. У трех (83,6%) из четырех беременных наблюдалась полная клиническая и гематологическая ремиссия на фоне комплексной терапии. Прием препарата Сорбифер Дурулес в третьем триместре позволил снизить частоту нежелательных исходов беременности у многорожавших женщин с ЖДА. Частота оперативного родоразрешения в исследуемой группе снизилась на 14,9%, аномалий родовой деятельности – на 20,8%, развития задержек внутриутробного развития ребенка – на 12,4%9.
В заключение профессор А.И. Мартынов подчеркнул, что своевременное выявление и коррекция ЖДА улучшают показатели здоровья женщин, течения беременности, родов и здоровья ребенка.
Эпидемии XXI в. и железодефицитные состояния: современный взгляд на проблему
Заведующая кафедрой акушерства и гинекологии факультета повышения квалификации врачей Читинской государственной медицинской академии, главный внештатный специалист по акушерству и гинекологии Дальневосточного федерального округа, д.м.н., профессор Татьяна Евгеньевна БЕЛОКРИНИЦКАЯ акцентировала внимание коллег на современных принципах лечения железодефицитных состояний у женщин во время эпидемий инфекционных заболеваний. Она напомнила, что эпидемией считается распространение какой-либо инфекционной болезни, значительно превышающее уровень обычной заболеваемости на данной территории. В свою очередь пандемия – эпидемия, характеризующаяся распространением инфекционного процесса не только в отдельно взятой стране, но и сопредельных государствах, а иногда одновременно во многих странах мира.
Острые респираторные вирусные инфекции – наиболее распространенные заболевания и одна из основных причин госпитализаций. Так, 33% всех госпитализаций беременных связаны именно с респираторными инфекциями. Установлено, что во время ежегодных эпидемических вспышек заболеваемость у беременных в два раза выше, чем у небеременных10, 11.
В XXI в. первым глобальным вызовом для России стала эпидемия гриппа H1N1, или свиного гриппа. В то время система отечественного здравоохранения была не готова к оказанию помощи беременным – отсутствовали эпидемиологические данные об особенностях клинического течения у них данного типа гриппа. В документах Всемирной организации здравоохранения (ВОЗ) и Центра по контролю и профилактике заболеваний США (Centers for Disease Control and Prevention, CDC) отсутствовали алгоритмы ведения беременных на фоне гриппа H1N1 и методы фармакологической профилактики осложнений.
О начале пандемии новой коронавирусной инфекции COVID-19, вызванной коронавирусом-2 острого респираторного синдрома, генеральный секретарь ВОЗ Тедрос Гебрейесус объявил 11 марта 2020 г. Перед системами здравоохранения всего мира были поставлены сложные задачи по оптимизации ресурсов и механизмов для обеспечения помощи населению в период пандемии.
Закономерность, которая наблюдалась во время эпидемии свиного гриппа, присутствует и сегодня: у беременных вирус SARS-CoV-2 выявляется значительно чаще (в 2,7–3 раза), чем в общей популяции.
С появлением новых научных и клинических данных подходы к лечению пациентов с коронавирусной инфекцией меняются. К настоящему времени было подготовлено и выпущено 13 версий временных методических рекомендаций Минздрава России по профилактике, диагностике и лечению коронавирусной инфекции, а также четыре рекомендации по организации оказания медицинской помощи беременным, роженицам и новорожденным. Между тем эффективные средства этиотропной терапии против SARS-CoV-2 отсутствуют. В этом текущая ситуация отличается от эпидемии гриппа A (H1N1). Тогда в арсенале врачей имелись эффективные противовирусные препараты (осельтамивир, занамивир).
Факторами риска тяжелого течения COVID-19 у беременных и женщин в послеродовом периоде считаются возраст старше 35 лет, избыточная масса тела и ожирение, хроническая артериальная гипертензия, сахарный диабет. Тем не менее, как показывает реальный клинический опыт, даже в отсутствие указанных факторов риска коронавирусная инфекция протекает в тяжелой форме. Целью одного исследования стало выявление ко-факторов, установление особенностей клинического течения и исходов COVID-19 у беременных и небеременных раннего репродуктивного возраста в отсутствие известных факторов риска и преморбидного фона. В ходе исследования показана ассоциативная связь инфекции COVID-19 у беременных с наличием ЖДА, вегетососудистой дистонии, принадлежностью к восточноазиатской популяции, курением. При этом ЖДА была наиболее значимым ко-фактором риска заболеваемости и тяжелого течения COVID-19 у беременных12.
В других исследованиях оценивали факторы риска летальности среди беременных и матерей при COVID-19. Установлено, что наиболее значимым фактором риска материнской летальности является ожирение. Ожирение у женщин повышало вероятность летального исхода при COVID-19 в 80,3 раза, хронической артериальной гипертензии – в 12,2, сахарного диабета – в 17,2, болезней органов дыхания – в 11,3, ЖДА – в 4,5 раза.
В целях профилактики железодефицита эксперты ВОЗ и Американской коллегии акушеров-гинекологов (American College of Obstetricians and Gynecologists) и CDC рекомендуют низкодозовые добавки железа всем беременным с первого триместра (уровень доказательности – А). В условиях, когда анемия беременных является серьезной проблемой общественного здравоохранения, ежедневный прием препаратов железа в дозе 60 мг в пересчете на железо предпочтительнее приема в более низкой дозе13.
Дефицит железа неблагоприятно отражается на течении беременности, родов, послеродового периода, состоянии плода и новорожденного. Последствия дефицита железа для беременных хорошо известны – нарушение функции плаценты, преэклампсия, преждевременные роды, риск кровопотери в родах, осложнения в послеродовом периоде. Нельзя забывать и об отдаленных последствиях для детей – замедлении моторного и речевого развития, нарушении координации, снижении иммунитета7.
Анемия – состояние, при котором в крови снижается количество эритроцитов и/или гемоглобина, участвующих в транспорте кислорода от легких к тканям. В результате развивается гипоксия, происходит активация перекисного окисления липидов, запускается системный воспалительный ответ.
Эквивалентом 60 мг элементарного железа, рекомендуемого ВОЗ, является 300 мг сульфата, 180 мг фумарата или 500 мг глюконата железа. Сорбифер Дурулес – комбинированный препарат, в состав которого входят железа сульфат 320 мг и аскорбиновая кислота 60 мг. По мнению экспертов ВОЗ, препарат, который используется для профилактики и лечения дефицита железа, должен содержать аскорбиновую кислоту, увеличивающую всасывание железа на 30%. Максимальной разовой дозой считается 100 мг элементарного железа, при которой всасывается до 14 мг металла. Препараты с замедленным высвобождением позволяют увеличить всасывание и снизить побочные эффекты.
К лекарственным железосодержащим препаратам для беременных предъявляется ряд требований. Приоритет имеют препараты двухвалентного железа – они лучше абсорбируются в кишечнике по сравнению с препаратами трехвалентного железа. Рекомендуется также использовать препараты двухвалентного железа с замедленным высвобождением из-за его более высокой степени абсорбции и переносимости. Суточная (от 100–120 до 300 мг) и курсовая доза (четыре месяца) рассчитывается исходя из степени тяжести анемического синдрома, висцеральных поражений, уровня сывороточного железа.
Сорбифер Дурулес обладает высоким коэффициентом всасывания в желудочно-кишечном тракте и практически не образует малодоступных сложных соединений, содержит аскорбиновую кислоту, улучшающую всасывание и усвоение железа. Препарат характеризуется пролонгированным действием, что сокращает частоту приема, и хорошо переносится пациентами14.
Сорбифер Дурулес восстанавливает нормальный уровень гемоглобина в крови в два раза быстрее, чем препараты трехвалентного железа. Не случайно Сорбифер Дурулес признан препаратом выбора у беременных с ЖДА15.
Продолжительность использования пероральных препаратов железа зависит от тяжести анемии и составляет 1–6 месяцев. Основанием для прекращения терапии служит нормализация не уровня гемоглобина, а содержания железа в депо – ферритин сыворотки16, 17.
В продолжение темы здоровья беременных профессор Т.Е. Белокриницкая остановилась на проблеме высокой распространенности избыточной массы тела и ожирения. Ожирение у беременных ассоциируется с высоким риском экстренного родоразрешения, мертворождения, невынашивания, развитием преэклампсии, раневой инфекции, задержкой роста плода, низкой оценкой новорожденного по шкале Апгар. Это отражено в клинических рекомендациях Российского общества акушеров-гинекологов.
Как уже отмечалось, ожирение – один из факторов риска заболеваемости и тяжести течения COVID-19. Доказано, что отклонение количества жировой ткани от нормы повышает риск инфицирования и осложнений на фоне COVID-1918.
COVID-19 существенно влияет на течение беременности. В метаанализе 42 исследований с участием 438 548 беременных убедительно показано: тяжелое течение COVID-19 сопряжено с преэклампсией, преждевременными родами, гестационным диабетом, рождением детей с низкой массой тела19.
Таким образом, ожирение – фактор риска тяжелого течения и неблагоприятных исходов COVID-19 вследствие хронического воспаления, тромбофилии, распространения вируса из пораженных органов в окружающую их жировую ткань и дальнейшего длительного выделения вируса (отсроченный цитокиновый шторм), а также снижения защитного кардиореспираторного резерва20.
Согласно рекомендациям Международной федерации гинекологов и акушеров (International Federation of Gynaecology and Obstetrics) (2020), беременные с ожирением нуждаются в микронутриентной поддержке. В состав добавок должна входить не только фолиевая кислота, но и витамин D, железо. Сегодня микронутриентная поддержка беременных рассматривается в аспекте снижения риска заражения COVID-19. В целях снижения риска заражения коронавирусной инфекцией беременным рекомендуются разнообразное сбалансированное питание, прием витаминов D, А, B, С, а также препаратов железа. Предотвращение дефицита микронутриентов в различных группах населения, в том числе среди беременных, способно помочь повысить их устойчивость к пандемии COVID-1921.
При наиболее опасных коморбидных заболеваниях (хронические заболевания легких, бронхиальная астма) на фоне COVID-19 витамин A оказывает протективный эффект, поскольку обладает антимикробными, иммуномодулирующими и антиоксидантными свойствами. Он стимулирует выработку антагонистов рецепторов интерлейкинов 1 и 1-бета альвеолярными макрофагами, ограничивает процесс инфильтрации легочной ткани. Витамины группы B блокируют связывание и активность протеазы при инфицировании SARS-CoV-2, ограничивая проникновение вируса в клетки22.
Витамин D усиливает реакции иммунитета, ослабляет интенсивность цитокинового шторма и отсроченно влияет на репликацию вируса, блокируя его. Доказано, что дефицит витамина D связан с высоким риском инфицирования, тяжелого течения и летальности от инфекции COVID-19.
Таким образом, адекватное микронутриентное обеспечение планирующих беременность и беременных в эпидемический период особенно актуально. Во время эпидемии респираторных инфекций, в частности COVID-19, потребность беременной в витаминах и минералах увеличивается до 88%23.
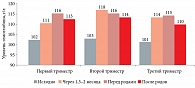
Как отметила профессор Т.Е. Белокриницкая, важным условием ведения беременных является мониторинг уровней ферритина и гемоглобина в динамике. При снижении уровня ферритина на фоне приема витаминно-минерального комплекса беременным дополнительно можно назначать препарат двухвалентного железа Сорбифер Дурулес. При этом ключевое значение для профилактики и лечения железодефицитных состояний у беременных имеет комплаентность, которая во многом зависит от эффективности и переносимости препарата. Данные исследования длительного применения железосодержащего препарата Сорбифер Дурулес во время беременности и в послеродовом периоде свидетельствуют не только о его высокой клинической эффективности, но и хорошей переносимости (рис. 3). Побочные отрицательные эффекты, требующие отмены препарата, отсутствуют. Доказанные эффективность и безопасность препарата Сорбифер Дурулес позволяют рекомендовать его для лечения ЖДА, а также профилактики ее развития24.
Анемия беременных, акушерская патология и перинатальные исходы
По словам заведующего отделом научно-образовательных программ департамента организации научной деятельности Национального медицинского исследовательского центра акушерства, гинекологии и перинатологии им. академика В.И. Кулакова, д.м.н., профессора Игоря Ивановича БАРАНОВА, актуальность вопросов железодефицитных состояний обусловлена их широкой распространенностью. Так, каждая пятая небеременная репродуктивного возраста и третья беременная имеют ЖДА25. Частота предлатентного и латентного дефицита железа в мире достигает 92%. Диагностика ЖДА и латентного дефицита железа остается недостаточной из-за неспецифических проявлений. Кроме того, четкие рекомендации по эффективной маршрутизации пациентов с дефицитом железа отсутствуют.
Высокой распространенности ЖДА в России способствуют низкий социально-экономический статус значительной части населения, связанный с недостаточным потреблением продуктов питания, богатых железом, низкая осведомленность населения о проблеме дефицита железа. Среди причин высокой частоты дефицита железа следует отметить высокое распространение редуцированных диет для контроля массы тела среди женщин фертильного возраста, отсутствие подготовки к беременности с позиций диагностики и устранения дефицита железа, а также низкую приверженность лечению латентного дефицита железа и ЖДА.
В рамках проекта SUPER IRON проведено исследование, целью которого стало изучение проблемы диагностирования и лечения латентного дефицита железа в России. Установлено, что у гинекологов отсутствует прямое распоряжение назначать лечение женщинам с ЖДА, тем более с бессимптомным латентным дефицитом. Пациенток направляют к гематологу, эндокринологу, гастроэнтерологу. Акушер-гинеколог может рекомендовать какой-либо препарат железа, пока пациентки будут самостоятельно искать причину такого состояния. Тем самым и больные, и врачи фактически пропускают состояние латентного дефицита железа.
Возникает закономерный вопрос: кто виноват? Дело в том, что выявление латентного дефицита железа не регламентируется порядками и стандартами оказания медицинской помощи. Важным шагом на пути решения этой проблемы стало внесение в современный алгоритм ведения беременных рекомендаций по исследованию уровня ферритина.
Профессор И.И. Баранов напомнил, что скрытый латентный и предлатентный дефицит железа у беременных формируется в 92% случаев и трудно поддается диагностированию26.
По данным Минздрава России за 2015–2019 гг., в стране частота анемии у женщин, завершивших беременность, достигла 30–35%.
Проблема дефицита железа – прежде всего проблема питания. Поэтому первичная профилактика ЖДА заключается в сбалансированном питании в любом возрасте.
Ежедневная потребность в эндогенном железе у взрослого человека составляет около 1–2 мг, ребенка – 0,5–1,2 мг. Обычная диета обеспечивает поступление от 5 до 15 мг элементарного железа в день. Важно помнить, что в двенадцатиперстной кишке и верхнем отделе тощей кишки всасывается не более 15% железа, содержащегося в пище.
Без сомнения, в развитии и распространении анемии не последнюю роль играют социальные и климатические условия, пищевые традиции. Основным источником железа служат продукты животного происхождения, содержащие гемовое железо. К сожалению, во многих продуктах, которые жители разных стран употребляют ежедневно, содержание железа низкое. Речь, в частности, идет о фастфуде, диетических продуктах. К слову сказать, негемовое железо, содержащееся в растительной пище, характеризуется сниженной биодоступностью.
Наиболее частые проявления железодефицита у женщин – общая слабость, упадок сил, эмоциональная лабильность, предрасположенность к стрессу и инфекциям, снижение умственной деятельности и производительности труда. С дефицитом железа у беременной могут быть связаны преэклампсия, плацентарная недостаточность, преждевременные роды, гипогалактия в послеродовом периоде. У ребенка отдаленные последствия железодефицита во время беременности проявляются нарушением моторики, когнитивной и психической функции, поведенческого развития.
С увеличением срока гестации возрастает потребность в витаминах и микроэлементах. Увеличение потребления железа в первом триместре беременности составляет 16%, во втором – 59%, в третьем – 67%.
У плода запасы железа создаются матерью: во время беременности она передает будущему ребенку около 300 мг железа. Наиболее активно процесс передачи происходит на 30-й неделе беременности и возрастает одновременно с увеличением массы плода – около 22 мг железа в неделю. Часть железа накапливается в запасах плаценты в виде плацентарного ферритина и при снижении запасов железа у матери начинает высвобождаться, обеспечивая растущие потребности плода в железе. Суммарная потеря железа, связанная с нормально протекающей беременностью, родами и лактацией, составляет около 1400 мг27.
Тяжелая анемия, манифестировавшая в первом триместре беременности, достоверно повышает риск преждевременных родов, преэклампсии, задержки роста плода, в послеродовом периоде – гипогалактии. На фоне развития дальнейшего железодефицитного состояния повышается вероятность материнской и младенческой летальности.
Плод получает железо от матери за счет активного транспорта через плаценту. У новорожденных, чьи матери страдали ЖДА, уровень ферритина, транспортного железа и коэффициент насыщения трансферрина железом значительно снижены. Корреляционная взаимосвязь между феррокинетическими параметрами у плода и концентрацией гемоглобина и сывороточного ферритина у матери указывает на то, что плод извлекает необходимое ему железо в количестве, пропорциональном его содержанию у матери. При дефиците железа у матери в неонатальном периоде у плода чаще диагностируются внутриутробная гипоксия и гипотрофия, нередко выявляются асфиксия и признаки внутриутробного инфицирования. У младенцев, родившихся от матерей с ЖДА, в период новорожденности наблюдаются значительная потеря массы тела и более медленное ее восстановление. Имеются данные о снижении уровня психомоторного развития у детей с ЖДА первых лет жизни. При этом нормализация уровня железа у таких детей приводит к положительному эффекту.
Целями лечения ЖДА являются устранение причины, лежащей в основе развития заболевания (коррекция питания, выявление и устранение источника постоянного кровотечения), и возмещение дефицита железа в организме. Важно помнить, что ЖДА невозможно вылечить с помощью какой-либо диеты.
Основные принципы лечения ЖДА сводятся к следующему:
- обязательное применение лекарственных железосодержащих препаратов, поскольку возместить дефицит железа другими способами невозможно;
- использование преимущественно препаратов железа для перорального приема;
- назначение препаратов железа в адекватных дозах, которые рассчитывают для каждого конкретного больного с учетом его массы тела и плана лечения;
- достаточная длительность курса лечения пероральными препаратами железа, составляющая при анемии легкой степени три месяца, средней степени – 4,5 месяца, тяжелой анемии – шесть месяцев;
- контроль эффективности терапии препаратами железа28.
Профессор И.И. Баранов рассказал о норвежском опыте профилактического применения препаратов железа при беременности. В Норвегии при первой явке беременной до 12 недель беременности определяют концентрацию сывороточного ферритина. При показателях уровня ферритина более 60 мкг/л нет необходимости в назначении препаратов железа. При уровне сывороточного ферритина 20–60 мкг/л назначение препаратов железа показано с 20-й недели беременности, менее 20 мкг/л – с 12–14-й недели, а при показателях менее 15 мкг/л рекомендовано незамедлительное начало лечения29.
Выбору препарата для коррекции железодефицитных состояний придается особое значение, поскольку лечение может быть длительным. При этом важна не только эффективность, но и отсутствие побочных эффектов.
Сегодня в многочисленных исследованиях доказаны преимущества препаратов двухвалентного железа перед препаратами трехвалентного железа в отношении биодоступности. Препараты двухвалентного железа, назначаемые в целях профилактики и лечения железодефицитных состояний, обеспечивают более быстрое наступление эффекта в плане сохранения целевого уровня или повышения уровня гемоглобина и нормализации гемодинамических показателей в периферической крови.
Так, применение препарата двухвалентного железа Сорбифер Дурулес для профилактики ЖДА у беременных способствует сохранению целевых показателей гемоглобина даже после родов (рис. 4)24.
Дурулес – это технология, которая обеспечивает постепенное высвобождение активного компонента в матрицы таблеток и равномерное поступление лекарственного препарата в кровь. В результате предотвращается развитие высоких концентраций железа и соответственно побочных эффектов.
На основании полученных данных можно сделать вывод, что препарат с замедленным высвобождением железа Сорбифер Дурулес характеризуется выраженной терапевтической эффективностью, хорошей переносимостью и обеспечивает высокую комплаентность.
Подводя итог, профессор И.И. Баранов подчеркнул, что российские эксперты продолжают работу над клиническими рекомендациями «Анемия, осложняющая беременность, деторождение и послеродовый период», которые позволят систематизировать подходы к профилактике и лечению железодефицитных состояний у женщин. На сегодняшний день важнейшей задачей врачей акушеров-гинекологов является своевременная профилактика, диагностика и лечение дефицита железа, в том числе латентного, у женщин репродуктивного возраста.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.