Злокачественные новообразования в практике детского гинеколога
- Аннотация
- Статья
- Ссылки
- English
Материал и методы. Поиск необходимой литературы осуществлялся в базах данных PubMed, Embase, Cochrane Library и Google Scholar. Основное внимание уделялось научным публикациям о распространенности злокачественных новообразований (ЗНО) в детской и подростковой популяции, разновидностях ЗНО, их клинических и лабораторных проявлениях, основных методах диагностики.
Результаты. В частности, выявлено 13 клинических случаев, 15 обзоров, четыре серии клинических случаев, одно популяционное ретроспективное когортное исследование. В 2022 г. было зарегистрировано 1 473 427 случаев ЗНО женской репродуктивной системы, 680 372 из них с летальным исходом. Гинекологические ЗНО составляют 4,2% всех ЗНО у девочек в возрасте от 0 до 18 лет.
Материал и методы. Поиск необходимой литературы осуществлялся в базах данных PubMed, Embase, Cochrane Library и Google Scholar. Основное внимание уделялось научным публикациям о распространенности злокачественных новообразований (ЗНО) в детской и подростковой популяции, разновидностях ЗНО, их клинических и лабораторных проявлениях, основных методах диагностики.
Результаты. В частности, выявлено 13 клинических случаев, 15 обзоров, четыре серии клинических случаев, одно популяционное ретроспективное когортное исследование. В 2022 г. было зарегистрировано 1 473 427 случаев ЗНО женской репродуктивной системы, 680 372 из них с летальным исходом. Гинекологические ЗНО составляют 4,2% всех ЗНО у девочек в возрасте от 0 до 18 лет.
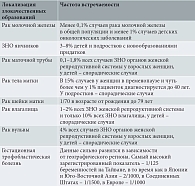
![Таблица 2. Рак яичников, маточных труб и первичный рак брюшины (классификация FIGO, 2021) [15]](/upload/resize_cache/iblock/f88/0b2nbq9im1x4pymp2fde3f8171o1xoeu/195_350_1/Karachentsova2.jpg)
![Таблица 3. Рак эндометрия (классификация FIGO, 2023) [27]](/upload/resize_cache/iblock/53b/z2ssth5ml5v0c9fx3hwqv4ezlrtoyfrt/195_350_1/Karachentsova3.jpg)
![Таблица 4. Рак шейки матки (классификация FIGO, 2018) [29]](/upload/resize_cache/iblock/3c8/ptyc0ghivccay6q7uq2aqxq0429ooj7u/195_350_1/Karachentsova4.jpg)
![Таблица 5. Классификация BI-RADS (Breast Imaging-Reporting and Data System) [10]](/upload/resize_cache/iblock/121/72pqy7uerth6kx4tky9as7npmt6fu3sl/195_350_1/Karachentsova5.jpg)
Введение
По данным Всемирной организации здравоохранения на 2021 г., примерно 400 000 детей и подростков в возрасте от 0 до 19 лет заболевают раком ежегодно. Несмотря на то что гинекологические злокачественные новообразования (ЗНО) у детей и подростков встречаются редко, на их долю приходится 4,2% всех ЗНО у девочек в возрасте от 0 до 18 лет. Примерно 1% всех случаев рака яичников и влагалища в общей популяции приходится на указанную возрастную группу [1].
У детей и подростков отмечаются в основном стромальные карциномы, включая ювенильные гранулезоклеточные опухоли и опухоли из клеток Сертоли – Лейдига, рабдомиосаркомы и герминогенные опухоли яичников (табл. 1).
Материал и методы
Поиск соответствующей литературы осуществлялся в базах данных PubMed, Embase, Cochrane Library и Google Scholar. В данный обзор включены исследования за период 1986–2024 гг.
Результаты
Выявлено 13 клинических случаев, 15 обзоров, четыре серии клинических случаев, одно популяционное ретроспективное когортное исследование, одно многоцентровое ретроспективное исследование, одно экспериментальное доклиническое исследование, одно обсервационное и одно проспективное когортное исследование.
Рак молочной железы
Рак молочной железы (РМЖ) считается наиболее распространенной формой ЗНО и одной из ведущих причин смерти от онкологических заболеваний в мире. Частота встречаемости РМЖ среди детей и подростков составляет менее 0,1% случаев РМЖ в общей популяции и менее 1% случаев детских онкологических заболеваний [2].
Около 5–10% случаев РМЖ, диагностированных в мире, являются наследственными и приводят к генетической мутации, а ранний возраст постановки диагноза РМЖ обычно предполагает синдром наследственной предрасположенности к раку. Для РМЖ в аспекте мутаций важны гены BRCA1, BRCA2 и TP53, которые ассоциируются с более чем десятикратным увеличением относительного риска развития РМЖ [3].
Гены BRCA1 и BRCA2 принадлежат к группе ATM-опосредованных (аtaxia telangiectasia mutated, мутантный при атаксии-телеангиэктазии белок) генов репарации дезоксирибонуклеиновой кислоты (ДНК), которые играют ключевую роль в обеспечении целостности хромосом. Это гены-онкосупрессоры, вовлеченные в процесс гомологичной репарации двунитевых разрывов ДНК. Нарушение и утрата нормальной функции генов BRCA1 и BRCA2 приводят к ошибкам репарации повреждений ДНК. Это вызывает активацию генов контроля и регуляции клеточного цикла, осуществляющих ингибирование дальнейшего роста клеток с возникшими мутациями и индуцирующих апоптоз – запрограммированную клеточную гибель [4]. Накопление ошибок репарации разрывов ДНК влечет за собой нарушение регуляции клеточного цикла, апоптоза, дифференцировки клетки и, как следствие, нестабильность генома. Данное событие является ключевым в процессе канцерогенеза [5].
Наиболее часто встречающимся типом РМЖ у детей является секреторная карцинома (ювенильный рак) молочной железы, получившая свое название на основании гистологической картины: обильная секреция сульфатированных мукополисахаридов и муцина внутри- и внеклеточно наряду с зернистой эозинофильной цитоплазмой. При объективном обследовании секреторная карцинома представляет собой медленно растущее, безболезненное уплотнение в молочной железе. Выделения из сосков и их втягивание наблюдаются относительно редко [2].
Кроме того, в литературе описаны случаи протоковой карциномы in situ, инвазивной протоковой, инвазивной тубулярной и папиллярной внутрикистозной карцином [2].
Особого внимания заслуживает случай трижды негативного РМЖ у восьмилетней пациентки, описанный в Китае в 2023 г. [6].
Трижды негативный РМЖ – тип опухоли молочной железы с неблагоприятным прогнозом, поскольку в ней отсутствуют или экспрессируются низкие уровни рецепторов эстрогена, прогестерона и эпидермального фактора роста человека 2 (HER-2) [6].
У девочки под соском правой молочной железы было обнаружено образование плотной консистенции около 1,5 см в диаметре с четкими границами и хорошей подвижностью. Пациентке выполнили две операции: удаление образования и эксцизионную биопсию передних грудных лимфатических узлов с помощью эндоскопа. Позже провели флуоресцентную гибридизацию in situ (FISH) для гена ETV6, которая выявила слияние генов ETV6-NTRK3. После выписки девочка находилась под наблюдением специалиста в течение года с хорошим прогнозом [6].
Согласно данным современной литературы, ультразвуковое исследование (УЗИ) – основной метод изучения уплотнений молочной железы у детей и подростков благодаря доступности и диагностической специфичности. Образования визуализируются в виде округлых или овальных включений с четкими или частично микродольчатыми краями, гипоэхогенными по отношению к жировой ткани с неоднородной структурой [2].
В ряде исследований последних лет показано, что система BI-RADS (Breast Imaging-Reporting and Data System, визуализация молочных желез – система отчетности и базы данных) успешно применяется для дифференциальной диагностики злокачественных и доброкачественных образований молочной железы [7, 8]. Тем не менее вопрос об уровне ее точности остается спорным. Для четкой верификации необходимы дополнительные результаты (биопсия) [9, 10].
Помимо УЗИ используется магнитно-резонансная томография (МРТ) для визуализации более глубоколежащих структур, сосудов и лимфатических узлов, тонкоигольная аспирация (fine needle aspiration, FNA), эксцизионная биопсия [2]. Маммография не является методом выбора, поскольку ее точность снижается из-за высокой плотности железистой ткани молочной железы подростка и воздействия ионизирующего излучения [11, 12].
Таким образом, РМЖ крайне редко встречается у детей и требует скрупулезного диагностического поиска как со стороны педиатра, так и со стороны детского гинеколога. Требуется дальнейшее проведение исследовательских работ и применение геномного профилирования с целью определения уникального молекулярного профиля опухоли [2, 6].
Злокачественные новообразования яичников
Большинство новообразований яичников, обнаруживаемых у детей и взрослых, доброкачественные. При этом ЗНО яичников отмечаются у 3–8% детей и подростков с новообразованиями придатков и составляют 1–2% всех случаев рака у детей [13].
Новообразования яичников подразделяют на эпителиальные и неэпителиальные.
Эпителиальные опухоли – наиболее распространенный подтип новообразований яичников, составляющий примерно 90% ЗНО. Такие опухоли встречаются у взрослых пациенток. В возрастной категории младше 20 лет они регистрируются с частотой менее одного случая на 100 тыс. пациенток в год [5]. Эпителиальные опухоли возникают в основном после менархе, поскольку их развитие может быть спровоцировано гормональной стимуляцией [13].
Неэпителиальные опухоли – редкий подтип новообразований, составляющий ~10% ЗНО яичников и включающий в основном герминогенные и стромальные опухоли полового тяжа. В молодом возрасте чаще возникают неэпителиальные опухоли яичников. При этом некоторые новообразования встречаются преимущественно у подростков [14].
Существует классификация FIGO, на основании которой стадию онкологического процесса определяют по анатомической распространенности (табл. 2) [15].
Дисгерминома – опухоль, развивающаяся из половых клеток, не подвергшихся дифференцировке, относится к герминогенным опухолям. Является наиболее распространенной злокачественной опухолью яичников и наиболее распространенным ЗНО яичников у детей в целом. Большинство случаев (82%) приходится на возрастную категорию 10–29 лет, а меньшинство (6%) – на детей младше десяти лет [16]. Дисгерминома – наиболее распространенное ЗНО половых желез у людей с дисгенезией половых желез, развивающееся на фоне гонадобластомы. Прослеживается связь между дисгерминомой и хромосомными аномалиями, такими как синдром Шерешевского – Тернера [13].
Незрелая тератома яичника представляет собой редкий тип герминогенной опухоли, которая может возникать либо в чистом виде, либо в сочетании с другими компонентами герминогенной опухоли. Они составляют менее 1% всех случаев рака яичников. Как правило, незрелые тератомы яичников поражают девушек до 20 лет с пиком заболеваемости в возрасте от 16 до 20 лет, а специфические факторы риска включают задержку полового созревания, первичную аменорею, а также расовую и этническую принадлежность [14].
Опухоли стромы полового тяжа возникают из клеток полового тяжа (клеток Сертоли, гранулезных клеток) и стромальных клеток (тека-клеток, фибробластов и клеток Лейдига) и составляют 10–20% всех новообразований яичников у детей. Наиболее распространенными опухолями этой группы считаются ювенильная гранулезоклеточная опухоль и опухоль Сертоли – Лейдига [13].
Наиболее важной целью диагностики новообразований яичников является оценка вероятности ЗНО, поскольку лечение доброкачественных и злокачественных опухолей различается. Диагностика включает в себя стандартные методы визуализации, такие как УЗИ и МРТ малого таза. Важную роль в определении злокачественности образования играет определение опухолевых маркеров: альфа-фетопротеина (характерен для незрелой тератомы, опухоли желточного мешка, эмбриональной карциномы, иногда опухоли из клеток Сертоли – Лейдига), лактатдегидрогеназы (при дисгерминоме), бета-субъединицы хорионического гонадотропина человека (дисгерминома, эмбриональная карцинома, негестационная хориокарцинома), СА-125 (злокачественные эпителиальные опухоли) и ингибина (ювенильная гранулезоклеточная опухоль). Данные о наличии онкомаркеров особенно ценны, когда анализируются в совокупности с клинической картиной и данными методов визуализации [13].
Рак маточных труб
Поражение маточных труб можно разделить на три категории:
- интраэпителиальная карцинома (карцинома in situ). Предположительно первично возникает в маточной трубе и представляет собой внутрипросветное образование;
- распространенная серозная карцинома, ассоциированная с интраэпителиальной карциномой. Это опухоль, облитерирующая как маточную трубу, так и яичник. Вопрос о том, можно ли в таких случаях предположить первичное происхождение из тканей фаллопиевых труб, остается спорным;
- интраэпителиальная карцинома, обнаруженная в ходе гистологического исследования после совершения снижающей риск сальпингоофорэктомии (risk-reducing salpingo-oophorectomy – tubal intraepithelial carcinoma). В этом случае следует начать соответствующее лечение [17].
Первичная карцинома маточных труб встречается с частотой 0,1–1,8% всех случаев ЗНО органов женской репродуктивной системы у взрослых женщин. У детей и подростков данный вид рака встречается крайне редко. В 1986 г. V. Gatto, M.A. Selim, M. Lankerani наблюдали первичную карциному фаллопиевых труб у 19-летней девушки. В своей работе они упомянули, что в литературе описано менее 1000 случаев данного заболевания, причем у подростков только три: два в 1932 г. и одно в 1966 г. Исследователи описали четвертый случай. Пациентка, 19 лет, без беременностей и родов в анамнезе, жалобы на периодические боли в правом подреберье в течение четырех лет. При УЗИ органов малого таза в апреле 1983 г. обнаружено образование размером 4 × 3 × 3 см, которое приняли за перекрут кисты правого яичника. Проведена диагностическая лапароскопия, в ходе которой обнаружено образование в области фимбриального отдела маточной трубы. Выполнена частичная сальпингэктомия справа. Патологоанатомическое заключение: папиллярная цистаденокарцинома в стенке правой маточной трубы. В феврале 1984 г. были проведены дилатация и кюретаж полости матки, диагностическая лапаротомия, интраоперационное цитологическое исследование лаважа брюшной полости, биопсия парааортальных лимфатических узлов, биопсия брюшины малого таза, аппендэктомия и оментэктомия. На основании этих данных поставлен диагноз: серозная цистаденокарцинома маточной трубы стадии IA (по FIGO). Дальнейшее лечение не проводилось. Во время обследования в январе 1985 г. отклонений не выявлено [18].
Таким образом, первичная карцинома маточных труб у детей и молодых девушек – крайне редкое заболевание. Существует риск несвоевременной диагностики ввиду бессимптомного течения либо неспецифической клинической картины: кровотечение, боль внизу живота, выделения из влагалища и объемное образование в области малого таза, которое можно обнаружить при физикальном или инструментальном обследовании [18].
Рак тела матки
ЗНО матки у детей встречаются редко по сравнению с популяцией женщин старше 18 лет, где они представляют собой одни из наиболее распространенных злокачественных опухолей женской репродуктивной системы. Рак эндометрия обычно возникает у 15% женщин в пременопаузе и чуть более чем у 1% пациенток в возрасте до 40 лет. У подростков зарегистрировано лишь несколько случаев развития рака эндометрия [19]. Встречаются случаи аденокарцином [20–22], сарком [23, 24].
В последние годы, согласно статистике, заболеваемость эндометриоидной аденокарциномой (ЭАК) в возрасте до 40 лет возросла с 5 до 10% [25]. Известными факторами риска развития гиперплазии или рака эндометрия являются метаболический синдром, отсутствие родов в анамнезе, артериальная гипертензия и сахарный диабет. Все вышеперечисленное является фактором риска развития синдрома поликистозных яичников (СПКЯ). В подростковом возрасте ЭАК также коррелирует с наличием у пациенток СПКЯ, и клиническая картина схожа с таковой у женщин пожилого возраста: ЭАК дебютирует в виде аномальных маточных кровотечений, которые не удается купировать эстрогенами и прогестинами [20, 21]. Сообщается о случае ЭАК у пациентки с синдромом Коудена – редким аутосомно-доминантным заболеванием, поражающим примерно одного из каждых 200 тыс. человек. При наличии данного заболевания наблюдается мутация зародышевой линии в гомологе фосфатазы и тензина (PTEN), который кодирует супрессор опухолей, антагонизирующий путь фосфатидилинозитол-3-киназы (PI3K/AKT) и митоген-активируемой протеинкиназы. Синдром Коудена ассоциирован с развитием гамартом, а также с повышенным пожизненным риском развития карцином молочной железы (25–50%), щитовидной железы (10%), почек (13–34%), колоректального рака (16%) и рака эндометрия (13–19%) [22].
Саркомы матки составляют около 3–9% ЗНО матки. Они классифицируются по гистологическому типу и типу составляющих их клеток: лейомиосаркома (около 40%), карциносаркома (40%) и стромальная саркома эндометрия (15%). Остальные 5% случаев составляют гетерогенную группу сосудистых и лимфатических сарком [1, 19].
Описан чрезвычайно редкий случай опухоли желточного мешка матки у девочки двух лет, поступившей в стационар пекинской больницы с жалобами на влагалищное кровотечение и объемное образование в области малого таза. Диагноз был подтвержден с помощью биопсии. После шести циклов химиотерапии в сочетании с цисплатином, этопозидом и блеомицином (два из них проведены постоперационно) и лапароскопической гистерэктомии пациентка была выписана из стационара. В течение 18 месяцев наблюдения рецидива заболевания не отмечалось [26].
Классификация рака эндометрия (рака тела матки) по FIGO [27] представлена в табл. 3.
Рак шейки матки
В мире рак шейки матки (РШМ) является четвертым по частоте онкологическим заболеванием у женщин [28].
Гистологически двумя наиболее частыми подтипами РШМ являются плоскоклеточный рак (75%) и аденокарцинома (20–25%). Светлоклеточная карцинома шейки матки считается чрезвычайно редким и высокоинвазивным вариантом аденокарциномы и составляет всего 4% всех аденокарцином шейки матки [28].
Шейка матки была первым органом, для которого Международная федерация гинекологии и акушерства (FIGO) в 1958 г. разработала систему клинического стадирования рака. Впоследствии была введена классификация TNM (tumor, nodes, metastasis – опухоль, узлы, метастазы) для описания анатомического распространения опухолевого процесса. В 2018 г. Комитет онкогинекологии FIGO пересмотрел классификацию: теперь она включает в себя данные клинической картины, результаты рентгенологических и гистологических исследований (табл. 4) [29].
Существуют и другие классификации РШМ, одна из них – ВПЧ-ассоциированные и ВПЧ-неассоциированные типы. Последние чаще встречаются в подростковом возрасте. Среди них выделяют саркомы (в детском возрасте обычно встречается ботриоидная рабдомиосаркома), аденокарциномы [30, 31].
Рабдомиосаркома (РМС) – злокачественная опухоль, развивающаяся из эмбриональных мезенхимальных клеток, которые потенциально способны дифференцироваться в клетки поперечно-полосатой мышечной ткани. РМС часто встречается у детей и подростков. В настоящее время РМС подразделяют на четыре гистологических подтипа: эмбриональные, альвеолярные, веретеноклеточные, или склерозирующие, и плеоморфные. Из этих подтипов эмбриональная РМС – одна из самых редких форм [30].
Ботриоидная РМС является подтипом эмбриональных РМС, который развивается из мускулатуры внутренних органов, покрытых слизистой оболочкой, и имеет гроздевидно-полипозное строение. 30% РМС возникают в мочеполовых путях, главным образом во влагалище, менее 0,5% – в шейке матки. Лечение РМС шейки матки варьируется от радикального хирургического до более щадящего консервативного подхода, включающего химио- и лучевую терапии [30, 31].
Светлоклеточная аденокарцинома шейки матки составляет всего 4% всех случаев аденокарциномы, около 2/3 связаны с внутриматочным воздействием диэтилстильбестрола (DES) [1, 28]. Этот вывод впервые был сделан в исследовании 1971 г., когда была установлена связь между терапией DES у матери во время беременности и светлоклеточным раком влагалища и шейки матки у дочерей (восемь случаев). Многие современные исследования подтверждают эту теорию: DES характеризуется эстрогенной и антиандрогенной активностью и препятствует развитию мюллеровых протоков на четвертой-пятой неделе гестации, из которых позже развиваются в том числе шейка матки и верхние 2/3 влагалища. Наиболее серьезным побочным эффектом приема DES во время беременности является светлоклеточная карцинома шейки матки у девочек в будущем [28].
Рак влагалища
ЗНО влагалища в детском возрасте носят спорадический характер. В этой категории наиболее распространены РМС, опухоли желточного мешка, ВПЧ-ассоциированные ЗНО [1, 19, 32].
РМС женской репродуктивной системы у детей составляет всего 3,5% случаев, из которых около половины – РМС влагалища [32]. Чаще встречается в возрастной группе 0–9 лет. Пациентки жалуются на выделения с неприятным запахом, ощущение инородного тела во влагалище. Гистопатологически новообразование состоит из плеоморфных клеток с умеренным количеством эозинофильной цитоплазмы, везикулярным ядром (повышенный уровень гормональной и белковой активности, что может свидетельствовать о нахождении клеток в состоянии активного злокачественного роста) с выступающими ядрышками и обширными участками некроза. По данным иммуногистохимии, опухолевые клетки дают положительную реакцию на десмин и миогенин [32].
Опухоли желточного мешка (ОЖМ) влагалища встречаются у детей до трех лет, по строению сходны с яичниковыми ОЖМ. Они характеризуются кровотечением и наличием полиповидного образования, выступающего из влагалища [33, 34].
При микроскопическом исследовании патогномоничным признаком ОЖМ являются тельца Шиллера – Дюваля – центральный сосуд, окруженный атипичными крупными плеоморфными клетками внутри кистозных пространств (миксоидная строма). Иммуногистохимические исследования показывают очагово-положительную реакцию на альфа-фетопротеин (АФП), более диффузно-положительную – на плацентарную щелочную фосфатазу (PLAP) и цитокератин (AE1/AE3) и отрицательную – на маркеры скелетных мышц (десмин, мио-D1 и миогенин), гладкомышечный актин и CD30 [34].
Описано около 100 случаев опухолей энтодермального синуса (endodermal sinus tumor, EST), происходящих из влагалища. Данный вид ЗНО относится к злокачественным герминогенным, на долю которых приходится 3% всех злокачественных опухолей детского возраста. EST – одна из злокачественных опухолей половых клеток, которая обычно возникает в яичниках молодых пациенток. Первичная EST во влагалище встречается крайне редко. EST обычно возникают у детей в возрасте до трех лет, проявляются вагинальным кровотечением [35].
Рак вульвы
Рак вульвы в детском возрасте встречается крайне редко, что затрудняет получение информации о его клинико-патологическом профиле. A.L. Strickland и O.A. Fadare в обзоре англоязычной литературы за период 1970–2020 гг. приводят следующие данные: зарегистрировано менее 100 ЗНО вульвы у пациенток в возрасте 0–25 лет, примерно 50% из них – РСМ, 10% – инвазивные плоскоклеточные карциномы, 10% – опухоли желточного мешка, 10% – саркома Юинга/примитивные нейроэктодермальные опухоли и 10% – меланома [36].
Гестационные трофобластические неоплазии
Гестационная трофобластическая болезнь (ГТБ) определяет спектр пролиферативных нарушений трофобласта. Гистологически ГТБ подразделяют на доброкачественные формы – полные и частичные пузырные заносы – и злокачественные формы, которые также называют гестационными трофобластическими неоплазиями (гестационная хориокарцинома, трофобластическая опухоль плацентарного ложа, эпителиоидная трофобластическая опухоль и инвазивный пузырный занос) [37].
В исследовании E.M.H. Uberti и соавт. среди 583 беременных девочек-подростков у 124 (21,3%) была диагностирована ГТБ. Пациентки с данным диагнозом проходят курс профилактической химиотерапии под контролем уровня хорионического гонадотропина человека и вакуумную аспирацию полости матки. Когда диагностируется эта патология беременности, молодые пациентки нуждаются в ранней клинической и психологической помощи, чтобы после лечебных мероприятий и выздоровления они могли вернуться к обычной жизни и планировать беременность в будущем. В настоящее время существует консенсус относительно того, что наблюдение за пациентками с ГТБ должно проводиться в специализированных центрах [38].
Передача рака плоду и новорожденному в перинатальном периоде
Онкологические заболевания во время беременности встречаются примерно один раз на 1000 беременностей. Передача рака от матери ребенку происходит у одного младенца на 500 тыс. матерей, больных раком. Описано несколько механизмов передачи раковых клеток плоду и новорожденному [39].
Гестационная хориокарцинома – ЗНО, происходящее из трофобласта, имеет предполагаемую частоту 1 на 50 тыс. беременностей. Хориокарцинома новорожденных считается чрезвычайно редким ЗНО у детей, возникающим в результате передачи гестационной хориокарциномы из плаценты или организма матери плоду через пуповину. Зарегистрировано всего около 40 случаев, включая мертворождения. Генетический анализ данного заболевания проводится редко. Тем не менее предполагается, что многие случаи хориокарциномы новорожденных развиваются во время беременности у женщины с онкологическим заболеванием. Клетки хориокарциномы в плаценте переходят к плоду через пуповину. В этом состоянии клетки хориокарциномы, происходящие из трофобластов эмбрионального происхождения, генетически идентичны клеткам плода [39].
Описано два случая, когда рак шейки матки роженицы передался плоду и перерос в рак легких. Предполагается, что в момент прохождения плодом родовых путей кровь и амниотическая жидкость, содержащие клетки РШМ матери, могут остаться на коже ребенка. В момент первого вдоха вместе с воздухом в дыхательные пути попадают амниотическая жидкость или кровь. Таким образом, раковые клетки матери передаются новорожденному через дыхательные пути. Материнское происхождение опухолей легких у детей подтверждено при использовании методов секвенирования нового поколения и полимеразной цепной реакции (ПЦР) с использованием набора праймеров к ВПЧ. Показано, что опухоли как у ребенка, так и у матери положительны на один и тот же тип ВПЧ [40].
Обсуждение
Использование системы O-RADS (Ovarian-Adnexal Reporting and Data System), разработанной Американским колледжем радиологии, – неотъемлемое требование эхографической оценки состояния яичников и корректного заключения [41, 42].
При УЗИ органов малого таза предпочтительно использовать трансвагинальный доступ, а при больших размерах опухоли еще и трансабдоминальный. У девочек, не ведущих половую жизнь, используется трансабдоминальный доступ, но при диагностической необходимости возможно проведение трансректального УЗИ.
Классификация O-RADS включает шесть категорий, которые отражают риск злокачественности выявленных новообразований в области придатков матки [41]:
- O-RADS 0 – устанавливается при неполноценной оценке в связи с техническими причинами затрудненной визуализации;
- O-RADS 1 – соответствует фолликулу и желтому телу размером ≤ 3 см;
- O-RADS 2 – с очень высокой вероятностью доброкачественное образование (риск злокачественности новообразования 1%). В эту группу включены функциональные кисты яичников размерами от 3 см, опухоли кистозного строения с гладкими стенками и образования, соответствующие классическим критериям доброкачественного характера, если максимальный размер вышеперечисленных менее 10 см;
- O-RADS 3 – образование, имеющее низкий риск злокачественности (от 1 до < 10%). Начиная с этого уровня в систему стратификации риска добавляется оценка цветовой шкалы в допплеровском режиме УЗИ. Данная группа включает в себя патологию яичника из группы O-RADS 2 размерами ≥ 10 см; однокамерные опухоли кистозного строения с неровной внутренней стенкой (толщиной до 3 мм) любого размера; многокамерные образования кистозного строения с гладкими внутренними стенками размером < 10 см, без твердого компонента, с оценкой в допплеровском режиме менее 4 (от слабого до умеренного кровотока); солидное образование или опухоль с плотным содержимым (≥ 80%) любого размера с гладким контуром внутренней бессосудистой стенки. Присутствие допплеровского кровотока оценивается как диагностический признак твердой ткани, но его отсутствие менее информативно. В этом варианте поражение следует рассматривать как твердое по классификации IOTA. Контрольное значение размера 10 см принято на основании опыта диагностики ЗНО с использованием данных IOTA 1–3;
- O-RADS 4 – промежуточная группа поражений со средним риском злокачественности (от 10 до 50%): многокамерные образования кистозного строения с гладкими внутренними стенками, размером ≥ 10 см, без твердого компонента, с оценкой в допплеровском режиме ≤ 3 или 4 с любым размером образования; с неровными внутренними стенками и/или нестабильной перегородкой, любого размера, с любой оценкой цветовой гаммы; с твердым/плотным компонентом, любого размера, с допплеровской оценкой 1–2 (нет – слабый поток). Кроме того, к этой категории относят однокамерные новообразования кистозного строения: с наличием 1–3 папиллярных выступов или твердого/плотного компонента, любого размера, любой выраженности кровотока, а также солидное образование (плотность ≥ 80%) с гладкой поверхностью, любого размера, цветовой оценкой ≤ 3 (от легкой до умеренной). Следует отметить, что под сосочковым выступом подразумевается твердый компонент высотой ≥ 3 мм, который берет начало из стенки или перегородки образования и выступает в его полость;
- O-RADS 5 – категория поражений с высоким риском злокачественности (≥ 50%), определяется критериями, которые достоверно предсказывают ЗНО, такие как однокамерные образования кистозного строения с ≥ 4 папиллярными выступами, любого размера, с любой выраженностью кровотока; многокамерные образования с твердым компонентом, любого размера, с умеренным или сильным кровотоком; солидные образования (плотность ≥ 80%) любого размера, с гладким или неровным контуром стенки, очень выраженным кровотоком в ней. На оценку O-RADS 5 также будет указывать наличие асцита и/или перитонеальных узелков.
Согласно исследованию, проведенному Американским колледжем радиологии, O-RADS имеет высокую диагностическую эффективность у детей с опухолями яичников. Высокая чувствительность и отрицательная прогностическая ценность могут помочь избежать несвоевременного установления диагноза ЗНО яичников у детей. Четкая и доступная для понимания классификация демонстрирует высокую согласованность между УЗИ-специалистами с разным уровнем опыта. Таким образом, необходимы проспективные многоцентровые исследования, чтобы получить более надежные доказательства диагностической эффективности O-RADS для детей [42].
Применение маммографии в педиатрии ограничено из-за того, что у пациенток либо недостаточно ткани молочной железы для проведения надлежащей компрессии, либо у них имеется плотная фиброгландулярная ткань, которая может маскировать идентификационные данные выявления отклонений от нормы. В связи с этим основным методом визуализации, используемым для оценки состояния молочных желез у детей и подростков, является УЗИ молочных желез [43].
В многоцентровом ретроспективном исследовании J. Davis и соавт. пришли к выводу, что существующая система классификации BI-RADS переоценивает риск развития рака у пациенток в возрасте от 0 до 21 года. Не рекомендовано определение типа новообразований среди детей и подростков, поскольку данная классификация новообразований молочной железы создавалась согласно данным УЗИ женщин в репродуктивном периоде и не была предназначена для использования среди пациенток в возрасте 0–18 лет и пожилых женщин. Таким образом, необходимы дальнейшие исследования с перспективой создания ультразвуковой классификации новообразований молочных желез среди детей и подростков [43, 44].
Вывод
Девочки с ЗНО органов репродуктивной системы представляют особую группу пациенток, требующих индивидуального междисциплинарного подхода. Решение о ведении таких пациенток должно приниматься консилиумом врачей разных специальностей. Поскольку, по данным исследований, показатели общей выживаемости высоки, предпочтение следует отдавать методам лечения, сохраняющим фертильность.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Финансирование. Работа выполнена без спонсорской поддержки.
Е.V. Sibirskaya, PhD, Prof., I.V. Karachentsova, PhD, P.O. Nikiforova, A.A. Kovaleva
Russian Children’s Clinical Hospital – a Branch of N.I. Pirogov Russian National Research Medical University
N.I. Pirogov Russian National Research Medical University
Russian University of Medicine
Contact person: Polina O. Nikiforova, pol_nikiforova@mail.ru
The aim is to systematize and summarize current data on malignant neoplasms of the reproductive system in girls and adolescents. The oncological alertness of a pediatric gynecologist can improve the diagnosis, routing, and treatment of patients in this age group.
Material and methods. The necessary literature was searched in the databases PubMed, Embase, Cochrane Library and Google Scholar. The main attention was paid to scientific publications concerning the prevalence, variety, basic diagnostic methods, clinical and laboratory manifestations of malignant neoplasms in children and adolescents.
Results. 13 clinical cases, 15 reviews, four series of clinical cases, and one population-based retrospective cohort study were identified. In 2022, 1,473,427 cases of malignant neoplasms of the female reproductive system were registered, 680,372 of them with fatal outcome. Gynecological malignancies account for 4.2% of all malignancies in girls aged 0 to 18 years.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.