Значение нейропатии в диагностике и лечении эректильной дисфункции
- Аннотация
- Статья
- Ссылки



В структуре половых нарушений на долю сахарного диабета приходится более 40% случаев (4), т.е. практически каждый второй больной, страдающий нарушением половой функции, – пациент с сахарным диабетом. Эректильная дисфункция (ЭД) – типичное осложнение сахарного диабета, которое наряду с другими более хорошо изученными осложнениями (диабетическая микро- и макроангиопатия, диабетическая полинейропатия, диабетическая ретинопатия и др.) приводит к значительному ухудшению качества жизни пациента.
Даже сама мысль о возможности развития нарушения половой функции у любого мужчины негативно воздействует на психическое состояние, может стать причиной депрессии, которая, в свою очередь, может вести к развитию ЭД. Понятно, что для активного выявления ЭД необходимо как понимание данной проблемы, так и знание способов ее решения. Не только уролог, андролог, сексопатолог, диабетолог и эндокринолог, но и врач общей практики должен понимать биологические и психологические основы сексуальности, уметь собирать сексуальный анамнез. Врач, избегающий этих крайне важных для больного вопросов, фактически признает, что сексуальные проблемы больного его не интересуют (2).
Эректильная дисфункция: определение, классификация нейрогенной ЭД
Эректильная дисфункция – неспособность достигать и (или) поддерживать эрекцию достаточную для проведения полового акта в половине и большем числе случаев (1).
При постановке диагноза эректильной дисфункции необходимо определить причину нарушений, только на основании знания которой возможно провести дифференциальную диагностику разных форм ЭД и подобрать соответствующее патогенетическое лечение. Различать ее формы очень важно, поскольку они отличаются не только подходами к лечению, но и прогнозом в отношении восстановления половой функции. Классификация различных форм эректильной дисфункции представлена в таблице 1.
Предположить психогенный характер эректильной дисфункции следует у пациентов резко возникшей ЭД на фоне отсутствия соматической патологии. Любая сексуальная неудача может сопровождаться страхом ожидания неудачи. Результатом этого является частая концентрация внимания на эрекции и как следствие – уменьшение психогенного компонента ее возникновения.
Длительное течение ЭД нередко приводит к тому, что половая жизнь отходит на второй план, возникает, так называемый, «синдром дезактуализации», при котором происходит уменьшение влияния психогенного компонента на течение эректильной функции.
Органический характер эректильной дисфункции следует предположить у пациентов с наличием тех или иных соматических заболеваний (артериальная гипертония, ожирение, гипогонадизм и т.д.).
В таблице 2 представлены признаки, помогающие в проведении дифференциальной диагностики между психогенной и органической формами эректильной дисфункции.
Выявление у пациента определенных факторов риска, ведущих к возникновению органической эректильной дисфункции, также помогает в проведении дифференциальной диагностики.
К выявлению нарушений половой функции стоит относится очень внимательно, поскольку нередко именно нарушение со стороны половой функции, особенно у пациентов с сахарным диабетом, являются первым признаком возникновения нейропатии. На ранних стадиях нейропатии единственной жалобой может являться ощущение холода в области головки полового члена, что мы называем синдромом холодной головки полового члена.
Помочь в постановке диагноза органической ЭД, обусловленной нейропатией, может проведение достаточно простого теста – определение температурной чувствительности полового члена (метод Калинченко-Роживанова).
Определение нейропатии полового члена проводится с помощью прибора Тиотерм (рисунок 1), у которого имеются два разных конца – металлический (холодный) и пластмассовый (теплый). Пациенты с нейропатией не ощущают разницы между холодным и теплым концом прибора
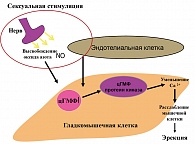
Нейротрансмиттеры, которые опосредуют эректильный ответ, еще недостаточно изучены, но, по крайней мере, включают ацетилхолин и другие не-адренергические, не-холинергические (NANC) мессенжеры. Конечным нейротрансмиттером является активный вазодилятатор – оксид азота, NO (6), который проникает внутрь гладкомышечных клеток кавернозных тел, т.е. действует внутриклеточно, вызывая повышение уровня циклического гуанозин-моно-фосфата (цГМФ). ЦГМФ запускает сложную цепочку реакций (рисунок 2), которая, что в конечном итоге ведет к расслаблению гладкомышечных клеток и возникновению эректильного ответа. ЦГМФ в дальнейшем расщепляется в кавернозных телах под действием фермента фосфодиэстеразы V типа, которая является специфичной для кавернозных тел, и таким образом происходит спад эрекции – детумисценция.
Основным источником секреции оксида азота – основного нейромедиатора эрекции являются кавернозные нервы, поэтому нейропатия играет важную, если не доминирующую роль в развитии ЭД, поскольку при нормальном состоянии сосудов и нормальном эндокринном статусе, при наличии нейропатии возникновение нормальной эрекции невозможно.
Определение чувствительности полового члена (метод Калинченко-Роживанова) не вошло в рутинную практику обследования даже пациентов с сахарным диабетом и ЭД, хотя известно что нейропатия является у пациентов с сахарным диабетом как 1, так и 2 типа, – основным патогенетическим фактором в развитии и поддержании ЭД, а также фактором, снижающим эффективность как ингибиторов ФДЭ-5 типа, так и других методов терапии.
Следует отметить, что сахарный диабет является не единственной причиной развития нейрогенной эректильной дисфункции. Когда определение чувствительности полового члена вошло в нашу рутинную практику мы стали выявлять достаточную распространенность нейрогенной ЭД и у мужчин без сахарного диабета.
Мы предлагаем следующую рабочую классификацию нейрогенной ЭД:
- диабетическая нейрогенная ЭД;
- травматическая нейрогенная ЭД (нередко наблюдается после операций на органах малого таза и половом члене);
- токсическая нейрогенная ЭД (развивается на фоне алкогольной зависимости, длительного приема лекарственных препаратов);
- возрастная нейрогенная ЭД (возникает на фоне снижения секреции тестостерона).
В настоящее время наиболее изучена диабетическая нейропатия, и дискуссии о патогенезе диабетической нейропатии касаются в основном взаимного влияния и взаимодействия метаболических и васкулогенных факторов. Наиболее популярной метаболической гипотезой является возможность полиолового обмена, в основе которой лежит тот факт, что неиспользованная глюкоза при СД метаболизируется по полиоловому пути и под воздействием ферментов альдозоредуктазы и сорбитолдегидрогеназы превращается в сорбитол и фруктозу. Накопление в нервных клетках этих продуктов обмена, как известно, ведет к развитию нейропатии, поскольку сорбитол и фруктоза – продукты ферментативного гликозилирования глюкозы, – плохо проникают через клеточные мембраны, что приводит к осмотическому дисбалансу и отеку.
Выраженность нейропатии коррелирует со степенью компенсации сахарного диабета. Гипергликемия – важный фактор прогрессирования нейропатии, поскольку поступление глюкозы в нейроны, шванновские клетки и их отростки не зависит от инсулина. Клинически это положение подтверждается данными о снижении на 40-60% прогрессирования нейропатии при оптимальном контроле содержания глюкозы в крови у пациентов. Выявляемые объективными морфологическими методами изменения нейронов, редукция числа аксонов, демиелинизация, дегенерация волокон, реиннервация за счет спраутинга (ветвление аксона и дендритов нейрона), обусловлены изменениями метаболизма нервных клеток и их отростков.
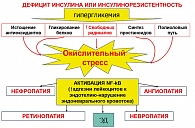
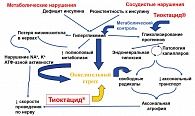
Комплекс других звеньев, сопровождающихся повреждением нервных волокон и снижением скорости нервного проведения, включает нарушение соотношения лактат/пируват, т.е. формирование псевдоишемии при активации полиолового пути метаболизма избытка глюкозы. При этом истощается содержание НАДФ, что ведет к снижению синтеза основного нейромодулятора и вазодилататора – NO, так как NO-синтетаза и альдозоредуктаза используют НАДФ в качестве субстрата. Усиление же оксидации глюкозы ведет к образованию активных кислородных радикалов и к оксидативному стрессу, что влечет прямое повреждение особо чувствительных мембран нервных клеток и их отростков. Патогенез окислительного стресса представлен на рисунке 3. Истощение миоинозитола, нарушение активности протеинкиназы С, уменьшение активности Na+, K+-ATФазы нервных волокон также являются прямым следствием избытка глюкозы.
Окислительный стресс наблюдается не только при сахарном диабете, окислительный стресс является одной из основных причин старения, кроме того, на фоне приема лекарственных препаратов или несбалансированного питания также отмечается усиление окислительного стресса. Поэтому, скорее всего, патогенез нейропатии при сахарном диабете, возрастной нейропатии и токсической нейропатии схож, в связи с чем и подходы к лечению нейропатии должны быть такие же как подходы к лечению диабетической нейропатии.
Лечение нейрогенной эректильной дисфункции
В настоящее время выбор средств для лечения эректильной дисфункции достаточно велик, что позволяет практически каждому пациенту с нарушением эрекции подобрать эффективное лечение, начиная от медикаментозных и заканчивая, в случае их неэффективности, хирургическими методами лечения. Таким образом, следует помнить о том, что неизлечимых форм эректильной дисфункции на сегодняшний день нет. Тем не менее количество пациентов резистентных к классической терапии, которой сегодня по праву является применение ингибиторов ФДЭ 5 типа, достаточно велико. Значительный вклад в резистентность к терапии ингибиторами ФДЭ 5 типа вносит гиподиагностика нейрогенной ЭД.
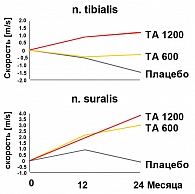
В последние годы в качестве патогенетической терапии диабетической нейропатии используется альфа-липоевая (тиоктовая) кислота (Тиоктацид), обладающая выраженным антиоксидантным действием. Кроме того, что крайне важно при эректильной дисфункции, прием тиоктацида ведет к усилению проведения возбуждения по нерву (рисунок 4).
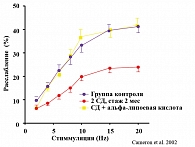
Патогенетическое действие Тиоктацида при эректильной дисфункции было наглядно показано в работе N.E. Camеron (2002), который индуцировал диабет у крыс и показал, что назначение альфа-липоевой кислоты восстанавливает вызванное нейропатией нарушение расслабления гладких мышц кавернозной ткани до показателей, наблюдаемых в группе контроля (рисунок 5).
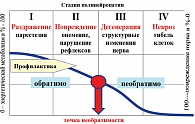
Важно отметить, что чем раньше начато лечение препаратом, тем большего эффекта мы ожидаем, поскольку процент обратимых изменений уменьшается с длительностью нейрогенной ЭД. Установлено, что альфа-липоевая кислота (Тиоктацид) является физиологическим антиоксидантом, оказывающим воздействие на избыточное образование свободных радикалов, происходящее вследствие окислительного стресса (рисунок 6).
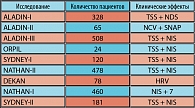
Высокая эффективность и патогенетическое действие Тиоктацида доказано многочисленными экспериментальными и клиническими исследованиями (ALADIN, DECAN, ORPIL, SYDNEY). По мнению М.И. Балаболкина, при участии альфа-липоевой кислоты также происходит регенерация и восстановление других важнейших антиоксидантов в организме (цикл витаминов Е и С). Кроме того, Тиоктацид оказывает выраженное нейропротективное, эндопротективное, а также гепатопротективное действие, способствуя уменьшению выраженности жирового гепатоза, обладает липотропным действием.
В исследовании ALADIN (таблица 3) было показано, что парентеральное введение Тиоктацида в дозе 600 мг в течение трех недель уменьшает симптомы диабетической полинейропатии, поэтому при тяжелых формах нейрогенной ЭД мы рекомендуем начинать терапию парентально (10-15 капельниц) с последующим приемом 600 мг препарата в виде таблеток 1 раз в день за 30-40 мин. до еды в течение 3 месяцев (7).
В России имеется несколько препаратов альфа-липоевой кислоты, но только Тиоктацид показал свою эффективность в двойных слепых плацебо-контролируемых исследованиях, что подтверждается в мета-анализе. Тиоктацид – один из самых изученных антиоксидантов для лечения полиневропатий.
Важно, что альфа-липоевая кислота – является действующим веществом с критической биодоступностью. В отдельных случаях это приводит к тому, что при пероральной терапии альфа-липоевой кислотой терапевтически эффективный уровень не достигается, и отклик пациента на лечение отсутствует. Около 20-30% пациентов не отвечают на пероральное лечение обычной формулой альфа-липоевой кислоты.
Компания «МЕДА» создала особую формулу, Тиоктацид БВ (быстрое высвобождение), с высокой биодоступностью альфа-липоевой кислоты, которая обеспечивает высокий уровень всасывания препарата и особую концентрацию действующего вещества в плазме крови, что ведет к усилению терапевтического эффекта. Таким образом, Тиоктацид БВ – единственная лекарственная форма АЛК, у которой отсутствуют выраженные колебания концентрации в плазме крови.
Вышеуказанные данные, к сожалению, не могут быть экстраполированы на другие (дженерические) аналоги тиоктовой кислоты так, как их эффективность не была подтверждена двойными слепыми рандомизированными плацебо-контролируемыми исследованиями по стандартам GCP.
И главное – дженерики тиоктовой кислоты до сих пор создаются с применением старых технологий, не предусматривающих БВ-форм таблетированных препаратов.
Таким образом, сегодня – альфа-липоевая кислота является единственным патогенетическим средством в лечении нейрогенной ЭД.
Механизм действия Тиоктацида обеспечивает:
- увеличение эндоневрального кровотока,
- уменьшение эндоневрального окислительного стресса за счет восстановления эндоневральной антиоксидантной системы;
- увеличение эндоневрального поглощения глюкозы, что ведет к увеличению запаса энергии в нерве;
- повышение исходно пониженного уровня миоинозитола в диабетическом нерве;
- нейротрофическую поддержку;
- улучшение эндотелиальной дисфункции.
Накопленный нами значительный опыт применения Тиоктацида у пациентов с нейрогенной ЭД на фоне сахарного диабета наглядно демонстрирует значительно большую эффективность препарата в отношении улучшения эрекции у пациентов, которые принимают Тиоктацид в постоянном режиме, без перерывов (рисунок 7). Это и понятно, окислительный стресс – основная причина развития нейрогенной ЭД у больных с сахарным диабетом присутствует всегда, поскольку нет пациентов с сахарным диабетом, имеющих постоянную нормогликемию.
В связи с этим мы считаем, что необходимо изменение подходов к назначению Тиоктацида у пациентов не только сахарным диабетом, но и с возрастной нейропатией, и токсической (до тех пор, пока имеет место воздействие токсического фактора).
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.