Зофеноприл в лечении ишемической болезни сердца
- Аннотация
- Статья
- Ссылки
История исследования ренин-ангиотензиновой системы насчитывает 110 лет. В 1898 г. опубликованы наблюдения Tigerstedt и Bergman, которые обнаружили выделение некоего прессорного вещества почками. Это вещество впоследствии оказалось ренином. Первый пероральный иАПФ – каптоприл – появился на рынке в 1984 г. Сначала он использовался как гипотензивный препарат, однако затем была показана активность в отношении сердечной недостаточности и инфаркта миокарда, реноваскулярной гипертензии, диабетической нефропатии. Есть основания предполагать, что применение этих лекарств может задерживать развитие атеросклероза.
Сегодня использование иАПФ для лечения многих форм ИБС является стандартом. Значительное количество лекарственных препаратов из этой группы порой затрудняет выбор конкретного препарата. Иногда звучат предложения ограничить число лекарств каждого класса, запретив вывод на рынок новых представителей, если для них нет доказательств наличия существенных дополнительных свойств. Цель настоящего обзора – обсуждение преимуществ относительно нового (правда, только для России) лекарства – зофеноприла (Зокардис®, БЕРЛИН-ХЕМИ/МЕНАРИНИ).
Фармакокинетические, фармакодинамические свойства и метаболизм
Наряду с общими свойствами, каждый из представителей класса ингибиторов АПФ имеет некоторые отличия. Особенностями зофеноприла являются высокая липофильность и тканевая активность, двойной путь выведения с преобладанием экскреции с мочой (около 70%) и в меньшей степени – с желчью (20%) и фекалиями (10%) (1-6).
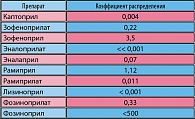
Зофеноприл – это пролекарство, которое быстро всасывается и почти полностью конвертируется в свой активный метаболит, зофеноприлат, путем деэтерификации. Зофеноприл-кальций химически стабилен, представляет собой белый кристаллический порошок с температурой плавления выше 250°C и молекулярным весом 448,59. Растворимость в воде составляет 0,3 мг/мл, pH насыщенного раствора – 6,7. Образование зофеноприлата происходит не только в сыворотке, но и в различных тканях, где пролекарство полностью и быстро расщепляется. Эта особенность отличает зофеноприл от других соединений класса иАПФ (рамиприл, фозиноприл, эналаприл), которые приобретают активность только в сыворотке и почках. С химической точки зрения зофеноприл характеризуется высоким октанол-водным коэффициентом распределения (0,22), что подтверждает его более высокую липофильность по сравнению со многими иАПФ и может способствовать увеличению способности зофеноприла достигать тканевого АПФ. Как видно из таблицы, фозиноприл, зофеноприл и их активные метаболиты высоко липофильны по сравнению с другими иАПФ (1).
In vitro cпособность зофеноприла ингибировать АПФ была впервые показана на легком кролика. При использовании в качестве экспериментальной модели подвздошной кишки морской свинки зофеноприл показал способность ингибировать сократительный ответ на ангиотензин-I при значительно более низком диапазоне концентраций, чем каптоприл, подтвердив 3-8-кратное превосходство зофеноприла в эффективности на эквимолярной основе. Интересно, что ингибирующая АПФ активность зофеноприла была испытана на гомогенатах различных тканей (аорта, мозг, легкие, почки и сыворотка), при этом было показано, что зофеноприл одинаково эффективно ингибирует АПФ в этих органах, демонстрируя в шесть раз более высокую активность, чем каптоприл, и в два раза большую, чем эналаприлат или фозиноприлат (1).
In vivo ингибиторная активность зофеноприла и других иАПФ изучалась на различных животных моделях (крысы, собаки и обезьяны) путем оценки прессорного ответа на ангиотензин-I после перорального приема. Зофеноприл вызывал дозозависимое и высокоспецифичное ингибирование этого ответа, и в 6-10 раз превосходил по эффективности каптоприл (2). Активность зофеноприла в отношении АПФ на тканевом уровне также оценивалась ex vivo на модели с использованием спонтанно гипертензивных крыс (SHR), при этом, несмотря на отсутствие отличий в степени блокирования сывороточного АПФ, некоторые значимые различия были обнаружены в способности различных соединений блокировать АПФ на тканевом уровне (3). В другом исследовании, проводимом на крысах, изучалась способность зофеноприла ингибировать АПФ на тканевом уровне в дозе 10 мг/кг количественной ауторадиографии in vitro с использованием в качестве радиолиганда (125I)351 А, тирозильного деривата зофеноприла (4). Ингибирование АПФ оценивалось в определенных участках сердца и крупных сосудов (аорта, легочная артерия, аортальный клапан и клапан легочной артерии, предсердия и левый желудочек) через 4 и 24 часа после начала лечения. Так же, как и в более ранних исследованиях, зофеноприл вызывал значимое (70-90%) ингибирование АПФ во всех отделах сердца через 4 часа, продолжавшееся и после 24 ч (5).
При исследовании на здоровых людях максимальное ингибирование плазменного АПФ наблюдалось приблизительно через 1-1,5 ч и продолжалось в среднем до 9,5 ч после однократного перорального приема зофеноприла.
У здоровых добровольцев зофеноприл, принятый однократно перорально в дозе 10 мг, в значительной степени и быстро гидролизировался со средним коэффициентом абсорбции 93%. Среднее время его удержания составило 3,3 часа, среднее время абсорбции 1,4 часа и время максимальной концентрации (tmax) – 0,4 часа. После перорального приема зофеноприлата (активного метаболита зофеноприла) почечный клиренс составил 3,1 мл/мин/кг, непочечный клиренс 8,3 мл/мин/кг, объем распределения в устойчивом состоянии (VdSS) – 1,3 л/кг, время полужизни (t½) – 5,5 часов и среднее время удержания 1,9 часа. Абсолютная биодоступность зофеноприлата составляла 78% на основании расчета времени под кривой концентрация–время для показателей крови и 65% при расчете на основании показателей мочевой экскреции (6).
В экспериментальных условиях показаны его антиишемическое, противовоспалительное и антиатерогенное свойства, а также способность инактивировать свободные радикалы, предотвращать эндотелиальную дисфункцию и восстанавливать чувствительность к нитратам. Высказываются предположения, что этими качествами зофеноприл обязан имеющейся в его молекуле дополнительной функциональной SH-группе (1, 7-11).
Особое свойство зофеноприла – антиоксидантная активность
Носительство SH-группы ассоциируется со способностью инактивировать свободные радикалы. Кроме того, эта особенность, возможно, способствует некоторым дополнительным фармакологическим свойствам зофеноприла, которые описаны на экспериментальных моделях, таким как предотвращение эндотелиальной дисфункции, восстановление чувствительности к нитратам, антиишемические, противовоспалительные и антиатерогенные эффекты (1, 7, 8). В работе С. Leva и соавт. (9) было показано улучшение функционального восстановления миокарда после ишемии и реперфузии. Зофеноприл при предварительном пероральном применении продемонстрировал защитное действие на изолированной модели с кардиоплегической остановкой сердца. Имеются экспериментальные данные, что зофеноприл (в отличие от сравнивавшегося с ним в данном исследовании эналаприла) может замедлять экспрессию некоторых молекул адгезии в эндотелиальных клетках и уменьшать образование внутриклеточных свободных радикалов (10).
Роль SH групп в уменьшении степени эндотелиальной дисфункции ингибиторами АПФ изучалась у крыс с сердечной недостаточностью после инфаркта миокарда посредством сравнения вазопротективных эффектов длительного лечения зофеноприлом (содержит SH группу), лизиноприлом (не содержит SH группы) или N-ацетилцистеином (только SH группа). Общая дилатация после рецептор-зависимой стимуляции ацетилхолином (АХ) была ослаблена у нелеченных крыс с инфарктом миокарда (-49%, P<0,05) (n=11) по сравнению с контрольными крысами без инфаркта миокарда (n=8), отчасти из-за нарушенного влияния NO на сосудистую стенку при инфаркте миокарда. Длительное лечение N-ацетилцистеином (n=8) избирательно восстанавливало вклад NO в общую, в том числе АХ дилатацию. Наоборот, оба ингибитора АПФ полностью нормализовывали общую дилатацию в ответ на АХ, включая часть, опосредуемую NO, причем без значимых отличий между зофеноприлом и лизиноприлом. Однако зофеноприл (но не лизиноприл) дополнительно потенцировал действие эндогенного NO после его А23187-индуцированного высвобождения из эндотелия, (+100%), так же, как и эффект экзогенного NO после применения нитроглицерина (+22%) и нитрита натрия (+36%). Эти данные позволяют предположить, что зофеноприл имеет потенциальное превосходство в уменьшении степени эндотелиальной дисфункции путем увеличения активности NO после его высвобождения из эндотелия в стенку сосуда (11).
Зофеноприл при инфаркте миокарда. Группа исследований Smile (Survival оf Myocardial Infarction: Long Term Evaluation)
Первый этап изучения зофеноприла проходил в то время, когда польза от применения ингибиторов АПФ при инфаркте миокарда не была очевидной. Поэтому в качестве средства сравнения использовали плацебо.
Начальный опыт использования зофеноприла при ИБС был получен в пилотном исследовании SMILE. 204 пациента с острым инфарктом миокарда (ОИМ) различной локализации получали зофеноприл 30 мг два раза в день. У больных из группы сравнения применялась традиционная терапия без использования каких-либо других препаратов из группы иАПФ. Больные включались в исследование в течение 24 часов от развития симптомов ОИМ и получали препарат в течение 12 месяцев после рандомизации. Исследование было, главным образом, направлено на изучение безопасности этого препарата при ОИМ. В ходе лечения отмечалась тенденция к снижению смертности у больных, получавших зофеноприл. Кроме того, у них было отмечено уменьшение частоты развития стенокардии, хронической сердечной недостаточности и желудочковых аритмий. Пилотное исследование SMILE не выявило какого-либо взаимодействия между зофеноприлом и внутривенными нитратами по воздействию на уровень систолического и диастолического артериального давления, что позволило сделать вывод об эффективности и безопасности применения зофеноприла при ОИМ (12). Положительные результаты пилотного исследования SMILE побудили предпринять более крупное исследование, с целью оценки влияния зофеноприла на прогноз больных с ОИМ.
В основной фазе исследования SMILE приняли участие 1556 пациентов, проходивших лечение с января 1991 по ноябрь 1992 года. Больные в возрасте от 18 до 80 лет с ОИМ передней локализации, которым не проводилась тромболитическая терапия, были рандомизированы в течение 24 часов от развития симптомов ОИМ для получения зофеноприла (n=772) или плацебо (n=784) в течение 6 недель. Начальная доза зофеноприла составила 7,5 мг, повторно препарат давался через 12 ч, после чего доза удваивалась до тех пор, пока систолическое АД оставалась >100 мм рт. ст. или до достижения суммарной дневной дозы 60 мг. Первичной конечной точкой были комбинированная смертность или тяжелая хроническая сердечная недостаточность (ХСН) в течение периода лечения (6 недель). Они были зафиксированы у 83 пациентов (10,6%) в группе плацебо и 55 пациентов (7,1%) в группе зофеноприла. Общее относительное снижение риска смерти или тяжелой СН составило 34% (95% СI 8-54%; р=0,018). Снижение риска составило 46% для тяжелой СН (95% СI 11-71%; р=0,018) и 25% для смерти (95% СI 11-60%; р=0,19). После 1 года наблюдения смертность оставалась значительно ниже в группе зофеноприла (10,0%), чем в группе плацебо (14,1%); снижение риска составило 29% (95% СI 6-51%; р=0,011). Таким образом, различие между двумя группами по смертности вносило в общий результат меньший вклад, чем различие по частоте развития тяжелой ХСН. Таким образом, лечение зофеноприлом (Зокардис®, БЕРЛИН-ХЕМИ/МЕНАРИНИ) значительно улучшало как краткосрочный, так и долгосрочный прогноз, если начиналось в первые 24 часа от развития симптомов ОИМ и продолжалось в течение 6 недель. Что касается вторичных конечных точек, то в течение 6 недель лечения стенокардия была зарегистрирована у 153 пациентов (19,5%) из группы плацебо и 128 пациентов (16,6%) из группы зофеноприла, снижение риска составило 18% (95% CI 6-37%; р=0,08). Группы не отличались по частоте развития повторных инфарктов миокарда, в то время как встречаемость ХСН была ниже на 29,6% (95% CI 1,1-49,9%) в группе больных, принимавших зофеноприл. Другой вторичной конечной точкой была общая смертность в течение 12 месяцев, которая составила 10,0% и 14,1% в группе плацебо и зофеноприла, соответственно (относительное снижение риска 29,4%; 95% CI 7,2-46,3%). Это различие в общей смертности было обусловлено, главным образом, снижением количества летальных исходов вследствие ХСН (28,5% против 35,1%) и внезапной смерти (12,9% против 22,5%). Анализ кривых выживания Kaplan-Meier показал прогрессивное разделение двух кривых на протяжении периода наблюдения, которые продолжалось и после отмены окончания 6-недельного периода лечения (13).
Эффективность зофеноприла по результатам исследования SMILE оценивалась и в отдельно взятых подгруппах пациентов высокого риска, включавших пожилых пациентов, а также пациентов с гипертензией, сахарным диабетом, перенесенным ранее инфарктом миокарда или имевших стенокардию в анамнезе.
У пожилых больных эффект лечения зофеноприлом на первичные и вторичные конечные точки был сравним с таковым в группе пациентов среднего возраста, кроме того, у пожилых больных не требовалось специальной коррекции дозы зофеноприла (14).
Из 1441 пациента, которые были осведомлены о контроле их артериального давления, 565 (39,2%) имели артериальную гипертензию (АГ) в анамнезе. После 6-недельного периода лечения, относительный риск смерти или тяжелой ХСН был ниже на 40% (RR=0,60; 95% CI 0,45-0,81; 2p<0,05) в группе пациентов с АГ, которые получали зофеноприл, а риск смерти в течение 1 года был ниже на 39% (RR=0,61; 95% CI 0,23-0,89; 2p<0,05). 6-недельная частота ХСН легкой и средней степени тяжести была также значительно снижена в группе зофеноприла группе с АГ (14,1% против 9,4%, соответственно; 2p<0,05). Польза от лечения зофеноприлом значительно увеличивалась у больных с АГ в анамнезе по сравнению с группой пациентов с нормальным АД, вероятно, из-за дополнительного эффекта лучшего контроля артериального давления (14).
В исследовании SMILE также было продемонстрировано, что зофеноприл оказывает благоприятное действие у пациентов с инфарктом миокарда и сахарным диабетом (СД). Из всех наблюдавшихся больных, у 303 (20,0%) был СД и отмечался более высокий уровень сердечно-сосудистых событий во время периода наблюдения. После 6 недель двойного слепого лечения зофеноприл значимо снижал как количество первичных конечных точек (8,6 в группе зофеноприла против 18,3% в группе плацебо; р=0,019), так и частоту встречаемости в течение 6 недель тяжелой ХСН (0%, 0–3,4% в группе зофеноприла против 3,9-12,7% в группе плацебо; р=0,001) у пациентов с СД, при этом его эффективность была выше, чем у пациентов без СД. Лечение зофеноприлом ассоциировалось с тенденцией к незначительному снижению смертности как в группе СД (8,6 против 11,6%), так и без него (6,6 против 5,1%). Наоборот, у больных с СД было отмечено статистически значимое снижение смертности на фоне лечения зофеноприлом, наблюдавшееся в течение первых 24 ч после рандомизации, по сравнению с плацебо (0,7%, 0-3,4% против 6,1%, 3,0-11,2%; р=0,013). Смертность же в течение 1 года была значимо ниже у больных, не имевших СД (9,1% в группе без СД против 13,8% у пациентов с СД; р=0,010), в то время как у больных с СД ее снижение не достигло статистической значимости. Эти данные показывают, что прогноз у пациентов с СД и ИМ может быть значительно улучшен при раннем назначении зофеноприла. Меньшее влияние на смертность в течение 1 года, вероятно, указывает на то, что необходимо длительное лечение для сохранения пользы от раннего ингибирования АПФ у пациентов с СД (13,7 против 16,5%; р=0,52) (15).
Интересно, что клиническая польза от применения зофеноприла (Зокардис®, БЕРЛИН-ХЕМИ/МЕНАРИНИ) значительно увеличивалась у пациентов, имевших в анамнезе стенокардию или ранее перенесших инфаркт миокарда. Положительные эффекты лечения зофеноприлом у таких пациентов, по существу, могут иметь место благодаря взаимодействию между ингибированием АПФ и множеством различных факторов, ответственных за прогрессирование ИБС и атеросклероза (например, контроль артериального давления, благоприятное влияние на ремоделирование левого желудочка, коронарная вазодилатация, ингибирование агрегации тромбоцитов, воздействия на уровни PAI-1, антиадренергические эффекты и т.д.) (14).
Еще один дополнительный анализ популяции SMILE был опубликован в 2006 г. В него вошли больные, которые по современным критериям соответствовали при поступлении определению «инфаркт миокарда без подъема сегмента ST». Следует обратить внимание, что о том, как следует лечить эту группу больных, к настоящему времени не вполне понятно. Все ключевые исследования с ингибиторами АПФ выполнялись до того, как эту группу больных стали специально выделять. Итак, в популяции SMILE из 1556 больных 526 (33,8%) отвечали критериям именно этого определения. При этом 253 больных попали в группу зофеноприла, а 273 – в группу плацебо. Через 6 недель лечения и в этой весьма специфической группе больных зофеноприл достоверно уменьшил частоту встречаемости первичной конечной точки (смерть + застойная сердечная недостаточность), частоту встречаемости выраженной сердечной недостаточности, а через год общая смертность оказалась существенно выше в группе плацебо (р=0,036). Таким образом, лечение зофеноприлом (Зокардис®, БЕРЛИН-ХЕМИ/МЕНАРИНИ) показано больным с инфарктом миокарда без подъема сегмента SТ, так же, как больным крупноочаговым инфарктом с подъемом сегмента ST (16).
В исследование SMILE-2 было включено 1024 пациента с ИМ, которым была проведена тромболитическая терапия в течение 12 часов от появления симптомов инфаркта. Исследование проводилось в нескольких странах, в том числе и в десяти учреждениях России. Больные в возрасте от 18 до 75 лет были рандомизированы для получения зофеноприла (30-60 мг/день) или лизиноприла (5-10 мг/день), при этом терапия обоими препаратами начиналась в течение 12 часов от завершения тромболитической терапии и продолжалась в течение 42 дней. Первичной конечной точкой исследования была частота тяжелой гипотензии (систолическое АД <90 мм рт. ст.) как связанной с применением препарата, так и с другими причинами. Общая частота тяжелой гипотензии была меньше при лечении зофеноприлом (10,9%) по сравнению с лизиноприлом (11,7%; p=0,38). Частота связанной с применением препарата тяжелой гипотензии (первичная конечная точка) была ниже в группе зофеноприла (6,7% против 9,8%; p=0,048) (17).
Согласно данным, полученным в ходе клинических исследований с применением зофеноприла, сообщавшиеся побочные эффекты были класс-специфичными, мягкими и транзиторными, и лишь в редких случаях были достаточно тяжелыми для того, чтобы потребовалась отмена препарата (14).
Среди серьезных побочных эффектов, была зарегистрирована тяжелая почечная недостаточность 1 пациента и сильный кашель у 3 пациентов в группе зофеноприла. Не было отмечено ни одного случая ангионевротического отека, и никаких существенных изменений гематологических или биохимических показателей в обеих группах (13).
Целью исследования SMILE-ISCHEMIA было изучение кардиопротективных эффектов зофеноприла у больных после ОИМ без нарушения систолической функции ЛЖ. 349 больных, перенесших ОИМ и имеющих ФВ ЛЖ >40%, получали зофеноприл в течение 6 месяцев в дозе 30-60 мг (n=177) или плацебо (n=172). Исследование было двойным слепым рандомизированным. Первичной конечной точкой была комбинированная частота значимых изменений ST-T на ЭКГ при холтеровском мониторировании, появления изменений на ЭКГ или симптомов стенокардии во время теста с физической нагрузкой, частота развития повторных ОИМ или потребность в коронарной реваскуляризации. Первичные конечные точки отмечались в у 20,3% больных, получавших зофеноприл, и у 35,9% больных из группы плацебо (р=0,001) несмотря на отсутствие различий в степени контроля АД, ФВ ЛЖ и сопутствующей терапии. Депрессия ST-T во время холтеровского мониторирования ЭКГ отмечалась у 22,7% больных из группы плацебо и 10,7% из группы зофеноприла (р=0,027). Депрессия ST-T во время теста с физической нагрузкой отмечалась у 14,2% и 26,7% больных, получавших зофеноприл или плацебо, соответственно (р=0,024). При этом доля больных, предъявлявших жалобы на боль ангинозного характера, была ниже в группе зофеноприла (4,7% против 14,3%; р=0,017), также у этих больных реже отмечалась значимая депрессия сегмента ST (14,2% против 26,7%; р=0,024) желудочковые нарушения ритма (3,8% против 10,5%; р=0,048). Частота больших сердечно-сосудистых событий была ниже в группе зофеноприла, реже отмечалось развитие и прогрессирование ХСН. Таким образом, результаты исследования SMILE-ISCHEMIA подтвердили кардиопротективную роль зофеноприла (Зокардис®, БЕРЛИН-ХЕМИ/МЕНАРИНИ) у больных нормальной ФВ поле ОИМ (18).
Программа SMILE продолжается, и в исследовании SMILE IV проводится сравнение эффективности зофеноприла (30-60 мг/сут.) в сочетании с ацетилсалициловой кислотой и рамиприла (5-10 мг/сут.) у больных, перенесших ОИМ и имеющих сниженную ФВ ЛЖ. Проводимое в настоящее время исследование ZAAMIS (Zofenopril After Acute Myocardial Infarction Study) спланировано для подтверждения его вазопротективного действия. В этом исследовании больные после первичного чрескожного коронарного вмешательства по поводу впервые развившегося ОИМ передней локализации получают терапию лизиноприлом или зофеноприлом. Первичной целью исследования ZAAMIS является сравнение эффектов зофеноприла и лизиноприла на оксидативный стресс у таких больных. Вторичными целями являются сравнение эффектов раннего (менее 6 ч от развития ОИМ) и позднего (более 24 ч) начала терапии иАПФ от развития ОИМ на нейрогормоны и маркеры оксидативного стресса, а также сравнение влияния зофеноприла и лизиноприла на функцию ЛЖ и ремоделирование в течение 6 недель.
Итак, следует приветствовать появление препарата Зокардис® в нашей стране. Существенным фактом при принятии решения о назначении этого лекарства должно быть то, что часть данных из контролируемых исследований получено на российской популяции и тот факт, что препарат вошел в Российские рекомендации по лечению острого инфаркта миокарда.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.