Золедроновая кислота в лечении остеопороза
- Аннотация
- Статья
- Ссылки
- English

Остеопороз (ОП) считается одним из самых распространенных хронических заболеваний костно-мышечной системы, поражающим как женщин, так и мужчин старшего возраста.
Эпидемиология остеопороза
Эпидемиологические исследования, проведенные в различных странах и регионах, свидетельствуют о высокой заболеваемости ОП. Реальную картину распространенности ОП в популяции удалось установить благодаря внедрению в клиническую практику денситометрии.
Так, в США около 55% лиц старше 50 лет имеют низкие показатели минеральной плотности костной ткани (МПК). При этом согласно прогнозу количество больных ОП к 2020 г. вырастет примерно в 1,5 раза [1], что обусловлено старением населения.
ОП в России выявляется в среднем у 30,5–33,1% женщин и у 22,8–24,1% мужчин старше 50 лет, что составляет более 10 млн человек [2].
Эпидемиология остеопоротических переломов
Низкоэнергетические переломы рассматриваются не только как основное проявление ОП, но и как его осложнение.
Частота переломов в популяции достаточно хорошо изучена. Крупное эпидемиологическое исследование EVOS (European Vertebral Osteoporosis Study) показало, что распространенность вертебральных переломов среди жителей Европы составляет 11,5% у женщин в возрасте 50–54 лет и достигает 34,8% в возрастной категории 75–79 лет [3]. Установлено, что частота вертебральных переломов у мужчин и женщин в возрасте 65–69 лет примерно одинаковая – 12–13%. Однако среди лиц более старшего возраста таковые преобладали у женщин. Этот факт может быть обусловлен более высокой продолжительностью жизни женщин по сравнению с мужчинами.
По данным литературы, около 40% женщин в возрасте старше 50 лет в будущем будут иметь хотя бы один вертебральный перелом [4]. При этом потенциальный риск перелома бедра у женщин старше 50 лет составляет 17,5%, а перелома костей предплечья – 16%. Среди мужчин расчетные показатели составили 6 и 2,5% соответственно.
Анализ эпидемиологических исследований свидетельствует о том, что частота вертебральных переломов зависит не только от пола и возраста, но и этнической принадлежности и места проживания. Так, распространенность позвоночных переломов выше у белых американцев, немцев, шведов. Самая низкая частота переломов отмечена среди финнов и испанцев.
Единственное проспективное популяционное исследование, проведенное в России, показало, что частота новых случаев вертебральных переломов в год составляет 5,9% у мужчин и 9,9% у женщин 50 лет и старше [5].
Факторы риска снижения МПК
Факторы риска снижения МПК представлены в таблице. Именно на основании выявления факторов риска ОП следует направлять пациентов на денситометрию. Необходимо отметить, что МПК в отсутствие низкоэнергетических переломов в анамнезе является лучшим предиктором переломов.
Факторы риска переломов
Низкая МПК не единственный фактор риска переломов. В настоящее время для расчета абсолютного риска переломов во многих странах принята модель FRAX, позволяющая оценить вероятность развития переломов (перелома бедра и всех основных остеопоротических переломов) в течение последующих десяти лет жизни.
Стратегия лечения
Учитывая высокую медико-социальную значимость ОП, несколько десятков лет назад стали разрабатывать лекарственные методы лечения, направленные на укрепление костной ткани и повышение ее качества.
Опыт клинического применения антиостеопоротических лекарственных средств антирезорбтивного (антикатаболического) или анаболического действия позволяет утверждать, что ОП – курабельное заболевание. Это означает, что в подавляющем большинстве случаев на фоне применения антиостеопоротических препаратов наблюдается увеличение МПК. Повышение МПК ассоциируется со снижением риска переломов.
Однако переносить результаты, полученные в ходе клинических исследований, на практику достаточно сложно: снижение риска переломов не всегда приводит к достижению основной цели лечения – отсутствию переломов. Снижение относительного риска остеопоротических переломов не тождественно излечению или выздоровлению.
В то же время благодаря арсеналу доступных методов лечения ОП в большинстве случаев удается достичь значений МПК, соответствующих возрастной норме. Иными словами, Z-критерий, указывающий на разницу между значением МПК у конкретного пациента и возрастным референтным показателем, стремится к нулю (в стандартном отклонении) или к 100%.
Одним из первых методов лечения ОП стала заместительная гормональная терапия (ЗГТ) эстрогенами. Крупномасштабные исследования подтвердили эффективность такого подхода: в первые несколько лет происходило повышение МПК. Получены также данные о снижении относительного риска переломов позвоночника и некоторых периферических переломов, включая перелом бедра [6]. Однако после прекращения терапии эстрогенами МПК вновь снижалась. Кроме того, продолжительность ЗГТ имеет возрастные ограничения.
Необходимо отметить, что эффективность ЗГТ доказать достаточно сложно, поскольку пик остеопоротических переломов приходится на 65–75 лет, когда ЗГТ уже не применяется.
Существуют также опасения в отношении использования эстрогенов из-за повышения риска развития некоторых онкологических заболеваний у женщин (инвазивный рак молочной железы, рак яичников).
Поскольку в ранний период менопаузы значительно ускоряется костная резорбция, осуществлялся поиск лекарственных средств, способных ее затормозить. В конце 1960-х гг. появился первый специфический препарат для лечения остеопороза – кальцитонин лосося. Однако впоследствии выяснилось, что он уступает по эффективности новому классу препаратов – бисфосфонатам.
На фармацевтический рынок для лечения ОП были одновременно выведены два препарата: алендронат и ризедронат. Ранее бисфосфонаты применялись при метастазах в кость и миеломной болезни.
Преимущества бисфосфонатов оказались неоспоримы. Во-первых, клинические исследования подтвердили их высокую эффективность. Результаты многочисленных метаанализов, систематических обзоров, рандомизированных клинических исследований свидетельствовали о том, что длительное применение антиостеопоротических препаратов у пациентов с диагнозом ОП приводит к снижению риска переломов проксимального отдела бедренной кости в среднем на 30–40%, вертебральных переломов – на 40–75%, основных остеопоротических переломов – на 20–30%. Относительный риск переломов снижался достаточно быстро. Уже через год от начала терапии достоверно уменьшался риск компрессионных переломов позвонков. К третьему году непрерывного использования антиостеопоротических препаратов достоверно снижался риск переломов бедра и других невертебральных переломов. Во-вторых, пероральные бисфосфонаты обладали хорошей переносимостью. Частота нежелательных явлений со стороны желудочно-кишечного тракта была низкой. В-третьих, удобство применения (один раз в неделю) способствовало сохранению высокой приверженности пациентов лечению. В-четвертых, стоимость лечения ОП бисфосфонатами оказалась невысокой, особенно в последние два десятилетия, когда на фармацевтическом рынке появились дженерики алендроната и ризедроната.
Продленные клинические исследования по алендронату и ризедронату подтвердили правильность выбора такой тактики лечения. Их основной эффект (снижение риска перелома) сохранялся в течение шести, восьми, десяти лет, что было крайне важно при лечении пациентов с тяжелым ОП, протекавшим с «каскадами» переломов.
Трудности в лечении постменопаузального ОП появились тогда, когда была зафиксирована плохая переносимость пероральных бисфосфонатов. На фоне проводимой терапии на первый план вышли такие нежелательные явления, как эзофагит и гастрит, сопровождающиеся болями в эпигастральной области, изжогой, горечью во рту, эндоскопически проявляющиеся дефектом слизистой оболочки пищевода и желудка. Для их предотвращения были синтезированы бисфосфонаты для парентерального (внутривенного) введения.
Золедроновая кислота
В 2007 г. опубликованы результаты большого по своей статистической мощности международного многоцентрового рандомизированного плацебоконтролируемого двойного слепого исследования HORIZON-PFT (Health Outcomes and Reduced Incidence with Zoledronic Acid Once Yearly – Pivotal Fracture Trial) [7]. Пациентки с ОП были рандомизированы на две группы: одна группа получала внутривенно золедроновую кислоту в дозе 5 мг, которая вводилась в течение 15 минут (день 0, месяц 12 и 24), вторая группа получала плацебо. Обе группы дополнительно получали терапию кальцием (1000–1500 мг/день в пересчете на элементарный кальций) и нативными формами витамина D3 (400–1200 МЕ/день). Больные наблюдались в течение трех лет.
В исследование включались женщины в возрасте 65–89 лет, у которых МПК шейки бедренной кости составила -2,5 стандартного отклонения по Т-критерию при наличии или отсутствии компрессионных переломов, установленных с помощью рентгеноморфометрии, или ≤ -1,5 стандартного отклонения при наличии двух компрессионных переломов легкой степени или одного средней степени тяжести.
Пациентки были разделены на две страты. В первую вошли те, кто не получал специфической антиостеопоротической терапии до рандомизации, во вторую – принимавшие ранее антиостеопоротические препараты (ЗГТ, селективные модуляторы эстрогеновых рецепторов, кальцитонин лосося). Критериями исключения служили выявленная в период скрининга гипо- или гиперкальциемия, а также низкая скорость клубочковой фильтрации (< 30 мл/мин/1,73 м2) или протеинурия. Основная конечная точка – новые вертебральные переломы в первой страте и переломы проксимального отдела бедренной кости в обеих стратах. Вторичные конечные точки – любые невертебральные переломы, клинические вертебральные переломы. Кроме того, изменение МПК в шейке бедра и поясничном отделе позвоночника, а также изменения маркеров костного обмена (сывороточного С-телопептида коллагена 1-го типа, костно-специфичной щелочной фосфатазы и N-терминального пропептида коллагена 1-го типа).
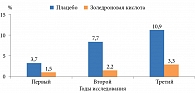
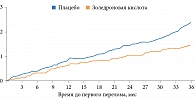
Три инфузии золедроновой кислоты в дозе 5 мг способствовали снижению риска всех основных остеопоротических переломов, включая вертебральные и переломы шейки бедра. Относительный риск вертебральных переломов уменьшился на 70% (рис. 1), что оказалось значительно выше по сравнению с бисфосфонатами, которые принимались внутрь (от 40 до 59%). Достоверно уменьшалась частота переломов шейки бедра – относительный риск через три года снизился на 41% (рис. 2). Отмечено также сокращение риска всех невертебральных переломов, клинических переломов, включая клинические вертебральные переломы, – на 25, 33 и 77% соответственно (р < 0,001).
В группе пациентов, получавших золедроновую кислоту, отмечено статистически значимое повышение МПК в общем показателе бедра на 6,02%, в шейке бедра – на 5,06%, поясничных позвонках – на 6,7%. Все три маркера костного обмена снизились к 12-му месяцу более чем на 50% и оставались на этом уровне в течение всего периода наблюдения.
В 2012 г. были опубликованы результаты продленной фазы исследования HORIZON-PFT. Был сделан вывод: длительное применение золедроновой кислоты (в течение шести лет) возможно лишь в случае тяжелого ОП с высоким риском вертебральных переломов.
Параллельно с HORIZON-PFT стартовало исследование HORIZON-RFT, целью которого стало изучение риска повторных переломов после перелома бедренной кости. В HORIZON-RFT было включено 2126 пациентов с низкоэнергетическим переломом бедра. Одна группа получала золедроновую кислоту, другая – плацебо. Медиана наблюдения – 1,9 года. Применение золедроновой кислоты привело к статистически значимому снижению относительного риска вертебральных переломов (на 46%), других новых остеопоротических переломов (на 39%) и невертебральных переломов (на 27%).
Один из наиболее важных вопросов клинической практики – влияние возраста пациента на эффективность и переносимость медикаментозной терапии.
Поскольку остеопению правомерно можно отнести к гериатрическим синдромам, результаты завершившихся исследований были пересмотрены с точки зрения оценки дополнительных факторов риска на конечные точки. Так, общее количество пациентов исследований HORIZON-PFT и HORIZON-RFT составило 4761 пациент старше 65 лет и 2083 пациента старше 75 лет. При проведении post hoc теста не было выявлено каких-либо различий в эффективности и переносимости золедроновой кислоты как среди мужчин, так и среди женщин. Однако отмечено, что антипереломный эффект в отношении вертебральных переломов был более выраженным среди женщин более молодого возраста.
Следующий этап клинических исследований был посвящен доказательству эффективности золедроновой кислоты для лечения ОП у мужчин [8], глюкокортикостероидного ОП [9]. Результаты, полученные в ходе сравнительных клинических исследований (с другими пероральными бисфосфонатами), позволили авторам утверждать, что эффект золедроновой кислоты на показатели МПК и маркеры костного обмена был не хуже, чем эффект алендроната и ризедроната соответственно. Продолжительность наблюдения за пациентами в сравнительных исследованиях, как правило, ограничивается одним или двумя годами, при этом не ставится задача доказать антипереломный эффект используемого лекарственного средства.
Возможность использования ибандроната (внутривенное введение) при постменопаузальном ОП оценивалась в клиническом исследовании DIVA (Dosing IntraVenous Administration). Авторы доказали сопоставимость влияния ибандроната на МПК и костные маркеры при различных режимах внутривенного введения (2 мг каждые два месяца или 3 мг каждые три месяца) по сравнению с ежедневным пероральным приемом 2,5 мг [10]. Через два года лечения в группе, получавшей 3 мг ибандроната внутривенно, прирост МПК в позвоночнике составил 6,3%, в группе, получавшей ибандронат перорально, только 4,8% (р < 0,05).
В результате бисфосфонаты для внутривенного введения стали использоваться наравне с пероральными бисфосфонатами. Основным показанием для назначения первых является плохая переносимость вторых. Желание пациента получать внутривенные формы дискретно (один раз в год для золедроновой кислоты и один раз в квартал для ибандроновой кислоты) может считаться относительным показанием.
Необходимо констатировать, что во многих странах Европы, а также в России на фармацевтическом рынке стали доминировать дженерики бисфосфонатов. Более широкое использование дженериков обусловлено необходимостью снижения затрат на лечение хронических заболеваний, требующих длительного применения лекарственных средств. В нашей стране несколько лет назад был зарегистрирован дженерик золедроновой кислоты – Резокластин ФС 5 мг (ЗАО «Ф-Синтез») в виде концентрата для приготовления раствора. Поскольку сравнительных исследований оригинального и воспроизведенного препарата золедроновой кислоты не проводилось, был обобщен клинический опыт ряда медицинских организаций, применявших Резокластин ФС 5 мг для лечения различных форм ОП (постменопаузального, глюкокортикостероидного, вторичного – на фоне хронических заболеваний). Российская ассоциация по остеопорозу инициировала ретроспективное исследование. В него вошли 23 пациента, получивших хотя бы одну инфузию и наблюдавшихся не менее одного года.
Основные результаты исследования опубликованы в 2014 г. Авторы показали, что Резокластин ФС обладает антирезорбтивным эффектом: снижение маркера костной резорбции С-телопептида коллагена 1-го типа на 79% через три месяца после первой инфузии. Отмечен прирост МПК в позвоночнике на 3,4% через год и на 5,7% через два года наблюдения после повторной инфузии, в шейке бедра – на 1,6 и 2,5% соответственно [11].
Заключение
Внутривенные формы бисфосфонатов стали широко использоваться при лечении ОП различного генеза. Появление отечественного препарата золедроновой кислоты (Резокластин ФС 5 мг) повысило доступность терапии при сохранении ее эффективности.
Ye.G. Zotkin
North-Western State Medical University named after I.I. Mechnikov
Contact person: Yevgeny Germanovich Zotkin, ezotkin@mail.ru
Osteoporosis is one of the most common chronic diseases of musculoskeletal system occurring both in elderly females and males. In order to minimize adverse events related to oral administration of bisphosphonates there were synthesized bisphosphonates for parenteral use (zoledronic acid). Clinical studies demonstrated its efficacy during post-menopause, glucocorticoid osteoporosis and osteoporosis in males. Several years ago, a generic form of zoledronic acid such as Rezoklastin FS has been registered in Russia. Clinical experience evidences that in terms of the main effects on bone tissue Rezoklastin FS at dose of 5mg was not inferior to the brand drug.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.