Эффективность и безопасность ведолизумаба в терапии язвенного колита в реальной клинической практике: пять лет наблюдения
- Аннотация
- Статья
- Ссылки
- English
Цель – оценить эффективность и безопасность терапии ведолизумабом (ВДМБ) в реальной клинической практике у больных язвенным колитом (ЯК) в течение пяти лет.
Материал и методы. В исследование были включены 136 пациентов с ЯК (мужчин 53,7%, женщин 46,3%), средний возраст – 33,8 ± 4,4 года, длительность заболевания – 3,1 ± 0,4 года (52,9% пациентов со средней степенью тяжести, 72,1% с тотальным поражением и 64,4% c хроническим рецидивирующим течением, в 17,6% случаев – внекишечные проявления (ВКП)).
Результаты. Через 12 недель 53 (38,9%) пациента с ЯК достигли клинического ответа, 72 (52,9%) – клинической ремиссии, 13 (9,5%) не ответили или недостаточно ответили на терапию. Через 24 недели клиническая ремиссия наблюдалась у 72,1%, клинический ответ – у 18,4% пациентов. Из 112 пациентов, которым была проведена колоноскопия, на 24-й неделе клинико-эндоскопическая ремиссия – у 68 (60,7%). Через 52 недели терапии эндоскопическая ремиссия сохранялась у 68 (60,7%) пациентов, эндоскопический ответ – у 40 (36,6%), клиническая ремиссия – у 112 (82,3%) и клинический ответ – у 21 (15,4%). Через пять лет терапии ВДМБ эндоскопическая ремиссия сохранялась у 70 (51,5%) пациентов, эндоскопический ответ – у 36 (26,5%), клиническая ремиссия – у 105 (77,2%) и клинический ответ – у 19 (14,0%). Выживаемость терапии ВДМБ у пациентов с ЯК составила 90,4% через 12 месяцев и сохранялась в течение года, 82,3% через два года, 81,6% через пять лет. Бесстероидная ремиссия составила 91,0%. Регресс ВКП через 24 недели отмечен у 58,3% пациентов с ЯК.
Заключение. Наше клиническое наблюдение 136 больных ЯК продемонстрировало высокую эффективность и безопасность ВДМБ.
Цель – оценить эффективность и безопасность терапии ведолизумабом (ВДМБ) в реальной клинической практике у больных язвенным колитом (ЯК) в течение пяти лет.
Материал и методы. В исследование были включены 136 пациентов с ЯК (мужчин 53,7%, женщин 46,3%), средний возраст – 33,8 ± 4,4 года, длительность заболевания – 3,1 ± 0,4 года (52,9% пациентов со средней степенью тяжести, 72,1% с тотальным поражением и 64,4% c хроническим рецидивирующим течением, в 17,6% случаев – внекишечные проявления (ВКП)).
Результаты. Через 12 недель 53 (38,9%) пациента с ЯК достигли клинического ответа, 72 (52,9%) – клинической ремиссии, 13 (9,5%) не ответили или недостаточно ответили на терапию. Через 24 недели клиническая ремиссия наблюдалась у 72,1%, клинический ответ – у 18,4% пациентов. Из 112 пациентов, которым была проведена колоноскопия, на 24-й неделе клинико-эндоскопическая ремиссия – у 68 (60,7%). Через 52 недели терапии эндоскопическая ремиссия сохранялась у 68 (60,7%) пациентов, эндоскопический ответ – у 40 (36,6%), клиническая ремиссия – у 112 (82,3%) и клинический ответ – у 21 (15,4%). Через пять лет терапии ВДМБ эндоскопическая ремиссия сохранялась у 70 (51,5%) пациентов, эндоскопический ответ – у 36 (26,5%), клиническая ремиссия – у 105 (77,2%) и клинический ответ – у 19 (14,0%). Выживаемость терапии ВДМБ у пациентов с ЯК составила 90,4% через 12 месяцев и сохранялась в течение года, 82,3% через два года, 81,6% через пять лет. Бесстероидная ремиссия составила 91,0%. Регресс ВКП через 24 недели отмечен у 58,3% пациентов с ЯК.
Заключение. Наше клиническое наблюдение 136 больных ЯК продемонстрировало высокую эффективность и безопасность ВДМБ.





Язвенный колит (ЯК) является хроническим воспалительным заболеванием кишечника, которое поражает слизистую оболочку толстой кишки (СОТК) и проходит с чередованием фаз активности и ремиссии [1].
Патогенез ЯК включает генетическую предрасположенность, дефекты муцинозного барьера, нарушения местного и системного иммунного ответа, микробиоту кишечника и факторы окружающей среды [1]. Заболеваемость ЯК растет, достигая от 0,6 до 24,3 на 100 тыс. человек, распространенность – 505 на 100 тыс. человек в развитых странах.
Целями терапии ЯК на первом этапе являются купирование симптомов заболевания, достижение клинического ответа и клинической ремиссии. Целями долгосрочного лечения пациентов с ЯК являются заживление СОТК, нормализация иммунобиологических маркеров заболевания, профилактика рецидивов, улучшение качества жизни больных ЯК и предотвращение ивалидизации пациентов [2].
В последние два десятилетия достигнут значительный прогресс в терапии воспалительных заболеваний кишечника (ВЗК), благодаря появлению генно-инженерных биологических препаратов (ГИБП) и синтетических таргетных иммуносупрессоров, в первую очередь ингибиторов фактора некроза опухоли альфа (ФНО-α) и блокаторов янус-киназ. Однако сохраняется потребность в новых препаратах для индукции и поддержания ремиссии, так как часть пациентов с ЯК не отвечают на терапию блокаторами ФНО-α или теряют со временем ответ на лечение [3, 4].
Ведолизумаб (ВДМБ) – моноклональное антитело, блокирующее миграцию лейкоцитов в слизистую оболочку кишечника вследствие ингибирования альфа-4-бета-7-интегрина. Эффективность ВДМБ для индукции и поддержания ремиссии у пациентов с ВЗК доказана в клинических исследованиях GEMINI 1, 2 и 3 [5–7]. Кроме того, долгосрочная эффективность и безопасность препарата подтверждены результатами исследований долгосрочной безопасности (GEMINI-LTS), в которые были включены участники исследования GEMINI [8]. По состоянию на 2020 г. продемонстрированы данные по эффективности и безопасности применения ВДМБ в течение восьми лет наблюдения. Через 400 недель лечения 217 (33,0%) из 658 пациентов с ЯК и 197 (28,1%) из 700 пациентов с болезнью Крона находились в клинической ремиссии и 230 (35,0%) из 657 и 232 (33,1%) из 700 соответственно имели клинический ответ. Следует отметить, что показатели частоты как клинического ответа, так и клинической ремиссии были достоверно выше у бионаивных пациентов в сравнении с теми, кто ранее получал терапию ингибиторами ФНО-α [8]. Анализ безопасности выявил отсутствие повышенного риска любых инфекций, в том числе серьезных инфекций, связанных с ВДМБ. Большинство инфекций были легкой или средней степени тяжести и отвечали на стандартное лечение, в то время как пациенты продолжали терапию ВДМБ [8].
Однако в аспекте реальной клинической практики участники рандомизированных контролируемых исследований (РКИ) не являлись репрезентативными. Из всех пациентов, с которыми врачи сталкиваются в повседневной практике, только около трети могли бы соответствовать критериям включения в исследование GEMINI [9].
ВДМБ зарегистрирован в России в 2016 г. для лечения больных язвенным колитом и болезнью Крона. В настоящее время опыт применения ВДМБ в реальной клинической практике в России описан в многочисленных публикациях, но период наблюдения составлял не более 12 месяцев [10–12].
Строгие критерии включения, применяемые в РКИ, ограничивают популяции пациентов и возможность экстраполировать полученные данные исследований на реальную клиническую практику. Поэтому особенно важным является проведение исследований, оценивающих эффективность и безопасность ВДМБ в реальной клинической практике, что помогает принять оптимальное решение в лечении больных ЯК [7].
Данное исследование представляет собой анализ пятилетнего опыта применения препарата ВДМБ у больных с тяжелым и среднетяжелым ЯК в отделении лечения воспалительных заболеваний кишечника Московского клинического научно-практического центра (МКНЦ) им. А.С. Логинова.
Цель – оценить эффективность и безопасность терапии ВДМБ в реальной клинической практике у больных ЯК средней и тяжелой степени в течение пяти лет наблюдения.
Материал и методы
В отделении лечения воспалительных заболеваний кишечника МКНЦ им. А.С. Логинова наблюдали
136 больных язвенным колитом, которые получали ВДМБ в период с июня 2017 г. по сентябрь 2022 г. Период наблюдения за пациентами, включенными в аналитическую группу, составил от 156 до 260 недель.
Были проанализированы пол, возраст пациента на момент начала терапии ВДМБ, возраст на момент постановки диагноза, длительность заболевания, характер течения заболевания, тяжесть и протяженность ЯК, наличие кишечных осложнений, наличие и локализация внекишечных проявлений (ВКП) (табл. 1), предшествующее лечение: терапия препаратами 5-аминосалициловой кислоты (5-АСК), иммуносупрессорами, глюкокортикостероидами (ГКС), ГИБП, а также их количество перед назначением ВДМБ (табл. 2), показатели активности воспалительного процесса перед началом терапии ВДМБ (табл. 3).
Большинство пациентов, включенных в исследование, имели среднетяжелое (52,9%) и тяжелое (33,8%) течение заболевания, у 72,1% диагностировано тотальное поражение толстого кишечника, у 17,6% пациентов имелись внекишечные проявления, преимущественно с поражением суставов (13,2%).
Показанием для назначения ВДМБ послужил непрерывный характер течения заболевания у 39 (28,7%) пациентов с ЯК, стероидорезистентность – у 17 (12,5%) пациентов, стероидозависимость – у 36 (26,5%), первичная неэффективность или потеря ответа на ГИБП – у 62 (45,6%) больных ЯК.
До начала исследования большинство больных получали препараты 5-АСК (98,2%), иммуносупрессоры (57,1%) и глюкокортикостероиды (73,2%). ГИБП получали более половины пациентов – 37 (66,1%), в том числе 18 (32,1%) – два или более ГИБП. В 23,5% случаев назначали инфликсимаб, другие ингибиторы ФНО-α применяли несколько реже (6,6–15,4%), преимущественно во второй и третьей линиях биологической терапии. Адалимумаб получал 21 (15,4%) пациент, голимумаб – 9 (6,6%) пациентов с ЯК. Таким образом, при ЯК ВДМБ преимущественно использовали в качестве препарата первой и второй линии терапии.
ВДМБ назначали по стандартной схеме согласно инструкции по медицинскому применению, рекомендуемый режим дозирования препарата: 300 мг вводят в виде в/в инфузии на нулевой, второй и шестой неделях, далее каждые восемь недель. В случае отсутствия терапевтического эффекта к 10-й неделе у пациентов с ЯК необходимо рассмотреть вопрос о целесообразности дальнейшей терапии ВДМБ.
Оценка эффективности (динамика клинических проявлений, лабораторных показателей активности воспалительного процесса и эндоскопической картины) была проведена через 3, 6, 12 и 60 месяцев от начала терапии ВДМБ.
Критерии оценки лечения:
- обострение (рецидив, атака) ЯК – появление типичных симптомов заболевания у больных ЯК в стадии клинической ремиссии, спонтанной или медикаментозно поддерживаемой. На практике признаками клинического обострения являются увеличение частоты дефекаций с выделением крови и/или характерные изменения, обнаруживаемые при эндоскопическом исследовании толстой кишки [13];
- ремиссия ЯК – исчезновение основных клинических симптомов заболевания и заживление слизистой оболочки толстой кишки (глубокая ремиссия) [13];
- ранний клинический ответ – уменьшение или исчезновение клинических симптомов заболевания: снижение частичного индекса Мейо без эндоскопической оценки на 30% и более от исходного на восьмой неделе лечения;
- клиническая ремиссия – отсутствие примеси крови в стуле, отсутствие императивных/ложных позывов при частоте дефекаций не более трех раз в сутки [13] (частичный индекс Мейо без эндоскопической оценки от 0 до 3, при этом значение параметра кишечного кровотечения – 0);
- эндоскопический ответ – уменьшение эндоскопических признаков воспаления (только на шестом и 12-м месяцах): как минимум на 1 балл по шкале Мейо;
- эндоскопическая ремиссия – отсутствие видимых макроскопических признаков воспаления при эндоскопическом исследовании толстой кишки [13];
- бесстероидная ремиссия – отсутствие симптомов заболевания и признаков воспаления без повторного применения ГКС в течение 12 месяцев после их отмены;
- выживаемость терапии – время от начала биологической терапии до ее прекращения по медицинским показаниям.
Ответ на лечение оценивали при уменьшении индекса по шкале Мейо не менее чем на 30% от исходного, а ремиссия была определена как оценка по шкале Мейо 0–3 балла (табл. 4) [13]. Состояние СОТК оценивали по шкале Schroeder [14].
Отсутствие значительного улучшения симптомов, прекращение лечения ВДМБ или перевод на ГИБП с другим механизмом действия считали неудачей терапии. Оценивали также необходимость оптимизации терапии ВДМБ у пациентов с недостаточным клиническим ответом через 24 недели терапии (снижение частичного индекса Мейо менее 30%) и отсутствием нормализации лабораторных показателей (скорость оседания эритроцитов (СОЭ), С-реактивный белок (СРБ), гемоглобин, фекальный кальпротектин (ФКП)).
Для оценки динамики состояния пациента с возможностью продолжения терапии ВДМБ проводили клинико-лабораторный и инструментальный контроль на специализированном лицензированном оборудовании, проходящем регулярную плановую поверку в соответствующих структурных подразделениях МКНЦ
им. А.С. Логинова.
Статистический анализ выполняли с использованием пакета прикладных программ Microsoft® Office Excel 2003 (Microsoft, США) и Stastica 7,0 (StatSoft Inc, США).
В качестве количественных показателей оценивали среднее и стандартную ошибку. Качественные показатели оценивали в процентах и с помощью 95%-ного доверительного интервала (95% ДИ). Для определения значимости различий между средними величинами при нормальном распределении совокупностей применяли t-критерий Стьюдента. Относительные риски (OР) рассчитывали как события в одной группе к рискам события в другой группе, с 95% ДИ рассчитывали по четырехпольным таблицам сопряженности.
Результаты
Клинический ответ (первичная конечная точка – 12 недель)
Больным ЯК назначен ВДМБ внутривенно капельно 300 мг по индукционной схеме 0–2–6 недели. Ранний ответ на терапию ВДМБ оценивали на 12-й неделе. Быстрый клинический ответ, характеризующийся уменьшением интенсивности абдоминальных болей, урежением ложных позывов и частоты стула, уменьшением крови и слизи в стуле, улучшением общего самочувствия, на восьмой неделе зафиксирован у 71 (52,2%) из 136 пациентов, включенных в исследование.
Через 12 недель после окончания индукционного курса терапии оценивали клиническую активность по индексу Мейо, динамику показателей иммунобиологических маркеров, а также переносимость препарата ВДМБ.
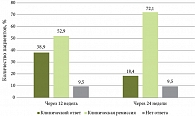
У 72 (52,9%) пациентов на 12-й неделе терапии была достигнута клиническая ремиссия по индексу Мейо, 53 (23,2%) пациента достигли показателей клинического ответа, у 13 (9,5%) не было отмечено положительной динамики (рис. 1). После проведенного индукционного курса у подавляющего большинства пациентов отмечена значительная положительная динамика лабораторных показателей воспаления в толстой кишке: концентрация ФКП снизилась в четыре раза, концентрация СРБ в сыворотке крови – в три раза, уровень гемоглобина поднялся на 25%. Динамика основных лабораторных показателей представлена в табл. 5.
В связи с отсутствием ответа на проводимую терапию за весь период наблюдения (260 недель) и сохраняющейся или незначительно уменьшившейся кровавой диареей, тенезмами, анемией, лейкоцитозом, сохраняющимся высоким уровнем СРБ, СОЭ, прокальцитонина и ФКП 6 (4,4%) пациентам, не ответившим на терапию ВДМБ, были назначены ГИБП с другим механизмом действия, 6 (4,4%) пациентам – ГКС по схемам в соответствии с клиническими рекомендациями [13]. Один (0,8%) пациент с ЯК не завершил индукционный курс, так как был прооперирован до его окончания в связи со сверхтяжелой атакой ЯК.
Таким образом, через 12 недель от начала проводимой терапии из 136 (100,0%) пациентов, включенных в аналитическую группу, 53 (38,9%) пациента с ЯК достигли клинического ответа, 72 (52,9%) больных ЯК – клинической ремиссии, 13 (9,5%) совсем не ответили или недостаточно ответили на индукционный курс терапии ВДМБ. Нежелательных явлений (НЯ) на фоне индукционного курса препарата ВДМБ, которые потребовали бы его отмены, ни в одном случае клинического наблюдения отмечено не было.
Клиническая и клинико-эндоскопическая ремиссия (вторичная конечная точка – через 24 и 52 недели)
Поддерживающая терапия. После проведенного индукционного курса ВДМБ через 24 недели среди пациентов с ЯК клинической ремиссии достигли 72,1%, клинического ответа – 18,4% пациентов.
Заживление СОТК. У большинства пациентов, достигших клинической ремиссии на 12-й неделе, отмечено заживление СОТК на 24-й неделе. На 24-й неделе эндоскопическое исследование было проведено 88 пациентам, из данной группы у 41 (46,6%) была достигнута эндоскопическая ремиссия. Через 24 недели у всех пациентов (n = 123), ответивших на терапию ВДМБ, индекс Мейо в группе снизился в среднем с 10,1 ± 0,2 до 1,9 ± 0,2 балла.
На 52-й неделе обследовано 112 пациента на предмет заживления СОТК (колоноскопию 24 пациентам выполняли повторно) и у 68 (60,7%) пациентов из 112 зафиксировано заживление СОТК. Таким образом, из 112 пациентов, которым была проведена колоноскопия, клинико-эндоскопическая ремиссия достигнута у 68 (60,7%) больных ЯК. Среди 44 пациентов, у которых не удалось достичь полной клинико-эндоскопической ремиссии, 32 (28,6%) ранее получали ГИБП.
Таким образом, через 24 недели терапии среди пациентов с ЯК, которым выполнена колоноскопия, эндоскопическая ремиссия наблюдалась у 41 (46,6%) пациента, эндоскопический ответ – у 40 (36,6%), клиническая ремиссия – у 95 (72,1%) и клинический ответ – у 25 (18,4%) пациентов.
Через 52 недели терапии эндоскопическая ремиссия наблюдалась у 68 (60,7%) пациентов, эндоскопический ответ сохранялся у 40 (36,6%), клиническая ремиссия – у 112 (82,3%) и клинический ответ – у 21 (15,4%) пациента с ЯК.
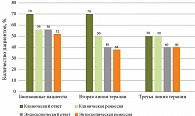
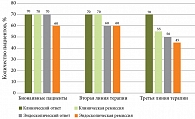
Мы проанализировали эффективность терапии в зависимости от проводимой ранее биологической терапии: у бионаивных пациентов и в качестве второй и третьей линии терапии, после блокаторов ФНО-α и ингибиторов янус-киназ. Результаты эффективности терапии ВДМБ представлены на рис. 2 и 3, что сопоставимо с ранее проведенными исследованиями [10].
В течение пятилетнего периода наблюдения вторичная потеря ответа развилась у 11 (8,1%) пациентов и у одного (0,7%) пациента отмечалось развитие НЯ.
Оптимизация терапии (введение препарата каждые четыре недели) в связи с развитием «ускользания» эффекта от проводимой терапии потребовалась 18 (13,2%) пациентам с ЯК, все они имели предшествующую терапию ГИБП. Среди больных ЯК, не получавших ранее анти-ФНО-α-препараты, оптимизация терапии ВДМБ потребовалась 2 (1,5%) пациентам (χ2 13,734; отношение шансов (ОШ) 0,08; 95% ДИ 0,018–0,364; р < 0,05). Таким образом, потребность в оптимизации терапии ВДМБ статистически выше у пациентов, получавших ранее один или несколько ГИБП.
Через пять лет терапии ВДМБ эндоскопическая ремиссия сохранялась у 70 (51,5%) пациентов, эндоскопический ответ – у 36 (26,5%), клиническая ремиссия – у 105 (77,2%) и клинический ответ – у 19 (14,0%) пациентов с ЯК.
Выживаемость терапии – это интегральная характеристика препарата, отражающая его эффективность, безопасность и длительность получения препарата до момента отмены по медицинским показаниям. Выживаемость терапии ВДМБ у пациентов с ЯК составила 90,4% через 12 месяцев и сохранялась в течение года, 82,3% – через два года, 81,6% – через пять лет.
Основной причиной отмены ВДМБ у пациентов с ЯК явилась потеря ответа на терапию и в одном случае – НЯ в виде появления артралгий de novo.
Бесстероидная ремиссия
Из 136 (100%) больных ЯК, получавших ВДМБ, не ответили или недостаточно ответили на терапию 13 (9,5%) пациентов. После завершения индукционного курса ведолизумаба ГКС были отменены у 99 (72,8%) пациентов, ответивших на лечение. Повторное назначение ГКС по поводу «ускользания» ответа на ВДМБ или обострения ЯК потребовалось у 11 (8,1%) из 136 пациентов. Таким образом, бесстероидная ремиссия у больных ЯК, ответивших на терапию ВДМБ (n = 123) в течение 12 месяцев, в реальной клинической практике составляет 91,0%.
Внекишечные проявления
До начала терапии ВДМБ внекишечные проявления зафиксированы у 24 (17,6%) из 136 пациентов с ЯК. У большинства пациентов, имеющих ВКП, у 18 (13,2%) имелись скелетно-мышечные проявления (артралгии, периферические артриты), у 4 (2,9%) – поражения кожи и слизистых, у 2 (1,5%) пациентов – заболевание печени (первичный склерозирующий холангит). На 12-й неделе терапии уменьшение интенсивности артралгий отмечено у 10 (55,5%) из 18 пациентов, регресс признаков поражения кожи и слизистых – у 2 (50,0%) из четырех пациентов, отсутствие динамики – у 8 (54,5%) и 2 (50,0%) пациентов соответственно. Таким образом, регресс внекишечных проявлений зафиксирован у 12 (50,0%) пациентов с ЯК из 24, имеющих ВКП.
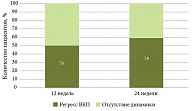
К 24-й неделе положительная динамика, характеризующаяся уменьшением болевого суставного синдрома и кожных проявлений, наблюдалась уже у 66,7% пациентов (12 из 18) и 50,0% пациентов (двое из четырех) соответственно (рис. 4). Регресс внекишечных проявлений через 24 недели отмечен у 14 (58,3%) пациентов с ЯК из 24, имеющих ВКП.
Утяжеления симптомов внекишечных проявлений любой локализации не наблюдалось ни у одного пациента.
Обсуждение
Регистрационные РКИ, являющиеся золотым стандартом, дают убедительные доказательства эффективности и безопасности лекарственного препарата, однако их результаты невозможно воспроизвести в условиях реальной клинической практики. В РКИ, регламентированных протоколом, в анализ включаются пациенты, которым выполняются все лабораторные и инструментальные исследования, предусмотренные протоколом. В реальной клинической практике в аналитическую группу включаются все пациенты, которым проводят лечение лекарственным препаратом, что позволяет оценить не только эффективность и безопасность, но и приверженность к лекарственной терапии, качество жизни пациентов.
Проведение дополнительных постмаркетинговых исследований необходимо для определения длительности применения, долгосрочной эффективности и безопасности препарата в условиях реальной клинической практики.
Наше исследование показало, что применение ВДМБ у пациентов с ЯК имеет хорошую эффективность. В данном исследовании, как и в других исследованиях ВДМБ в реальной практике, эффективность препарата по некоторым показателям оказалась выше, чем по результатам клинических исследований [10, 15]. Необходимо отметить, что в нашем исследовании большинство составляли пациенты, которые получали многокомпонентную противовоспалительную терапию, включавшую препараты 5-АСК и ГКС. Кроме того, больные ЯК в 45,6% случаев имели в анамнезе неэффективность одного препарата из группы блокаторов ФНО-α. Исследования подобной группы пациентов позволяют выявить ряд существенных закономерностей, которые могут повлиять на применение ВДМБ в реальной клинической практике [10]. В клинических исследованиях показано, что ВДМБ более эффективен у бионаивных пациентов [16]. Результаты нашего исследования также продемонстрировали, что при лечении больных ЯК эффективность ВДМБ при применении в качестве биологического препарата первой и второй линии была сопоставима. Через 12 месяцев терапии ВДМБ у подавляющего большинства пациентов (91%) была достигнута бесстероидная ремиссия, то есть больные ЯК, которые достигли клинической ремиссии, отменили прием ГКС, согласно клиническим рекомендациям, в течение первых 12 недель.
В данной работе мы проанализировали влияние ВДМБ на внекишечные проявления при ЯК. Согласно международному многоцентровому исследованию GETECCU ENEIDA, среди 77 пациентов с активными ВКП на исходном уровне ответ на ВДМБ через три месяца был отмечен у 23 (29,9%), ухудшение – у 13 (16,9%) и отсутствие изменений – у 41 (53,2%) пациента. Частота ответа составила 35,4% для периферического артрита, 11,8% для аксиального артрита, 35,7% для кожных ВКП и 33,3% для глазных ВКП. Таким образом, ВДМБ обеспечил достижение клинического ответа со стороны активных ВКП почти у трети пациентов после трех месяцев терапии. Ухудшение неактивных ВКП или развитие первичных ВКП во время терапии ВДМБ составило 4,5% [17]. В нашем исследовании 50,0% пациентов отметили регресс внекишечных проявлений через 12 недель, а через 24 недели уже у 58,3% пациентов отмечена положительная динамика со стороны ВКП. Только в одном случае (0,7%) появились артралгии de novo, которые потребовали отмены препарата.
Эффективность селективного препарата для купирования ВКП может быть объяснена с позиций эктопической экспрессии MAdCAM-1 и CCL 25 в сосудистом эндотелии портальных трактов [18]. Также лейкоциты СОТК у пациентов ВЗК способны фиксироваться к синовиальной мембране благодаря молекулам адгезии, связывая активированные лимфоциты, главным образом путем взаимодействия с белком адгезии сосудистого эндотелия VAP-1 [19]. Вышеописанный патофизиологический процесс позволяет объяснить эффективность селективного препарата ВДМБ при наличии у пациентов с ЯК ВКП.
С учетом растущего количества методов лечения, доступных для лечения ЯК, важно понимать влияние последовательности лечения на исходы. Данные клинических испытаний свидетельствуют о том, что пациенты с ЯК могут иметь лучшие результаты при использовании ВДМБ до терапии анти-ФНО-α [20]. Это наблюдение согласуется с результатами анализа данных реальной клинической практики у пациентов с ЯК, получавших лечение в различной последовательности.
Результаты нашего исследования продемонстрировали, что препарат имел удовлетворительную переносимость.
Заключение
Ведолизумаб – единственный биологический препарат для лечения ВЗК, селективно блокирующий воспаление в кишечнике. Терапия ВДМБ обеспечивает индукцию и длительное поддержание клинико-эндоскопической ремиссии при ЯК. Наибольший терапевтический эффект при терапии ВДМБ наблюдается у бионаивных пациентов при назначении в раннем периоде заболевания. Кроме того, применение ВДМБ в первой линии не снижает эффективность при применении биотерапии в последующих линиях терапии. При терапии ЖКТ-селективным препаратом отсутствует повышенный риск развития НЯ.
По мере того как появляется все больше генно-инженерных биологических препаратов с различными механизмами действия, выбор лечения должен зависеть от портрета пациента, его анамнеза, коморбидности, фенотипического варианта заболевания, планирования беременности, приверженности к лекарственной терапии и даже финансовых возможностей.
O.V. Knyazev, PhD, Prof., A.V. Kagramanova, PhD, I.A. Li, PhD, A.A. Lischinskaya, PhD, E.A. Sabelnikova, PhD, Prof., N.A. Fadeeva, PhD, T.V. Shkurko, PhD, B.A. Nanaeva, PhD, T.A. Baranova, M.Yu. Timanovskaуа, A.I. Parfenov, PhD, Prof.
A.S. Loginov Moscow Clinical Scientific Center
Ryzhikh National Medical Research Centre for Coloproctology
Scientific Research Institute of Healthcare and Medical Management of the Moscow City Health Department, Moscow
A.I. Yevdokimov Moscow State University of Medicine and Dentistry
Contact person: Oleg V. Knyazev, oleg7@bk.ru
In real clinical practice, unlike in the registered controlled trials, the analytical group includes all patients who are being treated with a drug.
The aim is to evaluate the efficacy and safety of vedolizumab (VDMB) therapy in real clinical practice in patients with ulcerative colitis (UC) for five years. Material and methods. The study included 136 patients with UC (men 53.7%, women 46.3%), average age – 33.8 ± 4.4 years, duration of the disease – 3.1 ± 0.4 years (52.9% of patients with moderate severity, 72.1% with total lesion and 64.4% with chronic recurrent course, in 17.6% of cases – extra-intestinal manifestations).
Results. After 12 weeks, 53 (38.9%) patients with UC achieved a clinical response, 72 (52.9%) achieved clinical remission, 13 (9.5%) did not respond or did not respond sufficiently to therapy. After 24 weeks, clinical remission reached 72.1%, clinical response – 18.4% of patients. Of 112 patients who underwent colonoscopy (CS), 68 (60.7%) had clinical and endoscopic remission at week 24. After 52 weeks of therapy, endoscopic remission persisted in 68 (60.7%) patients, endoscopic response – in 40 (36.6%), clinical remission – in 112 (82.3%) and clinical response – in 21 (15.4%). After five years of VDMB therapy, endoscopic remission persisted in 70 (51.5%) patients, endoscopic response in 36 (26.5%), clinical remission in 105 (77.2%) and clinical response in 19 (14.0%). The survival rate of VDMB therapy in patients with UC was 90.4% after 12 months and persisted for a year, 82.3% after two years, 81.6% after five years. Steroidal remission was 91.0%. The regression of extra-intestinal manifestations after 24 weeks was noted in 58.3% of patients with UC.
Conclusion. Our clinical observation of 136 patients with UC demonstrated the high efficacy and safety of VDMB.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.