Экспериментально-клиническое обоснование целесообразности использования спрея BIOZILAR в терапии острого риносинусита
- Аннотация
- Статья
- Ссылки
- English
Цель. Оценка эффективности спрея BIOZILAR с размером частиц серебра 3–4 нм в лечении схожего с острым воспалительным ринитом воспаления и восстановлении эпителия слизистой оболочки носа лабораторных животных (крыс), а также в лечении острого инфекционного риносинусита у взрослых.
Материал и методы. На клинических базах кафедры оториноларингологии Российского университета медицины было проведено двухэтапное экспериментально-клиническое исследование для оценки клинической эффективности, переносимости и безопасности спрея для полости носа и рта BIOZILAR. В экспериментальной части исследования оценивали восстановление эпителия слизистой оболочки полости носа лабораторных животных (крыс) после воздействия спрея при смоделированном раздражении, соответствующем явлениям при остром воспалительном рините. В клинической части исследования проводили субъективную и объективную оценку носового дыхания, микрофлоры и мукоцилиарного клиренса в полости носа, частоты использования деконгестантов у пациентов с острым инфекционным риносинуситом до и после лечения.
Результаты. На первом этапе исследования в основной группе лабораторных животных обнаружены: повышенное содержание бокаловидных клеток в эпителии слизистой оболочки; гиперпродукция слизи, содержащей лимфоциты. На втором этапе исследования по визуально-аналоговой шкале отмечено восстановление носового дыхания у 17 пациентов в основной группе и у 12 – в группе сравнения. Эти результаты подтверждены методом передней активной риноманометрии. Ко второму визиту (день 3 ± 1) отмечен рост всех показателей носового дыхания, которые к третьему визиту (день 7 ± 1) достигли нормальных значений у большинства пациентов. На втором визите отсутствовал рост патогенной микрофлоры в обеих группах. В день начала исследования в связи с наличием воспалительных изменений показатели скорости мукоцилиарного транспорта у большинства пациентов в обеих группах соответствовали нарушениям I–II степени. К заключительному визиту у всех пациентов данные показатели пришли в норму. Частота использования деконгестантов уменьшилась в четыре раза.
Заключение. Экспериментальное исследование, проведенное на животных, показало, что спрей Биозилар способствует более быстрому восстановлению эпителия слизистой оболочки полости носа, что может привести к более быстрому клиническому выздоровлению. Клиническое сравнительное наблюдательное исследование продемонстрировало эффективность спрея BIOZILAR в лечении пациентов с острым инфекционным риносинуситом. На фоне терапии отмечены выраженное улучшение самочувствия пациентов; восстановление носового дыхания, что подтверждено данными передней активной риноманометрии; уменьшение использования деконгестантов; подавление роста патогенной микрофлоры; положительное влияние на мукоцилиарный клиренс; высокая приверженность пациентов к применению этого средства.
Цель. Оценка эффективности спрея BIOZILAR с размером частиц серебра 3–4 нм в лечении схожего с острым воспалительным ринитом воспаления и восстановлении эпителия слизистой оболочки носа лабораторных животных (крыс), а также в лечении острого инфекционного риносинусита у взрослых.
Материал и методы. На клинических базах кафедры оториноларингологии Российского университета медицины было проведено двухэтапное экспериментально-клиническое исследование для оценки клинической эффективности, переносимости и безопасности спрея для полости носа и рта BIOZILAR. В экспериментальной части исследования оценивали восстановление эпителия слизистой оболочки полости носа лабораторных животных (крыс) после воздействия спрея при смоделированном раздражении, соответствующем явлениям при остром воспалительном рините. В клинической части исследования проводили субъективную и объективную оценку носового дыхания, микрофлоры и мукоцилиарного клиренса в полости носа, частоты использования деконгестантов у пациентов с острым инфекционным риносинуситом до и после лечения.
Результаты. На первом этапе исследования в основной группе лабораторных животных обнаружены: повышенное содержание бокаловидных клеток в эпителии слизистой оболочки; гиперпродукция слизи, содержащей лимфоциты. На втором этапе исследования по визуально-аналоговой шкале отмечено восстановление носового дыхания у 17 пациентов в основной группе и у 12 – в группе сравнения. Эти результаты подтверждены методом передней активной риноманометрии. Ко второму визиту (день 3 ± 1) отмечен рост всех показателей носового дыхания, которые к третьему визиту (день 7 ± 1) достигли нормальных значений у большинства пациентов. На втором визите отсутствовал рост патогенной микрофлоры в обеих группах. В день начала исследования в связи с наличием воспалительных изменений показатели скорости мукоцилиарного транспорта у большинства пациентов в обеих группах соответствовали нарушениям I–II степени. К заключительному визиту у всех пациентов данные показатели пришли в норму. Частота использования деконгестантов уменьшилась в четыре раза.
Заключение. Экспериментальное исследование, проведенное на животных, показало, что спрей Биозилар способствует более быстрому восстановлению эпителия слизистой оболочки полости носа, что может привести к более быстрому клиническому выздоровлению. Клиническое сравнительное наблюдательное исследование продемонстрировало эффективность спрея BIOZILAR в лечении пациентов с острым инфекционным риносинуситом. На фоне терапии отмечены выраженное улучшение самочувствия пациентов; восстановление носового дыхания, что подтверждено данными передней активной риноманометрии; уменьшение использования деконгестантов; подавление роста патогенной микрофлоры; положительное влияние на мукоцилиарный клиренс; высокая приверженность пациентов к применению этого средства.










Введение
Медицина – наука разноплановая. Но в настоящее время на все сферы медицины распространилась «эпидемия» антибиотикорезистентности. По оценке Всемирной организации здравоохранения, из-за неконтролируемого использования антибактериальных препаратов к 2050 г. ожидаемая смертность от антибиотикорезистентных бактерий составит до 10 млн человек в год [1]. Сложившаяся ситуация привела к поиску альтернативных препаратов для борьбы с бактериальной инфекцией.
Еще в древние времена люди знали антибактериальные свойства серебра. История сохранила множество примеров его применения, основанного на бактерицидном действии [2, 3]. Массовое использование серебра связано с изобретением его коллоидной формы в конце XIX века [4]. Препарат стали применять повсеместно против разных заболеваний – от простуды и сифилиса до психических расстройств [5]. В начале XX века из-за появления первых антибиотиков потребность в препаратах серебра резко снизилась, их продолжали использовать только для лечения ожоговых ран и профилактики неонатального конъюнктивита. В связи с ростом антибиотикорезистентности патогенной микрофлоры поиск путей применения серебра был продолжен. В оториноларингологии борьба с вирусным и бактериальным воспалением стала острой проблемой, учитывая подверженность лор-органов воздействию инфекционных агентов [6, 7]. Слизистая оболочка полости носа и околоносовых пазух обеспечивает организм человека очищенным воздухом, при этом аккумулируя весь спектр патогенных микроорганизмов, аллергенов и поллютантов. Особую важность в последнее время приобретает профилактика присоединения бактериального воспаления на фоне вирусного поражения [8, 9].
В конце XX века эффективность серебра как антимикробного средства была клинически доказана. Благодаря синтезу наночастиц серебра резко расширился спектр применения препаратов на его основе и повысился их противовоспалительный эффект. Спрей BIOZILAR состоит из наночастиц серебра размером 3–4 нм, которые способны находиться во взвешенном состоянии бесконечно долго. Концентрат стабилен в физрастворе, химически чист. В его составе – деионизированная вода и серебро. Благодаря уникально малому размеру частиц серебра этот препарат значительно эффективнее ранее известных. Спрей прошел ряд доклинических и клинических исследований. Однако в оториноларингологии его не исследовали.
На клинических базах кафедры оториноларингологии Российского университета медицины было проведено двухэтапное экспериментально-клиническое исследование, одобренное этическим комитетом.
Целью первого этапа исследования была оценка эффективности исследуемого средства (раствора наночастиц серебра) – спрея BIOZILAR – в лечении схожего с острым воспалительным ринитом воспаления и восстановлении эпителия слизистой оболочки носа лабораторных животных (крыс).
Экспериментальное исследование эффективности использования спрея BIOZILAR на лабораторных животных
Материал и методы
На первом этапе было проведено экспериментальное исследование действия спрея BIOZILAR на шести крысах-самцах массой от 319 до 360 г, полученных из вивария Российского университета медицины. Животные размещались в условиях вивария со средней продолжительностью светового дня, составляющей 12 часов, средней температурой воздуха 18–23 °C и относительной влажностью воздуха 40–60% в соответствии с ГОСТ 33216-2014 «Межгосударственный стандарт. Руководство по содержанию и уходу за лабораторными животными». Наблюдение за животными осуществлялось в течение шести дней, у животных был неограниченный доступ к воде и пище. На шестой день исследования была выполнена эвтаназия с применением комбинированного препарата на основе тилетамина и золазепама. Всем крысам в первый день для провокации острого ринита интраназально капельно с помощью лабораторного дозатора вводили нейтральный забуференный 10%-ный формалин в дозе 20 мкл. В результате воздействия формалина на слизистую оболочку полости носа у крыс происходило нарушение целостности поверхностных слоев слизистой оболочки, обусловленное сильным раздражением, соответствующее явлениям при остром воспалительном рините. В качестве терапии в основной группе вводили раствор наночастиц серебра размером 3–4 нм (спрей BIOZILAR) четыре раза в день в дозе 10 мкл. В контрольной группе вводили изотонический стерильный солевой раствор четыре раза в день в дозе 10 мкл. Лечение проводили в течение пяти дней. На шестой день был выполнен забор образцов слизистой оболочки полости носа.
Патологоанатомическое исследование производили с помощью метода световой микроскопии, которому предшествовала стандартная подготовка биоптатов (фиксация в нейтральном формалине, гистологическая проводка, заливка в парафин, окрашивание срезов гематоксилином и эозином).
Результаты
При гистологическом исследовании в основной группе были обнаружены следующие изменения:
- обильная воспалительная инфильтрация эпителия и собственной пластинки слизистой оболочки лимфоцитами;
- выход лимфоцитов на поверхность эпителия слизистой оболочки;
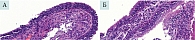
- повышенное содержание бокаловидных клеток в эпителии слизистой оболочки; гиперпродукция слизи, содержащей лимфоциты (рис. 1А).
На апикальной поверхности эпителиоцитов слизистой оболочки четко различимы реснички (рис. 1Б).
При гистологическом исследовании в группе контроля были обнаружены следующие изменения:
- разрыхление и некроз эпителия слизистой оболочки полости носа;
- расширение просвета кровеносных и лимфатических сосудов, слабый отек в рыхлой волокнистой соединительной ткани – компонента собственной пластинки слизистой оболочки;
- скудная инфильтрация эпителия и собственной пластинки слизистой оболочки лимфоцитами (рис. 2А);
- отсутствие четко дифференцируемых ресничек на апикальной поверхности эпителиоцитов (рис. 2Б).
Выводы
Таким образом, можно предположить, что исследуемое средство – раствор наночастиц серебра, спрей BIOZILAR – продемонстрировало модифицирующий эффект, который способствует более быстрому прекращению воспалительного процесса и, соответственно, восстановлению слизистой оболочки полости носа. В частности, раствор серебра положительно воздействует на слизистую оболочку носа, подвергшуюся химическому воздействию, способствует более быстрому восстановлению эпителия, что может привести к ускоренному клиническому выздоровлению.
Целью второго этапа исследования была оценка клинической эффективности, переносимости и безопасности спрея BIOZILAR с размером частиц серебра 3–4 нм в лечении острого инфекционного риносинусита на фоне острой респираторной вирусной инфекции у взрослых.
Клиническое исследование эффективности использования спрея BIOZILAR у пациентов с острым инфекционным риносинуситом
Материал и методы
На втором этапе проведено простое сравнительное наблюдательное клиническое исследование с формированием двух групп по 20 больных с острым инфекционным риносинуситом на фоне острой респираторной вирусной инфекции. В основной группе (группа 1), пациенты которой перед началом лечения заполнили форму информированного добровольного согласия, применялся спрей для полости носа и рта BIOZILAR с размером частиц серебра 3–4 нм по два впрыска в обе половины полости носа 4–5 раз в день в течение семи дней. В группе сравнения (группа 2) использовали протеинат серебра (2%-ный раствор) ежедневно по две капли в каждую половину носа три раза в день в течение семи дней. При необходимости было разрешено использовать местно сосудосуживающие средства, жаропонижающие препараты.
Результаты
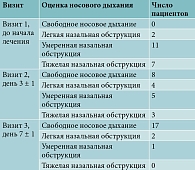
Был проведен анализ субъективной оценки носового дыхания по визуально-аналоговой шкале (ВАШ) в процессе лечения в обеих группах, где результаты от 0 до 1 балла интерпретировались как свободное носовое дыхание, от 2 до 4 – как легкая назальная обструкция, от 5 до 7 – как умеренная назальная обструкция, от 8 до 10 баллов – как тяжелая назальная обструкция (табл. 1, 2).
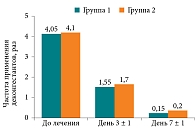
С учетом динамики улучшения носового дыхания были проанализированы частота и длительность применения деконгестантов (рис. 3). На первом визите было выяснено, что все пациенты использовали деконгестанты от двух до шести раз в день. В первой группе к третьему дню восемь пациентов отказались от сосудосуживающих препаратов полностью, шесть пациентов применяли их 1–2 раза в день и шесть – до 3–4 раз в день. К седьмым суткам двое больных применяли деконгестанты 1–2 раза в день. Во второй группе к третьему дню шесть пациентов отказались от сосудосуживающих препаратов полностью, семь пациентов применяли их 1–2 раза в день и семь – до 3–4 раз в день. К седьмым суткам трое больных применяли деконгестанты 1–2 раза в день.
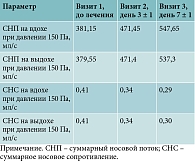
Для определения объективных показателей носового дыхания использовали переднюю активную риноманометрию (ПАРМ). Был выполнен анализ суммарного носового потока (СНП), а также суммарного носового сопротивления (СНС) на вдохе и выдохе при давлении 150 Па в первой и второй группе (табл. 3, 4).
В обеих группах, исходя из полученных данных при оценке СНП и СНС на вдохе и выдохе при давлении 150 Па, ко второму визиту была отмечена положительная динамика, которая сохранялась до конца терапии (день 7 ± 1).
Также был проведен забор биоматериала со слизистой оболочки полости носа для определения микрофлоры перед началом терапии и на 7-й день лечения.
На первом визите в первой группе получены следующие данные микробиологического исследования: Streptococcus pneumoniae обнаружены у восьми пациентов, Staphylococcus aureus – у четырех, Haemophilus influenzae – также у четырех. Не было выявлено роста патогенной микрофлоры в четырех случаях (табл. 5).
На втором визите был выполнен повторный забор отделяемого из полости носа. Получены следующие данные микробиологического исследования: H. influenzae обнаружены у двух пациентов, Str. pneumoniae – у трех, S. aureus – у одного. При этом у всех пациентов патогенные возбудители высеяны в этиологически незначимых количествах. Не было выявлено роста патогенной микрофлоры в 14 случаях (табл. 6).
На первом визите во второй группе получены следующие данные микробиологического исследования: Streptococcus pneumoniae обнаружены у шести человек, Staphylococcus aureus – у трех, Haemophilus influenzae – у шести. Не было выявлено роста патогенной микрофлоры в пяти случаях (табл. 7).
На втором визите во второй группе был выполнен повторный забор отделяемого из полости носа. Получены следующие данные микробиологического исследования: H. influenzae обнаружен у четырех человек, Str. pneumoniae – у трех, S. aureus – у одного. При этом у всех пациентов патогенные возбудители высеялись в этиологически незначимых количествах. Не было выявлено роста патогенной микрофлоры в 12 случаях (табл. 8).
Сравнительные характеристики результатов микробиологического исследования на первом и третьем визитах в группах 1 и 2 отображены на рис. 4.
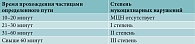
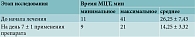
Также всем пациентам было проведено исследование мукоцилиарного клиренса в первый и в третий визит. В качестве частиц-метчиков выбран активированный уголь, частицы которого помещали на передний край нижней носовой раковины под контролем эндоскопа. Затем каждую минуту проверяли динамику продвижения частиц-метчиков в полости носа, а далее – по задней стенке глотки с помощью эндоскопа. Для оценки полученных результатов руководствовались данными, указанными в Национальном руководстве под редакцией М.Р. Богомильского (табл. 9). Результаты замера времени мукоцилиарного транспорта (МЦТ) приведены в табл. 10 и 11 и на рис. 5.
На день 14 ± 2 проводился телефонный контакт для контроля результатов лечения: не было ли рецидивов заболевания или повторного инфицирования пациентов.
В ходе исследования нежелательных явлений не отмечено. В первой группе три пациента обратили внимание на ощущение сухости и дискомфорта сразу после применения препарата, которое проходило самостоятельно в течение 5–10 минут. У двух пациентов было зафиксировано ухудшение состояния на 6–7-й день лечения: у одного диагностирован острый левосторонний бактериальный риносинусит средней степени тяжести, у другого – острый двусторонний бактериальный риносинусит легкого течения. В обоих случаях проведены курсы системной антибактериальной терапии с положительным эффектом.
Во второй группе 13 пациентов обратили внимание на ощущение сухости и дискомфорта сразу после применения протеината серебра, которое проходило самостоятельно в течение 5–10 минут. У трех пациентов было отмечено ухудшение состояния на 6–7-й день лечения: у двух больных диагностирован острый правосторонний бактериальный риносинусит легкой и средней степени тяжести, у одного – острый двусторонний бактериальный риносинусит легкого течения. Во всех трех случаях проведены курсы системной антибактериальной терапии с положительным эффектом.
В первой группе все пациенты полностью соблюдали кратность и длительность применения препарата. В контрольной группе шесть пациентов досрочно завершили курс лечения из-за дискомфорта во время применения средства.
Выводы
Согласно данным сравнительного наблюдательного исследования, проведенного на клинических базах кафедры оториноларингологии Российского университета медицины, подтверждена эффективность спрея BIOZILAR в лечении пациентов с острым инфекционным риносинуситом на фоне острой респираторной вирусной инфекции. Эффективность препарата была сопоставима с эффективностью протеината серебра.
На фоне терапии уже на третий день отмечено восстановление носового дыхания за счет купирования воспалительных проявлений заболевания и выраженное улучшение самочувствия пациентов как основной группы, так и группы сравнения. Эти результаты подтверждены объективным методом обследования (ПАРМ). Ко второму визиту (день 3 ± 1) отмечен рост всех показателей носового дыхания, которые к третьему визиту (день 7 ± 1) достигли нормальных значений у большинства пациентов.
Быстрое улучшение носового дыхания при использовании препаратов серебра позволяет уменьшить или отменить использование сосудосуживающих средств и снизить нагрузку деконгестантами на ранних этапах лечения.
Анализ микрофлоры полости носа показал, что спрей BIOZILAR эффективно подавляет рост патогенной микрофлоры, как и протеинат серебра.
Проведено исследование мукоцилиарного клиренса методом применения частиц-метчиков. В день начала исследования в связи с наличием воспалительных изменений показатели скорости МЦТ у большинства пациентов в обеих группах соответствовали нарушениям I–II степени. К заключительному визиту у всех пациентов данные показатели пришли в норму, что говорит о восстановлении слизистой оболочки полости носа за счет купирования воспаления и отсутствия негативного влияния средства.
В ходе исследования нежелательных явлений не было. Три пациента отметили ощущение сухости и дискомфорта сразу после применения спрея BIOZILAR, которое проходило самостоятельно в течение 5–10 минут, и 13 пациентов отметили такие же симптомы после применения протеината серебра.
У двух пациентов в первой группе и у трех во второй группе отмечено ухудшение состояния и необходимость назначения антибактериальной терапии на 6–7-й день лечения. Во всех случаях проведены курсы системной антибактериальной терапии с положительным эффектом.
Заключение
Таким образом, спрей BIOZILAR в эксперименте и клинической практике оказался эффективным средством в лечении острого инфекционного риносинусита на фоне острой респираторной вирусной инфекции. При относительно равной микробиологической активности исследуемых средств у пациентов в группе, получавшей BIOZILAR, приверженность к терапии была выше благодаря более комфортному применению, вследствие чего клиническая эффективность спрея также оказалась несколько выше протеината серебра.
A.Yu. Ovchinnikov, PhD, Prof., N.A. Miroshnichenko, PhD, Prof., Yu.O. Nikolaeva, PhD, E.L. Tumanova, PhD, Prof., E.Yu. Rudenko, PhD, Ass. Prof., P.I. Ovchinnikov, D.A. Bakulin, PhD
Russian University of Medicine, Moscow
Pirogov Russian National Research Medical University, Moscow
Contact person: Andrey Yu. Ovchinnikov, lorent1@mail.ru
Relevance. The uncontrolled use of antibacterial drugs has led to the evolution of antibiotic resistance, more frequent hospitalizations, an increase in the length of patient stay in the hospital, and an increase in mortality from infections caused by antimicrobial-resistant bacteria. In this regard, the search for effective alternative methods of treating such diseases, including ENT organs, continues.
Aim. Evaluation of the effectiveness of BIOZILAR spray with the silver particles 3–4 nanometers in size in the treatment of inflammation similar to acute inflammatory rhinitis and restoration of the epithelium of the nasal mucosa of laboratory animals (rats), as well as in the treatment of acute infectious rhinosinusitis in adults.
Material and methods. A two-stage experimental and clinical trial was conducted at the clinical bases of the Department of Otorhinolaryngology of the Russian University of Medicine to evaluate the clinical efficacy, tolerability and safety of BIOZILAR nasal and oral spray. In the experimental part of the study, the restoration of the epithelium of the nasal mucosa of laboratory animals (rats) after exposure to spray with simulated irritation corresponding to the phenomena of acute inflammatory rhinitis was evaluated. In the clinical part of the study, a subjective and objective assessment of nasal respiration, microflora and mucociliary clearance in the nasal cavity, and the frequency of decongestant use in patients with acute infectious rhinosinusitis before and after treatment was performed.
Results. At the first stage of the study, an increased content of goblet cells in the epithelium of the mucous membrane was found in the main group of laboratory animals; hyperproduction of mucus containing lymphocytes. At the second stage of the study, recovery of nasal breathing was noted on a visual analog scale in 17 patients in the main group and in 12 in the comparison group. These results were confirmed by anterior active rhinomanometry. By the second visit (day 3 ± 1), an increase in all indicators of nasal breathing was noted, which by the third visit (day 7 ± 1) reached normal values in most patients. At the second visit, there was no growth of pathogenic microflora in both groups. On the day of the start of the study, due to the presence of inflammatory changes, the mucociliary transport rates in most patients in both groups corresponded to grade I–II disorders. By the final visit, these indicators returned to normal in all patients. The frequency of decongestant use decreased by four times.
Conclusion. An experimental study conducted on animals has shown that BIOZILAR spray promotes faster restoration of the epithelium of the nasal mucosa, which can lead to a faster clinical recovery. A clinical comparative observational study demonstrated the effectiveness of BIOZILAR spray in the treatment of patients with acute infectious rhinosinusitis. Against the background of therapy, there was a marked improvement in the well-being of patients; restoration of nasal breathing, which was confirmed by the data of anterior active rhinomanometry; reducing the use of decongestants; inhibiting the growth of pathogenic microflora; positive effect on mucociliary clearance; high patient adherence to the use of this drug.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.