Эндотелиопротективное действие Криопреципитата при лечении гнойного пиелонефрита
- Аннотация
- Статья
- Ссылки
- English
Материал и методы. С 2017 по 2018 г. на базе кафедры урологии и андрологии с курсами специализированной хирургии Алтайского государственного медицинского университета в городской больнице № 11 Барнаула проведено проспективное контролируемое рандомизированное когортное исследование с участием 30 больных в возрасте от 20 до 45 лет с диагнозом «острый гнойный пиелонефрит». Все пациенты получали стандартную консервативную терапию. Лечение больных первой группы (n = 15) предусматривало дополнительное проведение трансфузионной терапии Криопреципитатом, произведенным Алтайским краевым центром крови (Барнаул). Пациентам второй группы (n = 15) на третьи-четвертые сутки после госпитализации проводилось оперативное вмешательство в объеме декапсуляции пораженной почки, предусматривающее вскрытие гнойного очага. Наряду с комплексным обследованием определялось содержание классических маркеров дисфункции эндотелия в плазме крови: эндотелина 1 (с использованием реактивов Endothelin (1–21), Biomedica) и фактора Виллебранда (с использованием реагента VWF:Ag, Siemens).
Результаты. Уровни эндотелина 1 и фактора Виллебранда у больных при поступлении в стационар превышали соответствующие значения практически здоровых людей (по медиане в 3,1–3,3 и 3,5–3,6 раза соответственно). Вне зависимости от проводимого лечения наблюдалось повышение концентрации эндотелина 1. В частности, после шести-семи дней терапии как в первой, так и во второй группе содержание эндотелина 1 превысило исходные значения (при поступлении в стационар) в 1,8–2,0 раза. Фактор Виллебранда в первой группе (введение Криопреципитата) уменьшился в 3,3 раза, тогда как во второй группе (хирургическое вмешательство) – только в 2,2 раза (полученные значения высоко достоверны, р < 0,002). Эти данные свидетельствуют о том, что применение Криопреципитата, несмотря на высокое содержание в составе фактора Виллебранда, снижает уровень этого маркера в крови и, следовательно, оказывает эндотелиопротективное действие.
Выводы. Применение Криопреципитата в составе консервативной терапии гнойного пиелонефрита оказывает эндотелиопротективное действие на сосуды, способствуя ограничению воспалительного процесса и его регрессии.
Материал и методы. С 2017 по 2018 г. на базе кафедры урологии и андрологии с курсами специализированной хирургии Алтайского государственного медицинского университета в городской больнице № 11 Барнаула проведено проспективное контролируемое рандомизированное когортное исследование с участием 30 больных в возрасте от 20 до 45 лет с диагнозом «острый гнойный пиелонефрит». Все пациенты получали стандартную консервативную терапию. Лечение больных первой группы (n = 15) предусматривало дополнительное проведение трансфузионной терапии Криопреципитатом, произведенным Алтайским краевым центром крови (Барнаул). Пациентам второй группы (n = 15) на третьи-четвертые сутки после госпитализации проводилось оперативное вмешательство в объеме декапсуляции пораженной почки, предусматривающее вскрытие гнойного очага. Наряду с комплексным обследованием определялось содержание классических маркеров дисфункции эндотелия в плазме крови: эндотелина 1 (с использованием реактивов Endothelin (1–21), Biomedica) и фактора Виллебранда (с использованием реагента VWF:Ag, Siemens).
Результаты. Уровни эндотелина 1 и фактора Виллебранда у больных при поступлении в стационар превышали соответствующие значения практически здоровых людей (по медиане в 3,1–3,3 и 3,5–3,6 раза соответственно). Вне зависимости от проводимого лечения наблюдалось повышение концентрации эндотелина 1. В частности, после шести-семи дней терапии как в первой, так и во второй группе содержание эндотелина 1 превысило исходные значения (при поступлении в стационар) в 1,8–2,0 раза. Фактор Виллебранда в первой группе (введение Криопреципитата) уменьшился в 3,3 раза, тогда как во второй группе (хирургическое вмешательство) – только в 2,2 раза (полученные значения высоко достоверны, р < 0,002). Эти данные свидетельствуют о том, что применение Криопреципитата, несмотря на высокое содержание в составе фактора Виллебранда, снижает уровень этого маркера в крови и, следовательно, оказывает эндотелиопротективное действие.
Выводы. Применение Криопреципитата в составе консервативной терапии гнойного пиелонефрита оказывает эндотелиопротективное действие на сосуды, способствуя ограничению воспалительного процесса и его регрессии.
Введение
Эндотелий кровеносных сосудов выполняет множество задач. Среди них регуляция транспорта биологически активных веществ, обеспечение барьерной и секреторной функций, участие в фагоцитозе, контроль диффузии воды, электролитов, продуктов метаболизма, адгезии и агрегации тромбоцитов. Кроме того, эндотелиальные клетки отвечают за депонирование и экспрессию целого ряда факторов, регулирующих коагуляционные и фибринолитические реакции. Эндотелий также задействован в регуляции сосудистого тонуса, окислительного стресса, воспалительных реакциях. Он способен продуцировать микровезикулы, играющие важную роль в инициации гемокоагуляции [1].
Выделяют такое понятие, как дисфункция эндотелия – ключевое звено в патогенезе многих заболеваний человека: инсульта, диабета первого и второго типа, острого коронарного синдрома, патологии периферических сосудов, роста опухолей и метастазов, хронической почечной недостаточности, ревматоидного артрита, вирусных инфекций и др. [3]. При эндотелиальной дисфункции возникает дисбаланс между продукцией вазодилатирующих, ангиопротективных, антипролиферативных факторов (оксида азота, простациклина, тканевого активатора плазминогена, натрийуретического пептида С-типа, эндотелиального гиперполяризующего фактора) и вазоконстрикторных, протромботических, пролиферативных факторов (эндотелина 1, супероксид-аниона, тромбоксана А2, ингибитора тканевого активатора плазминогена 1) [4]. Тромбин, интерлейкин 1, фактор некроза опухоли альфа, интерферон гамма, эндотоксин, гомоцистеин, окислители, а также гипоксия резко снижают антитромбогенные свойства (существующие в состоянии покоя) эндотелия сосудов.
При воспалительных процессах происходит активация полиморфноядерных лейкоцитов, которая является фактором риска повреждения эндотелия и формирования органной дисфункции. Активированные нейтрофилы способны нарушать функционирование микроциркуляторного русла за счет повышения проницаемости эндотелия, адгезии лейкоцитов к эндотелию, образования в капиллярах «пробок», высвобождения вазоактивных продуктов, деформации и компрессии капилляров вследствие интерстициального отека, вызванного активными формами кислорода. Кроме снижения тканевой перфузии, активация лейкоцитов приводит к повреждению эндотелия через высвобождение цитотоксических медиаторов, активных форм кислорода, лизосомальных ферментов, простаноидов [5].
С учетом результатов многочисленных экспериментальных и клинических работ, не вызывает сомнения важная роль эндотелиальных механизмов в развитии и прогрессировании хронического гломерулонефрита. И это объяснимо, если учесть, что около 30% всей эндотелиальной выстилки сосудов организма локализуется в почках (включая их микрососудистое русло и более крупные почечные сосуды) [2].
Установлено, что адгезия и миграция лейкоцитов положительно коррелируют с продолжительностью ишемии [6]. При этом ускоряется локальный тромбоз, связанный с экспрессией тканевого фактора лейкоцитарного происхождения, создаются условия для формирования микроагрегатов лейкоцитов [7]. Вышеописанные процессы приводят к функциональной недостаточности эндотелия сосудов почек, которую относят к критическим факторам развития системной воспалительной реакции [8]. В доступной литературе не обнаружено способов восстановления поврежденного эндотелия кровеносных сосудов почек при остром воспалительном процессе. В этой связи большой интерес вызвал Криопреципитат, получаемый из плазмы крови человека. Криопреципитат считается устаревшим в гематологической практике, в частности при гемофилии А, обусловленной врожденным дефицитом фактора свертывания крови VIII [9], но входит в протоколы по лечению массивных кровотечений, связанных с гипофибриногенемией (менее 1,0 г/л) [10].
Предполагается, что Криопреципитат может использоваться в терапии ряда заболеваний, в том числе связанных с инфекцией и воспалением [11]. Как известно, Криопреципитат обогащен высоко адгезивными белками: фибриногеном, фибронектином, фибринстабилизирующим фактором (фактором XIII), антигемофильным глобулином (фактором VIII) и фактором Виллебранда. В состав препарата входит и антитромбин III [12]. Согласно имеющимся данным, Криопреципитат способствует усилению гемостатических, регенераторных, противовоспалительных и иммуномодулирующих реакций в тканях [13]. Есть данные, что использование препарата позволяет активировать неоангиогенез [14], снизить интенсивность воспалительной реакции и макрофагальную защиту [15].
Цель исследования
Изучить эндотелиопротективные свойства Криопреципитата в рамках комплексной терапии гнойного пиелонефрита.
Материал и методы
В период с 2017 по 2018 г. на базе кафедры урологии и андрологии с курсами специализированной хирургии Алтайского государственного медицинского университета в городской больнице № 11 (Барнаул) проведено проспективное контролируемое рандомизированное когортное исследование с участием 30 больных (шести мужчин, 24 женщин) в возрасте от 20 до 45 лет с диагнозом «острый гнойный пиелонефрит». Работа одобрена локальным этическим комитетом Алтайского государственного медицинского университета (протокол № 14 от 18.11.2016), все участники подписали информированное согласие.
Критерии включения в исследование:
- пациенты обоего пола в возрасте от 20 до 45 лет;
- отсутствие гнойно-воспалительных процессов вне почечной локализации;
- отсутствие заболеваний крови и сердечно-сосудистой системы;
- признаки гнойного процесса в почках (карбункул почки, апостематозный пиелонефрит).
Критерии исключения:
- беременность;
- ВИЧ-инфекция, гепатиты В и С, иные иммунодефицитные и вирусные заболевания;
- вторичный пиелонефрит;
- абсцесс почки.
В рамках исследования все пациенты с гнойным пиелонефритом получали стандартное консервативное лечение – комплексную консервативную антибактериальную, дезинтоксикационную и противовоспалительную терапию. Использовались антибактериальные препараты широкого спектра действия: цефалоспорины третьего и четвертого поколения, фторхинолоны, аминогликозиды – как в монотерапии, так и в комбинации в зависимости от тяжести состояния пациента. Антибактериальную терапию продолжали в среднем в течение трех-четырех дней после нормализации температуры тела.
Рандомизация взятых в исследование пациентов осуществлялась с использованием генератора случайных чисел в программе Microsoft Excel. В результате больные были разделены на две группы, сопоставимые по возрасту, полу и этнической принадлежности.
Больным первой группы (n = 15) проводилась трансфузионная терапия Криопреципитатом, произведенным Алтайским краевым центром крови (Барнаул). Криопреципитат вводился внутривенно от трех до пяти доз в сутки в течение трех – пяти дней. Больным второй группы (n = 15) на третьи-четвертые сутки после поступления в стационар выполнялось оперативное вмешательство в объеме декапсуляции пораженной почки, предусматривающее вскрытие гнойного очага.
При поступлении в стационар и на шестые-седьмые сутки лечения оценивали тяжесть состояния, учитывая:
- время возникновения и выраженность клинических проявлений, длительность заболевания (в том числе время от повышения температуры тела и появления боли в поясничной области до госпитализации), эпизоды нарушения сознания;
- интенсивность боли в покое и при пальпации почек (динамика жалоб на боль в поясничной области оценивалась по 10-балльной Вербальной шкале оценки боли [16]), колебания температуры тела, артериального давления, частоты сердечных сокращений, частоты дыхательных движений, коморбидность и предшествующие заболевания;
- данные функциональных методов обследования (ультразвукового исследования с допплерографией, обзорной и внутривенной урографии, мультиспиральной компьютерной томографии, магнитно-резонансной томографии почек);
- наличие синдрома системного воспалительного ответа по ранее предложенным критериям [17];
- оценку органной недостаточности у пациентов с септическим процессом по упрощенной Шкале оценки органной недостаточности в динамике (Quick Sequential Organ Failure Assessment – qSOFA) [18].
Наряду с этим определялось содержание классических маркеров дисфункции эндотелия в плазме крови: эндотелина 1 (с использованием реактивов Endothelin (1–21), Biomedica) и фактора Виллебранда (с использованием реагента VWF:Ag, Siemens). В первом случае применялся фотометр для микропланшет Bio-Rad 680 (Bio-Rad), во втором – автоматический коагулометр Sysmex CA-1500 (Sysmex). Для получения допустимых значений изучаемых маркеров эндотелиопатии соответствующие исследования (по эндотелину 1 и фактору Виллебранда) проведены у десяти практически здоровых доноров 20–35 лет.
Взятие венозной крови осуществлялось из локтевой вены в пробирки Vacuette с буферным раствором цитрата натрия в соотношении 9:1 (9NC Coagulation sodium citrate 3,2%). Кровь центрифугировали при 1400 g в течение 15 минут при комнатной температуре. Перед проведением иммуноферментных анализов плазму хранили при температуре -40 оС в низкотемпературном холодильнике MDF-192 (Sanyo) от суток до месяца.
Данные расчета достоверности различия показателей до и после лечения статистически обрабатывались с помощью критериев Вилкоксона, Фишера. Сравнение между группами проводилось с помощью непараметрического метода U-теста Манна – Уитни. Критический уровень значимости различий (р) определен как р < 0,05.
Результаты
При оценке тяжести состояния у всех без исключения пациентов, включенных в исследование, был выявлен синдром системного воспалительного ответа. По шкале qSOFA 2 балла набрали два пациента первой группы и один пациент второй группы, 1 балл – по два пациента в каждой группе (признаки нарушения сознания во всех случаях отсутствовали). На шестые-седьмые сутки лечения в обеих группах признаков данного синдрома не обнаружено, состояние пациентов нормализовалось (0 баллов по шкале qSOFA).
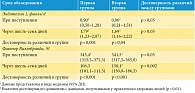
По итогам предварительного этапа, у десяти практически здоровых доноров устанавливалось содержание двух исследуемых в данной работе маркеров дисфункции эндотелия. Медиана уровня эндотелина 1 составила 0,29 фмоль/мл (95% ДИ 0,21–0,38), а содержания фактора Виллебранда – 96,9% (95% ДИ 92,8–101,0). Результаты оценки содержания и динамики изменения уровня данных маркеров эндотелиопатии в группах представлены в табл. 1. Значения медиан уровней эндотелина 1 и фактора Виллебранда у больных при поступлении в стационар превышали соответствующие значения практически здоровых людей в 3,1–3,3 и 3,5–3,6 раза соответственно. Эти данные свидетельствуют об интенсивном системном ответе эндотелия кровеносных сосудов на формирование патологического процесса, воспаление и инфекцию, связанные с развитием гнойного процесса в почках.
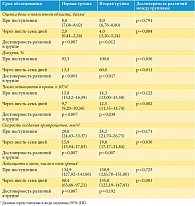
Была установлена разнонаправленная динамика рассматриваемых показателей. Так, наблюдалось стабильное увеличение уровня эндотелина 1 вне зависимости от проводимой терапии. В частности, после шести-семи дней лечения как в первой, так и во второй группе содержание эндотелина 1 превысило исходные (при поступлении в стационар) значения в 1,8–2,0 раза. Противоположная динамика наблюдалась в отношении уровня фактора Виллебранда. В первой группе (введение Криопреципитата) этот показатель снизился в 3,3 раза, а во второй группе (хирургическое вмешательство) – в 2,2 раза (полученные значения высоко достоверны, р < 0,002). Эти данные свидетельствуют о том, что применение Криопреципитата, несмотря на высокое содержание в составе препарата фактора Виллебранда, снижает уровень этого маркера в крови и, следовательно, оказывает эндотелиопротективное действие. Динамика других клинико-лабораторных показателей у больных гнойным пиелонефритом в зависимости от проводимого лечения представлена в табл. 2.
Положительный эффект от применения Криопреципитата в сравнении с оперативным лечением гнойного пиелонефрита проявился в уменьшении болевого синдрома, ослаблении дизурических симптомов, снижении числа лейкоцитов в моче и скорости оседания эритроцитов, отражающей в числе прочего выраженность воспалительной реакции. Наряду с этим у больных первой группы на шестые-седьмые сутки наблюдалась положительная динамика по данным ультразвукового исследования. Так, при поступлении у пациентов первой и второй групп отмечались признаки развития гнойного пиелонефрита и очаги гнойного процесса (карбункулы почки у пяти пациентов первой группы и шести больных второй группы, апостематозный пиелонефрит у шести и четырех пациентов соответственно). На шестые-седьмые сутки у пациентов первой группы определялись только диффузно-неоднородные изменения паренхимы почек, что подтверждало регресс гнойного процесса в почках. Во второй группе на шестые-седьмые сутки ультразвуковое исследование не проводилось из-за операционной раны. Срок пребывания в стационаре также отличался: в первой группе он составил 10,8 ± 1,6 суток, в то время как во второй группе – 12,3 ± 1,2 суток.
Обсуждение
Повреждение сосудистого эндотелия при сепсисе – краеугольный камень развития органной дисфункции, имеющей прямое отношение к исходам гнойного пиелонефрита. В настоящем исследовании прослежена динамика некоторых основных маркеров эндотелиопатии в ходе лечения гнойного пиелонефрита, в том числе с заменой оперативного вмешательства консервативной терапией, дополненным системным применением Криопреципитита, что привело к положительным результатам. Эти предварительные данные, полученные на небольшой когорте больных, требуют подтверждения в дальнейших исследованиях и потенциально могут послужить основой для изменения стандартов ведения пациентов с гнойным пиелонефритом.
Выводы
Применение Криопреципитата в составе консервативной терапии гнойного пиелонефрита оказывает эндотелиопротективное действие на кровеносные сосуды, способствуя ограничению воспалительного процесса и его регрессии.
Yu.G. Chernova, A.I. Neymark, DM, PhD, Prof., A.P. Momot, DM, PhD, Prof.
Altay State Medical University, Barnaul
Altay Branch of the Federal State Budgetary Institution "National Medical Research Center of Hematology", Barnaul
Contact person: Yuliya Gennadyevna Chernova, yulya.samchuk14@mail.ru
Purpose: to investigate endothelioprotective activity of Cryoprecipitate in the framework of complex therapy of purulent pyelonephritis.
Material and methods. From 2017 to 2018, it was conducted a prospective controlled randomized cohort study involving 30 patients aged 20 to 45 years with a diagnosis of acute purulent pyelonephritis at the Department of Urology and Andrology of the Altay State Medical University with courses of specialized surgery – City Hospital № 11 (Barnaul).
All patients received standard conservative therapy. The treatment of patients of the first group (n = 15) provided additional transfusion therapy with Cryoprecipitate produced by the Altay Regional Blood Center (Barnaul). Patients of the second group (n = 15) on the third-fourth day after hospitalization underwent surgical treatment of decapsulation of the affected kidney, with the opening of the purulent focus. Along with the complex examination, the content of classical markers of endothelial dysfunction in blood plasma – endothelin 1 (using reagents Endothelin (1–21), Biomedica) and von Willebrand factor (using reagent VWF:Ag, Siemens) was determined.
Results. Levels of endothelin 1 and von Willebrand factor in patients on admission to the hospital exceeded the corresponding values of healthy people (by median in 3.1–3.3 and 3.5–3.6 times respectively). The treatment revealed an increase in the level of endothelin 1, regardless of the therapeutic intervention characteristics.
In particular, after six to seven days of therapy in both the first and the second group, the content of endothelin 1 exceeded the initial values (when admitted to hospital) in 1.8–2.0 times. Von Willebrand factor in the first group (Cryoprecipitate) decreased in 3.3 times, while in the second group (surgery) only in 2.2 times (the values obtained are highly reliable, p < 0.002). These data indicate that the use of Cryoprecipitate, despite the high content in the composition of von Willebrand factor, reduces the level of this marker in the blood and therefore provide endothelioprotective effect.
Conclusions. The use of Cryoprecipitate in the composition of conservative treatment of purulent pyelonephritis has endothelioprotective effect on the blood vessels, helping to limit the inflammatory process and its regression.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.