Кардиоваскулярные эффекты ингибиторов ДПП-4 с точки зрения доказательной медицины. TECOS: много ответов, остались ли вопросы? Конгресс «Эндокринология Северо-Запада России – 2015». Сателлитный симпозиум компании MSD
- Аннотация
- Статья
- Ссылки


TECOS: результаты крупнейшего исследования по оценке сердечно-сосудистой безопасности ситаглиптина
Исследование TECOS (NCT00790205) – двойное слепое рандомизированное (1:1) плацебоконтролируемое клиническое исследование, предусматривающее оценку сердечно-сосудистых исходов у 14 671 пациента с сахарным диабетом (СД) типа 2 на фоне приема ситаглиптина 100 мг/сут по сравнению с приемом плацебо при добавлении их к проводимой более трех месяцев антидиабетической терапии (пероральные сахароснижающие препараты ± инсулин). Медиана длительности терапии составила три года1. Как отметил заведующий отделением терапевтических и хирургических методов лечения диабетической стопы Эндокринологического научного центра, д.м.н., профессор Гагик Радикович ГАЛСТЯН, исследование начато с некоторым опережением требований Управления по санитарному надзору за качеством пищевых продуктов и медикаментов, но в соответствии с ними. Дизайн исследования TECOS разработан независимыми группами специалистов из Университета Дьюка (США) и Оксфордского университета (Великобритания). Статистическая обработка результатов также проводилась названными выше группами.
На данный момент уже завершены два долгосрочных исследования со схожим дизайном, в которых оценивалась сердечно-сосудистая безопасность ингибиторов дипептидилпептидазы типа 4 (ДПП-4) – саксаглиптина (SAVOR-Timi) и алоглиптина (EXAMINE). Их результаты показали более высокую частоту госпитализаций по поводу хронической сердечной недостаточности (СН) у пациентов с СД типа 2 на фоне приема указанных препаратов.
Сравнивая эти два исследования с исследованием TECOS, профессор Г.Р. Галстян констатировал, что для исследования TECOS характерны максимальная длительность экспозиции на препарате (три года), сроки наблюдения (5,7 года) и число событий (1690).
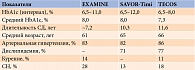
В исследовании TECOS также был выбран наиболее узкий интервал целевого уровня HbA1c – 6,5–8% по сравнению с исследованиями EXAMINE (6,5–11%) и SAVOR-Timi (6,5–12%), благодаря чему необходимости в частом изменении сахароснижающей терапии не возникало и минимизировалось влияние динамики гликемического контроля на сердечно-сосудистые исходы. Исходно средний уровень HbA1c у участников исследования TECOS составил 7,3%, EXAMINE и SAVOR-Timi – 8,0% (см. таблицу).
Длительность СД во всех трех исследованиях была достаточно высокой, однако наибольшей у участников исследования TECOS (11,6 против 7,2 года в EXAMINE и 10,3 года в SAVOR-Timi). Процентное соотношение пациентов с сопутствующими сердечно-сосудистыми рисками (артериальная гипертензия, дислипидемия, курение) во всех трех исследованиях было достаточно высоким. Наибольшее число больных, имеющих в анамнезе СН, было в исследовании EXAMINE (28%), поскольку в нем участвовали пациенты, перенесшие инфаркт миокарда (ИМ), наименьшее – в исследовании SAVOR-Timi (13%). В исследовании TECOS таких больных было 18%.
Таким образом, TECOS – крупное международное исследование, спланированное с целью сравнения влияния ситаглиптина с влиянием плацебо на частоту сердечно-сосудистых исходов при дополнении к стандартной терапии СД типа 2 в группах с минимальными различиями по показателям гликемии. При превышении целевого уровня HbA1c допускалась интенсификация сахароснижающей терапии. Доза зашифрованного препарата корректировалась в зависимости от показателей скорости клубочковой фильтрации (СКФ). В случае сниженной СКФ (от 30 до 50 мл/мин/1,73 м2) дозу ситаглиптина снижали до 50 мг.
Основная цель исследования TECOS – показать, что риск сердечно-сосудистых явлений у пациентов, получавших ситаглиптин в дополнение к стандартной терапии, не больше (non-inferior) риска, наблюдаемого у пациентов, получавших стандартную терапию без ситаглиптина.
В исследовании TECOS первичная комбинированная конечная точка – время до сердечно-сосудистой смерти, нефатального ИМ, нефатального инсульта, госпитализации по поводу нестабильной стенокардии. Это стало отличием исследования TECOS от двух других исследований. Следует отметить, что комитет по клиническим результатам, оценивающий компоненты конечных точек, не имел доступа к данным о распределении пациентов и проводил независимую оценку всех потенциальных сердечно-сосудистых событий. Вторичные комбинированные конечные точки – время до первичного события, входящего в состав первичной конечной точки, первый фатальный или нефатальный ИМ, первый фатальный или нефатальный инсульт, смерть от всех причин, госпитализация по поводу СН или сердечно-сосудистая смерть, динамика уровня HbA1c, изменение функции почек, расчетной СКФ, соотношения «альбумин/креатинин», у пациентов, не получавших инсулин исходно, – время до начала постоянной инсулинотерапии, у всех пациентов – время до начала применения следующего дополнительного препарата (следующий сахароснижающий препарат или постоянное применение инсулина), обращение за медицинской помощью (например, госпитализация, амбулаторный визит).
Основные критерии включения в исследование TECOS:
1) СД типа 2 (HbA1c ≥ 6,5% и ≤ 8,0%);
2) стабильная монотерапия, или двойная комбинированная терапия с применением метформина, пиоглитазона или препаратов сульфонилмочевины, или стабильная доза инсулина в сочетании с метформином или без него;
3) возраст ≥ 50 лет;
4) сердечно-сосудистое заболевание в анамнезе, которое устанавливали при наличии:
-
ИМ;
-
коронарной реваскуляризации;
-
коронарной ангиографии с выявлением не менее одного стеноза ≥ 50%;
-
ишемического инсульта;
-
поражения сонных артерий со стенозом ≥ 50%;
-
заболевания периферических артерий с объективными симптомами;
5) способность посещать работников здравоохранения не реже двух раз в год.
Критерии исключения:
1) СД типа 1 или кетоацидоз в анамнезе;
2) два и более эпизода тяжелой гипогликемии в течение 12 месяцев до включения в исследование;
3) расчетная СКФ < 30 мл/мин/1,73 м2;
4) применение другого ингибитора ДПП-4, аналога глюкагоноподобного пептида 1 (ГПП-1) или тиазолидиндиона, кроме пиоглитазона, в течение предшествующих исследованию трех месяцев;
5) цирроз печени;
6) запланированное вмешательство с целью реваскуляризации;
7) беременность или планирование беременности.
Важно подчеркнуть, что 95% участников завершили исследование.
Среди пациентов преобладали мужчины – 70%. Индекс массы тела больных составил 30,2 ± 5,6 кг/м2, СКФ – 74,9 мл/мин/1,73 м2.
Участников рандомизировали на две группы: группу ситаглиптина (n = 7332) и группу плацебо (n = 7339). Группы были равнозначны по наличию предшествующих сердечно-сосудистых заболеваний (73,6 и 74,5%), длительности заболевания и уровню HbA1c (7,2%). На монотерапии находились около 48% пациентов, двойную комбинированную терапию получали около 51% пациентов.
Исследование предусматривало достижение одинаковых показателей HbA1c в группах.
Влияние гликемии на риск развития сердечно-сосудистых событий исключалось.
Тем не менее была получена небольшая, статистически достоверная, но клинически не значимая разница между группами в отношении динамики показателей HbA1c. К концу исследования она составила менее 0,29% (p < 0,0001). Это было достигнуто благодаря интенсификации сахароснижающей терапии в обеих группах, которая достоверно (р < 0,001) чаще проводилась у пациентов группы плацебо. Пациенты группы ситаглиптина значительно позже прибегали к инсулинотерапии по сравнению с пациентами группы плацебо. Важно и то, что частота тяжелой гипогликемии была сопоставимой – 2,2 и 1,9% соответственно.
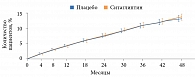
Анализ первичной комбинированной конечной точки продемонстрировал идентичность показателей в обеих группах (рис. 1). Так, частота госпитализаций по поводу нестабильной стенокардии в группе ситаглиптина составила 1,5% случаев, в группе плацебо – 1,6%. В целом компоненты первичной конечной точки зафиксированы у 11,4% пациентов в группе ситаглиптина и у 11,6% пациентов в группе плацебо. Отношение рисков (ОР) составило 0,98 при 95%-ном доверительном интервале (ДИ) 0,88–1,09.
Таким образом, при анализе первичной комбинированной конечной точки ситаглиптин не уступал плацебо и не превосходил его.
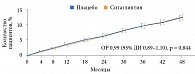
Аналогичный результат получен и в отношении вторичной комбинированной конечной точки (рис. 2).
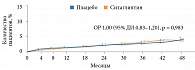
По словам профессора Г.Р. Галстяна, основная интрига исследования TECOS заключалась в том, каковы будут результаты показателя «госпитализация вследствие СН», поскольку в исследовании SAVOR-Timi отмечено достоверное его повышение (на 27%), а в исследовании EXAMINE – недостоверное (на 19%). «С моей точки зрения, результаты исследования TECOS позволили в значительной степени вздохнуть свободно, потому что данный параметр был абсолютно идентичен в обеих группах, то есть больные, получавшие ситаглиптин, и больные, получавшие плацебо, имели одинаковую частоту госпитализаций по поводу СН. Это является очень важным сигналом для медицинского сообщества о том, что ситаглиптин имеет профиль сердечно-сосудистой безопасности», – пояснил докладчик (рис. 3).
ОР по данному показателю составило 1,0 при верхней границе 1,2.
Во всех трех исследованиях не продемонстрировано достоверного повышения частоты случаев острого панкреатита. Так, в исследовании TECOS подтвержденные случаи панкреатита были редкими, но в числовом выражении встречались чаще в группе ситаглиптина, чем в группе плацебо (23 случая против 12 соответственно). Важные данные получены в отношении риска развития рака поджелудочной железы. Рак поджелудочной железы чаще выявляли в группе плацебо, чем в группе ситаглиптина (14 случаев против 9 соответственно). По другим злокачественным новообразованиям различий в группах не отмечено.
Аналогичная тенденция наблюдалась при анализе частоты развития серьезных нежелательных явлений. Частота инфекций и смертей от них в группах не различалась.
На основании результатов исследования TECOS можно констатировать, что терапия ситаглиптином не уступает стандартной сахароснижающей терапии и не превосходит ее. Добавление ситаглиптина к сахароснижающей терапии оказалось безопасным в отношении риска развития нового сердечно-сосудистого события.
TECOS: от теории к практике. Ситаглиптин как универсальный инструмент в оркестре сахароснижающей терапии
Когда говорят о СД типа 2, ни у кого не вызывает сомнений, что речь идет о масштабном многофакторном заболевании. Поэтому, по мнению начальника кафедры военно-полевой терапии Военно-медицинской академии, главного эндокринолога Комитета по здравоохранению Санкт-Петербурга, д.м.н., профессора Юрия Шавкатовича ХАЛИМОВА, управление заболеванием должно включать целый комплекс мероприятий: обучение и самоконтроль, нормализацию углеводного обмена без риска гипогликемии, коррекцию факторов риска развития сердечно-сосудистых заболеваний, снижение массы тела. Если эти мероприятия оказываются неэффективными, приходится лечить сосудистые осложнения СД.
Современное управление СД типа 2 предусматривает индивидуальный подход к определению целей и выбору сахароснижающего препарата. Приоритетом в выборе сахароснижающего средства должны стать эффективность и безопасность в отношении риска развития гипогликемии, а также отсутствие влияния на массу тела, удобство приема, доступность, наличие плейотропных эффектов, возможность комбинации с другими пероральными препаратами, долгосрочность эффекта, благоприятное влияние на течение СД и клинические исходы. В связи с вышесказанным именно ингибиторы ДПП-4, в частности ситаглиптин, являются наиболее оптимальными препаратами для персонифицированной терапии.
Ингибиторы ДПП-4 воздействуют на патогенетический механизм СД, регулируют секрецию глюкагона в глюкозозависимом режиме. В экспериментальных условиях доказано их положительное влияние на массу и функцию бета-клеток. Не меньший интерес представляют негликемические эффекты ингибиторов ДПП-4, большая часть которых независима от глюкагоноподобного пептида 1: влияние на артериальное давление, липиды, факторы воспаления, эндотелий, кардиомиоциты. Как следствие, возможность предупреждать развитие и прогрессирование микроангиопатии. Важно отметить, что исследования в этом направлении продолжаются.
В настоящее время зарегистрировано пять препаратов ингибиторов ДПП-4: ситаглиптин, вилдаглиптин, саксаглиптин, линаглиптин и алоглиптин. Они различаются прежде всего химической структурой и периодом полувыведения. Практически все они достигают максимального эффекта к концу первых суток применения. Однако сравнительная характеристика по ингибирующей активности от 0 до 96 часов после приема последней дозы препарата продемонстрировала их неоднородность. Только ситаглиптин показывает долгосрочный ингибирующий эффект – до 48 часов. Можно предположить, что это станет преимуществом для пациентов, которые обладают низкой комплаентностью.
Одним из признанных международных алгоритмов лечения СД типа 2 считается совмеcтный консенсус Американской диабетической ассоциации и Европейской ассоциации по изучению диабета, обновленный вариант которого опубликован в 2015 г. Если рассмотреть представленные в консенсусе шесть основных классов препаратов, большинство из них – и метформин, и сульфонилмочевина, и даже новая группа ингибиторов натрий-глюкозного котранспортера 2 имеют некоторые ограничения при выборе, за исключением ингибиторов ДПП-4.
Ингибиторы ДПП-4 являются идеальным партнером для метформина. Согласно данным ретроспективного анализа, проведенного с использованием крупной электронной базы данных медицинских записей США (n = 12 566), старт терапии с комбинации «метформин + ситаглиптин (Янумет)» позволяет сохранить более чем на полгода достигнутый сахароснижающий эффект по сравнению со стартом с монотерапии метформином2.
Другое исследование показало, что сахароснижающее действие комбинированной терапии, включающей ситаглиптин и метформин, и комбинированной терапии препаратом сульфонилмочевины (глимепиридом) и метформином сопоставимо3. Целевой уровень HbA1c < 7% был достигнут в 63 и 59% случаев соответственно. При этом комбинация «ситаглиптин + метформин» способствовала снижению на 104-й неделе массы тела на 2,3 кг и частоты гипогликемических эпизодов в шесть раз (по сравнению с комбинацией «сульфонилмочевина + метформин»).
Гипогликемия является основной причиной госпитализации больных СД. Во французском нерандомизированном открытом многоцентровом трехлетнем исследовании реальной клинической практики Odyssee первичной целью стало сравнение продолжительности терапии СД типа 2 ситаглиптином или препаратами сульфонилмочевины в комбинации с метформином, вторичными – изменение уровня HbA1c, массы тела и частоты случаев симптоматической гипогликемии у больных СД типа 24. Пациенты первой группы (n = 1874) принимали ситаглиптин с метформином, второй (n = 733) – препараты сульфонилмочевины (в подавляющем большинстве Гликлазид МВ) с метформином.
Оба вида терапии показали умеренный сахароснижающий эффект – за 36 месяцев наблюдения уровень HbA1c снизился на 0,6%, однако количество эпизодов симптоматической гипогликемии в группе «ситаглиптин + метформин» было в два раза меньше, чем в группе «препарат сульфонилмочевины + метформин» – 9,7 против 21% случаев соответственно.
В крупном наблюдательном ретроспективном когортном двухлетнем исследовании, проведенном в Великобритании, целью которого стала оценка частоты развития гипогликемических осложнений и клинических исходов у 253 690 пациентов, показано преимущество включения в схему лечения ингибиторов ДПП-45. Применение препаратов сульфонилмочевины с метформином сопровождалось повышением частоты эпизодов гипогликемии в четыре раза через 12 месяцев и в пять раз через 24 месяца (по сравнению с комбинацией «ингибиторы ДПП-4 + метформин»).
Из-за оптимального сочетания эффективности и безопасности ингибиторы ДПП-4 наряду с метформином были внесены в национальные и международные рекомендации как препараты для старта терапии СД типа 2. Ингибиторы ДПП-4 также являются препаратами второй и третьей линии в случае, если не назначались ранее, а также у пожилых пациентов (алгоритмы Международной федерации диабета за 2013 г.). К преимуществам использования ситаглиптина, саксаглиптина и линаглиптина у пожилых больных относятся однократный прием, безопасность при снижении функции почек, низкий риск развития гипогликемии.
По словам профессора Ю.Ш. Халимова, ингибиторы ДПП-4 являются перспективными препаратами для комбинации с инсулином. Ингибиторы ДПП-4 на сегодняшний день могут активно использоваться в пошаговой интенсификации инсулинотерапии для продолжительного контроля СД типа 2. Доказано, что терапия ситаглиптином в дозе 100 мг/сут у пациентов с СД типа 2 и неудовлетворительным гликемическим контролем при использовании схемы «инсулин + метформин» способствует снижению дозы инсулина на 5 ЕД и сопровождается сокращением числа случаев гипогликемий6. Полученные данные позволили сделать вывод: добавление ситаглиптина к инсулину у пациентов с неудовлетворительной компенсацией диабета обеспечивает достижение цели на меньшей дозе инсулина, улучшение качества гликемического контроля, уменьшение числа гипогликемических эпизодов. При этом терапия не приводит к повышению массы тела и хорошо переносится.
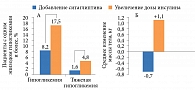
В другом исследовании пациентов, применявших базальный инсулин, распределили в группу инсулинотерапии с добавлением ситаглиптина в дозе 100 мг/сут (n = 70) и группу инсулинотерапии с режимом повышения дозы инсулина (n = 70). Добавление ситаглиптина к инсулину оказалось более эффективным, чем титрация дозы базального инсулина, в отношении снижения уровня HbA1c – -0,42 против -0,22% соответственно через 24 недели терапии. Кроме того, на фоне применения комбинации «ситаглиптин + инсулин» отмечено сокращение в два раза числа эпизодов гипогликемии и в три раза случаев тяжелой гипогликемии при положительном влиянии на массу тела (-1,8 кг, р < 0,05) (рис. 4).
Было также доказано, что добавление ситаглиптина к инсулинотерапии уменьшает вариабельность гликемии вследствие снижения уровня прандиальной и постпрандиальной гликемии без повышения риска развития гипогликемии и увеличения массы тела. Это способствовало улучшению гликемического контроля, снижению потребности в инсулине, риска сердечно-сосудистых осложнений и, возможно, микроангиопатии, а также более долгосрочному гликемическому контролю.
На сегодняшний день имеются данные целого ряда широкомасштабных исследований реальной клинической практики, демонстрирующие высокий уровень безопасности сахароснижающей терапии ситаглиптином.
Важная информация о кардиопротективных свойствах ингибиторов ДПП-4 в целом и ситаглиптина в частности получена при ретроспективном анализе датского регистра (2007–2011 гг.), включавшего 40 028 больных СД типа 2 без предшествующего ИМ, перенесенного ранее инсульта7.
Пациенты получали метформин с препаратами сульфонилмочевины, ингибиторами ДПП-4, агонистами ГПП-1 или инсулин. Отмечено изменение терапевтических предпочтений: снижение доли пациентов, использовавших комбинацию «метформин + препараты сульфонилмочевины», и увеличение доли пациентов, принимавших комбинацию «ситаглиптин + метформин» (до 61,9%). На фоне последней ОР общей смертности снизилось на 35%, сердечно-сосудистой – на 43%, комбинированных конечных точек (ИМ, инсульт, сердечно-сосудистые события) – на 30%.
Данные о кардиальных аспектах использования ситаглиптина были получены после завершения крупного исследования TECOS1. Доказано, что с помощью интенсивного контроля гликемии возможно снизить сердечно-сосудистые риски, однако для этого требуется несколько лет.
Как показал анализ результатов исследований SAVOR-Timi, EXAMINE и TECOS, ситаглиптин обладает самым высоким профилем безопасности по сравнению с саксаглиптином и алоглиптином. Отмечены его преимущества в отношении сердечно-сосудистой безопасности, снижения риска хронической СН, улучшения гликемического контроля и снижения частоты эпизодов гипогликемии, а также в отношении сокращения дозы инсулина и риска развития панкреатита, рака поджелудочной железы.
Серьезным осложнением СД является диабетическая нефропатия, которая может привести к развитию почечной недостаточности. Нефропротективные свойства ситаглиптина также изучались в ряде исследований. Так, в японском рандомизированном контролируемом исследовании приняли участие 85 пациентов с СД типа 2, средний возраст которых составил 64,2 года8. Цель исследования – оценить влияние ситаглиптина на микроальбуминурию. Полученные результаты позволили сделать вывод: ситаглиптин наряду с улучшением гликемического контроля оказывает протективный эффект – предотвращает прогрессирование альбуминурии.
Согласно экономическим расчетам, только в 2013 г. на покупку ситаглиптина (Янувия) и комбинации ситаглиптина с метформином (Янумет) в мире было израсходовано свыше 80 млрд долл. США, что составляет более 50% финансовых затрат. «Анализ за 2014 г. показал, что эта тенденция сохраняется, и с каждым годом в мире увеличивается число пациентов, использующих данные препараты. Это показатель того, что мы с вами все чаще делаем выбор в пользу новой и безопасной терапии ингибиторами ДПП-4», – отметил профессор Ю.Ш. Халимов.
Заключение
Результаты многолетнего исследования TECOS подтверждают профиль сердечно-сосудистой безопасности ситаглиптина у больных с высоким риском сердечно-сосудистых осложнений: отсутствие статистически достоверных различий по показателю частоты комбинированных сердечно-сосудистых событий (смерти от сердечно-сосудистых заболеваний, нефатального ИМ, нефатального инсульта, нестабильной стенокардии, требующей госпитализации) по сравнению с традиционным лечением. Было также продемонстрировано отсутствие увеличения числа госпитализаций по поводу СН в группе пациентов, получавших ситаглиптин, по сравнению с пациентами контрольной группы, получавшими плацебо.
Представленные данные многочисленных исследований реальной клинической практики доказали, что ситаглиптин в моно- и комбинированной терапии способствует улучшению гликемического контроля, снижению потребности в инсулине, риска сердечно-сосудистых осложнений и, следовательно, является универсальным препаратом для персонифицированной терапии СД.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.