Климактерический синдром, расстройства сна и мелатонин
- Аннотация
- Статья
- Ссылки
- English
Однако в постменопаузе секреция мелатонина снижена у женщин как с нарушениями сна, так и без таковых. Женщинам в возрасте от 45 до 60 лет можно рекомендовать прием препаратов мелатонина в дозе 3 мг в вечернее время и светотерапию в ранние утренние часы в спектре «голубой волны» по 15–20 минут, что позволит нормализовать секрецию мелатонина и улучшить качество жизни.
Однако в постменопаузе секреция мелатонина снижена у женщин как с нарушениями сна, так и без таковых. Женщинам в возрасте от 45 до 60 лет можно рекомендовать прием препаратов мелатонина в дозе 3 мг в вечернее время и светотерапию в ранние утренние часы в спектре «голубой волны» по 15–20 минут, что позволит нормализовать секрецию мелатонина и улучшить качество жизни.
Введение
В жизни каждой женщины наступает переходный период от репродуктивной фазы к постменопаузе – климактерий (климакс, климактерический период, от греч. climacter – ступень лестницы). В течение этого периода на фоне возрастных изменений в репродуктивной системе доминируют инволюционные процессы, характеризующиеся постепенным снижением и «выключением» функции яичников: сначала репродуктивной, а затем и гормональной, что проявляется прекращением фертильности и менструации [1].
По данным зарубежных исследователей, в период менопаузы те или иные проблемы, связанные со сном, отмечают от 25 до 50% женщин (для сравнения, в фертильном возрасте 15%) [2, 3]. Большинство ученых связывают это с гормональными и метаболическими изменениями, происходящими в организме женщины.
Женщины в целом страдают нарушениями сна чаще, чем мужчины, с возрастом гендерные различия частоты нарушений сна становятся все более значимыми [4]. И у мужчин, и у женщин ухудшаются показатели эффективности сна, увеличивается время засыпания и бодрствования после засыпания, значимо снижается время быстрого сна [5]. Однако, по данным анализа структуры сна 50–60-летних людей, у женщин по сравнению с мужчинами больше число пробуждений, меньше представленность глубоких стадий фаз медленного и быстрого сна, увеличена длительность первой стадии медленноволновой фазы сна. Таким образом, паттерн сна у женщин в климактерическом периоде свидетельствует о большей фрагментированности, нарушении сегментарной организации и ухудшении эффективности сна [6].
Причины нарушения сна у женщин в климактерическом периоде
С возрастом цикл «сон – бодрствование» у женщины претерпевает существенные метаморфозы, что связано с физиологическими изменениями в органах и тканях организма при старении, прежде всего дегенерацией нейронов головного мозга. Подобные изменения архитектуры сна у женщин во многом обусловлены изменением гормонального статуса при наступлении менопаузы.
Одну из основных ролей в регуляции циркадианных ритмов отводят эпифизу и вырабатываемому им гормону мелатонину. Известны возрастные особенности секреции мелатонина, которые затрагивают не только уровень, но и суточную кривую выработки данного гормона [7]. Предполагают, что изменение секреции мелатонина при наступлении и развитии менопаузы влияет на метаболические процессы и способствует формированию различных заболеваний, в частности нарушений сна [8]. При этом уровень секреции гормона мелатонина коррелирует со степенью тяжести климактерического синдрома [9].
Помимо многообразия биологических регуляторных эффектов мелатонин обладает антиоксидантной активностью, играет важную роль в развитии окислительного стресса [10]. В предыдущих исследованиях нами было показано, что у женщин наблюдаются повышение активности процессов перекисного окисления липидов и угнетение системы антиоксидантной защиты, наиболее выраженное в период постменопаузы [11].
Доказано, что у женщин с сохраненным менструальным циклом половые гормоны влияют на сон. Так, прогестерон оказывает прямой седативный эффект, стимулируя бензодиазепиновые рецепторы, что способствует повышению активности гамма-аминомасляной кислоты – важнейшего тормозного медиатора, ответственного за наступление сна [12].
Механизм влияния на процесс сна эстрогенов сложнее, чем прогестерона. Показано, что эстрогены удлиняют фазу быстрого сна, уменьшают время засыпания и общее количество спонтанных пробуждений в течение ночи, увеличивают общую продолжительность сна. Доказано, что при проведении гормональной заместительной терапии у женщин в климактерическом периоде увеличивается представленность глубоких стадий медленноволновой фазы сна и фазы быстрого сна, следовательно, улучшается качество сна [13].
Эстрогены участвуют в процессе терморегуляции и способствуют поддержанию наиболее низкой температуры тела в течение ночи. При их дефиците возникает недостаточное снижение ночной температуры тела, что ведет к нарушениям структуры сна – его фрагментации и увеличению представленности поверхностных стадий.
Доказано, что менопауза ассоциирована со смещением пика выработки кортизола во время сна на более раннее время [14]. Эстрогены помогают регулировать время выработки кортизола во время сна и тем самым нормализовать его паттерн, улучшать качество бодрствования и настроение. Кроме того, эти гормоны могут оказывать прямое влияние на настроение через рецепторы в центральной нервной системе за счет модуляции активности нейротрансмиттеров (серотонина и норадреналина). Эстрогены увеличивают как количество постсинаптических серотониновых рецепторов, так и их чувствительность. Они являются агонистами некоторых рецепторов серотонина и гамма-аминомасляной кислоты, также селективно усиливают активность норадреналина в головном мозге за счет снижения активности моноаминоксидазы. Все эти эффекты эстрогенов предполагают возможность их использования в качестве антидепрессантов [15].
Исходя из вышеизложенного, логично предположить, что нарушения сна у женщин в климактерическом периоде могут быть обусловлены как дегенеративными процессами в головном мозге при физиологическом старении, так и инволютивными гормонально-метаболическими изменениями.
Исследования эффективности сна у женщин в климактерическом периоде
L. Maartens и соавт. (2011) провели анкетирование женщин разного возраста и выявили, что жалобы на нарушение сна чаще предъявляют женщины, находящиеся в периоде пери- и постменопаузы [16].
Проспективное крупномасштабное исследование, выполненное учеными Медицинского университета г. Лексингтон (США) среди лиц в возрасте от 47 до 69 лет, показало, что основным симптомом инсомнии у женщин в постменопаузе (физиологической или хирургической) было затрудненное засыпание [17].
Вместе с тем неожиданными оказались результаты Wisconsin Sleep Cohort Study, в рамках которого оценивалось качество сна у женщин в пременопаузе, пери- и постменопаузе (n = 589). Использовались такие методы, как полисомнография и ведение дневника сна в течение четырех – восьми лет [18]. По данным анкетирования в пре- и перименопаузе значительного ухудшения качества сна не отмечалось. Анализ мониторирования в течение ночи показателей полисомнографии показал, что эффективность сна (удлинение общего времени сна и медленноволновой фазы сна) в период постменопаузы и перименопаузы была выше, чем в пременопаузе.
Большое количество работ посвящено роли вазомоторных симптомов, возникающих при нарушении вегетативной регуляции гипоталамуса, обусловленных изменением гормонального статуса у женщин в климактерическом периоде, в генезе инсомнии. Так, по данным Y. Erlik и соавт. (1981), существует взаимосвязь между частотой ночных «приливов» и количеством пробуждений во время сна [19]. Впоследствии J. Shaver и соавт. (1988) обнаружили, что одним из немногочисленных различий, по данным полисомнографии, у женщин с различным менопаузальным статусом (пре-, пери- и постменопаузой) является уменьшение эффективности сна на фоне выраженных вазомоторных реакций [20].
В ходе исследования, проведенного среди женщин в постменопаузальном периоде, S. Woodward и R. Freedman (1994) выявили статистически значимое снижение эффективности сна (до 95–90%), изменение архитектуры сна и более продолжительное время бодрствования в течение ночи у женщин, предъявляющих жалобы на «приливы» [21].
Роль нарушения вегетативной регуляции у женщин климактерического периода в генезе симптомов инсомнии подтверждается положительным эффектом заместительной гормональной терапии на процесс поддержания сна, его продолжительность и эффективность [22].
Результаты собственного исследования структуры нарушений сна у женщин в климактерическом периоде
В Сомнологическом центре Научного центра проблем здоровья семьи и репродукции человека (Иркутск) нами было проведено исследование структуры нарушений сна у женщин в климактерическом периоде.
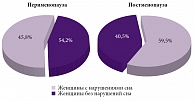
Анализ данных анкетирования по опроснику Стэнфордского центра изучения сна показал, что из 146 женщин, включенных в исследование, около половины опрошенных (n = 69, 47,2%) не предъявляли жалоб на нарушения сна (рис. 1).
Был проведен детальный анализ данных анкетирования женщин с нарушениями сна (n = 77, 52,8%). Частота нарушений сна оказалась выше у женщин в постменопаузе, чем в перименопаузе, – 59,5 против 45,8%.
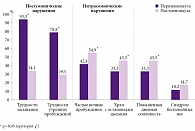
В перименопаузе женщины чаще всего предъявляли жалобы на трудности засыпания (более 20 минут от момента выключения света) (n = 31, 93,3%) и ранние утренние пробуждения (n = 26, 78,8%). В постменопаузе женщин больше всего беспокоили ночные пробуждения (два и более раз за время ночного сна) – 25 (54,9%) случаев (данное нарушение отмечалось у 14 (42,4%) женщин в перименопаузе, p < 0,001) (рис. 2).
Учитывая данные оценки субъективной выраженности симптомов инсомнии, было определено среднее значение индекса тяжести инсомнии. У женщин в перименопаузе этот показатель равнялся 21,3 ± 0,54, а в постменопаузе – 24,8 ± 0,31 (p > 0,05), что в обоих случаях соответствует выраженным нарушениям сна. Несмотря на отсутствие статистически значимых различий, наблюдается тенденция роста данного индекса и соответственно выраженности инсомнических расстройств по мере прогрессирования менопаузы.
Со слов окружающих, жалобы на храп и остановки дыхания во время сна чаще наблюдались у женщин в постменопаузе, чем в перименопаузе: 20 (45,5%) и 8 (33,3%) случаев соответственно (p < 0,001).
Можно предположить, что для женщин в перименопаузальном периоде наиболее характерны пресомнические и постсомнические расстройства, в то время как в постменопаузе доминируют интрасомнические нарушения.
Сравнительный анализ данных анкетирования показал, что суммарный балл по шкале оценки дневной сонливости Эпворта оказался у женщин в постменопаузе в 1,63 раза выше, чем у женщин в перименопаузе: 19,93 ± 0,78 против 12,2 ± 0,42 (p < 0,05). Это позволило предположить наличие более тяжелой степени синдрома обструктивного апноэ сна у женщин в постменопаузальном периоде.
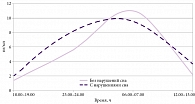
Нами было также определено содержание мелатонина в слюнной жидкости в разное время суток, что дало возможность составить представление о циркадианном ритме секреции данного гормона у женщин в разные фазы климактерия в зависимости от наличия у них нарушений сна (рис. 3).
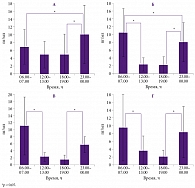
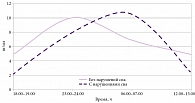
У женщин в перименопаузе, не имеющих нарушений сна, наибольшее содержание мелатонина отмечалось в ночные часы – 10,03 ± 7,38 пг/мл (рис. 4). К утру уровень мелатонина снижался до 6,86 ± 4,42 пг/мл, в дневные и вечерние часы составлял 4,91 ± 3,36 и 4,94 ± 5,20 пг/мл соответственно. Такая суточная секреция мелатонина является физиологической. У пациенток с нарушениями сна секреция мелатонина в течение суток была изменена. Самый высокий уровень данного гормона был зарегистрирован в утренние часы – 10,52 ± 6,20 пг/мл. Концентрация мелатонина у пациенток с нарушениями сна в дневные, вечерние и ночные часы была ниже, чем у пациенток без нарушений сна, в 2,2 (p < 0,05), 2,3 (p < 0,05) и 1,3 раза соответственно. При этом в утренние часы уровень мелатонина у женщин с нарушениями сна был в 1,5 раза выше (p < 0,05), чем у женщин без нарушений сна.
У женщин в постменопаузе без нарушений сна наивысший пик секреции мелатонина приходился на утренние часы – 11,02 ± 8,16 пг/мл (рис. 5). В дневные и вечерние часы содержание мелатонина понижалось до 2,21 ± 1,16 и 1,42 ± 1,30 пг/мл соответственно. К ночи уровень гормона значимо повышался до 5,66 ± 2,25 пг/мл относительно вечернего времени. У женщин с нарушениями сна отмечалась похожая тенденция распределения секреции мелатонина. В ранние утренние и ночные часы содержание мелатонина было наибольшим и составляло 9,54 ± 8,49 и 8,29 ± 6,59 пг/мл соответственно. В дневные и вечерние часы уровень мелатонина практически не отличался – 3,60 ± 3,78 и 2,02 ± 1,79 пг/мл соответственно.
Таким образом, в перименопаузе нарушения сна связаны с измененной секрецией мелатонина в течение суток. Однако в постменопаузе данной связи не выявлено: снижение секреции мелатонина наблюдалось как при нарушениях сна, так и без таковых. С биоритмологической позиции климактерический синдром характеризуется клинической реализацией дезадаптации организма женщины в условиях, требующих повышенной активности адаптивной системы организма. При наступлении менопаузы у женщин с нарушениями сна и соответственно климактерическим синдромом можно говорить о связи дезадаптации с пониженным уровнем мелатонина в организме. В постменопаузе на формирование дезадаптивных процессов у женщин, вероятно, оказывают влияние другие факторы.
Выводы
Изучение особенностей циркадианного ритма секреции мелатонина как одного из основных регуляторов процесса сна и установление патогенетической роли мелатонина в формировании нарушений сна у женщин климактерического периода позволили нам разработать патогенетические рекомендации по коррекции нарушений сна у женщин в климактерическом периоде и патогенетически обосновать применение препаратов мелатонинового ряда в качестве заместительной таргетной терапии нарушений сна.
С целью нормализации и сдвига хронобиологических ритмов секреции мелатонина женщинам в климактерическом периоде мы рекомендуем проводить терапию препаратами мелатонина (прием в дозе 3 мг в вечерние часы) и светотерапию в ранние утренние часы в спектре «голубой волны» по 15–20 минут. Показано, что прием 3 мг мелатонина в течение трех – шести месяцев позволяет повысить качество и продолжительность сна, снизить уровень лютеинизирующего и фолликулостимулирующего гормонов, восстановить овариальный цикл, значительно улучшить функцию щитовидной железы, уменьшить частоту «горячих приливов» с сердцебиением, полностью исключить утреннюю депрессию и улучшить настроение [23].
Представленный в России лекарственный препарат мелатонина Мелаксен («Юнифарм Инк.», США) широко применяется в качестве адаптогена для нормализации биологических ритмов [24]. Результаты нашего исследования позволяют рекомендовать использовать этот препарат в гинекологической эндокринологии для коррекции нарушений сна при климактерическом синдроме у женщин в возрасте от 45 до 60 лет.
I.M. Madayeva, N.V. Semenova, I.N. Danusevich, L.I. Kolesnikova
Scientific Center for Family Health and Human Reproduction Problems, Irkutsk
Contact person: Irina Mikhaylovna Madayeva, nightchild@mail.ru
From 25 to 50% of women with menopause have different problems with sleep in comparison with 15% fertile ones. We studied the diurnal secretion of melatonin in women in different phases of climax. In premenopausal women disordered sleep is associated with changes of daily melatonin secretion, but in postmenopausal state melatonin secretion decreases in both sleep disorders and control groups. The use of 3 mg melatonin in women from 45 to 60 years during dim light and 15–20 min of bright light therapy in the morning could be recommended for improving sleep in these patients.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.