Комбинированная терапия гастроэзофагеальной рефлюксной болезни
- Аннотация
- Статья
- Ссылки
- English
Материал и методы. Обследовано 40 больных ГЭРБ с рефлюкс-эзофагитом. Больные были рандомизированы на две группы: 19 больных первой группы (8 мужчин и 11 женщин, возраст – 48,0 [39,0;60,5] лет) получали комбинированную терапию: пантопразол 40 мг в сутки и Альфазокс 10 мл четыре раза в день; 21 пациент второй группы (13 мужчин и 8 женщин, возраст – 47,0 [33,0; 64,0] лет) получали пантопразол 40 мг в сутки. Продолжительность терапии составила 28 дней. Оценивали динамику частоты и выраженности симптомов заболевания по шкале Likert. По данным эзофагогастродуоденоскопии оценивали эффективность лечения эрозивного эзофагита.
Результаты. Отмечены преимущества в уменьшении выраженности симптомов в первой группе. В первый день комбинированного лечения изжога купирована у 64% пациентов (критерий χ2, р < 0,05). К четвертому дню лечения в этой группе изжога сохранялась у 11% больных и у 42% пациентов, получавших монотерапию пантопразолом (критерий χ2, р < 0,05). Комбинированная терапия была более эффективна в снижении выраженности и частоты возникновения отрыжки и дисфагии (критерий Вилкоксона, p < 0,01, критерий χ2, р < 0,05). На фоне комбинированной терапии у всех больных достигнута эндоскопическая ремиссия рефлюкс-эзофагита, у 25% больных в контрольной группе сохранялись эрозии слизистой оболочки пищевода (критерий χ2, р = 0,033).
Выводы. Проведенное исследование показало преимущества комбинированной терапии (ИПП + Альфазокс) как в достижении симптоматического ответа, так и в улучшении эндоскопической картины у пациентов с эрозивным рефлюкс-эзофагитом.
Материал и методы. Обследовано 40 больных ГЭРБ с рефлюкс-эзофагитом. Больные были рандомизированы на две группы: 19 больных первой группы (8 мужчин и 11 женщин, возраст – 48,0 [39,0;60,5] лет) получали комбинированную терапию: пантопразол 40 мг в сутки и Альфазокс 10 мл четыре раза в день; 21 пациент второй группы (13 мужчин и 8 женщин, возраст – 47,0 [33,0; 64,0] лет) получали пантопразол 40 мг в сутки. Продолжительность терапии составила 28 дней. Оценивали динамику частоты и выраженности симптомов заболевания по шкале Likert. По данным эзофагогастродуоденоскопии оценивали эффективность лечения эрозивного эзофагита.
Результаты. Отмечены преимущества в уменьшении выраженности симптомов в первой группе. В первый день комбинированного лечения изжога купирована у 64% пациентов (критерий χ2, р < 0,05). К четвертому дню лечения в этой группе изжога сохранялась у 11% больных и у 42% пациентов, получавших монотерапию пантопразолом (критерий χ2, р < 0,05). Комбинированная терапия была более эффективна в снижении выраженности и частоты возникновения отрыжки и дисфагии (критерий Вилкоксона, p < 0,01, критерий χ2, р < 0,05). На фоне комбинированной терапии у всех больных достигнута эндоскопическая ремиссия рефлюкс-эзофагита, у 25% больных в контрольной группе сохранялись эрозии слизистой оболочки пищевода (критерий χ2, р = 0,033).
Выводы. Проведенное исследование показало преимущества комбинированной терапии (ИПП + Альфазокс) как в достижении симптоматического ответа, так и в улучшении эндоскопической картины у пациентов с эрозивным рефлюкс-эзофагитом.


Гастроэзофагеальная рефлюксная болезнь (ГЭРБ) – одно из самых распространенных кислотозависимых заболеваний. Средняя распространенность ГЭРБ в мире оценивается на уровне 13,3% (95% доверительный интервал (ДИ) 12,0–14,6%) [1], в Москве составляет 23,6% [2], в городах России – 13,3% (95% ДИ 11,3–14,3%) [3]. ГЭРБ – это состояние, развивающееся, когда рефлюкс содержимого желудка вызывает появление беспокоящих пациента симптомов и/или развитие осложнений. Ведущие симптомы ГЭРБ – изжога и регургитация (отрыжка кислым, горьким, содержимым желудка), наиболее частым осложнением ГЭРБ является рефлюкс-эзофагит [4].
Высокая распространенность с тенденцией к увеличению заболеваемости, хроническое рецидивирующее течение болезни, негативно влияющие на качество жизни и психологический статус больных, а также сложности лечения отличают ГЭРБ от других заболеваний органов пищеварения и определяют актуальность разработки новых подходов к терапии.
Медицинское изделие Альфазокс обладает способностью усиления барьерной функции слизистой оболочки пищевода (эзофагопротективным действием). Оно представляет собой комбинацию гиалуроновой кислоты и хондроитина сульфата на биоадгезивном носителе полоксамер 407. Этот макромолекулярный комплекс покрывает слизистую оболочку пищевода, создавая вязкий защитный барьер в отношении повреждающих компонентов гастроэзофагеального рефлюкса (ГЭР) [5].
Эзофагопротективное действие Альфазокса было доказано экспериментально ex vivo на модели свиней [6]. Клинические исследования показали эффективность его применения у больных с неэрозивным и эрозивным эзофагитом для купирования симптомов ГЭРБ [7, 8]. Многоцентровое рандомизированное двойное слепое плацебоконтролируемое исследование доказало эффективность и безопасность применения Альфазокса в течение 15 дней в комбинированной терапии с ингибиторами протонной помпы (ИПП) у больных неэрозивной формой гастроэзофагеальной рефлюксной болезни (НЭРБ) и выявило преимущества в устранении клинических проявлений заболевания и улучшении качества жизни пациентов по сравнению с монотерапией ИПП [9].
С декабря 2019 г. по ноябрь 2020 г. на базе МКНЦ им. А.С. Логинова проведено пилотное проспективное открытое рандомизированное клиническое исследование по оценке эффективности комбинации медицинского изделия Альфазокс и пантопразола 40 мг в сравнении с монотерапией пантопразолом 40 мг при лечении больных ГЭРБ с рефлюкс-эзофагитом в параллельных группах в течение четырех недель.
Материал и методы
В исследование были включены 40 больных с эндоскопической картиной эрозивного рефлюкс-эзофагита и симптомами ГЭРБ (изжога, регургитация, загрудинная боль и отрыжка). Критериями исключения были пищевод Барретта; прием антисекреторных препаратов (ИПП и H2-блокаторы), альгинатов и антацидов менее чем за 10 дней до визита; эрозивно-язвенные поражения желудка и двенадцатиперстной кишки; злокачественные новообразования; оперативные вмешательства на желудке или объемные операции на желудочно-кишечном тракте в анамнезе; беременность и лактация.
Перед включением в исследование проводили оценку клинической картины заболевания и эзофагогастродуоденоскопию (ЭГДС). Оценку степени рефлюкс-эзофагита проводили по Лос-Анджелесской эндоскопической классификации 1994 г. [10].
Распределение больных по группам осуществляли методом компьютерной рандомизации. Первую группу составили 19 больных, получавших комбинированную терапию: пантопразол 40 мг за 30 минут до завтрака и Альфазокс в дозе 10 мл через час после трех основных приемов пищи и перед сном. Факт и кратность приема препаратов больной отмечал в индивидуальном дневнике пациента. Во вторую группу вошел 21 пациент, получавший монотерапию пантопразолом в дозе 40 мг за 30 минут до завтрака.
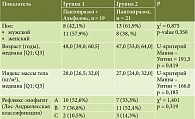
Группы больных были сопоставимы по полу, возрасту, индексу массы тела, а также выраженности рефлюкс-эзофагита (табл. 1).
До начала и после окончания исследования оценивали выраженность и частоту возникновения симптомов ГЭРБ (изжога, отрыжка, регургитация, одинофагия, дисфагия и нарушение ночного сна). Выраженность симптомов оценивалась по пятибалльной шкале Likert: 0 – симптом отсутствует; 1 – симптом причиняет небольшое беспокойство; 2 – симптом причиняет беспокойство; 3 – симптом причиняет сильное беспокойство и мешает повседневной деятельности; 4 – непереносимый симптом, не позволяющий осуществлять повседневную деятельность. Частоту симптома оценивали по следующей шкале: 0 – 0 дней в неделю; 1 – один день в неделю; 2 – два-три дня в неделю; 3 – 4–7 дней в неделю.
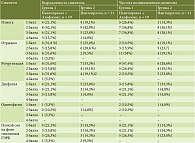
До начала лечения группы были сопоставимы по среднему баллу как выраженности, так и частоты симптомов (табл. 2). Не было достоверного различия при распределении больных в зависимости от симптомов по балльной оценке (табл. 3).
Закончили прием препаратов и прошли заключительную оценку выраженности и частоты симптомов все 19 больных из исследовательской группы и 19 пациентов контрольной группы. Двое больных из контрольной группы прервали исследование (по собственному желанию и в связи с заболеванием COVID-19). Контрольную ЭГДС провели 16 больным из исследовательской группы и 16 пациентам из контрольной. Пятеро больных не явились на эндоскопию в связи с эпидемиологической обстановкой в марте – мае 2020 г.; один больной не допущен к контрольной ЭГДС из-за положительного теста ПЦР к COVID-19.
Для систематизации и анализа полученных результатов была создана электронная база данных. Статистическую обработку данных проводили с помощью пакета программ Microsoft Office Excel (Microsoft, США) с учетом нормальности распределения признака. Использовали критерий χ2, U-критерий Манна – Уитни, Т-критерий Вилкоксона. Статистически значимыми считали различия при р < 0,05.
Результаты исследования
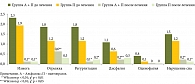
Проведен анализ динамики симптомов на фоне лечения у больных, закончивших исследование (исследовательская группа – 19 больных, группа контроля – 19 больных). Данные, представленные на рис. 1 и 2, свидетельствуют, что как комбинированная терапия, так и лечение ИПП к 28-му дню обеспечили положительную клиническую динамику.
В обеих группах выявлено достоверное уменьшение выраженности и частоты возникновения изжоги (в исследовательской группе критерий Вилкоксона 0,0; р < 0,01; в контрольной группе критерий Вилкоксона 0,0; р < 0,01) и большая доля пациентов с устраненным симптомом изжоги на фоне терапии (в исследовательской группе критерий χ2 30,5; р < 0,01; в группе контроля χ2 27,6; р < 0,01).
При оценке динамики симптома отрыжки отмечено преимущество комбинированной терапии. В исследовательской группе зафиксировано достоверное снижение выраженности отрыжки (критерий Вилкоксона16,0; p < 0,01) и частоты возникновения данной жалобы (критерий Вилкоксона 7,5; р < 0,01), кроме того, достоверна и доля пациентов с устраненным симптомом на фоне проведенного лечения (критерий χ2 4,2; р < 0,04). В группе больных, получавших монотерапию пантопразолом, наблюдалась положительная динамика выраженности (критерий Вилкоксона 0,0; p < 0,01) и частоты отрыжки (критерий Вилкоксона 8,0; p < 0,01), однако сохранялся высокий процент пациентов, которых отрыжка продолжала беспокоить (критерий χ2 4,886; р < 0,180).
Была показана достоверная динамика регургитации в обеих группах: отмечен регресс ее выраженности (в группе исследования критерий Вилкоксона 3,0; p < 0,01; в контрольной группе критерий Вилкоксона 0,0; p < 0,01) и частоты возникновения (в исследовательской группе критерий Вилкоксона 11,0; р < 0,01; в группе контроля критерий Вилкоксона 0,0; р < 0,01); в обеих группах достигнута высокая доля пациентов с купированным симптомом (в группе исследования критерий χ2 14,0; р < 0,01; в контрольной – χ2 11,49; р < 0,01).
Выявлено достоверное облегчение дисфагии на фоне терапии в исследовательской группе: выраженность (критерий Вилкоксона 22,5; p < 0,01) и частота возникновения (критерий Вилкоксона 22,5; p < 0,01) и увеличение доли больных без дисфагии (критерий χ2 5,54; р < 0,019). В контрольной группе выраженность дисфагии (критерий Вилкоксона 7,0; p < 0,106) и частота ее возникновения (критерий Вилкоксона 12,0; p < 0,728) сохранялись.
Достоверных различий в динамике симптома одинофагии не выявлено в обеих группах.
В связи с купированием симптомов ГЭРБ, прежде всего изжоги и регургитации, у больных в обеих группах выявлена достоверная динамика улучшения ночного сна: как по выраженности (в исследовательской группе критерий Вилкоксона 23,0; p < 0,01; в контроле – критерий Вилкоксона 0,0; p < 0,01 ), так и по частоте симптома (в исследовательской группе критерий Вилкоксона 14,0; p < 0,01; в контроле – критерий Вилкоксона 0,0; p < 0,01), в обеих группах достигнута высокая доля пациентов с нормализованным ночным сном (исследовательская – критерий χ2 11,0; р < 0,01; контрольная – критерий χ2 9,662; р < 0,01).
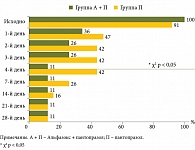
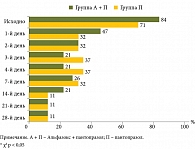
До начала исследования изжога беспокоила 100% пациентов исследовательской группы и 91% больных контрольной группы. В первые сутки изжога купирована у 64% пациентов (критерий χ2 20,476, р < 0,05), получавших комбинированную терапию, и у 44% больных (критерий χ2 9,106, р = 0,059) в группе контроля. В течение первых дней терапии доля пациентов с купированной изжогой увеличилась в обеих группах (рис. 3), к четвертому дню лечения не испытывали изжогу 89% больных первой группы, а во второй группе больных – 58% (критерий χ2 4,885, р = 0,027). С пятых суток приема препаратов статистически значимых межгрупповых отличий не выявлено.
Данные, представленные на рис. 4, свидетельствуют, что в начале терапии в обеих группах достоверно снизилась доля пациентов с симптомом регургитации (в исследовательской группе – критерий χ2 14,25; р < 0,05; в контрольной – критерий χ2 15,55; р < 0,05), однако статистически значимых межгрупповых отличий на фоне терапии не отмечено (критерий χ2 1,15; р = 0,283).
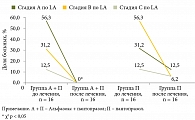
Проведен анализ динамики эпителизации эрозий слизистой оболочки пищевода на фоне проводимого лечения у больных, закончивших принимать участие в исследовании (рис. 5). Сопоставление доли пациентов первой и второй групп с достигнутой эндоскопической ремиссией продемонстрировало преимущество комбинированного лечения (критерий χ2 4,571; р = 0,033).
К 28-му дню лечения у всех больных исследовательской группы зафиксирована эпителизация эрозий пищевода, что свидетельствовало об эффективности комбинированного лечения (критерий χ2 34,105; р < 0,01). В группе контроля достоверной динамики улучшения эндоскопической картины не выявлено (критерий χ2 2,57; р = 0,109). У 4 (25%) больных, прошедших контрольное эндоскопическое исследование, сохранялся эрозивный эзофагит. При этом у 2 (12,5%) больных на фоне терапии пантопразолом отмечено снижение стадии эзофагита со стадии В до стадии А по Лос-Анджелесской классификации; у 2 (12,5%) пациентов эндоскопической динамики не было, сохранялся эзофагит стадии С и стадии В по Лос-Анджелесской классификации.
Обсуждение
В основе патогенеза ГЭРБ лежат моторные нарушения, приводящие к дисфункции антирефлюксных механизмов и возникновению патологического ГЭР, источником которого является «кислотный карман». Результат воздействия ГЭР на слизистую оболочку пищевода определяется его составом, длительностью воздействия, адекватностью клиренса пищевода и резистентностью слизистой оболочки пищевода [11]. Экспериментальные модели продемонстрировали наибольший повреждающий потенциал для слизистой оболочки пищевода ГЭР, состоящего из кислоты, пепсина и конъюгированных желчных кислот, при этом неконъюгированные желчные кислоты могут вызывать повреждение при более высоких значениях pH. По результатам исследования J. Tack, у людей также отмечен синергический повреждающий эффект кислотного и дуоденогастрального рефлюксов [12].
Резистентность слизистой оболочки пищевода к воздействию повреждающих агентов зависит от сохранности ее барьерной функции [13]. В межклеточных пространствах поверхностных слоев слизистой пищевода содержатся мукополисахариды, обеспечивающие его защиту от физических и химических повреждений. При электронной и световой микроскопии выявляются гистопатологические изменения слизистой пищевода, вызванные ГЭР [14, 15]. Расстояние между клетками увеличивается, что приводит к повышению проницаемости и проникновению в подслизистый слой пищевода ионов водорода и других веществ, включая пепсин и желчные кислоты, которые раздражают рецепторы, вызывая ощущение изжоги [16]. Установлено расширение межклеточных пространств у всех больных ГЭРБ как при эндоскопически негативной форме, так и при рефлюкс-эзофагите. Поэтому они рассматриваются как гистологический маркер ранних повреждений слизистой оболочки пищевода вследствие рефлюкса. У больных функциональной изжогой межклеточные пространства не расширены [17].
Целью лечения ГЭРБ является устранение симптомов, а при эрозивном эзофагите – заживление эрозий и предупреждение осложнений [18]. При лечении больных используется комплексный подход, традиционно включающий диету и модификацию образа жизни, назначение препаратов, снижающих повреждающий потенциал ГЭР. В меньшей степени реализованы подходы, направленные на улучшение клиренса пищевода и защиту его слизистой оболочки. Широкое применение нашли антациды, химически нейтрализующие содержимое желудка, поступившее в пищевод, альгинаты, физически препятствующие рефлюксу [19], и ингибиторы протонной помпы, уменьшающие кислотопродукцию в желудке с целью повышения pH и уменьшения объема рефлюктата [20]. Антациды и альгинаты используются для скорой помощи при изжоге [21]. ИПП является основным фармакологическим средством для лечения ГЭРБ, обеспечивающим контроль симптомов и заживление повреждений слизистой оболочки пищевода [22]. Вместе с тем до 40% больных ГЭРБ не получают адекватного облегчения симптомов с помощью ИПП [23].
Дополнительное повышение защитных свойств слизистого барьера наряду с кислотосупрессией является важным компонентом лечения ГЭРБ [18]. Решение этой задачи стало возможным с появлением медицинского изделия Альфазокс, в состав которого входят низкомолекулярная (80–100 кДа) гиалуроновая кислота и низкомолекулярный (10–20 кДа) хондроитина сульфат, растворенные в биоадгезивном носителе (полоксамер 407). Альфазокс покрывает слизистую оболочку пищевода, ограничивает контакт компонентов ГЭР с поверхностью эпителия и оказывает местное лечебное воздействие [24].
Проведенное нами исследование отражает преимущество комбинированной терапии, включавшей ИПП и Альфазокс, по сравнению с монотерапией ИПП как по динамике снижения частоты возникновения симптомов, так и по доле больных с симптомами в первые дни лечения. В первый день комбинированного лечения изжога купирована у 64% пациентов (критерий χ2, р < 0,05). К четвертому дню лечения в этой группе изжога сохранялась у 11% больных и у 42% пациентов, получавших монотерапию пантопразолом (χ2, р < 0,05). Отмечено преимущество комбинированной терапии в снижении выраженности и частоты возникновения отрыжки и дисфагии (критерий Вилкоксона, p < 0,01; критерий χ2, р < 0,05). К 28-му дню на фоне комбинированной терапии у всех больных достигнута эндоскопическая ремиссия рефлюкс-эзофагита, в контрольной группе эрозии сохранялись у 25% больных (критерий χ2, р = 0,033).
В ходе ранее проведенных исследований оценивали эффективность Альфазокса в комбинации с ИПП у больных НЭРБ. В двойном слепом рандомизированном плацебоконтролируемом исследовании B. Palmieri и соавт. основными показателями эффективности были суммарная оценка интенсивности симптомов (SSSI) за 14-дневный терапевтический период и разница в степени интенсивности симптомов (SSID). На момент окончания терапии Альфазоксом было отмечено значимо более низкое абсолютное значение SSSI по сравнению с группой плацебо. Начиная с первой недели терапии Альфазоксом значения SSID стабильно превышали показатели группы плацебо и достигли максимума через две недели лечения. Полное устранение симптомов чаще наблюдалось на фоне терапии Альфазоксом: 52% по сравнению с 12% в группе плацебо, p = 0,01. Кроме того, в группе Альфазокса было отмечено более быстрое купирование симптомов по сравнению с группой плацебо [25].
В ходе многоцентрового рандомизированного двойного слепого плацебоконтролируемого исследования V. Savarino и соавт. проведена оценка эффективности и безопасности комбинации ИПП и Альфазокса течение 15 дней у больных НЭРБ. В группе Альфазокса наблюдалось вдвое большее уменьшение оценки выраженности симптомов по сравнению с группой плацебо (‑3,1 ± 3,1 по сравнению с ‑1,5 ± 3,0; p = 0,002; популяция ITT), значимое уменьшение количества дней с наличием симптомов по сравнению с плацебо (‑6,07 и ‑3,96; p = 0,0059; популяция ITT) и статистически значимое улучшение общего состояния здоровья и социального функционирования (опросник SF-36). Отмечен высокий уровень безопасности Альфазокса [9].
В недавно опубликованном исследовании И.В. Матошиной и соавт. представлены предварительные данные об эффективности комбинации ИПП и Альфазокса у больных с эрозивным эзофагитом C и D по Лос-Анджелесской классификации. Подобно нашей работе, больные были рандомизированы на две группы: основная получала пантопразол и Альфазокс в течение четырех недель, группа сравнения – монотерапию пантопразолом. Помимо оценки динамики симптомов и выраженности рефлюкс-эзофагита авторами был проведен морфологический анализ слизистой оболочки пищевода с определением уровня экспрессии белка плотных контактов клаудина-1. До начала лечения по исследуемым параметрам группы не отличались. На контрольном визите в группе Альфазокса отмечено более быстрое купирование клинических симптомов, более выраженная положительная динамика по данным эндоскопии и морфологии с повышением экспрессии белка клаудина-1 [26].
Заключение
Проведенное нами исследование демонстрирует преимущества комбинации ИПП и Альфазокса в купировании клинических проявлений гастроэзофагеальной рефлюксной болезни (изжоги, отрыжки, регургитации, дисфагии, а также нормализации ночного сна) и эпителизации эрозий слизистой оболочки пищевода по сравнению с монотерапией ИПП. Полученные данные подтверждают, что компоненты медицинского изделия Альфазокс (гиалуроновая кислота и хондроитина сульфат) усиливают барьерную функцию слизистой оболочки пищевода, способствуют ограничению воздействия на нее агрессивных факторов, снижают выраженность воспаления и способствуют заживлению эрозивных повреждений слизистой оболочки пищевода.
O.I. Berezina, PhD, E.R. Valitova, PhD, E.V. Bystrovskaya, PhD, D.S. Bordin, PhD, Prof.
A.S. Loginov Moscow Clinical Scientific Center
Tver State Medical University
A.I. Yevdokimov Moscow State University of Medicine and Dentistry
Contact person: Olga I. Berezina, o.berezina@mknc.ru
Objective: to evaluate the benefits of co-administration of the esophagoprotector Alfazox and the proton pump inhibitor (PPI) for the relief of symptoms and epithelialization of esophageal mucosal erosions in patients with gastroesophageal reflux disease (GERD).
Material and methods. 40 patients with GERD with reflux esophagitis were examined. Patients were randomized into two groups: 19 patients of the first group (8 men and 11 women, age 48,0 [39,0;60,5] years) received combination therapy: pantoprazole 40 mg per day and Alfazox 10 ml four times a day; 21 patients from the second group (13 men and 8 women, age 47,0 [33,0; 64,0] years) received pantoprazole 40 mg per day. The duration of therapy was 28 days. The dynamics of the frequency and severity of symptoms of the disease were evaluated on the Likert scale. According to the EGDS data, the effectiveness of the treatment of erosive esophagitis was evaluated.
Results. The advantages in reducing the severity of symptoms in the first group were noted. On the first day of combined treatment, heartburn was stopped in 64% of patients (χ2 p < 0.05). By the fourth day of treatment in this group, heartburn persisted in 11% of patients and in 42% of patients receiving pantoprazole monotherapy (χ2 p < 0.05). Combination therapy was more effective in reducing the severity and frequency of belching and dysphagia (Wilcoxon p < 0.01, χ2 p < 0.05). Against the background of combined therapy, endoscopic remission of reflux esophagitis was achieved in all patients, and erosion of the esophageal mucosa persisted in 25% of patients in the control group (χ2 p = 0.033).
Conclusions. The study showed the advantages of combination therapy (PPI + Alfazox) both in achieving the symptomatic response and in improving the endoscopic picture in patients with erosive reflux esophagitis.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.