Снижение риска рецидива симптоматики при применении эзофагопротектора у пациентов, которым требуется временная отмена антисекреторной терапии
- Аннотация
- Статья
- Ссылки
- English
Материал и методы. В проспективное сравнительное исследование селективно были отобраны пациенты, которые длительно (не менее одного месяца) принимали ИПП по поводу основного заболевания и которым требовалась временная отмена антисекреторной терапии ввиду объективных медицинских причин. В исследование были включены пациенты с эндоскопически и/или рН-метрически верифицированной ГЭРБ, а также гистологически верифицированным пищеводом Барретта. В процессе рандомизации пациентов сформированы две равные группы в зависимости от получаемой терапии на время отмены ИПП: первая группа получала антациды в режиме «по требованию», вторая группа – антациды в режиме «по требованию», а также эзофагопротектор Альфазокс в дозе 10 мл четыре раза в сутки (после каждого приема еды и на ночь). Период наблюдения за пациентами составил две недели. Эпизоды изжоги пациенты регистрировали в личных дневниках.
Результаты. В исследование были включены 60 пациентов (28 мужчин и 32 женщины), которым в силу разных причин требовалась отмена ИПП в течение двух недель. Средний возраст обследованных составил 43,1 ± 5,3 года. Было выделено две группы по 30 человек, дифференцированных по методу купирования рецидива изжоги – монотерапия антацидами по требованию или Альфазокс 10 мл четыре раза в день в комбинации с антацидом по требованию. К окончанию двухнедельного периода наблюдения частота рецидива симптоматики в первой группе составила 36,7%, тогда как во второй группе – 13,3%. Применение эзофагопротектора Альфазокса способствовало достоверному регрессу риска рецидива изжоги (отношение шансов 0,2657; 95%-ный доверительный интервал (ДИ) 0,07328–0,9637; p = 0,0438) в сравнении с группой пациентов, которая получала только антациды в режиме «по требованию». При анализе популяции пациентов, у которых произошел рецидив симптоматики, было продемонстрировано, что среднее количество эпизодов изжоги в первой группе составило 6,18 (95% ДИ 4,1930–8,1706), а у пациентов второй группы – 4,50 (95% ДИ 0,7121–8,2879).
Заключение. Настоящее проспективное сравнительное исследование продемонстрировало, что использование эзофагопротектора Альфазокса способствует снижению риска рецидива симптоматики ГЭРБ у пациентов, которым требуется временная отмена терапии ИПП.
Материал и методы. В проспективное сравнительное исследование селективно были отобраны пациенты, которые длительно (не менее одного месяца) принимали ИПП по поводу основного заболевания и которым требовалась временная отмена антисекреторной терапии ввиду объективных медицинских причин. В исследование были включены пациенты с эндоскопически и/или рН-метрически верифицированной ГЭРБ, а также гистологически верифицированным пищеводом Барретта. В процессе рандомизации пациентов сформированы две равные группы в зависимости от получаемой терапии на время отмены ИПП: первая группа получала антациды в режиме «по требованию», вторая группа – антациды в режиме «по требованию», а также эзофагопротектор Альфазокс в дозе 10 мл четыре раза в сутки (после каждого приема еды и на ночь). Период наблюдения за пациентами составил две недели. Эпизоды изжоги пациенты регистрировали в личных дневниках.
Результаты. В исследование были включены 60 пациентов (28 мужчин и 32 женщины), которым в силу разных причин требовалась отмена ИПП в течение двух недель. Средний возраст обследованных составил 43,1 ± 5,3 года. Было выделено две группы по 30 человек, дифференцированных по методу купирования рецидива изжоги – монотерапия антацидами по требованию или Альфазокс 10 мл четыре раза в день в комбинации с антацидом по требованию. К окончанию двухнедельного периода наблюдения частота рецидива симптоматики в первой группе составила 36,7%, тогда как во второй группе – 13,3%. Применение эзофагопротектора Альфазокса способствовало достоверному регрессу риска рецидива изжоги (отношение шансов 0,2657; 95%-ный доверительный интервал (ДИ) 0,07328–0,9637; p = 0,0438) в сравнении с группой пациентов, которая получала только антациды в режиме «по требованию». При анализе популяции пациентов, у которых произошел рецидив симптоматики, было продемонстрировано, что среднее количество эпизодов изжоги в первой группе составило 6,18 (95% ДИ 4,1930–8,1706), а у пациентов второй группы – 4,50 (95% ДИ 0,7121–8,2879).
Заключение. Настоящее проспективное сравнительное исследование продемонстрировало, что использование эзофагопротектора Альфазокса способствует снижению риска рецидива симптоматики ГЭРБ у пациентов, которым требуется временная отмена терапии ИПП.

Введение
Гастроэзофагеальная рефлюксная болезнь (ГЭРБ) представляет собой чрезвычайно распространенное в мировой популяции кислотозависимое заболевание, при котором соляная кислота желудочного сока выступает основным повреждающим фактором при развитии клинических симптомов и морфологических проявлений [1, 2]. Для данного заболевания характерной чертой является хронический, рецидивирующий паттерн симптоматики, оказывающий существенное негативное влияние на качество жизни больных [3–5]. Текущие эпидемиологические данные свидетельствуют, что показатели распространенности и заболеваемости ГЭРБ имеют неуклонную тенденцию к росту во многих регионах мира [6, 7]. Согласно последнему метаанализу J.S. Nirwan и соавт. (2020), обобщившему результаты 102 исследований, глобальная распространенность ГЭРБ составляет 13,98% (95% доверительный интервал (ДИ) 12,47–15,56%) [8]. Медико-социальное значение ГЭРБ определяется ее главной ролью в развитии предракового состояния, известного как пищевод Барретта (ПБ), при котором специализированный цилиндрический эпителий с бокаловидными клетками замещает нормальный неороговевающий многослойный плоский эпителий дистального отдела пищевода [9, 10]. Согласно недавнему метаанализу L.H. Eusebi и соавт. (2021), обобщившему результаты 44 исследований, частота гистологически верифицированного ПБ у пациентов с ГЭРБ составляет 7,2% (95% ДИ 5,4–9,3%), тогда как эндоскопические признаки ПБ выявляются у 12,0% больных (95% ДИ 5,5–20,3%) [11].
С учетом того что ГЭРБ является классическим кислотозависимым заболеванием, препаратами первой линии при индукции и поддержании ремиссии данной болезни являются ингибиторы протонной помпы (ИПП) [1, 2, 12, 13]. Купирование изжоги в первые сутки применения ИПП происходит примерно у 31% пациентов с ГЭРБ (95% ДИ 0,30–0,32) [14]. При эмпирическом лечении ГЭРБ относительный риск ремиссии изжоги в плацебоконтролируемых исследованиях с использованием ИПП составляет 0,37 (95% ДИ 0,32–0,44) [15]. В метаанализе P.W. Weijenborg и соавт. (2012) терапия ИПП в течение четырех недель приводила к полному купированию изжоги как у пациентов с эрозивной формой заболевания (отношение шансов (ОШ) 0,72; 95% ДИ 0,69–0,74), так и у лиц с неэрозивным фенотипом (ОШ 0,49; 95% ДИ 0,44–0,55) [16]. Вместе с тем с учетом хронического и рецидивирующего течения ГЭРБ после инициального курса ИПП (4–12 недель) для стабильного контроля симптоматики заболевания требуется длительная поддерживающая терапия, которая может назначаться неопределенно долго, повторными курсами, а при наличии ПБ – пожизненно [2, 9, 17]. В клинической практике нередко возникают ситуации, при которых требуется временная (от одной недели до месяца) отмена ИПП для валидного проведения ряда диагностических мероприятий, включая диагностику и контроль эрадикации H. pylori, рН-импедансометрию, а также лабораторный скрининг атрофического гастрита [2, 18, 19]. Отмена ИПП может привести к рецидиву симптоматики у значимой части пациентов, что негативно скажется на их качестве жизни. В ряде исследований частота рецидива при отмене ИПП достигала 60–80% [20–22]. Использование антацидных препаратов для снижения риска рецидива симптоматики на время отмены ИПП малоэффективно ввиду выраженной краткосрочности их действия. В этой связи перспективным представляется оценка эффективности эзофагопротектора Альфазокса, использующегося для формирования макромолекулярного комплекса, обволакивающего слизистую оболочку пищевода и выступающего в качестве механического барьера в отношении соляной кислоты, пепсина и желчных кислот, попадание которых и последующий контакт с эпителием дистального отдела пищевода приводят к индукции симптоматики ГЭРБ [23].
Цель проспективного сравнительного исследования – оценить эффективность эзофагопротектора в снижении риска рецидива симптоматики ГЭРБ у пациентов, которым требуется временная отмена терапии ИПП.
Материал и методы
В исследование селективно отбирали пациентов, которые длительно (не менее одного месяца) принимали ИПП по поводу основного заболевания и которым требовалась временная отмена антисекреторной терапии ввиду объективных медицинских причин. Были включены пациенты с эндоскопически и/или рН-метрически верифицированной ГЭРБ, а также гистологически верифицированным ПБ. Пациенты с ПБ и дисплазией высокой степени в исследовании участия не принимали.
В процессе рандомизации пациентов сформировано две равные группы в зависимости от получаемой терапии на время отмены ИПП: первая группа получала антациды в режиме «по требованию»; вторая группа – антациды в режиме «по требованию», а также эзофагопротектор Альфазокс в дозе 10 мл четыре раза в сутки (после каждого приема еды и на ночь). Период наблюдения за пациентами составил две недели. Эпизоды изжоги пациенты регистрировали в личных дневниках.
Статистическую обработку данных проводили с помощью специального программного обеспечения MedCalc 19.7.1 (Бельгия) в среде Microsoft Windows 10 (США). Анализировали такие показатели, как частота рецидива изжоги (в относительном соотношении), кумулятивная частота изжоги (в абсолютном соотношении) и среднее количество эпизодов изжоги на одного пациента за период наблюдения (в абсолютном соотношении). Статистические гипотезы проверяли с помощью непараметрического U-критерия Манна – Уитни и параметрического критерия Фишера. Различия между группами считались достоверными при р < 0,05.
Результаты
В проспективное сравнительное исследование было включено 60 пациентов (28 мужчин и 32 женщины). Средний возраст обследованных составил 43,1 ± 5,3 года. В нозологической структуре преобладали пациенты с неэрозивной рефлюксной болезнью (n = 32), затем расположились больные эрозивным рефлюкс-эзофагитом (n = 13) и ПБ (n = 15). Основные причины временной отмены антисекреторной терапии с применением ИПП приведены в таблице.
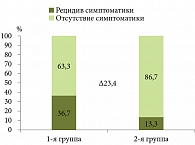
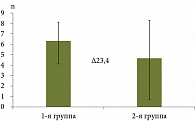
К окончанию двухнедельного периода наблюдения частота рецидива симптоматики в первой группе составила 36,7% (в 11 случаях из 30), тогда как во второй группе – всего 13,3% (в четырех случаях из 30) (рис. 1). Таким образом, применение эзофагопротектора Альфазокса способствовало достоверному регрессу риска рецидива изжоги (ОШ 0,2657; 95% ДИ 0,07328–0,9637; p = 0,0438) в сравнении с группой пациентов, которая получала только антациды в режиме «по требованию». Кумулятивная частота эпизодов рефлюкса в первой группе составила 68 единиц, а во второй группе – 20 единиц. Анализ популяции пациентов, у которых произошел рецидив симптоматики, показал, что среднее количество эпизодов изжоги в первой группе составило 6,18 (95% ДИ 4,1930–8,1706), а у пациентов второй группы – 4,50 (95% ДИ 0,7121–8,2879)
(рис. 2).
Обсуждение
ГЭРБ – широко распространенное кислотозависимое заболевание, развивающееся на фоне первичного нарушения двигательной функции верхних отделов пищеварительного тракта, классическим проявлением которого является изжога [1, 24]. На сегодняшний день антисекреторная терапия с использованием ИПП является терапией первой линии при индукции и поддержании ремиссии ГЭРБ [12, 13, 24–27]. В рутинной клинической практике нередко бывают ситуации, при которых требуется временная (от одной недели до месяца) отмена ИПП для валидного проведения ряда диагностических мероприятий, что может привести к рецидиву симптоматики у значимой части пациентов [2, 18, 19, 21, 22]. Предупреждение рисков рецидива с применением современных групп препаратов является важной задачей современной гастроэнтерологии, так как от его успеха зависит качество жизни пациента – главного интегрального показателя качественной медицинской помощи [2]. Эзофагопротекторы – это новая фармакологическая группа, представителем которой является биоадгезивная формула на основе гиалуроновой кислоты и хондроитина сульфата (Альфазокс), созданная для защиты слизистой оболочки пищевода [1, 23, 28]. Настоящее сравнительное исследование на популяции пациентов, которым требуется временная отмена терапии ИПП, продемонстрировало, что применение эзофагопротектора Альфазокса в сочетании с антацидами способствовало регрессу риска рецидива изжоги. Представляется, что такая эффективность обусловлена механизмом действия препарата. Так, Альфазокс оказывает заживляющее и восстанавливающее действие по отношению к эпителию пищевода, а благодаря высокой способности к биоадгезии обеспечивает защиту слизистой оболочки органа в течение длительного времени, снижая вероятность контакта соляной кислоты с эпителиоцитами, что необходимо для индукции симптоматики заболевания [23]. Согласно клиническим исследованиям, Альфазокс способствует заживлению эрозий пищевода, в том числе в сочетании с ИПП у пациентов с ГЭРБ [29, 30]. В исследовании V. Savarino и соавт. (2017) комбинация Альфазокса и ИПП позволила более эффективно добиться регрессии клинических проявлений заболевания и улучшения качества жизни пациентов (согласно опроснику SF36) по сравнению с монотерапией ИПП [31]. Полученные в нашем исследовании результаты подтверждают, что оптимизация схем лечения ГЭРБ с использованием эзофагопротекторов открывает новые перспективы ведения этой непростой группы пациентов, в том числе в нетривиальных клинических ситуациях.
Заключение
Настоящее проспективное сравнительное исследование продемонстрировало, что использование эзофагопротектора Альфазокса способствует снижению риска рецидива симптоматики ГЭРБ у пациентов, которым требуется временная отмена терапии ИПП.
Yu.A. Kucheryavy, PhD, P.R. Movtaeva, D.N. Andreev, PhD, R.I. Shaburov, PhD, D.T. Dicheva, PhD
Ilyinsky Hospital
A.I. Yevdokimov Moscow State University of Medicine and Dentistry
Contact person: Dmitry N. Andreev, dna-mit8@mail.ru
Objective: to evaluate the effectiveness of an esophagoprotector in reducing the risk of recurrent symptoms of gastroesophageal reflux disease (GERD) in patients who requiring temporary cancellation of therapy with proton pump inhibitors (PPIs).
Material and methods. For the prospective comparative study there were selectively chose patients who had been taking PPIs for a long time (at least one month) for the underlying disease and who required temporary discontinuation of antisecretory therapy due to objective medical reasons. The study included patients with endoscopically and/or pH-metrically verified GERD, as well as histologically verified Barrett's esophagus. In the process of randomization of patients, two equal groups were formed, depending on the therapy received at the time of PPI withdrawal: group 1 received antacids on demand, group 2 received antacids on demand, as well as the esophagoprotector Alfasoxx at a dose of 10 ml four times a day (after each meal and at night). The follow-up period was two weeks. The patients recorded episodes of heartburn in their personal diaries.
Results. The study included 60 patients (28 men and 32 women). The average age of the examined patients was 43.1 ± 5.3 years. By the end of the two-week follow-up period, the frequency of recurrent symptoms in group 1 was 36.7%, while in group 2 it was 13.3%. The use of the esophagoprotector Alfasoxx contributed to the significant regression of the risk of heartburn recurrence (odds ratio 0.2657; 95% confidence interval (CI) 0.07328-0.9637; p = 0.0438) in comparison with the group of patients who received only antacids in the on-demand mode. When analyzing the population of patients who had relapsed symptoms, it was demonstrated that the average number of heartburn episodes in group 1 was 6.18 (95% CI 4,1930-8,1706), and in group 2 – 4.50 (95% CI 0,7121-8,2879).
Conclusion. This prospective comparative study demonstrated that the use of the esophagoprotector Alfasoxx helps to reduce the risk of relapse of GERD symptoms in patients requiring temporary cancellation of PPI therapy.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.