Комплексный подход к лечению осложнений сахарного диабета
- Аннотация
- Статья
- Ссылки



Лечение центральных и периферических неврологических осложнений сахарного диабета
По словам к.м.н., доцента кафедры нервных болезней Первого Московского государственного медицинского университета им. И.М. Сеченова Игоря Алексеевича СТРОКОВА, среди поздних осложнений сахарного диабета (СД) наиболее часто наблюдается дистальная симметричная сенсорно-моторная полинейропатия (ДПН).
Принято выделять следующие стадии ДПН:
- N0 – объективные признаки нейропатии отсутствуют;
- N1 (субклиническая) – нет выраженной нейропатической симптоматики, однако нарушения со стороны нервной системы выявляются при обследовании;
- N2a (симптомная) – наличие типичных жалоб пациента или выраженного неврологического дефицита;
- N2b – в патологический процесс вовлекаются двигательные волокна (пациент не может ходить на пятках);
- N3 (инвалидизация) – поражение периферических нервов приводит к нарушению трудовой и социальной адаптации больного1.
Диагностика ДПН предполагает выявление типичной нейропатической симптоматики (боль, жжение, онемение, парестезии) и неврологического дефицита (нарушение чувствительности всех модальностей, снижение или отсутствие сухожильных рефлексов в ногах). Нейропатические симптомы оцениваются по шкале TSS (Total Symptom Score – Общая оценка симптомов), неврологический дефицит – по шкале NIS-LL (Neuropathy Impairment Score Lower Limb – Шкала нейропатических нарушений, нижние конечности).
Для подтверждения поражения соматических нервных волокон применяется электронейромиография, оценки порога возбудимости тонких волокон, проводящих болевую, температурную чувствительность, – количественное сенсорное тестирование, исследования вариабельности сердечного ритма – мониторирование электрокардиографии.
Методом ранней диагностики патологии периферических нервов у больных СД в настоящее время считается биопсия икроножного нерва.
Основные причины развития поздних осложнений СД – нарушение внутриклеточного метаболизма и окислительный стресс. Поражение эндоневральных сосудов является следствием метаболических нарушений, а в дальнейшем становится самостоятельным фактором развития патологии периферических нервов. По мнению докладчика, это еще раз подтверждает слова А.С. Ефимова: «Диабет начинается как болезнь обмена, а заканчивается как сосудистая патология».
Следовательно, адекватный контроль течения СД является приоритетным для профилактики и эффективности лечения ДПН.
Интенсивная терапия инсулином больных СД 1 типа может уменьшить риск развития сосудистых осложнений и ДПН, хотя не в состоянии полностью исключить возникновение или привести к серьезному регрессу симптоматики2, 3. Как показывают результаты проспективных исследований, интенсивная терапия СД 2 типа не способствует достоверному уменьшению риска развития ДПН. Это также подтверждают данные исследования ADVANCE, в ходе которого было отмечено отсутствие влияния интенсивной терапии диабета на возникновение и прогрессирование полинейропатии у пациентов с СД 2 типа4. Именно поэтому, подчеркнул И.А. Строков, наряду с нормализацией углеводного обмена необходима терапия ДПН.
Среди активно применяемых препаратов с мощным антиоксидантным и нейропротективным действием особого внимания заслуживает Актовегин. Препарат Актовегин – высокоочищенный гемодиализат, получаемый методом ультрафильтрации из крови телят. В состав препарата входят органические низкомолекулярные соединения; технология получения Актовегина исключает наличие белковых компонентов, обладающих антигенными и пирогенными свойствами. Актовегин содержит более 200 активных компонентов: олигопептиды, аминокислоты, нуклеозиды, продукты углеводного и жирового обмена (инозитолфосфат-олигосахариды), микроэлементы и электролиты (Na, K, P, Mg, Cu).
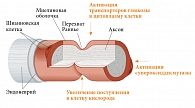
Интерес к применению Актовегина при ДПН обусловлен не только антиоксидантными свойствами препарата, но и способностью улучшать утилизацию кислорода и глюкозы в клетке, что крайне важно при СД, когда в тканях формируется энергетическая недостаточность (рисунок).
Увеличение поглощения кислорода сосудистой стенкой приводит к снижению периферического сосудистого сопротивления, и, как следствие, улучшается кровоснабжение тканей. Поскольку Актовегин обладает сразу несколькими свойствами (нейрометаболическим, антигипоксантным и антиоксидантным), его прием позволяет уменьшить количество принимаемых пациентами препаратов.
Чтобы правильно оценить механизм действия любого вещества, необходимо изучить его возможности у здоровых добровольцев. Как правило, подобные исследования проводятся с участием 8–10 человек. В нашем случае, по словам докладчика, в исследовании приняли участие 28 мужчин в возрасте 19–26 лет5. Цель работы – оценить активацию сосудодвигательной и метаболической функции микрососудистого эндотелия на фоне приема Актовегина. Оценка микроциркуляторных процессов в коже проводилась с помощью компьютерной капилляроскопии и лазерной допплеровской флоуметрии. После определения параметров микроциркуляции участникам проводилась инфузия 250 мл 10%-ного раствора Актовегина в левую кубитальную вену. Через два часа после окончания инфузии микроциркуляцию исследовали повторно.
На основании полученных данных был сделан вывод: механизмы терапевтического эффекта Актовегина являются универсальными, что позволяет поставить его в один ряд с препаратами, применяемыми для коррекции дисфункции сосудистого эндотелия.
«Результаты исследований, проведенных нашей рабочей группой, показали, что назначение Актовегина больным СД 2 типа и ДПН приводит к достоверному уменьшению уровня малонового диальдегида как в сыворотке крови, так и в мембранах эритроцитов (р < 0,01), существенному улучшению у большинства обследованных характеристик капиллярного кровотока (капилляроскопия ногтевого ложа)», – отметил И.А. Строков. Таким образом, была продемонстрирована способность Актовегина уменьшать выраженность окислительного стресса, улучшать состояние системы микроциркуляции и, как следствие, снижать клинические проявления ДПН.
Эффективность и безопасность Актовегина у больных СД 2 типа и диабетической полинейропатией доказана в ходе многоцентрового рандомизированного двойного слепого плацебоконтролируемого клинического исследования в параллельных группах, которое было проведено в 2008 г. на базе 26 клинических центров6. Терапию Актовегином получал 281 пациент (20 внутривенных инфузий 250 мл 20%-ного раствора с последующим приемом драже в дозе 600 мг/сут в течение 140 дней), плацебо – 286 больных (схема приема та же).
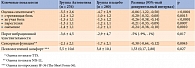
На фоне терапии Актовегином у больных наблюдалось достоверное улучшение всех ключевых показателей состояния (табл. 1).
Так, в конце исследования в группе Актовегина достоверно уменьшились выраженность симптомов ДПН (р < 0,0001) по сравнению с группой плацебо, порог вибрационной чувствительности по сравнению с исходным значением (р = 0,017) и с группой плацебо (-3,6 против -2,9), выраженность сенсорной симптоматики (р = 0,0045). При этом Актовегин продемонстрировал профиль безопасности, сравнимый с профилем безопасности плацебо.
В течение всего исследования определялась глюкоза натощак и уровень гликированного гемоглобина. Полученные данные свидетельствуют, что эффективность лечения связана с действием препарата, а не с улучшением контроля СД.
У больных СД и ДПН часто наблюдается нарушение равновесия. Согласно данным разных авторов, пациенты с СД и полинейропатией в 15 раз больше получают повреждения при ходьбе, чем больные СД без ДПН, распространенность сенситивной атаксии у пациентов с диабетом и ДПН варьирует от 10 до 90%7.
«Мы провели комплексное обследование 102 больных СД 1 и 2 типа. Чтобы оценить, насколько они способны удерживать равновесие, была сделана компьютерная динамическая постурография», – пояснил И.А. Строков.
В зависимости от результатов пациенты были разделены на три группы: первая – без снижения вибрационной, тактильной и мышечно-суставной чувствительности, вторая – со снижением вибрационной и/или тактильной чувствительности, но без нарушения мышечно-суставной чувствительности, третья – со снижением всех трех видов чувствительности.
Участники были сопоставимы по возрасту, индексу массы тела, степени компенсации СД. Однако пациенты третьей группы дольше страдали СД, нежели пациенты первой группы (р < 0,01), и именно у них чаще выявлялась инвалидность. На нарушение равновесия жаловались 63 (61,8%) больных, в основном из третьей группы.
Корреляционный анализ позволил предположить, что ДПН с поражением толстых нервных волокон является независимым фактором, приводящим к нарушению равновесия.
Отобранные для проведения реабилитационных мероприятий пациенты с нарушением равновесия были разделены на две группы по 10 человек. Первая группа получала терапию Актовегином сначала в виде внутривенных инфузий в дозе 2,0 г/сут (14 процедур), затем перорально в дозе 1200 мг/сут (83 дня). Вторая группа не получала дополнительного лечения, проводилась только компенсация СД.
Динамика клинических и инструментальных показателей через три месяца свидетельствовала о статистически значимом снижении общего количества симптомов полинейропатии и числа жалоб на нарушение равновесия (до 40%) в группе Актовегина.
В последние годы все больше внимания уделяется диабетической энцефалопатии (ДЭ). Диабетическая энцефалопатия – это доказуемые когнитивные нарушения у больных СД, развившиеся в результате метаболических нарушений из-за длительной гипергликемии, при исключении других причин их формирования8.
Статистика показывает, что у больных СД в два раза выше риск развития деменции и болезни Альцгеймера, а при сочетании СД и артериальной гипертензии риск развития когнитивных нарушений возрастает в шесть раз. Когнитивные нарушения снижают способность адекватно контролировать гликемию и увеличивают риск развития типичных осложнений, угрожающих жизни пациента.
Данные исследований показывают, что применение Актовегина приводит к уменьшению апоптоза нейронов, увеличению количества синаптических связей, улучшению мышления больных с ДЭ. Таким образом, Актовегин может положительно влиять на когнитивные функции у больных СД 2 типа с умеренными когнитивными нарушениями и повышать их общую активность.
Завершая выступление, И.А. Строков подчеркнул, что антигипоксантные, нейропротективные и антиоксидантные свойства Актовегина позволяют использовать его при таких неврологических осложнениях СД, как диабетическая полинейропатия и ДЭ.
Современные подходы к ведению пациентов с диабетической стопой
Нейропатия наряду с атеросклерозом артерий нижних конечностей является одним из главных факторов риска развития синдрома диабетической стопы (СДС). Диабетическая стопа – это инфекция, язва и/или деструкция глубоких тканей стопы в сочетании с неврологическими нарушениями и/или снижением магистрального кровотока в артериях нижних конечностей различной степени тяжести. Как отметила д.м.н., профессор кафедры эндокринологии и диабетологии Российской медицинской академии последипломного образования Ирина Владимировна ГУРЬЕВА, примерно 15% больных СД имеют высокую вероятность развития СДС в течение жизни, только 2/3 всех язв заживает без хирургического вмешательства, а медиана заживления превышает два месяца.
Стратегия заживления язвы включает мероприятия по контролю гликемии, нагрузки на опорные зоны, инфекции, состояния раны и кровоснабжения, а также обучение пациентов. На первом месте в стандартах лечения стоит обработка раны с полным удалением некротизированных и нежизнеспособных тканей хирургическим, ферментативным или механическим путем. Процедура преследует две цели: первая (главная) – удаление остатков тканей и инородных частиц, без чего невозможно заживление, вторая – создание условий для эффективной дезинфекции, поскольку некоторые антисептики инактивируются в присутствии омертвевших тканей9. В реальной клинической практике врачи часто не используют данный метод, хотя он позволяет перевести рану из хронического состояния в острую фазу и ускорить заживление раневого дефекта.
Риск язвенных дефектов стоп резко возрастает при заболевании периферических артерий (ЗПА), которое отмечается у 10–40% больных СД. ЗПА считается независимым фактором риска ампутаций, поэтому пациентам для исключения этой патологии необходимо проводить скрининговые тесты. Признаками ЗПА являются перемежающая хромота или наличие болей покоя, отсутствие пульсации на обеих артериях стопы при пальпации, сигнала или монофазный допплеровский сигнал от одной и обеих артерий стопы, лодыжечно-плечевой индекс менее 0,09.
Комплексное лечение СДС предполагает использование антигипоксических и антиоксидантных средств. Учитывая механизм действия Актовегина, его нейропротективные свойства, включение препарата в схему лечения представляется весьма перспективным.
И.В. Гурьева отметила, что целесообразность и эффективность применения Актовегина у больных с нейроишемическим болевым синдромом при периферической ангиопатии были подтверждены результатами ее работы. В открытом сравнительном пилотном рандомизированном исследовании оценивалась эффективность препаратов Актовегин и сулодексид для лечения нейроишемических болей при перемежающей хромоте у больных СД 1 и 2 типа. Пациенты в группе Актовегина получали препарат внутривенно в дозе 2000 мг/сут в течение двух недель с последующим переходом на пероральный прием в дозе 1200 мг/сут в течение шести недель. В группе сулодексида препарат назначался внутривенно в дозе 1200 ЛЕ/сут с последующим переходом на пероральный прием в дозе 1000 ЛЕ/сут10.
Оба препарата продемонстрировали способность увеличивать время ходьбы до появления боли. Однако эффективность Актовегина была значительно выше. Результаты исследования показали, что абсолютный прирост максимальной ходьбы до появления болевых ощущений в группе Актовегина был почти в два раза выше по сравнению с группой сулодексида – 160,1 против 84,9 с, относительный прирост также был выше в группе Актовегина и составил 95,1% (p < 0,01) (табл. 2).
У пациентов из группы Актовегина отмечалось достоверное улучшение состояния периферических сосудов и скорости проведения возбуждения.
Был сделан вывод, что Актовегин эффективен для лечения неврологических и сосудистых осложнений СД и его прием значительно улучшает качество жизни пациентов.
«Неврологические осложнения сахарного диабета, безусловно, являются междисциплинарной проблемой, решение которой требует разнонаправленного подхода. Только объединив усилия, мы сможем добиться успеха в лечении», – отметила профессор И.В. Гурьева.
Заключение
Данные экспериментальных и клинических исследований подтверждают целесообразность применения Актовегина для терапии сосудистых осложнений и поражений нервной системы при СД. Актовегин, зарекомендовавший себя в качестве мощного антигипоксанта, антиоксиданта и нейрометаболика, может быть показан пациентам с диабетической полинейропатией, ДЭ и СДС, а также с другими микро- и макрососудистыми осложнениями СД для эффективной нейропротекции.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.