Место препарата Цернилтон® в лечении хронического простатита и доброкачественной гиперплазии предстательной железы (обзор опыта применения)
- Аннотация
- Статья
- Ссылки
- English
Вопросы терапии хронического простатита и доброкачественной гиперплазии предстательной железы (ДГПЖ) ввиду широкой распространенности и значимости не теряют своей актуальности. По данным M.M. Collins и соавт., простатит является самым частым урологическим заболеванием у мужчин моложе 50 лет и третьим по частоте (после ДГПЖ и рака простаты) – у мужчин старше 50 лет [1]. По данным различных авторов, хроническим простатитом страдают от 8 до 35% пациентов в возрасте от 20 до 40 лет [2]. ДГПЖ диагностируется преимущественно у мужчин более старшего возраста. Распространенность ДГПЖ варьирует от 11,3% в возрастной группе 40–49 лет до 81,4% в группе 80 лет [3].
Изменения в предстательной железе могут быть обусловлены нарушением гормонального равновесия между андрогенами и эстрогенами. Однако нет четкого понимания того, какие клеточные и молекулярные процессы лежат в основе патогенеза ДГПЖ и приводят к возникновению клинических симптомов [4]. Ряд исследователей указывают на роль воспаления в увеличении простаты и развитии ДГПЖ [5]. В двух из наиболее крупных исследований по проблеме ДГПЖ (MTOPS и Reduce) была показана связь между воспалением простаты, выявленным при гистологическом исследовании, и увеличением простаты или усилением тяжести симптомов [6, 7]. Обнаруженная взаимосвязь воспалительного процесса в предстательной железе и развития ДГПЖ обусловливает актуальность поиска эффективных методов профилактики рецидивов хронического простатита [8].
Согласно рекомендациям Европейской ассоциации урологов (European Association of Urology), к первой линии терапии хронического простатита относятся антибактериальные препараты [9]. Длительность антибиотикотерапии, как правило, составляет от четырех до шести недель [10]. С учетом рецидивирующего характера заболевания велика вероятность проведения повторного курса антимикробной терапии. Следовательно, повышается риск возникновения нежелательных явлений и развития антибиотикорезистентности [11]. Это заставляет искать альтернативные возможности лечения хронического простатита и ДГПЖ.
Фитотерапия, известная еще со времен Древнего Египта [12], утратила значение с появлением синтетических препаратов. Однако неудачи традиционной терапии привели к тому, что фитотерапия возвращает свои позиции в лечении некоторых заболеваний [13]. В настоящее время активно создаются и изучаются лекарственные препараты на основе природных соединений [14]. В состав фитопрепаратов входят различные биологические вещества, которые могут оказывать влияние на механизмы развития заболевания. Кроме того, фитотерапевтические препараты отличают высокий профиль безопасности и низкая токсичность [15]. Фитотерапия ДГПЖ/хронического простатита на протяжении многих лет пользуется популярностью в Европе и в последние годы находит применение и в Америке [2]. Так, в странах Центральной Европы растительные препараты являются одними из основных компонентов лечения при минимально выраженных симптомах нижних мочевых путей (СНМП) [16].
Препараты Цернилтон® и Цернилтон® форте содержат микробиологически ферментированный экстракт пыльцы разновидных растений в виде гидрофильной (Graminex T60) и липофильной (Graminex GBX) фракций. Гидрофильная фракция ответственна за противовоспалительный и противоотечный эффект препарата Цернилтон®. Она подавляет циклооксигеназу и 5-липооксигеназу, под действием которых из арахидоновой кислоты образуются лейкотриены и простагландины – ключевые медиаторы воспалительной реакции. В исследовании in vivo показано ингибирование стромальной пролиферации в связи с усиленным апоптозом преимущественно из-за Gramineх T60.
Липофильную фракцию Graminex GBX составляют фитостеролы [17–22]. Данные субстанции, по мнению S. Madersbacher, являются важнейшей составляющей фитотерапии [23]. Graminex GBX обеспечивает непосредственное спазмолитическое действие и блокаду альфа-1-адренорецепторов, а также блокаду 5-альфа-редуктазы – фермента, которому отводится ключевая роль в развитии ДГПЖ [17–22]. По результатам исследований in vivo, липофильная фракция защищает эпителиальные клетки в ацинусах предстательной железы [19]. Данные свойства препарата Цернилтон® обусловливают доказанное в ходе различных исследований воздействие на патогенетическую составляющую роста ДГПЖ и ликвидацию симптомов хронического простатита.
Впервые опыт применения препарата Цернилтон® для лечения хронического простатита и ДГПЖ был описан в 1962 г. [24]. С тех пор было проведено большое количество исследований эффективности препарата Цернилтон® при лечении ДГПЖ и хронического простатита. Следует отметить Кокрановский отчет, представленный в рекомендациях Европейской ассоциации урологов по лечению СНМП/ДГПЖ, согласно которому применение препарата Цернилтон® как метод лечения имеет наивысший уровень доказательности [25].
T. Wilt в 2000 г. опубликовал систематический обзор плацебоконтролируемых и сравнительных исследований, в которых оценивалась эффективность и безопасность применения растительной субстанции пыльцы разновидных растений у мужчин с ДГПЖ [26]. Всего были проанализированы результаты лечения 444 пациентов, длительность наблюдения составила от 12 до 24 недель. У пациентов, которые получали Цернилтон®, чаще, чем у пациентов в группе плацебо, отмечались улучшение субъективных ощущений (в 2,4 раза, 95% доверительный интервал (ДИ) 1,21–4,75) и снижение частоты ночного мочеиспускания (в 2,05 раза, 95% ДИ 1,41–3,00). Кроме того, авторы подчеркнули отсутствие серьезных побочных эффектов на фоне приема препарата Цернилтон® [26, 27].
В 1988 г. в исследовании, проведенном Н. Becker и соавт., приняли участие 96 пациентов с ДГПЖ, разделенных на две группы. Первая группа (n = 48) принимала две таблетки препарата Цернилтон® три раза в день в течение трех месяцев, вторая – плацебо (n = 48) в том же режиме. На фоне лечения снизилась частота дневного мочеиспускания (48,8% в группе лечения и 19,5% в группе плацебо) и эпизодов ночной поллакиурии (68,8 и 37,2% соответственно). Значительно уменьшилась выраженность ощущения неполного опорожнения мочевого пузыря (37,1 против 7,7% больных в группе плацебо) [28].
В плацебоконтролируемом исследовании A.C. Buck и соавт. приняли участие 53 больных ДГПЖ, ожидавших оперативного лечения. В основной группе (n = 28) пациенты принимали Цернилтон® по две таблетки два раза в день в течение шести месяцев, в контрольной (n = 24) – плацебо по такой же схеме. Частота ночных мочеиспусканий снизилась у 60% пациентов основной группы и у 30% – контрольной. 69% больных основной группы отметили уменьшение выраженности симптоматики, в то время как в группе плацебо – только 29%. По объективным данным обследования, в основной группе в большей степени, чем в группе сравнения, уменьшились объем остаточной мочи (-43,5 мл и 20 мл) и переднезадний размер простаты (-5,3 и -1,6 мм соответственно) [29].
Имеется ряд сравнительных исследований, в которых отмечались общее улучшение состояния пациентов, уменьшение симптомов заболевания, частоты ночных микций и уровня простатического специфического антигена на фоне применения препарата Цернилтон®.
M. Maekawa и соавт. провели сравнительное исследование эффективности препарата Цернилтон® и смеси аминокислот (глутамина, аланина и глицина). Исследование с участием 159 больных продолжалось три месяца. О субъективном улучшении состояния заявили 49,1% пациентов, получавших Цернилтон®, и 41,2% больных, принимавших смесь аминокислот. Кроме того, было отмечено уменьшение размеров предстательной железы при ультразвуковом исследовании, а также увеличение средней и максимальной скорости мочеиспускания при урофлоуметрии [30].
В сравнительном исследовании по изучению эффективности препарата Цернилтон® (n = 20) и бета-ситостеролового экстракта (n = 20) H. Brauer выявил значимое симптоматическое улучшение на фоне лечения препаратом Цернилтон®. У пациентов, принимавших Цернилтон®, было отмечено существенное уменьшение уровня простатического специфического антигена (на 2,5 нг/мл, p < 0,01). У больных, получавших бета-ситостероловый препарат, подобных изменений не наблюдалось [31].
S. Dutkiewicz провел сравнение эффективности препарата Цернилтон® и экстракта африканской сливы Pygeum africanum (Таденан). В исследовании приняли участие 89 мужчин с установленным диагнозом ДГПЖ. Динамика состояния пациентов отслеживалась по Международной шкале суммарной оценки симптомов при заболеваниях простаты (International Prostate Symptom Score – IPSS). Субъективные симптомы заболевания в большей степени уменьшились на фоне применения препарата Цернилтон® (78%). В группе сравнения этот показатель составил 55% [32].
Крупное клиническое рандомизированное исследование с параллельными группами провели N.C. Li и соавт. 906 мужчин с СНМП принимали альфа-адреноблокаторы, ингибиторы 5-альфа-редуктазы и препарат Цернилтон®. Эффективность терапии оценивалась по следующим критериям: сумма баллов по шкале IPSS, показатели уродинамического исследования (урофлоуметрия), ультразвуковое исследование предстательной железы, в частности объема транзиторной зоны и количества остаточной мочи. Все препараты улучшали как субъективные, так и объективные проявления СНМП. Однако прием альфа-1-адреноблокаторов и ингибиторов 5-альфа-редуктазы сопровождался побочными эффектами, которые зачастую ухудшают качество жизни пациентов и в дальнейшем могут привести к снижению комплаентности и прекращению терапии. В группе пациентов, принимавших препарат Цернилтон®, выраженных побочных эффектов зарегистрировано не было [33].
В исследовании J. Hayashi и соавт. 20 больных ДГПЖ получали препарат Цернилтон® в течение 13 недель. По окончании терапии 92% мужчин отметили уменьшение выраженности ощущения неполного опорожнения мочевого пузыря, 85% – снижение частоты ночного мочеиспускания, 56 и 53% пациентов – уменьшение напряжения при мочеиспускании и времени задержки перед микцией соответственно [34].
F.M. Wagenlehner и соавт. провели многоцентровое рандомизированное проспективное двойное слепое плацебоконтролируемое исследование по применению препарата Цернилтон® у пациентов с хроническим простатитом. Пациенты основной группы получали препарат Цернилтон® по две таблетки три раза в день в течение 12 недель, контрольной – плацебо. Эффективность лечения оценивалась по Индексу шкалы симптомов хронического простатита и синдрома тазовых болей у мужчин по версии Национального института здоровья США (National Institute of Health Chronic Prostatitis Symptom Index – NIH-CPSI). По итогам исследования отмечено улучшение показателей в домене боли, качества жизни (p = 0,0250) и увеличение общей суммы баллов по NIH-CPSI (p = 0,0126) в основной группе по сравнению с группой плацебо. По окончании лечения в основной группе было отмечено улучшение по домену боли (p = 0,0086), качества жизни (p = 0,0250), а также по общей сумме баллов по NIH-CPSI. Значимых побочных эффектов у пациентов обеих групп не выявлено [35].
В исследование препарата экстракта пыльцы разновидных растений без группы сравнения, проведенное E. Rugendorff, были включены 90 мужчин с хроническим простатитом. У пациентов имелись сопутствующие заболевания (камни простаты, склероз шейки мочевого пузыря, стриктура уретры). Успех терапии в целом составил 57,7%. На фоне лечения 68, 70, 55 и 48% пациентов избавились от дискомфорта, боли, учащенного мочеиспускания в ночное и дневное время соответственно. Улучшение состояния пациентов получило объективное подтверждение. По данным урофлоуметрии, через три месяца от начала терапии максимальная объемная скорость мочеиспускания возросла с 15,9 ± 5,2 до 19,0 ± 7,2 мл/с и через шесть месяцев достигла 23,9 ± 10,6 мл/с (p < 0,001). У абсолютного большинства пациентов не было зафиксировано побочных эффектов [36].
В открытом исследовании А.C. Buck и соавт. изучали эффективность и безопасность лечения препаратом Цернилтон® 15 больных хроническим простатитом. Длительность терапии составляла от одного до 18 месяцев. Было сделано заключение об эффективности препарата Цернилтон®: состояние пациентов улучшилось в 86,7% случаев [37].
T. Suzuki и соавт. наблюдали 24 пациента на протяжении трех месяцев. Субъективное улучшение наблюдалось в 96% случаев, объективное – у 76%. По данным ультразвукового исследования, положительные структурные изменения предстательной железы по окончании терапии имели место у всех пациентов [38].
В российском сравнительном исследовании эффективности и безопасности разных доз препарата Цернилтон® было обследовано и пролечено 78 пациентов с установленным диагнозом «хронический неинфекционный простатит» [39]. Методом рандомизации пациенты были разделены на две группы: первая группа (n = 55) получала экстракт пыльцы разновидных растений по две таблетки три раза в день, вторая группа (n = 23) – по одной таблетке три раза в день в течение трех месяцев. Дизайн исследования предусматривал три визита: при включении в исследование, по завершении терапии и через три месяца после окончания лечения. Проводилась оценка субъективных (шкала NIH-CPSI, шкала частоты симптомов, линейная шкала, шкалы Sex-4, IPSS, качества жизни) и объективных (анализ секрета простаты, ультразвуковое исследование простаты, урофлоуметрия с определением количества остаточной мочи) показателей.
Анализ субъективных ощущений (шкала NIH-CPSI, линейная шкала выраженности симптомов, шкала частоты симптомов, шкала Sex-4, шкала качества жизни) показал улучшение состояния пациентов в обеих группах на третьем визите по сравнению с первым визитом.
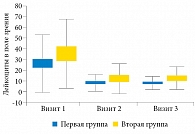
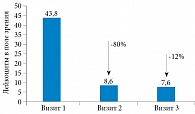
Как в первой, так и во второй группе уменьшилось количество лейкоцитов в поле зрения в секрете предстательной железы (71 и 65% соответственно, p < 0,001) (рис. 1 и 2). Максимальная скорость мочеиспускания на третьем визите в первой группе увеличилась на 3% (p = 0,55), во второй – на 1,5% (p = 0,66). Объем остаточной мочи уменьшился на 66% (p = 1) в первой группе и на 100% (p = 1) во второй группе.
Отмечен длительный эффект двойной дозы препарата Цернилтон®. Объем предстательной железы в первой группе стабильно уменьшался, статистически значимое различие по сравнению с первым визитом отмечалось и на втором, и на третьем визите. К третьему визиту объем предстательной железы в первой группе уменьшился на 9% (p = 0,01), во второй – на 0,5%. Таким образом, сравнительный анализ эффективности доз препарата Цернилтон® при лечении больных хроническим абактериальным простатитом выявил достоверные различия в пользу двойной дозы препарата по влиянию на число лейкоцитов в секрете предстательной железы и объем предстательной железы.
Исходя из положительного опыта проведенных исследований, можно сделать вывод о том, что препараты Цернилтон® и Цернилтон® форте обладают как симптоматическими, так и патогенетическими свойствами в терапии хронического простатита и ДГПЖ. Ввиду возможного кумулятивного эффекта данных препаратов они могут быть рекомендованы пациентам в качестве профилактики возникновения рецидивов хронического простатита. Применение препаратов Цернилтон® по две таблетки три раза в день или Цернилтон® форте по одной капсуле три раза в день – подтвержденная и обоснованная схема лечения хронического простатита и ДГПЖ.
L.G. Spivak, D.V. Platonova
FSBEI HE ‘I.M. Sechenov First Moscow State Medical University’ of the Ministry of Healthcare of the Russian Federation
Contact person: Leonid Grigoryevich Spivak, leonid.spivak@gmail.com
A brief review on clinical studies of using Cernilton® is presented. The extract of various plant species pollen may be used for prevention and therapy of patients with benign prostatic hyperplasia and chronic prostatitis.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.