Консервативная терапия (тамсулозин + финастерид) доброкачественной гиперплазии предстательной железы как альтернатива оперативному лечению
- Аннотация
- Статья
- Ссылки
- English
Симптомы нижних мочевыводящих путей (СНМП) – одна из наиболее распространенных жалоб у взрослых мужчин [1]. СНМП могут значительно ухудшать качество жизни пациентов и вызывать беспокойство [2].
СНМП объединяют три группы симптомов: накопительные (учащенное мочеиспускание в дневное время и ноктурия), миктурические (медленная или прерывистая струя мочи, разбрызгивание струи мочи, затрудненное начало мочеиспускания и натуживание при мочеиспускании) и постмиктурические (чувство неполного опорожнения мочевого пузыря и терминальное «подкапывание») [3].
Причинами СНМП могут быть гиперактивный мочевой пузырь, нарушение активности/гипоактивность детрузора, а также иные структурные или функциональные изменения мочевыводящих путей и окружающих тканей [4]. Однако, как правило, СНМП связаны с инфравезикальной, или доброкачественной, простатической обструкцией. Доброкачественная простатическая обструкция в свою очередь часто вызвана доброкачественным увеличением предстательной железы, обусловленным гистологическими изменениями – доброкачественной гиперплазией предстательной железы (ДГПЖ) [3, 5].
Известно, что ДГПЖ носит прогрессирующий характер [6]. Среди факторов, которые могут привести к ухудшению состояния, – возраст старше 45 лет, суммарный балл по Международной шкале оценки симптомов заболеваний предстательной железы (International Prostate Symptom Score – IPSS) не менее 8, максимальная скорость мочеиспускания менее 15 мл/с, объем предстательной железы не менее 30 см3, уровень простатического специфического антигена более 1,4 нг/мл, объем остаточной мочи более 50 мл [7].
Терапия СНМП направлена на улучшение качества жизни пациентов посредством уменьшения степени расстройств мочеиспускания и предотвращения возможных осложнений [8]. Определяя терапевтическую тактику при ДГПЖ, необходимо удостовериться в отсутствии других причин СНМП. Сегодня, согласно рекомендациям Европейской ассоциации урологов, к основным методам лечения ДГПЖ относятся динамическое наблюдение, медикаментозная терапия (ее основу составляют ингибиторы 5-альфа-редуктазы и альфа-адреноблокаторы), оперативное и минимально инвазивное лечение [1]. В индустриально развитых странах объем хирургических вмешательств по поводу ДГПЖ занимает второе место среди всех хирургических операций, уступая только удалению катаракты [9]. Однако в век активного развития медикаментозной терапии доля оперативного лечения уменьшается.
Динамическое наблюдение считается вариантом выбора в случае невыраженных симптомов (суммарный балл по IPSS ≤ 7) и/или легкого беспокойства при отсутствии факторов риска прогрессирования заболевания [10, 11].
При наличии факторов риска тактика динамического наблюдения нецелесообразна ввиду того, что ранняя инициация лечения снижает риск прогрессирования ДГПЖ [12], а если проведение консервативной терапии откладывается, то лекарственные препараты назначаются уже при выраженных симптомах ДГПЖ [13].
При отсутствии выраженной симптоматики, но наличии факторов риска прогрессирования может быть показано превентивное назначение ингибиторов 5-альфа-редуктазы [14]. Эта группа препаратов обладает патогенетическим действием в отношении механизмов, лежащих в основе заболевания, и способна влиять на размер предстательной железы. Принцип действия ингибиторов 5-альфа-редуктазы связан с подавлением конверсии тестостерона в дигидротестостерон, что приводит к уменьшению объема простаты и купированию проявлений заболевания, в особенности у пациентов с большим объемом предстательной железы [10]. В целом ингибиторы 5-альфа-редуктазы хорошо переносятся и вызывают незначительное количество побочных реакций. Как правило, они наблюдаются в начале терапии и не приводят к отказу от лечения [15]. Основные нежелательные эффекты связаны с сексуальной функцией и включают снижение либидо, эректильную дисфункцию и нарушение эякуляции [1].
Наиболее распространенный вариант терапии у пациентов с умеренными и выраженными СНМП – назначение альфа-1-адреноблокаторов, которые блокируют одноименные рецепторы в гладкой мускулатуре мочевого пузыря и простаты, что приводит к снижению мышечного тонуса. Однако данная группа препаратов не влияет на объем предстательной железы, не предотвращает дальнейший рост гиперплазии простаты, не снижает уровень простатического специфического антигена, что подчеркивает целесообразность применения альфа-1-адреноблокаторов в отсутствие факторов дальнейшего прогрессирования заболевания ДГПЖ [16]. При этом, как и все лекарственные препараты, альфа-1-адреноблокаторы могут становиться причиной возникновения побочных эффектов: головной боли, слабости, головокружения, заложенности носа и ретроградного семяизвержения. Все препараты из группы антагонистов альфа-1-адренорецепторов обладают сходным клиническим действием, хотя частота побочных эффектов может несколько отличаться [1]. Из используемых сегодня в клинической практике альфа-1-адреноблокаторов лучшее соотношение по эффективности и переносимости имеет тамсулозин, поэтому он назначается чаще других препаратов данной группы [17, 18]. Его востребованность, вероятно, обусловлена сочетанием положительного действия на симптомы ДГПЖ и минимального негативного влияния на сердечно-сосудистую систему [13]. Таким образом, использование альфа-1-адреноблокаторов в терапии ДГПЖ позволяет улучшить качество жизни, а также уменьшить выраженность симптомов и накопления, и опорожнения [19]. Прием данной группы препаратов в режиме монотерапии может быть рекомендован для быстрого купирования симптоматики у пациентов со средневыраженными СНМП при низком риске прогрессирования ДГПЖ [17].
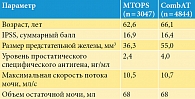
При симптомах умеренной и выраженной степени тяжести (суммарный балл по IPSS > 8) целесообразно проведение комбинированной терапии [11]. При сравнении монотерапии альфа-1-адреноблокаторами, ингибиторами 5-альфа-редуктазы и их комбинации оказалось, что последняя эффективнее снижает выраженность симптомов нарушенного мочеиспускания, улучшает показатели уродинамики и предупреждает прогрессирование заболевания [20]. К наиболее крупным исследованиям, подтвердившим преимущества комбинированной терапии, относятся MTOPS и CombAT (таблица) [1, 21].
MTOPS – двойное слепое рандомизированное плацебоконтролируемое исследование, в котором приняли участие 3047 пациентов. Они были разделены на четыре группы: получение доксазозина (4–8 мг/сут), финастерида (5 мг/сут), комбинации данных препаратов и плацебо с целью изучения влияния медикаментозной терапии на прогрессирование ДГПЖ. Наблюдение велось на протяжении пяти лет. Сопоставлялись выраженность симптомов по шкале IPSS, объем предстательной железы, а также изменения клинического прогрессирования заболевания. Оно определялось как увеличение суммы баллов по шкале IPSS, возникновение острой задержки мочи, острой почечной недостаточности, связанной с ДГПЖ, рецидивирующих инфекций мочевых путей, недержания мочи. По результатам исследования, наиболее выраженное уменьшение объема предстательной железы (-16%) было отмечено в группе финастерида, чуть менее выраженное (-13%) – в группе комбинированной терапии. В группе доксазозина, напротив, за четыре года наблюдения зарегистрирован значительный рост объема предстательной железы (на 18%). Комбинированная терапия показала наибольшую эффективность в отношении улучшения симптоматики по шкале IPSS. Так, в группе комбинированной терапии сумма баллов по шкале IPSS по сравнению с исходным уровнем снизилась на 7 баллов, в группе финастерида – на 5 баллов, в группе доксазозина – на 6 баллов и в группе плацебо – на 4 балла. Снижение риска прогрессирования ДГПЖ составило 67% в группе комбинированного лечения, 39% в группе доксазозина и 34% в группе финастерида. Риск возникновения острой задержки мочи снизился соответственно на 79% в группе комбинированной терапии, на 31% в группе монотерапии доксазозином и на 67% в группе монотерапии финастеридом. Таким образом, в исследовании MTOPS было продемонстрировано преимущество многостороннего подхода у пациентов с симптомами ДГПЖ и риском прогрессирования заболевания [21].
Исследование CombAT также показало преимущество комбинированной терапии в отношении уменьшения симптоматики и риска прогрессирования заболевания. Выполнен сравнительный анализ возможностей комбинированной терапии и монотерапии ингибитором 5-альфа-редуктазы и альфа-1-адреноблокатором в отношении отдаленных исходов заболевания (острой задержки мочи, необходимости оперативного лечения) у пациентов с высоким риском прогрессирования ДГПЖ. В исследовании приняли участие 4844 пациента, которые методом рандомизации были разделены на три группы:
- комбинированная терапия (дутастерид 0,5 мг/сут + тамсулозин 0,4 мг/сут, n = 1610);
- монотерапия дутастеридом (0,5 мг/сут, n = 1623);
- монотерапия тамсулозином (0,4 мг/сут, n = 1611).
Лечение проводилось в течение 48 месяцев. Исследование CombAT продемонстрировало эффективность долгосрочной комбинированной терапии в отношении не только субъективных данных, но и объективных параметров оценки мочеиспускания. Одновременный прием дутастерида и тамсулозина оказался эффективнее в отношении улучшения симптомов, статистически значимо снижая суммарный балл IPSS по сравнению с каждым из вариантов монотерапии (p < 0,001). Через 24 месяца средний суммарный балл по IPSS снизился по сравнению с исходными данными на 6,2 для комбинированного лечения и на 4,9 и 4,3 для дутастерида и тамсулозина соответственно. В период дальнейшего наблюдения в течение 24–48 месяцев достоверное преимущество комбинированной терапии по сравнению с терапией тамсулозином продолжало увеличиваться (с 1,8 до 2,5 балла по IPSS), а по сравнению с монотерапией дутастеридом – сохранялось (от 1,3 до 0,96 балла по IPSS).
Еще один показатель эффективности терапии в исследовании СombAT – время до первого эпизода острой задержки мочи или необходимость хирургического лечения по поводу ДГПЖ. Статистически значимое увеличение времени отмечено в группе комбинированной терапии по сравнению с группой тамсулозина (p < 0,001). Статистического различия между группой комбинированной терапии и группой дутастерида не наблюдалось (p = 0,18). Частота нежелательных явлений, связанных с лечением, в группе комбинированной терапии была выше. Это не оказало существенного влияния на переносимость лечения и частоту отмены лечения по причине приема препаратов. Нежелательные явления при комбинированной терапии соответствовали таковым при монотерапии каждым из препаратов, и в целом комбинированная терапия хорошо переносилась в течение 48 месяцев исследования. Исследование подтвердило более высокую эффективность комбинации (альфа-1-адреноблокаторы + ингибиторы 5-альфа-редуктазы) по сравнению с монотерапией по результатам относительно долгосрочных наблюдений [22].
Таким образом, комбинированная терапия альфа-1-адреноблокатором и ингибитором 5-альфа-редуктазы превосходит монотерапию при длительных сроках наблюдения, демонстрируя хорошие результаты по эффективности и безопасности у пациентов с увеличенным размером предстательной железы и высоким риском прогрессирования ДГПЖ. Необходимость постоянного длительного приема препаратов обусловливает актуальность вопроса стоимости лечения. Зачастую высокая цена ограничивает применение оригинальных препаратов. В практике можно использовать дженерические препараты, которые выпускаются по стандартам Надлежащей производственной практики (GMP) [1].
В последние десятилетия эффективность комбинированной терапии альфа-1-адреноблокатором и ингибитором 5-альфа-редуктазы настолько высока, что в большинстве случаев вопрос об оперативном лечении откладывается на неопределенное время [23]. У пациентов с СНМП средней и тяжелой степени, факторами риска прогрессирования состояния и отсутствием абсолютных показаний к хирургическому лечению комбинированная терапия может быть рекомендована в качестве альтернативы операции.
Согласно рекомендациям Международного согласительного комитета по проблеме ДГПЖ, хирургическое лечение ДГПЖ показано в следующих случаях:
- задержка мочеиспускания (острая или хроническая);
- повторная массивная гематурия, связанная с ДГПЖ;
- почечная недостаточность, обусловленная ДГПЖ;
- камни в мочевом пузыре;
- рецидивирующая инфекция мочевых путей;
- большой дивертикул мочевого пузыря.
Выбор метода оперативного лечения зависит от нескольких параметров, но ведущим является объем предстательной железы [24].
Задача врача-уролога – принимать решение о назначении лечения совместно с пациентом, предоставляя ему подробную информацию обо всех существующих и приемлемых вариантах терапии, применимых к клиническому состоянию пациента, информируя о преимуществах, рисках и стоимости каждого из них [25].
L.G. Spivak, D.V. Platonova
I.M. Sechenov First Moscow State Medical University
Contact person: Darina Vladimirovna Platonova, darina_mma@mail.ru
The article provides a brief overview of options of benign prostatic hyperplasia treatment. For patients at risk of disease progression and symptoms of moderate severity, combination therapy with 5-alpha-reductase inhibitor and alpha-1-adrenoblocker seems to be optimal.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.