Оптимальная инсулинотерапия для пациентов с сахарным диабетом типа 2
- Аннотация
- Статья
- Ссылки



В настоящее время во всем мире накоплены доказательства того, что эффективный контроль СД типа 2 может свести до минимума или предотвратить развитие многих из связанных с ним осложнений.
Следует отметить, что стратегии, которые были разработаны в последнее время, действительно позволили улучшить гликемический контроль у больных СД. Результаты, полученные в рамках исследования «Контроль за диабетом и его осложнениями» (DCCT) продемонстрировали возможность снижения риска развития ретинопатии, нефропатии и нейропатии в среднем на 50%. Кроме того, результаты данного исследования четко продемонстрировали, что агрессивный контроль гликемии наряду с нормализацией показателей артериального давления значительно снижает риск развития ишемической болезни сердца, цереброваскулярных заболеваний и периферической ангиопатии у больных СД типа 2. Таким образом, были закончены споры о необходимости обеспечения хорошего гликемического контроля в плане предотвращения долгосрочных осложнений.
В развитие исследования DCCT в 1994 г. был инициирован клинический протокол EDIC (The Epidemiology of Diabetes Intervention and Complications), в котором приняли участие 1375 пациентов с СД типа 1 из 1425 пациентов, участвовавших в исследовании DCCT. Необходимо особо отметить, что несмотря на некоторое ухудшение показателей гликемического контроля у этих пациентов было четко зафиксировано сохранение достигнутых в рамках DCCT клинических эффектов, что позволило сделать заключение о наличии у больных СД сосудистой или метаболической памяти. Кроме того, было выдвинуто предположение, что чем быстрее будут достигнуты цели лечения и чем дольше они будут зафиксированы, тем более значимы могут быть проявления метаболической и сосудистой памяти. Несомненно, что механизмы формирования метаболической или сосудистой памяти нуждаются в детальном изучении.
Результаты, полученные в рамках исследований DCCT и EDIC, явились хорошим стимулом применения аналогичного подхода по отношению и к больным СД типа 2.
Таким образом, настало время расширения или переопределения концепции терапии при СД, целью которой должно быть снижение риска развития и прогрессирования осложнений диабета посредством реализации программы мероприятий по уменьшению сосудистого риска на регулярной, долгосрочной основе.
Как известно, причиной развития и прогрессирования осложнений заболевания является именно хроническая гипергликемия (4), поэтому жесткий контроль гликемии является в настоящий момент основой профилактики развития и прогрессирования сосудистых осложнений СД. До недавнего времени доминирующее значение имели только уровень гликированного гемоглобина (HbA1c) и показатели гликемии натощак (5). По последним данным результатов международных исследований, ведущая роль в достижении целевых значений показателей HbA1c принадлежит уровню постпрандиальной гликемии (6-12). Доказано, что гипергликемия после еды тесно связана с развитием макрососудистых осложнений диабета, а также является ранним признаком СД типа 2. Из результатов исследования DECODE (The Diabetes Epidemiology: Collaborative Analysis of Diagnostic Criteria in Europe) следует, что гипергликемия через 2 часа после пероральной нагрузки глюкозой достоверно увеличивала риск смерти от любых причин, в то время как повышенный уровень гликемии натощак имел меньшее прогностическое значение.
В таблице 1 представлены последние работы по взаимосвязи постпрандиальной гликемии и сердечно-сосудистой заболеваемости.
Хорошо известно, что гипергликемия при СД типа 2 тесно связана с двумя патофизиологическими дефектами: инсулинорезистентностью и дисфункцией b-клеток поджелудочной железы, которые приводят к повышению уровня сахара крови. Прогрессирующее снижение функционального резерва b-клеток поджелудочной железы приводит в конечном итоге к дефициту эндогенной секреции инсулина. Поэтому со временем b-клетки становятся неспособными обеспечить адекватную секрецию инсулина для поддержания хорошего метаболического контроля. Следовательно, с течением времени многим пациентам с СД типа 2, кроме соблюдения диеты, дозированной физической нагрузки и применения пероральных сахароснижающих препаратов (ПССП) с позиции современных жестких критериев метаболических процессов для поддержания оптимального гликемического контроля может потребоваться инсулинотерапия с целью предупреждения острых и поздних осложнений заболевания.
Однако назначение инсулинотерапии связано с определенными проблемами как для больных, так и для врачей. Очень часто пациенты негативно относятся к этому методу лечения из-за боязни инъекций, сложностей обучения технике инсулинотерапии, а также из-за страха перед гипогликемией и увеличением массы тела (18). У врачей в большинстве случаев просто не хватает времени и ресурсов для обучения пациентов и для последующего тщательного наблюдения за больными, переведенными на инсулинотерапию. Поэтому решить эти проблемы, вероятно, возможно только с помощью современных препаратов инсулина, обладающих улучшенными фармакокинетическими и фармакодинамическими свойствами, а также с помощью усовершенствованных систем доставки инсулина.
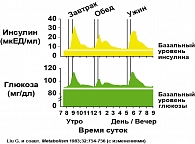
Основной целью инсулинотерапии у пациентов с СД типа 2 является коррекция инсулинодефицита моделированием нормальной секреции инсулина b-клетками поджелудочной железы, избегая гипер- или гипогликемии. Понятно, что успех назначенной инсулинотерапии зависит от того, насколько близко мы можем воссоздать собственную физиологическую секрецию во время еды для контроля постпрандиальной гликемии (ППГ) и базальную секрецию для контроля тощаковой гликемии (ГКН), а также гликемии между приемами пищи (рисунок 1).
В настоящее время для пациентов, которые не нуждаются или не готовы к использованию интенсивных режимов инсулинотерапии, реальной альтернативой является использование готовых смесей, которые обеспечивают удобный, эффективный и безопасный режим инсулинотерапии.
Таким образом, основными причинами разработки готовых смесей на основе аналогов человеческого инсулина были наличие одновременного эффективного и простого в применении комбинированного препарата и использование физиологических преимуществ аналога инсулина ультракороткого действия.
Одним из наиболее удачных примеров реализации такого подхода является инсулин Хумалог® Микс® 25 (Eli Lilly, США), представляющий собой готовую смесь из 75% протаминизированной суспензии инсулина лизпро и 25% инсулина лизпро (Хумалог®). Протаминизированный компонент обеспечивает потребность в базальном инсулине, так как является аналогом инсулина средней продолжительности действия, а компонент с ультракоротким действием контролирует колебания постпрандиальной гликемии.
Использование готовых смесей инсулина в различных странах сильно варьируется: от более 60% всех используемых инсулинов в Германии до 20-30% в Канаде и США (13). В большинстве стран отмечается устойчивая тенденция к увеличению использования именно смешанных инсулинов. Готовые смеси позволяют максимально индивидуализировать лечение. Кроме того, данные современных зарубежных и отечественных исследований свидетельствуют, что готовые смеси на основе аналогов человеческого инсулина, состоящие из ультракороткого и продленного инсулинов, обеспечивают такой же контроль гликемии, как и при использовании более интенсивных режимов инсулинотерапии у пациентов с СД типа 2.
Ультракороткие аналоги, входящие в состав современных инсулиновых смесей имеют фармакокинетические и фармакодинамические свойства, близко повторяющие профиль действия эндогенной прандиальной секреции инсулина, что обеспечивает адекватное снижение сахара крови после приема пищи. По сравнению с простым человеческим инсулином ультракороткий компонент смеси действует гораздо быстрее и тем самым обеспечивает лучший контроль постпрандиальной гликемии (7). Более того, поскольку вариабельность абсорбции и клиренса менее выражена, аналоги инсулина ультракороткого действия обеспечивают более близкий к физиологическому сахароснижающему профилю по сравнению с простым человеческим инсулином (15-17).
Стоит заметить, что у некоторых пациентов готовые смеси могут поддерживать хороший гликемический контроль в течение длительного периода заболевания. Таким образом, смешанные инсулины на основе аналогов человеческого инсулина удобны в применении в отношении приема пищи и количества инъекций, повышая тем самым качество жизни пациентов, а также обеспечивают имитацию физиологической секреции инсулина.
Готовые смеси инсулинов наиболее удобны для пациентов со стабильным режимом дня и питания, а также лиц пожилого возраста. Хорошо известно, что одним из недостатков человеческого инсулина является необходимость его введения за 30-40 минут до приема пищи для того, чтобы пик концентрации инсулина в плазме совпадал с максимальным подъемом уровня постпрандиальной гликемии.
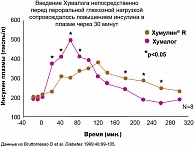
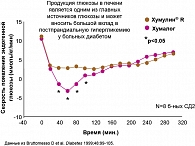
Однако практика показывает, что в реальной жизни большинство пациентов такой режим введения короткого инсулина не соблюдает, что отрицательно сказывается на эффективности и безопасности инсулинотерапии. Поэтому важно отметить, что введение Хумалог® Микс® 25 возможно как непосредственно перед едой, так и в течение 15 минут после приема пищи. Входящий в состав смеси ультракороткий аналог инсулина Хумалог восстанавливает ранний пик секреции инсулина после приема пищи и подавляет эндогенную секрецию глюкозы печенью (рисунки 2, 3). Подобная гибкость применения инсулина повышает качество жизни и обеспечивает высокую комплаэнтность пациентов в лечении СД типа 2.
Необходимо отдельно отметить категорию пожилых пациентов с СД типа 2, у которых использование интенсифицированной инсулинотерапии с частым измерением уровня гликемии практически невозможно из-за сложностей в обучении, а также из-за высокого риска гипогликемий. Этим больным необходим удобный и простой режим инсулинотерапии, который не только бы улучшал метаболический контроль диабета, но и минимизировал риск развития гипогликемий.
Введение инсулина после приема пищи может быть особенно удобным как раз для пожилых пациентов, которые часто забывают сделать инъекцию перед едой. Так, M. Herz et al. (2001) проведено открытое, 16-недельное исследование с параллельными группами больных СД типа 2 в возрасте от 60 до 80 лет, получающих препараты сульфонилмочевины и имеющих недостаточную компенсацию диабета (уровень HbA1c в 1,2 раза выше верхней границы целевых значений). Пациенты были рандомизированы в две группы. Первая группа получала инсулин Хумалог® МиксÔ 25 непосредственно перед едой (n = 37), а вторая – в течение 15 минут (n = 35) после начала приема пищи. Важно отметить, что как средний уровень HbA1c, так и уровень глюкозы крови, а также масса тела в двух группах исходно не различались. В конце исследования уровень HbA1c в группах, вводивших инсулин до и после приема пищи, был одинаковым (8,54 ± 0,22%). Средние дозы инсулина в группах, получавших инсулин до и после еды, составили 0,42 ± 0,03 ЕД/кг и 0,51 ± 0,03 ЕД/кг соответственно (p = 0,033). Не менее важно, что масса тела у пациентов с СД типа 2 в конце исследования по сравнению с исходными показателями достоверно не различалась (1,14 ± 0,46 кг и 0,89 ± 0,53 кг, p = 0,727). Частота эпизодов гипогликемии, которая оценивалась при уровне глюкозы крови ниже 3 ммоль/л, была низкой, особенно при введении инсулина после приема пищи (0,56 ± 0,42 эпизода/30 дней и 0,06 ± 0,04 эпизода/30 дней, p = 0,236) (таблица 2). Таким образом, введение Хумалог® Микс® 25 как до, так и после приема пищи обеспечивает сопоставимую компенсацию диабета при небольшом увеличении массы тела и низкой частоте эпизодов гипогликемий. Помимо этого, введение Хумалог® Микс® 25 после еды является безопасным и эффективным способом введения инсулина, что особенно актуально при инсулинотерапии у пожилых пациентов с СД типа 2 (1).
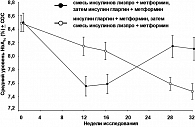
Интересные данные получены в специальном исследовании, проводимом в 12 диабетологических центрах Европы, целью которого являлось определение возможностей по повышению эффективности комбинированной терапии СД типа 2 (19). В 40-недельном рандомизированном открытом исследовании 97 пациентов с СД типа 2, у которых на фоне терапии ПССП в комбинации с инсулином НПХ или смесью человеческих инсулинов не удавалось добиться удовлетворительного контроля диабета, разделены на 2 группы. Исследование включало вводный период продолжительностью 4-8 недель, во время которого все пациенты получали инсулин НПХ в однократном режиме перед сном и метформин в дозе 1500-2550 мг/сут. в 2-3 приема. Все другие сахароснижающие препараты для лечения СД отменялись. В дальнейшем пациенты были распределены на две группы: одна группа пациентов в течение 16 недель получала терапию Хумалог® Микс® 25, который назначался перед завтраком и ужином в комбинации с метформином (1500-2550 мг/сут.). Затем пациенты переводились на лечение инсулином гларгин в однократном режиме перед сном в комбинации с метформином в той же дозировке в течение последующих 16 недель. Вторая группа больных получала лечение в обратной последовательности. Было показано, что уровень HbА1с у пациентов, получавших инсулин Хумалог® Микс® 25, оказался достоверно ниже (7,54 ± 0,87%), чем при применении инсулина гларгин (8,14 ± 1,03%) (рисунок 4). Уровни постпрандиальной гликемии после основных приемов пищи также были достоверно ниже при применении Хумалог® Микс® 25 в комбинации с метформином (рисунок 5). В то же время необходимо отметить, что показатели уровня глюкозы крови натощак оказались достоверно ниже при лечении инсулином гларгин в комбинации с метформином.
Необходимо отметить, что несмотря на более низкий уровень гликемии в 3 часа ночи на фоне терапии инсулином Хумалог® Микс™ 25 в комбинации метформином, частота ночных гипогликемий при этом была достоверно ниже (0,14 ± 0,49 эпизодов на 1 пациента за 30 дней), чем при комбинированной терапии инсулином гларгин с метформином (0,34 ± 0,85 эпизодов на 1 пациента за 30 дней). Однако общая частота гипогликемий была примерно одинаковой (0,61 ± 1,41 и 0,44 ± 1,07 эпизодов на 1 пациента за 30 дней, при применении инсулинов Хумалог® Микс™ 25 и гларгин, соответственно).
Таким образом, применение смеси инсулинов Хумалог® Микс™ 25 в комбинированной терапии с метформином у пациентов с СД типа 2 в режиме двух инъекций в сутки позволяет регулировать не только уровень гликемии натощак и перед основными приемами пищи, но и постпрандиальные колебания глюкозы крови. Это, безусловно, повышает эффективность лечения пациентов с СД типа 2, что положительно отражается на их качестве жизни.
Одним из важнейших показателей безопасности, характеризующих лечение инсулинами, являются частота и тяжесть гипогликемий. Хорошо известно, что по мере улучшения контроля гликемии возрастает и частота развития эпизодов гипогликемии.
Основной целью исследования M. Herz и соавт., опубликованном в 2002 г., было сравнение гликемического контроля и частоты гипогликемий для Хумалог® Микс™ 25 по сравнению с глибенкламидом при сравнении препрандиального и постпрандиального введения готовой смеси Хумалог® Микс™ 25 у наиболее сложной группы пациентов 60-80 лет с СД типа 2 и персистирующими гипогликемиями на терапии препаратами сульфонилмочевины. В этом 16-недельном открытом исследовании с параллельными группами пациенты случайным образом распределялись по группам с двумя возможными видами терапии: глибенкламид 15 мг/сут. (или до максимальной дневной дозы) и Хумалог® Микс™ 25. Группа Хумалог® Микс™ 25 была случайным образом разделена на подгруппы с препрандиальными (непосредственно перед завтраком и ужином) и постпрандиальными (в течение 15 мин. после начала завтрака и ужина) инъекциями препарата. Основными клиническими исходами были гликемический контроль и частота гипогликемий. В общей сложности было рандомизировано 143 пациента; 127 исследование завершили. Изменения уровня гликированного гемоглобина (HbA1c) от исходного уровня до конечного значения было значительно выше в группе терапии Хумалог® Микс™ 25, чем в группе глибенкламида (среднее ± СО, –1,14 ± 0,18%, по сравнению с –0,36 ± 0,15%, p = 0,001). Изменения HbA1c для препрандиального и постпрандиального введения Хумалог® Микс™ 25 значимого различия не имели (–1,20 ± 0,26%, по сравнению с –1,08 ± 0,26%, p = 0,748). Глюкоза в плазме крови (ГПК) натощак, 2-часовая постпрандиальная ГПК и средние дневные снижения ГПК были выше в группе терапии Хумалог® Микс™ 25, чем в группе терапии глибенкламида (p < 0,001); не было выявлено различий между препрандиальными и постпрандиальными инъекциями Хумалог® Микс™ 25 в отношении любого из этих параметров. Частота гипогликемий возросла в группе Хумалог® Микс™ 25 на 0,17 ± 0,02 эпизода на 1 пациента за 30 дней, но не изменилась при терапии глибенкламидом (p = 0,077). Масса тела увеличилась на 1,02 ± 0,35 кг в группе терапии Хумалог® Микс™ 25 и снизилась на 0,85 ± 0,18 кг в группе терапии глибенкламидом (p < 0,001). По сравнению с глибенкламидом терапия готовой инсулиновой смесью Хумалог® Микс™ 25 значительно улучшала показатели гликемического контроля у пациентов с СД типа 2 из старшей возрастной группы. Введение этого инсулина после принятия пищи не приводило к ухудшению гликемического контроля и хорошо переносилось пациентами. Приведем данные исследования (Tirgoviste C.I. и соавт., 2003), основной целью которого было сравнение показателей средних колебаний постпрандиальной гликемии после завтрака и ужина при терапии смесью Хумалог® Микс™ 25 и пероральной сахароснижающей терапии глибенкламидом у пациентов с СД типа 2. Также вторичными задачами было сравнение двух видов терапии по следующим параметрам: гликированный гемоглобин, глюкоза в плазме крови натощак, глюкоза в плазме крови перед ужином, частота гипогликемий, масса тела, удовлетворенность терапией (по данным опроса).
Описанное исследование является рандомизированным, открытым, с параллельными группами сравнением режимов двух терапий у пациентов с СД типа 2. Данное исследование состояло из двух периодов. Вводный период продолжался 10 ± 7 дней; все пациенты принимали глибенкламид. Период лечения продолжался 16 недель. Пациенты были случайным образом распределены в группы, где они получали либо глибенкламид 15 мг/сут., либо переводились на терапию Хумалог® Микс™ 25 перед завтраком и ужином. Оценка гликемического контроля проводилась по показателю HbA1c, показателям самоконтроля гликемии в плазме крови по 4 точкам и отчетам пациентов о случаях гипогликемии. Каждый участник заполнил опросный лист по степени удовлетворенности терапией. Участвовало 175 пациентов из двух стран: Румыния – 100 пациентов и Россия – 75 пациентов. 85 были рандомизированы в группу терапии Хумалог® Микс™ 25 и 90 – в группу с глибенкламидом. Анализ эффективности был проведен по данным 172 пациентов. Не было различий между группами терапии по демографическим параметрам (возраст, пол, рост, масса тела, индекс массы тела) и параметрам эффективности (HbA1c и показатели гликемии по данным самоконтроля). Средний возраст был 59,5 ± 8,2 лет; 35,5% (61/172) пациентов были мужчинами. Средний индекс массы тела был 27,2 кг/м2. Средняя длительность СД типа 2 – 10,2 ± 6,6 лет, средняя продолжительность терапии препаратами сульфонилмочевины – 5,8 ± 5,9 лет. Средние уровни HbA1c и гликемии натощак были соответственно 10,07 ± 1,4% и 11,6 ± 2,8 ммоль/л в группе терапии глибенкламидом и 9,85 ± 1,2% и 12,2 ± 2,9 ммоль/л – в группе терапии Хумалог® Микс™. В конце исследования все параметры эффективности улучшились больше в группе терапии Хумалог® Микс™ (HbA1c, показатели гликемии натощак и постпрандиальной гликемии). Средний HbA1c был значительно ниже в группе терапии Хумалог® Микс™, чем в группе терапии глибенкламидом (Хумалог® Микс™, 8,5 ± 1,3%; глибенкламид, 9,4 ± 1,8%; p = 0,001). Для всех значений гликемии по данным самоконтроля в группе с Хумалог® Микс™ наблюдалось более значительное снижение от исходных уровней: –1,4% по сравнению с –0,7% для HbA1c, (p = 0,004); –2,8 ммоль/л по сравнению с –1,1 ммоль/л для глюкозы в плазме крови натощак (p < 0,01); –5,1 ммоль/л по сравнению с –1,7 ммоль/л для утренней 2-часовой постпрандиальной глюкозы в плазме крови (p < 0,001); –2,2 ммоль/л по сравнению с –0,8 ммоль/л для вечерней препрандиальной глюкозы в плазме крови (p < 0,05); 4,4 ммоль/л по сравнению с –1,5 ммоль/л для вечерней 2-часовой постпрандиальной глюкозы в плазме крови (p < 0,001). Процент пациентов, испытавших не менее одного эпизода гипогликемии, был, как и ожидалось, выше в группе с Хумалог® Микс™ (44,7 по сравнению с 10,3%; p = 0,01). Пациенты были более удовлетворены терапией Хумалог® Микс™, чем глибенкламидом, по данным взвешенного комбинированного индекса опросника степени удовлетворенности терапией (2,0 ± 1,3 по сравнению с 0,7 ± 1,3). Таким образом, авторы сделали вывод о том, что когда более не удается поддерживать гликемический контроль при помощи пероральных сахароснижающих препаратов, терапия инсулином должна рассматриваться как следующий вариант лечения. Терапия Хумалог® Микс™ обеспечивала хороший общий гликемический контроль, а также удовлетворенность пациентов терапией.
Таким образом, готовая смесь инсулина лизпро Хумалог® Микс™ обладает сопоставимым профилем безопасности с другими препаратами инсулина, включая прогрессирование осложнений сахарного диабета и наличие антител к инсулину (2, 3, 14). Суммируя вышеизложенное, можно сделать следующие выводы относительно безопасности препарата:
- оба инсулина, входящие в состав препарата, хорошо переносятся;
- оба инсулина обладают сопоставимыми профилями побочных эффектов;
- не было описано случаев тяжелых гипогликемических состояний или серьезных побочных эффектов;
- не возникало каких-либо вопросов об аспектах безопасности препаратов.
- Преимущества применения Хумалог® Микс™ включают в себя:
- удобство и точность готовых смесей инсулинов в отличие от самостоятельного смешивания;
- быстрое начало действия;
- инъекции ближе ко времени принятия пищи;
- имитация естественного физиологического профиля;
- легкий переход с Хумулина 70/30 – «единица на единицу».
Инсулин лизпро Хумалог® Микс™ обладает ультракоротким действием, что характеризуется более быстрым началом действия (через 10-15 мин. после инъекции), более ранним пиком действия (через 60 мин. после введения) и более коротким периодом сахароснижающего действия (около 4 ч) по сравнению с обычным человеческим инсулином. Таким образом, ультракороткий аналог имеет более физиологический временной профиль активности, чем применяемые в настоящее время обычные инсулины короткого действия. Кроме того, согласно результатам исследования, выполненным в ФГУ «Эндокринологический научный центр Росмедтехнологий», при введении инсулина лизпро наблюдалась достоверно меньшая внутрииндивидуальная вариабельность. Следствием этого стала возможность лучшей предсказуемости сахароснижающего действия при многократном введении одинаковых доз одному и тому же пациенту и, помимо этого, возможность лучшего подбора дозы для разных пациентов.
Следует отметить, что клиническая эффективность инсулинотерапии определяется не просто снижением уровня гликированного гемоглобина (HbA1c), а снижением уровня HbA1c без увеличения риска развития сопутствующих гипогликемий. При терапии с использованием инсулиновых аналогов короткого действия отмечаются более быстрое всасывание аналогов, снижение риска гипогликемий, положительное влияние на показатели гликемии до и после приема пищи, а также эффективность терапии с использованием шприц-ручек и помповой терапии, которая является наиболее физиологической инсулинотерапией. Хумалог® Микс™ включен в список Б и может использоваться при лечении беременных и кормящих женщин, так как является одним из самых безопасных инсулиновых препаратов с наиболее длительным опытом применения в клинической практике.
Дополнительным преимуществом инсулина Хумалог® Микс™, повышающим приверженность инсулинотерапии, является возможность его введения непосредственно перед приемом пищи или сразу после приема пищи. Такой режим более удобен для пациентов, так как создает определенный временной резерв для введения и обеспечивает возможность поддержания эффективного контроля гликемии.
Терапия Хумалог® Микс™ эффективно снижает показатели постпрандиальной гликемии и таким образом способствует снижению сердечно-сосудистой заболеваемости и смертности у пациентов с СД типа 1 и 2. Установленным фактом является улучшение постпрандиального контроля у пациентов с СД типа 1 при терапии Хумалог® Микс™ (20, 21). Этот факт связан с быстрой скоростью абсорбции Хумалог® Микс™ (инсулина лизпро) после подкожной инъекции вследствие низкой склонности инсулина лизпро к комплексированию в месте инъекции (22, 23). Терапия инсулином лизпро также ассоциируется с более низкой, по сравнению с обычным человеческим инсулином, частотой гипогликемических эпизодов (20, 21). В исследовании P. Ebeling et al. (1997) переход пациентов с Хумулина Регуляр на инсулин лизпро Хумалог® Микс™ в качестве прандиального инсулина сопровождался значительным снижением средней гликемии в течение дня и уровней HbA1c, без повышения частоты гипогликемических эпизодов. Корректировка дозы заключалась в снижении дозы перед приемами пищи с увеличением базальной и общей дозы, а также количества инъекций базального инсулина. Быстрая скорость абсорбции и узкий пик действия инсулина лизпро (22, 23), а также повышение дозы базального инсулина могут объяснить снижение дозы до еды по сравнению с обычным человеческим инсулином. В то время как уровни постпрандиальной гликемии служат в качестве указателя для коррекции доз инсулина перед приемами пищи, следует опираться на показатели гликемии до еды при корректировке режима базального инсулина. Большая гибкость, ассоциирующаяся с терапией Хумалог® Микс™ – инсулином лизпро, – инъекция прямо перед едой, во время или сразу после приема пищи, рассматривается в качестве одного из основных преимуществ. Это наблюдение получило подтверждение в том факте, что свыше 80% пациентов решили, что режим интенсивной терапии инсулином лизпро в сочетании с базальным инсулином НПХ сопоставим или лучше, чем терапия обычным человеческим инсулином.
Таким образом, препаратом выбора для коррекции постпрандиальной гликемии и снижения риска сердечно-сосудистой заболеваемости является Хумалог® Микс™, самый первый и самый проверенный аналог инсулина ультракороткого действия с самой длительной историей безопасного применения. После серии из 4 публикаций в журнале «Diabetologia», который является официальным журналом Европейской Ассоциации по изучению сахарного диабета (EASD) на тему риска развития онкологической патологии при назначении аналогов инсулина (в основном это относилось к назначению аналога инсулина длительного действия гларгина (Лантуса) и его возможной взаимосвязи с раком), EASD было представлено заключение о том, что представленные результаты не являются исследованиями с окончательными выводами, а необходимы будущие исследования в этом направлении, и EASD не рекомендуют отменять терапию инсулином гларгин на основании данных этих исследований. В связи с этим и для того, чтобы предоставить полную информацию по любым аспектам, мы приводим последние данные об исследованиях митогенного потенциала инсулина Хумалог® Микс™ (инсулин лизпро).
Инсулин лизпро: исследования митогенного потенциала
В нескольких исследованиях in vitro оценивали митогенный потенциал аналогов инсулина в нормальных и трансформированных клетках. Исследования показали, что инсулин лизпро может обладать несколько более высоким сродством к рецептору ИФР-1, но по всем остальным параметрам митогенной активности сходен с человеческим инсулином. Инсулин лизпро продемонстрировал сходную с человеческим инсулином способность связываться с рецептором инсулина и в 1,5 раза более высокую, чем у человеческого инсулина, аффинность в отношении рецептора ИФР-1. Несмотря на это несколько более высокое сродство к рецептору ИФР-1, в клетках остеосаркомы человека у инсулина лизпро был более низкий, чем у человеческого инсулина (100%), митогенный потенциал (66% ± 10%), сопоставимый с митогенным потенциалом инсулина аспарт (58% ± 22%) (24). Кроме того, по скорости диссоциации с рецептором инсулин лизпро не отличался от человеческого инсулина (25). В исследовании с использованием эпителиальных клеток молочной железы человека продемонстрировано сходство митогенного потенциала инсулина лизпро и простого человеческого инсулина (25). Два дополнительных исследования инсулина лизпро in vitro не выявили признаков его повышенной митогенности (26, 27).
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.