Оптимизация аппликационной анестезии в подологии
- Аннотация
- Статья
- Ссылки
- English
Введение
В практике врачей, которые специализируются в ведении пациентов с патологиями в области стопы, вопрос анестезии имеет первостепенное значение. К сожалению, некоторые подологические манипуляции сопровождаются болью и дискомфортом, а обеспечение инфильтрационной или проводниковой анестезии не всегда представляется возможным в связи с противопоказаниями, такими как индивидуальная непереносимость препаратов, коагулопатии, тяжелые декомпенсированные формы сердечно-сосудистой патологии, эндокринопатии в стадии декомпенсации и др. В связи с этим возникает потребность в разработке и оптимизации методов аппликационной анестезии без нарушения кожного барьера.
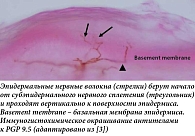
За болевую чувствительность кожи отвечают преимущественно свободные нервные окончания первичных афферентных нейронов. Сигнал проводится по двум типам волокон: Aδ-волокна (А-дельта) – тонкие миелинизированные, характеризуются способностью быстро проводить импульс, что ассоциируется с колющей болью; С-волокна – немиелинизированные, медленные, отвечают за жгучую и ноющую боль и зудоподобные ощущения. Окончания двух типов волокон, согласно современным литературным данным, располагаются в глубоких слоях эпидермиса (базальном и шиповатом) и сосочковом слое дермы [1, 2]. На уровне молекулярной трансдукции ноцицептивные стимулы активируют ионные каналы на окончаниях (в т.ч. семейство Transient Receptor Potential, TRP), что вызывает деполяризацию и генерацию потенциалов действия, при этом частота импульса коррелирует с интенсивностью стимула, что и воспринимается как боль [2]. Большинство манипуляций в области периунгвальной зоны вызывает стимуляцию именно этих свободных окончаний, поэтому клиническая задача аппликационной анестезии – довести эффективную концентрацию анестетика до уровня, где расположены Aδ- и С-волокна (рис. 1) [3].
В области стопы существуют определенные анатомо-физиологические особенности кожи, отличающие ее от других зон: существенно более толстый роговой слой и наличие блестящего слоя, что значительно влияет на трансэпидермальную проницаемость. В работе S. Brito и соавт. указано, что stratum corneum подошвенной части может быть в 16 раз толще тонкой кожи; при этом толщина эпидермиса на стопах может достигать ~600 мкм. Эффективность доставки действующих веществ зависит от гидратации, окклюзии и целостности барьера [4]. В связи с вышеперечисленными особенностями встает вопрос о разработке методов, усиливающих глубину проникновения анестетиков и уменьшающих время их экспозиции.
Комбинированный местный анестетик ЭМЛА
ЭМЛА представляет собой эвтектическую смесь двух амидных анестетиков (лидокаин 25 мг и прилокаин 25 мг) в виде 5%-ного крема, часто используемого для предотвращения боли во время венепункции и поверхностных хирургических вмешательств. Данная лекарственная форма облегчает диффузию действующих веществ и имеет преимущества по сравнению с кристаллическими монопрепаратами. Согласно данным электронного сборника лекарственных средств (Electronic Medicines Compendium), глубина проникновения препарата увеличивается со временем экспозиции и составляет через один час после аппликации – 2 мм, через 120 минут – 3 мм [5].
В рандомизированном сравнительном исследовании на здоровых добровольцах было продемонстрировано, что крем ЭМЛА обеспечивает статистически более выраженную кожную анестезию, чем 10%-ный крем лидокаина в виде монопрепарата (p < 0,001). Также были уточнены параметры оптимальной экспозиции: минимальное время аппликации перед воздействием иглой на глубину 4 мм, при котором пациенты отмечали приемлемую интенсивность боли, составило примерно 40,88 минуты для крема ЭМЛА, тогда как для 10%-ного крема лидокаина – около 45,38 минуты [6].
В исследовании C.F. Wahlgren и соавт. крем ЭМЛА наносили под окклюзионную повязку на левое бедро 16 испытуемым, затем проводили биопсию с помощью панча и оценивали боль по визуальной аналоговой шкале (ВАШ). Было продемонстрировано, что после 60 и 120 минут нанесения препарата средняя глубина введения панча, при которой пациенты ощущали приемлемую боль, составила 2,9 и 4,5 мм (p < 0,01) соответственно. После четырех часов экспозиции у всех пяти испытуемых, у которых продолжительность аппликации крема превышала 120 минут, было выполнено введение панча на глубину 6 мм, при которой пациенты оценивали боль как приемлемую [7].
В обзоре по применению местных анестетиков в дерматологии и хирургии (2023) подчеркнуто, что ЭМЛА является наиболее часто используемым топическим препаратом, содержащим лидокаин; обсуждается возможность применения ЭМЛА при малоинвазивных дерматологических и эстетических процедурах [8].
Таким образом, протоколы с экспозицией крема ЭМЛА более 60 минут являются физиологически обоснованными для достижения уровня, на котором снижается болевая чувствительность [5, 7, 9].
Методы оптимизации аппликационной анестезии
Для повышения эффективности топической анестезии в дерматологии и, в частности, в подологии применяют следующие методы: использование окклюзионных повязок, увеличение времени экспозиции, нанесение толстого слоя препарата, выбор эвтектических смесей, предварительная подготовка кожи в виде истончения рогового слоя. Отдельный интерес представляют пенетранты (энхансеры) – вещества, усиливающие трансэпидермальное проникновение анестетиков. Основным требованием к ним является отсутствие химических реакций с другими препаратами [10].
Примером наиболее изученного энхансера, который довольно часто применяется для повышения проницаемости кожи, является диметилсульфоксид (ДМСО).
В работе E.O. Bakhrushina и соавт. отмечено, что ДМСО способен усиливать пенетрацию веществ вследствие дезорганизации липидов рогового слоя, изменения водной среды и связывания с кератином; также описан механизм формирования водных каналов. Вместе с тем отмечается наличие нежелательных явлений в случае применения этого вещества в высокой концентрации, могут возникнуть аллергический и/или ирритантный контактный дерматиты, в связи с чем крайне важно проводить предварительную аллергическую пробу перед включением ДМСО в протокол аппликационной анестезии [1, 4, 11, 12].
В работе E. Greuber и соавт. при исследовании in vitro продемонстрирован эффект выраженного проникновения лидокаина в кожу в случае сочетания его с ДМСО (в 1,4 раза больше) по сравнению с контрольной группой, где применяли чистый раствор лидокаина [12]. Эти данные создают предпосылки и фармакологическое обоснование для включения ДМСО в протоколы, направленные на усиление эффекта местных анестетиков, особенно в подологии при работе с толстой кожей, когда нередко требуется увеличение стандартной экспозиции лекарственных средств.
Цель – оценить влияние оптимизированного протокола аппликационной анестезии (предварительная аппликация 25%-ного раствора диметилсульфоксида в течение 10 минут с последующим нанесением крема ЭМЛА под окклюзию на 60 минут) на выраженность болевого синдрома по ВАШ при малоинвазивном подологическом удалении вросшего ногтя по сравнению с выполнением аналогичного вмешательства без анестезии.
Материал и методы
В исследование были включены 32 пациента мужского и женского пола в возрасте от 23 до 46 лет с диагнозом онихокриптоз. Пациенты были распределены на две группы по 16 человек: в группе А (n = 16) проводили малоинвазивное удаление вросшего сегмента без анестезии, в группе Б (n = 16) перед вмешательством проводили аппликацию 25%-ного раствора диметилсульфоксида в течение 10 минут с последующим нанесением крема ЭМЛА (лидокаин + прилокаин) под окклюзию на 60 минут. Перед проводимыми манипуляциями все пациенты были ознакомлены с протоколом процедуры и подписали индивидуальное согласие. Участникам исследования в группе Б проводили аллергическую пробу: на область локтевого сгиба наносили небольшое количество 25%-ного раствора диметилсульфоксида в объеме, достаточном для равномерного смачивания участка, после чего проводили экспозицию в течение 20 минут. Далее участок кожи осматривали и фиксировали наличие или отсутствие местной реакции в виде эритемы, отека, мокнутия. Параллельно оценивали субъективную симптоматику в виде зуда и жжения. При наличии признаков непереносимости пациента исключали из исследования.
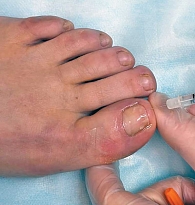
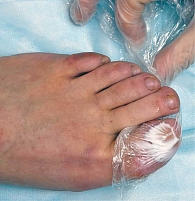
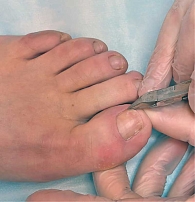
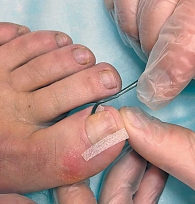
Пациентам из обеих групп проводили резекцию вросшего сегмента ногтевой пластины с помощью профессионального подологического оборудования и материалов: кюрета, щипцы для коррекции вросшего ногтя, перевязочный материал, антисептики. Протокол манипуляции представлен на рис. 2–5.
Интенсивность боли фиксировали во время выполнения вмешательства с использованием ВАШ, где 0 баллов соответствовало отсутствию боли, а 10 баллов – максимально возможной боли.
Статистический анализ выполняли в программе IBM SPSS Statistics. Для сравнения независимых групп по ВАШ применяли непараметрический U-критерий Манна – Уитни. Уровень статистической значимости оценивали при p ≤ 0,05 и p ≤ 0,01. Результаты представляли как описательные показатели и значения критерия Манна – Уитни.
Результаты
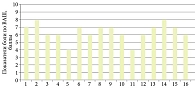
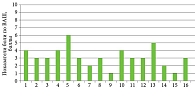
По данным описательной статистики, выраженность болевого синдрома в группе А была выше, чем в группе Б. Для группы А были характерны средние значения по ВАШ 6–7 баллов (медиана – 6,5), диапазон составил 4–8 баллов. В группе Б значения ВАШ были ниже: медиана – 3,0, диапазон – 1–6 баллов. Таким образом, наблюдалось снижение болевой реакции в группе Б, где вмешательство выполняли после аппликационной анестезии.
При межгрупповом сравнении получено эмпирическое значение критерия Uэмп = 10. Табличные (критические) значения для сравниваемых выборок составили Uкр = 83 при уровне значимости p ≤ 0,05 и Uкр = 66 при уровне значимости p ≤ 0,01. Поскольку Uэмп (10) меньше Uкр при p ≤ 0,01 (66), различия между группами по уровню боли по ВАШ являются статистически значимыми и находятся в зоне значимости на уровне p ≤ 0,01.
Нежелательных явлений в виде зуда, жжения, мокнутия, эритемы, везикул во время процедуры, а также через 45 минут и через 24 часа после не наблюдалось.
Полученные данные свидетельствуют о том, что применение протокола аппликационной анестезии в группе Б связано с достоверным снижением болевого синдрома при малоинвазивном подологическом удалении вросшего ногтя по сравнению с выполнением аналогичного вмешательства без анестезии. Результаты представлены на рис. 6 и 7.
Заключение
Результаты представленного исследования показали, что применение оптимизированного протокола аппликационной анестезии в подологической практике (предварительная аппликация 25%-ного раствора диметилсульфоксида в течение 10 минут с последующим нанесением крема ЭМЛА под окклюзию на 60 минут) ассоциировано с достоверным выраженным снижением интенсивности боли при малоинвазивном удалении вросшего ногтя по сравнению с проведением аналогичного вмешательства без анестезии. Различия между группами по визуально-аналоговой шкале боли статистически значимы по U-критерию Манна – Уитни (Uэмп = 10; зона значимости при p ≤ 0,01).
Предложенный протокол может применяться в клинической практике для повышения переносимости малоинвазивных вмешательств в области стопы. Вместе с тем при включении диметилсульфоксида в схему аппликационной анестезии важным условием является предварительная оценка индивидуальной переносимости (аллергическая проба) и соблюдение стандартных мер безопасности местного применения.
L.S. Kruglova, PhD, Prof., R.Yu. Mayorov
Central State Medical Academy of Department of Presidential Affairs, Moscow
Contact person: Roman Yu. Mayorov, roman1396@bk.ru
The success of podiatric procedures is largely determined by adequate patient tolerance. Infiltration or conduction anesthesia is limited in some patients due to contraindications. EMLA, a 5% cream containing a eutectic mixture of two amide anesthetics (lidocaine 25 mg and prilocaine 25 mg), is one of the most commonly used anesthetics in surgical and cosmetic practices. However, its use in podiatry remains understudied. Due to the anatomical features of foot skin, improved topical anesthesia techniques are needed to achieve deeper penetration of anesthetic agents and reduce their exposure time.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.