Обратимый субъективный когнитивный дефицит у пациентов с лекарственно-индуцированной головной болью
- Аннотация
- Статья
- Ссылки
- English
Цель – проанализировать встречаемость СКД у пациентов с ЛИГБ до и после лечения головной боли и выявить факторы, ассоциированные с его развитием.
Материал и методы. Проспективное исследование включило 171 пациента с ЛИГБ и 173 пациентов без ЛИГБ. В ходе обследования одновременно проводилось профессиональное полуструктурированное интервью и использовался опросник субъективного когнитивного дефицита PDQ-20. После лечения (не ранее 12 месяцев после первого интервью) у пациентов обеих групп повторно оценивали наличие СКД.
Результаты. До начала лечения СКД отмечался у 130 (76,0%) пациентов с ЛИГБ и 92 (53,2%) пациентов без ЛИГБ (p < 0,001; отношение шансов (ОШ) 2,8; 95%-ный доверительный интервал (ДИ) 1,8–4,8). Факторы, ассоциированные с наличием СКД у пациентов с ЛИГБ, включали: прием двух и более любых препаратов для купирования головной боли в день в течение ≥ 10 дней в месяц (59,2%; р = 0,02; ОШ 1,9; 95% ДИ 1,1–3,2), прием обезболивающих препаратов ночью (55,4%; р < 0,001; ОШ 3,3; 95% ДИ 1,9–5,9) и ночные головные боли (66,2%; р < 0,001; ОШ 2,8; 95% ДИ 1,6–4,8). После лечения СКД регрессировал у 97,3% пациентов с ЛИГБ и 98,5% пациентов без ЛИГБ. При этом ЛИГБ отсутствовала у 86,3% человек, частота возникновения головных болей снизилась до < 15 дней в месяц у 86,3% (р < 0,001; ОШ 0,4; 95% ДИ 0,3–0,7), частота приема обезболивающих препаратов – до < 10 дней в месяц у 86,3% (р < 0,001; ОШ 11,4; 95% ДИ 5,8–22,5). Отсутствие приема препаратов ночью зарегистрировано у 89,0% (р < 0,001; ОШ 10,9; 95% ДИ 4,9–24,1), ночных головных болей – у 87,7% (р <0,001; ОШ 15,8; 95% ДИ 7,3–34,2). Таким образом, лечение ЛИГБ, проведенное в соответствии с международными и отечественными рекомендациями, ассоциировано с регрессом СКД.
Выводы. Впервые показано, что СКД может быть обратимым состоянием, регрессирующим на фоне адекватного лечения ЛИГБ, снижения частоты возникновения головных болей, использования обезболивающих препаратов (в том числе ночью) и купирования ночных головных болей.
Цель – проанализировать встречаемость СКД у пациентов с ЛИГБ до и после лечения головной боли и выявить факторы, ассоциированные с его развитием.
Материал и методы. Проспективное исследование включило 171 пациента с ЛИГБ и 173 пациентов без ЛИГБ. В ходе обследования одновременно проводилось профессиональное полуструктурированное интервью и использовался опросник субъективного когнитивного дефицита PDQ-20. После лечения (не ранее 12 месяцев после первого интервью) у пациентов обеих групп повторно оценивали наличие СКД.
Результаты. До начала лечения СКД отмечался у 130 (76,0%) пациентов с ЛИГБ и 92 (53,2%) пациентов без ЛИГБ (p < 0,001; отношение шансов (ОШ) 2,8; 95%-ный доверительный интервал (ДИ) 1,8–4,8). Факторы, ассоциированные с наличием СКД у пациентов с ЛИГБ, включали: прием двух и более любых препаратов для купирования головной боли в день в течение ≥ 10 дней в месяц (59,2%; р = 0,02; ОШ 1,9; 95% ДИ 1,1–3,2), прием обезболивающих препаратов ночью (55,4%; р < 0,001; ОШ 3,3; 95% ДИ 1,9–5,9) и ночные головные боли (66,2%; р < 0,001; ОШ 2,8; 95% ДИ 1,6–4,8). После лечения СКД регрессировал у 97,3% пациентов с ЛИГБ и 98,5% пациентов без ЛИГБ. При этом ЛИГБ отсутствовала у 86,3% человек, частота возникновения головных болей снизилась до < 15 дней в месяц у 86,3% (р < 0,001; ОШ 0,4; 95% ДИ 0,3–0,7), частота приема обезболивающих препаратов – до < 10 дней в месяц у 86,3% (р < 0,001; ОШ 11,4; 95% ДИ 5,8–22,5). Отсутствие приема препаратов ночью зарегистрировано у 89,0% (р < 0,001; ОШ 10,9; 95% ДИ 4,9–24,1), ночных головных болей – у 87,7% (р <0,001; ОШ 15,8; 95% ДИ 7,3–34,2). Таким образом, лечение ЛИГБ, проведенное в соответствии с международными и отечественными рекомендациями, ассоциировано с регрессом СКД.
Выводы. Впервые показано, что СКД может быть обратимым состоянием, регрессирующим на фоне адекватного лечения ЛИГБ, снижения частоты возникновения головных болей, использования обезболивающих препаратов (в том числе ночью) и купирования ночных головных болей.
Введение
Лекарственно-индуцированной считается головная боль, возникающая 15 и более дней в месяц на протяжении не менее трех месяцев у пациента с первичной головной болью и развивающаяся как следствие регулярного чрезмерного использования обезболивающих препаратов для купирования головной боли (не менее 10–15 дней в месяц в зависимости от класса лекарственных средств) в течение не менее трех месяцев [1]. Одним из факторов, утяжеляющих течение и лечение головной боли, является наличие когнитивных нарушений [2–8].
В предыдущем исследовании мы впервые обнаружили наличие субъективного когнитивного дефицита (СКД) у 76% пациентов с лекарственно-индуцированной головной болью (ЛИГБ) [9]. СКД – это субъективное стойкое ощущение ухудшения когнитивных способностей, не связанное с каким-либо острым состоянием, сочетающееся с нормальным выполнением (в соответствии с возрастом и уровнем образования) стандартных тестов на выявление легких и умеренных когнитивных нарушений [10]. Для его диагностики M. Sullivan и соавт. в 1990 г. разработали опросник субъективного когнитивного дефицита (Perceived Deficits Questionnaire, PDQ). Впервые он был применен у пациентов с рассеянным склерозом для самостоятельной оценки наличия когнитивных нарушений [11]. Этот метод быстрой клинической оценки предоставляет информацию о состоянии когнитивных функций пациента [12].
Исследования СКД проводились у пациентов с мигренью, тревогой, депрессией, рассеянным склерозом, фибромиалгией, системной красной волчанкой и болезнью Альцгеймера [13–18]. Однако ранее исследований СКД до и после лечения заболеваний, способных влиять на его развитие, в том числе ЛИГБ, не выполнялось.
Цель – проанализировать встречаемость СКД у пациентов с ЛИГБ до и после лечения головной боли и выявить факторы, ассоциированные с его развитием.
Материал и методы
Проспективное исследование по типу «случай – контроль» проводилось на базе Международного центра лечения головных болей «Европа – Азия» (Екатеринбург) с марта 2021 г. по ноябрь 2025 г. Пациенты исследуемых групп (с ЛИГБ и без ЛИГБ) были сопоставимы по половозрастным характеристикам и обследовались параллельно.
Критерии включения:
- возраст 18 лет и старше;
- наличие ЛИГБ в основной группе и отсутствие – в контрольной;
- отсутствие нарушений речи, наркотической и алкогольной зависимости, тяжелых неврологических заболеваний в анамнезе (тяжелая черепно-мозговая травма, опухоли, операции на головном мозге, демиелинизирующие заболевания, эпилепсия, энцефалит, менингит, деменция);
- способность отвечать на вопросы интервью;
- согласие на дополнительные исследования (магнитно-резонансная томография, дуплексное сканирование брахиоцефальных артерий и другие) и консультации специалистов по показаниям.
Критерии невключения: основная жалоба – не головная боль, а боль иной локализации; отсутствие у пациента времени на интервью.
Критерии исключения: выявление вторичных видов головной боли после дополнительных обследований; невыполнение пациентом рекомендуемых дополнительных обследований.
СКД диагностировали при наличии ≥ 40 баллов по опроснику PDQ-20 [14]. Объективные исследования нарушений памяти с использованием других шкал и опросников не выполнялись.
Интервью пациентов с ЛИГБ и без ЛИГБ проводил невролог во время первой консультации, до лечения, а также в течение недели после консультации (телефонный разговор для уточнения дополнительной информации). Кроме того, пациенты обеих групп были проинтервьюированы в процессе динамического наблюдения после лечения, не ранее чем через 12 месяцев после первого интервью. Лечение проводилось в соответствии с международными и отечественными рекомендациями [19, 20] в течение 6–12 месяцев. Средний период наблюдения составил 29,3 месяца.
До и после лечения оценивали частоту возникновения головной боли, частоту использования препаратов для купирования головной боли в течение трех месяцев перед интервью, обезболивающих препаратов ночью, наличие ночных головных болей, а также СКД по шкале PDQ-20.
После первой консультации пациенты с ЛИГБ в зависимости от наличия СКД были разделены на две подгруппы, в которых оценивались факторы, ассоциированные с его наличием. Речь идет о демографических и коморбидных факторах, а также характеристике головных болей и приеме обезболивающих препаратов. Анализировалось влияние стресса, генерализованного тревожного и депрессивного расстройства, хронической инсомнии, COVID-19 в анамнезе и низкого уровня физической активности (≤ 3 часов интенсивной физической нагрузки в неделю).
Диагнозы головной боли установлены в соответствии с диагностическими критериями Международной классификации головных болей 3-го пересмотра [1]. Для диагностики хронической инсомнии использовалась Международная классификация расстройств сна (3-е издание, 2014 г.) [21], для диагностики тревожно-депрессивных расстройств – Госпитальная шкала тревоги и депрессии (Hospital Anxiety and Depression Scale, HADS).
Работа одобрена этическим комитетом Уральского государственного медицинского университета (протокол № 5 от 21 мая 2021 г.). Все пациенты были проинформированы о цели исследования и подписали информированное согласие на участие в нем.
Статистический анализ
Статистический анализ осуществлялся с помощью программ Stata (версия 14.0). Для количественных переменных рассчитывались средние значения, для качественных – проценты (долевое отношение). Определялось также отношение шансов (ОШ) с 95%-ным доверительным интервалом (ДИ). Статистически достоверные различия между частотой потенциальных факторов риска у пациентов с ЛИГБ и пациентов без нее оценивались с помощью непарного t-критерия и критерия χ2.
Результаты
Основную группу составил 171 пациент с ЛИГБ (средний возраст – 43,3 года, 82,3% женщин, 17,7% мужчин, 64,9% пациентов с мигренью, 35,1% пациентов с головной болью напряжения), контрольную – 173 пациента без ЛИГБ (средний возраст – 42,2 года, 76,1% женщин, 23,9% мужчин, 57,8% пациентов с мигренью, 42,2% пациентов с головной болью напряжения). Уровень образования в обеих группах не имел статистически значимых различий: начальное/основное общее образование имели 4,7% пациентов с ЛИГБ и 4,0% без ЛИГБ, среднее и среднее специальное – 29,8 и 22,5%, высшее и неоконченное высшее – 65,5 и 74,0% пациентов соответственно.
Лидирующим диагнозом среди пациентов с ЛИГБ была хроническая мигрень – 53,2% (р < 0,001; ОШ 5,9; 95% ДИ 3,6–9,8), среди пациентов без ЛИГБ – эпизодическая мигрень, 52,6% (р < 0,001; ОШ 0,3; 95% ДИ 0,2–0,4). Пациенты основной и контрольной групп для купирования приступа головной боли использовали следующие лекарственные средства: нестероидные противовоспалительные препараты (НПВП) – 147 (86,0%) и 140 (80,9%) (р = 0,2), триптаны – 63 (36,8%) и 46 (26,6%) (р = 0,04; ОШ 1,6; 95% ДИ 1,02–2,6), НПВП и триптаны – 39 (22,8%) и 31 (17,9%) (р = 0,3) соответственно.
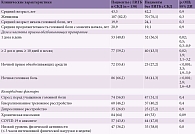
СКД имели 130 (76,0%) пациентов основной группы и 92 (53,2%) пациента – контрольной (p < 0,001; ОШ 2,8; 95% ДИ 1,8–4,8). Факторы, ассоциированные с наличием СКД у пациентов с ЛИГБ, представлены в табл. 1. Они включали: прием двух и более доз любых препаратов для купирования головной боли в день в течение ≥ 10 дней в месяц (59,2 и 43,5% соответственно; р = 0,02; ОШ 1,9; 95% ДИ 1,1–3,2); прием обезболивающих препаратов ночью (55,4 и 27,2%; р < 0,001; ОШ 3,3; 95% ДИ 1,9–5,9) и ночные головные боли (66,2 и 41,3% соответственно; р < 0,001; ОШ 2,8; 95% ДИ 1,6–4,8).
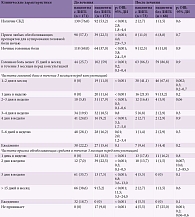
Результаты динамического наблюдения пациентов с ЛИГБ и без ЛИГБ до и после лечения, а также частота выявления СКД до и после лечения представлены в табл. 2.
После лечения СКД зафиксирован у 2 (2,7%) пациентов основной группы и 1 (1,5%) пациента – контрольной. На момент последнего интервью после лечения головная боль отсутствовала у 86,3% пациентов основной группы. При этом снижение частоты головной боли до одного-двух дней в месяц зарегистрировано у 41,1% пациентов. До начала лечения пациенты основной группы чаще, чем пациенты контрольной группы, принимали обезболивающие препараты для купирования приступа (≥ 15 дней в месяц): 38,6 и 5,2% соответственно (р < 0,001; ОШ 11,5; 95% ДИ 5,5–24,0). После лечения данный показатель в группах составил 2,7 и 1,5% соответственно (р = 0,6). До лечения жалобы на ночные головные боли предъявляли 69,0% пациентов основной группы, после лечения – 12,3%. Доля пациентов, принимающих любые обезболивающие препараты для купирования головной боли ночью, после лечения уменьшилась с 57,3 до 11,0%.
Таким образом, качественное лечение ЛИГБ, проведенное в соответствии с международными [19] и отечественными рекомендациями [20], показало возможность регресса СКД при устранении таких факторов, как прием обезболивающих препаратов ≥ 10 дней в месяц, прием любых обезболивающих препаратов для купирования головной боли ночью, наличие ночных головных болей, снижение частоты возникновения головной боли до < 15 дней в месяц.
Обсуждение
Наше исследование впервые показало, что СКД является фактором, ассоциированным с ЛИГБ, и может быть обратимым при адекватном лечении.
Потенциальные механизмы развития СКД у пациентов с ЛИГБ ассоциированы с негативным воздействием высокой частоты головной боли, ночной головной боли, чрезмерным приемом обезболивающих препаратов (в том числе ночью) и их влиянием на когнитивные функции. Наше исследование продемонстрировало, что на развитие СКД может влиять прием двух и более доз в день любых обезболивающих препаратов для купирования головной боли ≥ 10 дней в месяц.
В исследовании Y. Xiang и соавт. с участием пациентов с ЛИГБ показана взаимосвязь поражения белого вещества головного мозга и когнитивных нарушений, которые оценивались по Монреальской шкале [2]. Установлено, что продолжительность ЛИГБ и количество дней с головной болью в месяц служат значимыми предикторами когнитивных нарушений у пациентов данной группы. В нашем исследовании у пациентов с ЛИГБ в отличие от пациентов без ЛИГБ часто продолжительность головной боли превышала три года. При этом они имели высокую частоту возникновения головной боли (не менее 15 дней в месяц). Как следствие – избыточный прием препаратов для купирования приступов головной боли, в том числе ночью, и развитие СКД.
Используемые препараты для купирования головной боли, в частности НПВП, могут приводить к нарушению когнитивных функций [22]. Кроме того, прием НПВП (ибупрофен, диклофенак, пироксикам) нередко ассоциируется с развитием нарушений сна и депрессии [23]. Точные механизмы, ответственные за формирование данных нежелательных явлений НПВП, до конца не изучены, но могут быть обусловлены ингибированием простагландинов в центральной нервной системе, проникновением препаратов через гематоэнцефалический барьер, изменением активности нейромедиаторов и развитием гиперчувствительности на фоне регулярного приема НПВП [23]. Показано, что ибупрофен также задерживает наступление глубоких стадий сна за счет подавления уровня мелатонина [23]. Однако в другом исследовании влияния НПВП на когнитивные функции у пациентов с хронической мигренью не выявлено [24].
Пациенты с ЛИГБ могут принимать несколько препаратов для купирования головной боли, например НПВП и триптаны. Взаимодействие препаратов и их взаимное влияние, в том числе на когнитивные функции, требуют дальнейшего изучения [25].
Ночная головная боль вызывает проблемы со сном, включая его фрагментацию, аномальную продолжительность. Это связано с повышенным риском снижения когнитивных функций и деменции [26]. Механизмы, влияющие на это, включают нейровоспаление, нейродегенерацию и циркадианную десинхронизацию [26].
В настоящем исследовании хроническая мигрень была преобладающим диагнозом у пациентов с ЛИГБ. Жалобы на нарушение памяти, внимания, скорости обработки информации, затруднения при планировании и субъективный когнитивный дефицит часто встречаются у пациентов с хронической мигренью [4, 27]. Они могут быть следствием нейрохимических, электрических и атрофических изменений в зонах мозга, отвечающих за контроль боли и обеспечение когнитивных функций, аналогично процессам, происходящим в головном мозге при длительной депрессии [28]. Поскольку пациенты с хронической мигренью и другими типами хронической боли часто страдают депрессией, предполагается, что когнитивные нарушения у них вызваны ее наличием. Однако в нашем исследовании не установлено влияния тревожно-депрессивных расстройств на развитие СКД. Определенный вклад в нарушение когнитивных функций вносят изменения нервной системы на фоне хронической боли [4]. Предполагается, что когнитивные изменения во время приступа мигрени вызваны обратимой дисфункцией мозга на фоне центральной сенситизации. В результате происходят нейропластические изменения в областях мозга, отвечающих за анализ болевых и неболевых сигналов (снижение объема серого вещества дорсолатеральной префронтальной коры) [29–31]. По мере формирования хронической центральной сенситизации когнитивные нарушения становятся постоянными и сохраняются в межприступном периоде [28]. Таким образом, нарушения в ноци- и антиноцицептивных системах у пациентов с мигренью могут служить субстратом для формирования когнитивных нарушений.
Нейроэндокринная дисфункция способна влиять на развитие когнитивных нарушений. Показано, что у пациентов с хронической головной болью напряжения нарушения когнитивных способностей связаны с дисфункцией гипоталамо-гипофизарно-надпочечниковой и гипоталамо-гипофизарно-гонадной систем, а также системы «гипоталамус – гипофиз – щитовидная железа» [3]. Высокий уровень адренокортикотропного гормона ассоциируется с ухудшением общих когнитивных способностей и скорости мышления, а повышенный уровень тиреотропного гормона в сочетании с повышенным уровнем гонадотропин-рилизинг-гормона – с нарушением работы многозадачных систем. Повышенный уровень кортикотропин-рилизинг-гормона и кортизола, а также высокий уровень тиреотропин-рилизинг-гормона отрицательно влияют на продолжительность боли, качество сна и настроение [3]. Эти эффекты могут объясняться прямым влиянием уровня гормонов на когнитивные функции или косвенным влиянием на структуры мозга, связанные с познанием (префронтальная кора головного мозга и гиппокамп) [3].
Как показало наше исследование, субъективный когнитивный дефицит может быть обратимым состоянием при ЛИГБ и регрессирует после ее лечения. Хотя исследования СКД до и после лечения не проводились ранее, имеются работы, подтверждающие возможность регресса когнитивных нарушений при других состояниях, например после отмены или снижения дозы антихолинергических препаратов и вальпроевой кислоты, после лечения синдрома Кушинга и ряда других состояний [32, 33]. Кроме того, в одном исследовании регресс когнитивных нарушений выявлен через три месяца после лечения хронической мигрени [34]. Это свидетельствует о необходимости оценки когнитивных функций и их контроля до, в процессе и после лечения в целях профилактики и своевременной коррекции.
Заключение
Субъективный когнитивный дефицит у пациентов с ЛИГБ является многофакторным состоянием, связанным с избыточным использованием обезболивающих препаратов на фоне хронической головной боли и ассоциированных с ними факторов. Как показали результаты нашего исследования, СКД может быть обратимым состоянием, регрессирующим на фоне адекватного лечения ЛИГБ, снижения частоты возникновения головной боли и использования обезболивающих препаратов (в том числе ночью), купирования ночной головной боли. Это указывает на ведущую роль хронической головной боли и избыточного использования обезболивающих препаратов в генезе СКД у пациентов с ЛИГБ.
Рекомендации по практическому использованию полученных результатов сводятся к следующему.
- Необходимы своевременная оценка частоты возникновения головной боли и контроль использования обезболивающих препаратов со стороны врача и самого пациента, а также раннее назначение профилактического лечения.
- Нужно выявлять ситуации, когда недостаточно эффективное профилактическое лечение (из-за неправильно подобранного препарата, его неадекватной дозы или недостаточной продолжительности лечения) приводит к избыточному применению средств для купирования приступов головной боли (чаще, чем два дня в неделю).
- Профилактическое лечение головной боли при длительном проведении способно не только снизить частоту головной боли, но и улучшить когнитивные функции.
- Важно оценивать риск когнитивных нарушений при назначении фармакологического лечения для купирования головной боли. У всех пациентов, в том числе молодого и трудоспособного возраста, целесообразно оценивать когнитивные функции, в частности с использованием опросника PDQ-20 [11, 13, 14]. Кроме того, необходимо разъяснять пациентам опасность чрезмерного использования обезболивающих препаратов и их негативное влияние на когнитивные функции.
Авторы заявляют об отсутствии финансирования и конфликта интересов.
Ya.A. Knyazeva, D.V. Gilev, e.R. Lebedeva, PhD, Prof.
International Medical Headache Center ‘Europe-Asia’, Yekaterinburg
Ural State Medical University
Ural Federal University named after the First President of Russia B.N. Yeltsin
Contact person: Yana A. Knyazeva, neuro_k@mail.ru
Relevance. One of the factors aggravating the course and treatment of medication-overuse headache (MOH) may be the presence of subjective cognitive deficit, which could potentially be reversible and regress after treatment, but this has not been studied previously.
The purpose of this study is to analyze the occurrence of subjective cognitive deficit in patients with MOH before and after treatment of headaches and to identify factors associated with their development.
Material and methods. This prospective study included 171 patients with MOH and 173 patients without MOH, examined in parallel using a professional semi-structured interview and the perceived deficits questionnaire (PDQ-20) for evaluation of subjective cognitive deficit. After treatment (no earlier than 12 months after the first interview), patients in both groups were re-evaluated for subjective cognitive deficit.
Results. Before the start of treatment, 130 (76.0%) patients had subjective cognitive deficits among patients with MOH, 92 (53.2%) patients in the group without MOH (p < 0.001; OR 2.8; 95% CI 1.8–4.8). Factors associated with the presence of subjective cognitive deficits in patients with MOH included: taking ≥ 2 doses of any medications for headaches relieve per day for ≥ 10 days per month (59.2%; p = 0.02; OR 1.9; 95% CI 1.1–3.2); taking painkillers at night (55.4%; p < 0.001; OR 3.3; 95% CI 1.9–5.9) and night headaches (66.2%; p < 0.001; OR 2.8; 95% CI 1.6–4.8). After treatment, subjective cognitive deficits were absent in 97.3% of patients with MOH and in 98.5% of patients without MOH. At the same time, MOH was absent in 86.3%; the frequency of headaches became less than 15 days per month in 86.3% (p < 0.001; OR 0.4; 95% CI 0.3–0.7); taking painkillers decreased for less than 10 days per month in 86.3% (p < 0.001; OR 11.4; 95% CI 5.8–22.5); their nocturnal intake was absent in 89.0% (p < 0.001; OR 10.9; 95% CI 4.9–24.1), night headaches were absent in 87.7% (p < 0.001; OR 15.8; 95% CI 7.3–34.2). Thus, MOH treatment, conducted in accordance with international and Russian recommendations, is associated with regression of subjective cognitive deficit.
Conclusions. For the first time, it was found that subjective cognitive deficit can be a reversible condition that regresses against the background of adequate treatment of MOH, a decrease in the frequency of headaches and the use of painkillers (including at night) and the disappearance of night headaches.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.