Опыт применения ингибиторов тирозинкиназы у больных хроническим миелолейкозом в Самарской области
- Аннотация
- Статья
- Ссылки


Актуальность
Хронический миелоидный лейкоз (ХМЛ) – клональное миелопролиферативное заболевание, характеризующееся реципрокной хромосомной транслокацией t(9;22)(q34;q11.2), которая приводит к образованию филадельфийской хромосомы (Ph) и химерного гена BCR-ABL. Синтезируемый онкобелок Bcr-Abl является конститутивно активной тирозинкиназой, придающей лейкозным клеткам преимущество в выживании за счет усиленной пролиферации и сниженного апоптоза и увеличивающей геномную нестабильность посредством подавления репарации ДНК [1]. Более чем в 80% случаев ХМЛ диагностируется во время начальной, хронической фазы заболевания [2]. Без эффективного лечения пациенты с хронической стадией ХМЛ неизбежно переходят в продвинутые стадии и имеют сравнительно короткую продолжительность жизни.
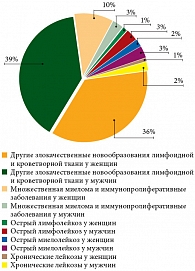
В течение последних 7 лет ХМЛ в Самарской области находится на пятом месте после злокачественных новообразований лимфоидной и кроветворной ткани, множественной миеломы и иммунопролиферативных заболеваний, острого миелобластного и острого лимфобластного лейкозов (рис. 1).
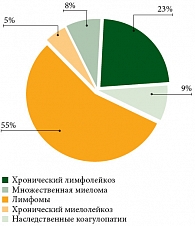
Кроме того, в структуре заболеваний пациентов, состоящих на учете в гематологическом реестре «7РЗ» по Самарской области, в 2012 г. ХМЛ также занимает 5-е место после лимфом, хронического лимфолейкоза, множественной миеломы и наследственных коагулопатий (рис. 2).
На сегодняшний день «золотым стандартом» в лечении пациентов с ХМЛ является иматиниб. Однако, несмотря на то что многие больные хорошо отвечают на терапию иматинибом, в последующем значительная часть пациентов теряет первоначальный ответ на лечение. Утрата чувствительности к иматинибу часто связана с мутациями BCR-ABL. Дазатиниб ингибирует BCR-ABL в 325 раз сильнее иматиниба, дает оптимальный результат и высокую частоту стойких ответов в хронической фазе ХМЛ, если назначается сразу после неудачи лечения иматинибом [3]. Несомненно актуальным является своевременный перевод больных ХМЛ на лечение ингибиторами тирозинкиназы (ИТК) 2-го поколения, поэтому в своей работе мы проанализировали результаты лечения больных ХМЛ иматинибом и дазатинибом по Самарской области для дальнейшей оптимизации лечебного процесса данных пациентов и определения фармакоэкономических показателей.
Материалы и методы исследования
Изучены результаты обследования и лечения 170 пациентов с ХМЛ в разных фазах заболевания, находящихся под наблюдением врачей-гематологов клиник Самарского государственного медицинского университета (СамГМУ), Самарской областной клинической больницы им. М.И. Калинина, Тольяттинской городской клинической больницы № 5. Хроническую фазу заболевания имеют 165 пациентов, фазу акселерации – 5 больных ХМЛ.
Всем больным при постановке диагноза и в сроки, обозначенные рекомендациями европейской организации European LeukemiaNet (ELN-2010) по лечению ХМЛ, выполнялись цитогенетическое и молекулярное исследования, а при необходимости определяли мутации гена ВСR-АВL и исследовали Рh-хромосому методом флуоресцентной гибридизации in situ (fluorescence in situ hybridization, FISH).
В настоящее время пациентам после постановки диагноза ХМЛ назначается иматиниб 400 мг. При неудаче в лечении доза иматиниба повышается до 600–800 мг в сутки. В отсутствие полного гематологического ответа, при потере полного цитогенетического ответа, при трансформации болезни в фазу акселерации больные по возможности переводятся на лечение ИТК 2-го поколения.
Нами проанализирована частота полного гематологического ответа, большого цитогенетического ответа, полного цитогенетического ответа, полного молекулярного ответа у 9 пациентов, проживающих на территории Самарской области и получающих терапию дазатинибом 100–140 мг в сутки более 12–18 месяцев.
В течение многих лет в НИИ гематологии, трансфузиологии и интенсивной терапии СамГМУ ведется работа по изучению качества жизни гематологических больных, в том числе при ХМЛ. Обследованы 35 пациентов с ХМЛ в возрасте от 30 до 74 лет (группы зрелого и пожилого возраста), получающих ИТК 2-го поколения, проживающих в Самарской области и других городах России. Группу сравнения составили 40 условно здоровых людей (отобраны методом случайной выборки), сопоставимых по полу и возрасту, у многих из которых имелись хронические заболевания.
В работе использован опросник для оценки качества жизни пациентов SF-36 (The Short Form-36). Пункты опросника (36) сгруппированы в восемь шкал: физическое функционирование (Physical Functioning, PF), ролевое (физическое) функционирование (Role-Physical Functioning, RP), интенсивность боли (Bodily pain, BP), общее здоровье (General Health, GH), жизнеспособность (Vitality, VT), социальное функционирование (Social Functioning, SF), эмоциональное функционирование (Role-Emotional, RE), психическое здоровье (Mental Health, MN). Результаты оцениваются в баллах, при этом максимальный балл (100) свидетельствует о высоком уровне качества жизни, а минимальный (0) – о низком уровне. Использовался также опросник FACT-BRM (functional assessment of cancer therapy-biologic response modifiers) – специфический опросник для оценки эффективности лечения и физического, эмоционального, социально-семейного и функционального благополучия пациентов с онкологическими заболеваниями, получающих в том числе таргетную терапию.
Результаты исследования
В настоящее время в Самарской области зарегистрировано 3 млн 167 тысяч человек, из них в городе проживает 80,3% населения. На октябрь 2013 г. в реестре пациентов с ХМЛ значится 170 человек. В Самаре проживает 43,5% больных, в городах области – 32,7%, а в сельских районах – 23,8% пациентов с ХМЛ. Среди больных ХМЛ соотношение мужчин и женщин равно 9:11 (1,2). Средний возраст мужчин составляет 49,7 ± 2,1 лет, женщин – 57,7 ± 3,1 лет; минимальный возраст – 11 лет, максимальный – 82 года. Ежегодно диагноз подтверждается у 0,7–1,0 на 100 000 населения в год, что совпадает с данными по России и несколько меньше по сравнению с мировой статистикой (1,0–1,5 на 100 000 человек) [4].
При необходимости больные ХМЛ поступают в одно из трех гематологических отделений Самарской области. Амбулаторное наблюдение проводится по месту жительства.
В настоящее время все пациенты получают терапию ИТК (табл. 1).
Иматиниб назначен 151 пациенту с ХМЛ (больше года препарат принимают 89,4% больных).
Иматиниб в дозе 400 мг более 1 года получают 94 пациента. Среди них у 83,0% (78 из 94) имеется полный цитогенетический ответ, а у 75,5% (71 из 94) – полный молекулярный ответ, сохраняющиеся более 12–20 месяцев.
На данный момент 41 больному ХМЛ увеличена доза иматиниба выше 400 мг/сут, только у 26,8% (у 11 из 41) имеется полный цитогенетический ответ и у 9,7% (4 из 41) получен полный молекулярный ответ. Мы расцениваем эскалацию дозы как фактор риска возникновения прогрессии заболевания, поэтому часть пациентов, принимающих иматиниб 600–800 мг/сут, могут нуждаться в переводе на ИТК 2-го поколения.
Общая пятилетняя выживаемость у больных ХМЛ, принимающих ИТК, составила 92,9%. Все умершие больные погибли в фазу бластного криза, из них у двух пациентов имелась мутация гена ВСR-ABL Т315I, а одна больная страдала тяжелым сопутствующим заболеванием.
Пятилетняя выживаемость без прогрессии зарегистрирована у 90,2% больных ХМЛ. Чаще трансформация в фазу акселерации и бластного криза происходила в первые три года, а у двух пациентов – на пятом году заболевания.
Бессобытийная пятилетняя выживаемость составила 48,6% (потеря полного гематологического, полного цитогенетического, полного и большого молекулярного ответов, смерть).
Пациентам, резистентным к иматинибу (с потерей или отсутствием гематологического и цитогенетического ответа, с непереносимостью препарата), были назначены ИТК 2-го поколения (нилотиниб и дазатиниб). С 2006 по 2010 г. в клиническое исследование по применению нилотиниба было включено 6–8 больных ХМЛ. С 2011 г. финансирование ИТК 2-го поколения осуществляется из средств регионального бюджета (нилотиниб принимают 10 человек, дазатиниб – 9 пациентов). У всех больных перед назначением ИТК 2-го поколения исследуются мутации гена ВСR-ABL, при выявлении которых отдается предпочтение в назначении того или иного препарата.
В настоящее время 37,1% больным (56 из 151), соответственно рекомендациям ELN-2009 по лечению ХМЛ, показано назначение препаратов 2-й линии. Из них на октябрь 2013 г. 34% пациентов принимают ИТК 2-го поколения. Необходимо отметить, что нередко препараты назначаются в связи с трансформацией заболевания в фазу бластного криза или неудачей длительного лечения высокими дозами иматиниба, ИТК 2-го поколения. Терапии дазатинибом следует 9 человек, из них трое пациентов получают препарат менее трех месяцев. Ниже представлены данные шести больных ХМЛ, принимающих препарат 10 месяцев и более (табл. 2).
Средний возраст пациентов составил 47,5 лет. Все больные страдают ХМЛ от 5 до 16 лет, имеют длительную предлеченность и принимают дазатиниб в качестве второй или третьей линии терапии. Срок лечения иматинибом, в том числе в дозе 600–800 мг, составил от 16 до 77 месяцев, а нилотинибом – от 8 до 54 месяцев.
Вероятнее всего, развитие вторичной резистентности к иматинибу связано с появлением мутации H396R в гене ВСR-ABL. Согласно данным литературы, эта мутация определяет низкую чувствительность к иматинибу [5], а наличие мутаций Y253H и F359C вызывает резистентность к нилотинибу [6].
По полученным результатам, у всех больных ХМЛ через 1–3 месяца от начала лечения дазатинибом зарегистрирован гематологический и полный гематологический ответы. При назначении дазатиниба полный молекулярный ответ достигнут через 1 год 9 месяцев у одной пациентки, через 10–12 месяцев частичный цитогенетический ответ – у четырех больных и снижение транскрипта гена ВСR-ABL на несколько логарифмов – у 5 пациентов, что связано, предположительно, с поздним назначением ИТК 2-го поколения. Раннее переключение пациентов на вторую линию терапии является важным предиктором успеха лечения, что соответствует данным литературы [7].
Мы сравнили результаты лечения всех больных ХМЛ, находившихся на терапии дазатинибом, за два года с результатами рандомизированного исследования START-R [3]. Как видно из данных табл. 3, результаты лечения наших пациентов сопоставимы по частоте достижения полного гематологического ответа и двухлетней выживаемости пациентов. Достижение полного цитогенетического и полного молекулярного ответов гораздо ниже, и мы расцениваем это как результат позднего назначения дазатиниба, когда у пациентов либо был утрачен, либо длительно отсутствовал полный гематологический ответ. Авторы исследования START-R отметили, что среди пациентов, которые получали дазатиниб после утраты большого цитогенетического ответа на иматиниб, удалось достичь полного цитогенетического ответа в 72% случаев, по сравнению с 42% случаев у пациентов, начавших лечение дазатинибом после утраты как большого цитогенетического, так и полного гематологического ответов. Данные исследования START-R свидетельствуют о том, что оптимальный результат достигается, если дазатиниб назначается сразу после развития резистентности к иматинибу [3].
Отметим, что все пациенты указывают на хорошую переносимость препарата. При назначении дазатиниба 100–140 мг в сутки у
2 больных наблюдалась цитопения. У одной пациентки гемограмма нормализовалась самостоятельно, цитопения купировалась через
6 месяцев на фоне лечения дазатинибом 140 мг. С учетом предшествующих назначению дазатиниба показателей гемограммы, нельзя исключить, что цитопения была обусловлена прогрессированием заболевания. У второго больного возникла необходимость отмены препарата (в предыдущем лечении иматинибом 400–300 мг у него наблюдалась выраженная трехростковая цитопения). В настоящее время больному проводится симптоматическое лечение.
Среди побочных эффектов следует выделить возникший у двух пациентов через 1–1,5 года плевральный выпот, купированный назначением мочегонных средств и не требовавший отмены препарата. Впоследствии плевральный выпот не рецидивировал. Возникновение плеврального выпота чаще связано с более высокими дозами дазатиниба [8]. По нашему наблюдению, при возникновении побочных эффектов после временной отмены препарата целесообразна коррекция дозы дазатиниба в соответствии с инструкцией по медицинскому применению препарата.
В последнее время в литературе широко обсуждается проблема качества жизни больных ХМЛ [9]. В данной работе мы проанализировали влияние ИТК 2-го поколения на качество жизни больных ХМЛ. В первую группу включили 35 пациентов с ХМЛ, получающих нилотиниб (800 мг) и дазатиниб (100 мг). Группу сравнения составили 40 условно здоровых лиц. В каждой группе выделяли людей зрелого и пожилого возраста.
Сравнение показателей у пациентов, принимающих ИТК 2-го поколения, и здоровых лиц показало, что качество жизни пациентов зрелого возраста снижено по шкалам физического благополучия (ощущение себя больным, побочные эффекты лечения, боли, тошнота, затруднение выполнения бытовых обязанностей, вынужденное пребывание в постели). Однако у больных ХМЛ пожилого возраста эти показатели намного выше, чем у представителей контрольной группы, многие из которых имеют хронические заболевания.
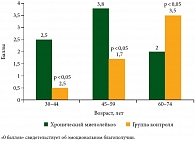
Чувство грусти, нервозность, мысли о смерти, беспокойство по поводу возможного ухудшения состояния (эмоциональное благополучие – опросник FACT-BRM) чаще сопровождают больных ХМЛ зрелого возраста и несколько реже – пациентов пожилого возраста по сравнению со здоровыми лицами того же возраста (рис. 3).
У пациентов с ХМЛ всех возрастов отмечена высокая моральная поддержка со стороны семьи и друзей (отношения с друзьями, поддержка семьи, друзей; духовная близость с родными людьми). При этом активному общению в социуме отдают предпочтение люди зрелого возраста. Таким образом, изучение качества жизни у больных ХМЛ имеет существенное значение для социальной адаптации пациентов, определяющее их трудовой прогноз и жизненный статус.
Заключение
В настоящее время иматиниб остается препаратом выбора при лечении больных ХМЛ. Препарат дазатиниб эффективен при лечении больных ХМЛ, о чем свидетельствуют полученные результаты двухлетней выживаемости пациентов, сопоставимые с данными литературы. Оптимальные результаты в лечении больных ХМЛ достигаются только при раннем применении дазатиниба, так как его позднее назначение уменьшает эффективность лечения и приводит к снижению бессобытийной выживаемости.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.