Предменструальный синдром: заблуждения и реалии. XXXIII Всероссийский конгресс с международным участием «Амбулаторно-поликлиническая помощь в эпицентре женского здоровья». Панельная дискуссия
- Аннотация
- Статья
- Ссылки




Предменструальный синдром и качество жизни современной женщины
Открывая симпозиум, заместитель директора Научного центра акушерства, гинекологии и перинатологии им. акад. В.И. Кулакова по научной работе, руководитель научно-поликлинического отделения, д.м.н., профессор, заслуженный деятель науки Вера Николаевна ПРИЛЕПСКАЯ отметила, что предменструальный синдром (ПМС), который еще называют синдромом предменструального напряжения, рассматривается как сложный патологический симптомокомплекс.
Некоторые исследователи считают, что ПМС возникает почти у каждой женщины и проявляется легкими симптомами, которые женщина не расценивает как болезненное состояние. В целом от 25 до 90% женщин страдают ПМС, в том числе от 2 до 19% – тяжелыми формами. Частота встречаемости ПМС зависит от возраста. У женщин до 30 лет признаки ПМС наблюдаются в 20% случаев, после 30 лет проявления ПМС отмечают практически половина женщин, после 40 лет – 55%1. Есть данные, что ПМС подвержены эмоционально лабильные пациентки астенического телосложения, с дефицитом массы тела, а также женщины, занимающиеся интеллектуальным трудом.
Качество жизни – показатель, интегрирующий физические, психологические, эмоциональные и социальные характеристики человека, что в целом отражает его способность адаптироваться к проявлениям болезни, в том числе не связанным со здоровьем. У женщин с ПМС способность адаптироваться к проявлениям болезни и социальной деятельности (на работе, в жизни) существенно нарушена. Для них характерны частая неоправданная смена настроения, агрессивность и повышенная конфликтность, депрессия2. Все это значительно снижает качество жизни женщины. Многие пациентки, страдающие ПМС, с ужасом ожидают наступления второй фазы цикла, понимая, что их поведение в этот период не будет соответствовать истинным характерологическим особенностям.
Среди факторов риска ПМС выделяют наследственность, острый или хронический эмоциональный стресс, предшествующие гинекологические заболевания, психические заболевания, умственное и эмоциональное напряжение и др.
Существует несколько теорий, представляющих этиопатогенетические механизмы возникновения ПМС: гормональная, аллергическая, теория «водной интоксикации», гиперадренокортикальной активности и увеличения альдостерона, психосоматическая теория. Однако вне зависимости от теоретического обоснования при ПМС всегда нарушена секреция основных гормонов: эстрогена, прогестерона, серотонина в лютеиновую фазу менструального цикла.
Типичные признаки ПМС хорошо известны: тянущие боли внизу живота, нагрубание молочных желез, отеки, головные боли, раздражительность и пр. В зависимости от преобладания в клинической картине тех или иных проявлений можно выделить четыре формы ПМС: нервно-психическую, отечную, цефалгическую, кризовую (рис. 1).
Среди основных принципов и методов лечения ПМС – соблюдение режима труда и отдыха, регулярные занятия спортом, рациональное питание, хороший сон.
Симптоматическая терапия, которая может быть назначена лечащим врачом, включает седативные препараты, антидепрессанты, спазмолитики, нестероидные противовоспалительные средства, при аллергических реакциях – антигистаминные, сосудистые препараты для улучшения кровообращения в центральной нервной системе, мочегонные при отечной форме, гормональные средства (гормональные контрацептивы). В основном это содержащие дроспиренон препараты, которые обладают целым рядом положительных свойств. Предпочтительнее назначать препараты в пролонгированном режиме.
Для коррекции психических расстройств при ПМС в качестве первой линии предлагается использовать селективные ингибиторы обратного захвата серотонина: флуоксетин, сертралин, пароксетин, циталопрам. Лечение прерывистыми курсами или в постоянном режиме дает высокий эффект. Но при выраженных психических расстройствах, в том числе при депрессии, женщине настоятельно рекомендуется проконсультироваться у психиатра или психоневролога.
Важную роль в лечении ПМС играет фитотерапия – применение лекарственных препаратов на растительной основе. Поскольку фитопрепараты – это лекарственные средства, созданные из экстрактов растений, состоящих в свою очередь из растительных клеток, то по структуре они имеют много общего с веществами, образующимися в клетках животных и человека. Переносимость этих веществ гораздо лучше, чем имеющих химическую основу. Кроме того, побочные реакции при приеме фитопрепаратов встречаются реже, часто они не столь значимы и менее выражены. Фитопрепараты имеют значительно меньше противопоказаний. Эффект фитопрепаратов наступает медленнее, но он более стойкий и продолжительный, чем у синтетических препаратов.
Национальная ассоциация по лечению ПМС США представила в 2016 г. обновленное руководство, в котором отмечает эффективность фитопрепарата, созданного на основе плодов витекса священного (Vitex agnus-castus) (уровень рекомендации В)3. Витекс священный известен во всем мире и используется с древних времен. Он обладает допаминергическими свойствами, избирательно блокирует синтез пролактина, снижает уровень фолликулостимулирующего гормона, способствует устранению дисбаланса половых гормонов, проявляет антиоксидантный эффект, воздействует на опиоидные рецепторы.
Экстракт витекса священного, который входит в состав препаратов Циклодинон® и Мастодинон®, эффективно снижает проявления ПМС. Были получены статистически достоверные изменения средних показателей ПМС-опросников после трех менструальных циклов лечения по сравнению с исходными данными. При этом побочные реакции не возникли ни у одной пациентки на фоне приема препарата, содержащего витекс священный4.
Было изучено качество жизни пациенток с ПМС средней и тяжелой степени тяжести до и после лечения фитопрепаратом на основе витекса священного и комбинированным оральным контрацептивом, содержащим 20 мкг этинилэстрадиола и 3 мг дроспиренона, в режиме «24 + 4». В результате лечения улучшилось состояние пациенток, качество их жизни. Более выраженный эффект отмечен в отношении обменно-эндокринных и физических проявлений ПМС (снижения аппетита, вздутия живота, мастодинии, масталгии и болевых проявлений)5.
Заканчивая выступление, профессор В.Н. Прилепская еще раз напомнила, что ПМС – это патологический симптомокомплекс, который значительно снижает качество жизни женщины. Его этиология и патогенез до настоящего времени изучены недостаточно, но определены направления в диагностике, лечении и профилактике, которым необходимо следовать. Лечение ПМС должно быть дифференцированным, учитывать состояние общего и репродуктивного здоровья женщины, сопутствующие заболевания, степень тяжести ПМС, переносимость терапии и т.д. Своевременно назначенное лечение позволит предотвратить переход легкой формы ПМС в тяжелую.
Клинические проявления и лечение предменструального синдрома
Доклад ведущего научного сотрудника Научного центра акушерства, гинекологии и перинатологии им. акад. В.И. Кулакова, к.м.н. Эльмиры Робертовны ДОВЛЕТХАНОВОЙ был посвящен клиническим и лечебным аспектам ПМС.
Все множество симптомов ПМС можно разделить на поведенческие и физические. К поведенческим относятся усталость, раздражительность, забывчивость, нарушение сна, лабильное настроение, интенсивный гнев, конфликтность, снижение интереса к обычной деятельности, социальная изоляция, трудности с концентрацией. К физическим – нарушение аппетита, различные желудочно-кишечные расстройства, вплоть до тошноты и рвоты, повышенная чувствительность груди – масталгия, мышечные и головные боли, повышение температуры, отечность, прибавка в весе и т.д. Обилие проявлений – на сегодня известно более 200 симптомов – обусловлено сложной этиологией ПМС.
Достоверные и общедоступные критерии диагностики ПМС отсутствуют. Необходимо опираться в первую очередь на тщательно собранный анамнез и характерные клинические симптомы (психоэмоциональные, обменно-эндокринные и др.), цикличность их проявления (до менструации) и исчезновения (после нее). Диагноз ПМС устанавливается в соответствии с критериями МКБ-10, при наличии одного или нескольких симптомов и периодичности (симптомы беспокоят женщину только в лютеиновой фазе менструального цикла).
Дифференциальную диагностику ПМС в первую очередь проводят с различными психическими заболеваниями, поскольку в его клинической картине часто преобладает именно психоневрологическая симптоматика. Требуется исключить большое депрессивное состояние, дистимические состояния, генерализованную тревожность, панические расстройства, биполярные болезни. Сходные симптомы могут иметь анемия, аутоиммунные заболевания, гипотиреоз, диабет, судорожные состояния, эндометриоз, синдром хронической усталости и др.
Перед назначением лечения требуется комплексное обследование, направленное на выявление гинекологической и сопутствующей экстрагенитальной патологии. При необходимости для консультации привлекаются смежные специалисты: психоневролог, гастроэнтеролог, терапевт. Женщин с тяжелой формой ПМС целесообразно направлять в специализированные учреждения для более глубокого обследования, возможно для выполнения молекулярно-генетического исследования. Получены данные, которые свидетельствуют об ассоциации полиморфизма ряда генов с клиническими симптомами заболевания.
Лечение ПМС достаточно разнообразно, поскольку требуется нивелировать все проявления и симптомы, которые беспокоят женщину. Назначаются гормональные препараты, антидепрессанты, диуретики, различные витаминные препараты и микроэлементы, польза от которых подтверждена рядом исследований, противовоспалительные средства, рекомендуется изменить рацион питания и регулярно выполнять физические упражнения, при необходимости проводится психотерапия.
В качестве гормональной терапии используются комбинированные оральные контрацептивы, гестагенные препараты.
В большом количестве публикаций говорится об успешном применении при ПМС витаминов и микроэлементов.
Пиридоксин (витамин В6) – кофактор, необходимый для синтеза катехоламинов и допамина. Витамин осуществляет коррекцию обмена в нейротрансмиттерах, что обосновывает его применение при депрессивных состояниях, раздражительности, отеках, головной боли, метеоризме. Ранее пиридоксин назначали в достаточно больших дозах – до 500 мг, но на сегодняшний день считаются эффективными небольшие дозы (от 50 до 200 мг на протяжении всего менструального цикла или с 16-го по 28-й день на протяжении трех месяцев).
Витамин Е облегчает масталгию и может быть назначен в течение всего менструального цикла, но лучше – в лютеиновую фазу.
Дефицит магния может привести к симптомам ПМС. Женщины, которые получали содержащие магний препараты, отмечали улучшение состояния. Уменьшить уровень усталости и выраженность депрессии у женщин с ПМС возможно с помощью приема препаратов кальция.
В 2016 г. Королевская коллегия акушеров и гинекологов Великобритании представила руководство по ведению женщин с ПМС, в котором рекомендует использовать, помимо витаминных препаратов, растительные экстракты: гингко билобу, шафран и витекс священный6.
Витекс священный проявляет целый ряд эффектов, оказывая влияние на патогенетические механизмы развития ПМС: секрецию пролактина, гонадотропного рилизинг-гормона, фолликулостимулирующего и лютеинизирующего гормонов.
Э.Р. Довлетханова выделила два препарата, содержащих витекс священный, – Мастодинон® и Циклодинон®. Циклодинон® представляет собой лекарственный растительный монопрепарат. Его назначают для лечения нарушения менструального цикла, вызванного недостаточностью лютеиновой фазы. Препарат также влияет на симптомы ПМС, устраняя головную боль, отеки, нормализуя психическую лабильность, масталгию. Курс лечения составляет не менее трех месяцев, без перерывов на время менструации и при необходимости может быть продлен.
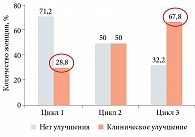
Проведенное в Научном центре акушерства, гинекологии и перинатологии им. акад. В.И. Кулакова исследование подтвердило эффективность применения Циклодинона у женщин с ПМС средней тяжести и тяжелыми формами. Были отмечены достоверное уменьшение проявлений ПМС, улучшение качества жизни (рис. 2)7.
Мастодинон® – комбинированный лекарственный фитофармацевтический препарат. Наибольшую эффективность препарат продемонстрировал в лечении фиброзно-кистозной мастопатии, синдрома мастодинии, а также ПМС. Длительность курса лечения составляет не менее трех месяцев без перерыва на время менструации.
В целом ряде исследований было доказано, что Мастодинон® нормализует состояние вегетативной нервной системы при ПМС и купирует болезненные состояния в молочных железах. Одно из исследований показало положительную динамику индекса Кердо, который отражает наличие и степень вегетативного дисбаланса между симпатическим и парасимпатическим влиянием на сердечно-сосудистую систему, на фоне лечения Мастодиноном8. У пациенток после терапии Мастодиноном наблюдалась нормализация функционального состояния симпатического и парасимпатического отделов вегетативной нервной системы.
В заключение Э.Р. Довлетханова отметила ряд преимуществ фитопрепаратов перед синтетическими средствами: широкий терапевтический спектр действия, благоприятный профиль безопасности, хорошая переносимость, практически отсутствие побочных эффектов. Кроме того, фитопрепараты могут использоваться столь длительно, сколько это необходимо. И что немаловажно, применять фитопрепараты могут женщины, имеющие противопоказания к гормональной терапии.
Таким образом, тактика ведения пациенток с ПМС должна быть дифференцирована с учетом тяжести течения. Важную роль играют профилактические меры, направленные на улучшение физического и психоэмоционального состояния женщины с помощью диеты, максимального снижения психоэмоциональных нагрузок, коррекции образа жизни, физических упражнений и, возможно, физиотерапевтического лечения.
Молочные железы и гормоны
Неотъемлемой составляющей женской репродуктивной системы являются молочные железы. Заведующая кафедрой акушерства и гинекологии Российской медицинской академии непрерывного профессионального образования, д.м.н., профессор Наталия Михайловна ПОДЗОЛКОВА напомнила, что молочные железы подвержены влиянию множества гормонов, в том числе гормонов щитовидной железы, надпочечников, а также поджелудочной железы.
Основную роль в регуляции процессов в молочной железе играют эстрогены, прогестерон, андрогены и пролактин. Их нормальное соотношение – залог здоровья молочной железы. При нарушении физиологического гормонального равновесия могут возникать различные патологические состояния.
В репродуктивном периоде синтез эстрогенов осуществляется в яичниках, в постменопаузе – внегонадно (в печени, жировой и мышечной ткани, ткани молочной железы). Эстрогены усиливают васкуляризацию (отек соединительной ткани), стимулируют гипертрофию междольковой соединительной ткани (вызывают фиброзные изменения), усиливают синтез ДНК и митотическую активность в эпителии протоков (гиперпролиферация и формирование кист). Не случайно ряд факторов риска развития рака молочной железы связан с воздействием эстрогенов. Это и возраст менархе, и время наступления менопаузы, и индекс массы тела, и время назначения менопаузальной гормональной терапии. На взаимодействии эстрогенов и прогестерона строится гормональный баланс, который определяет здоровье молочной железы. Прогестерон блокирует рецепторы эстрогена, что приводит к уменьшению всасывания жидкости и соответственно уменьшению отека и боли, а также стимулирует продукцию ферментов, метаболизирующих эстрадиол. За счет подавления пролиферации и уменьшения сдавления млечных протоков происходит уменьшение фиброза и размеров кист.
Как было показано в исследованиях, циркулирующие в крови различные концентрации свободного эстрадиола и эстрона не влияют на риск возникновения рака молочной железы. Изменение концентрации гестагенов в крови также практически не оказывает влияния на злокачественные новообразования. Таким образом, концентрация половых гормонов в крови не так важна, но происходящее на уровне органа-мишени (местный уровень гормонов) имеет первостепенное значение.
Локальная гиперэстрогения – причина доброкачественных заболеваний молочных желез: циклической мастодинии, фиброаденомы (четко ограниченной доброкачественной опухоли), кист, доброкачественной дисплазии молочных желез. Основные симптомы доброкачественной дисплазии молочной железы, или мастопатии, – болезненные ощущения в молочных железах различного характера и интенсивности (масталгия или мастодиния), усиливающиеся в предменструальные дни, ощущение увеличения объема молочных желез, уплотнения, обнаруживаемые и самой женщиной при самоосмотре. В то же время мастопатия может протекать и бессимптомно. Следовательно, циклическая мастодиния – повод для того, чтобы тщательно проверить молочные железы у пациентки.
Особое внимание необходимо обратить на увеличение плотности молочной железы, что наблюдается у 20% женщин в раннем репродуктивном периоде. В старшем возрасте гормональные заболевания начинают конкурировать по частоте с раком молочной железы. И чем больше плотность молочной железы, тем выше вероятность злокачественных новообразований. В 2006 г. во Франции была опубликована статья, которая выделила циклическую масталгию как фактор возможной патологии молочной железы9. На сегодняшний день считается, что это один из клинических маркеров рака молочной железы.
Еще один важный гормон – пролактин, который в основном вырабатывается в аденогипофизе. Основной регулятор выработки пролактина – дофамин, но есть еще источники внегипофизарной продукции пролактина, в том числе эпителий молочной железы. Наиболее характерное проявление гиперпролактинемии – симптомокомплекса, возникающего на фоне повышенного содержания пролактина в крови, – нарушение функции репродуктивной системы. Однако однозначное мнение о том, имеет ли отношение пролактин к формированию доброкачественных и злокачественных заболеваний молочной железы, еще не сложилось. Одни исследования корреляцию не выявляют10, результаты других подтверждают эту связь11.
На сегодняшний день признана роль пролактина в развитии дисгормональных заболеваний молочной железы и рака молочной железы при повышенном локальном синтезе пролактина маммарным эпителием. Под влиянием высокой локальной концентрации пролактина повышаются клеточная пролиферация, подвижность клеток, васкуляризация опухоли. Высокая локальная концентрация пролактина приводит к 60%-ному росту риска ER+ рака, снижению эффективности лечения рака молочной железы с увеличением вероятности рецидивов, а также развитию гиперплазии и интраэпителиальной неоплазии, сходных с in situ12. Предполагается вклад пролактина и в развитие рака простаты, языка, колоректального рака и рака матки и яичников. Это обусловлено тем, что пролактин-индуцированный белок, экспрессия которого регулируется пролактином, стимулирует пролиферацию опухолевых клеток и повышает их способность к инвазии. Если у женщины на протяжении длительного периода времени наблюдается гиперпролактинемия, не исключено, что у нее может развиться рак молочной железы13.
Особенности патогенеза ПМС обусловили новые направления в лечении пациенток с проявлениями данного синдрома, а также с гиперпролактинемией, используемые в настоящее время – каберголин и Мастодинон® и перспективные – моноклональные антитела, которые блокируют экстрацеллюлярную часть пролактиновых рецепторов, то есть затрудняют реализацию проканцерогенного эффекта пролактина (сейчас проходят первую фазу клинических исследований).
В России зарегистрированы три препарата, показанные при мастодинии. С одной стороны, важно привести в равновесие соотношение эстрогенов и прогестерона на уровне клетки – так действует Прожестожель. С другой стороны, необходимо нормализовать метаболизм – таков механизм Индинола форте и фитопрепарата Мастодинон®. Важно отметить, что Мастодинон® оказывает дофаминергическое действие, влияя на содержание пролактина. Нормализация соотношения гормонов на уровне органов-мишеней уменьшает риск возникновения доброкачественных изменений молочной железы. Исследования демонстрируют эффективность лечения масталгии при использовании Мастодинона. Более чем 70% пациенток, принимавших Мастодинон® в течение трех месяцев, отмечали снижение интенсивности масталгии.
Заключение
В ходе симпозиума было отмечено, что тактика ведения пациенток с ПМС должна быть дифференцированной. Лечение проводится в основном в условиях диспансерного наблюдения, а выбор метода и длительность лечения зависят от тяжести течения синдрома, состояния здоровья женщины, гинекологического статуса результатов обследования. Женщин с тяжелыми формами ПМС целесообразно направлять в специализированные учреждения для более глубокого обследования.
Эксперты сделали акцент на возможностях фармакотерапии ПМС, отмечая эффективность и безопасность применения фитопрепаратов Циклодинон® и Мастодинон® («Бионорика»).
Мастодинон® – растительный негормональный препарат для лечения диффузных форм мастопатии, мастодинии и ПМС. Прием препарата способствует нормализации гормонального фона, устраняет боли в молочных железах, улучшает самочувствие во время менструации. Применяется при ПМС, фиброзно-кистозной мастопатии, нарушении менструального цикла и/или бесплодии. Циклодинон® – растительный негормональный препарат для лечения нарушений менструального цикла, ПМС и мастодинии. Применяется при нарушениях менструального цикла, связанных с гиперпролактинемией и недостаточностью лютеиновой фазы, масталгии и ПМС. Удобен благодаря однократному суточному приему.
Хотя фармакологические эффекты витекса священного были известны в течение длительного времени и использовались в лечении различных нарушений, фармакологические механизмы были уточнены компанией «Бионорика» в ходе научных исследований. Высококачественный экстракт витекса священного, который является компонентом растительных препаратов Мастодинон®
и Циклодинон®, создается по запатентованной методике, благодаря чему сохраняются все лечебные свойства растения.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.