Применение биоактивного концентрата мелкой морской рыбы (препарата Алфлутоп®): 25 лет в России – исследования и практические выводы
- Аннотация
- Статья
- Ссылки
- English
он является одним из наиболее широко используемых симптоматических медленно действующих лекарственных средств при остеоартрите в России.
В статье представлены результаты экспериментальных исследований, доказавших молекулярно-клеточные механизмы действия Алфлутопа. Установлено, что препарат стимулирует пролиферацию хондроцитов, активирует синтез внеклеточного матрикса посредством модуляции трансформирующего фактора роста β, ингибирует гиалуронидазу, а также уменьшает окислительный стресс и активность внеклеточной экспрессии генов провоспалительных цитокинов (интерлейкинов 1β,
6 и 8). Приведены также данные многочисленных клинических исследований, свидетельствующие об эффективности Алфлутопа
при остеоартрите субклинической и развернутой стадий, заболеваниях околосуставных тканей, в качестве антивозрастной терапии у пожилых, о высоком профиле его безопасности у коморбидных больных, в частности у пациентов с гастропатиями, вызванными приемом нестероидных противовоспалительных препаратов, сахарным диабетом, артериальной гипертензией, дислипидемией.
Собранная на сегодняшний день доказательная база служит обоснованием широкого применения Алфлутопа в ревматологической, травматологической, ортопедической, неврологической, терапевтической практике, а также
в спортивной медицине.
он является одним из наиболее широко используемых симптоматических медленно действующих лекарственных средств при остеоартрите в России.
В статье представлены результаты экспериментальных исследований, доказавших молекулярно-клеточные механизмы действия Алфлутопа. Установлено, что препарат стимулирует пролиферацию хондроцитов, активирует синтез внеклеточного матрикса посредством модуляции трансформирующего фактора роста β, ингибирует гиалуронидазу, а также уменьшает окислительный стресс и активность внеклеточной экспрессии генов провоспалительных цитокинов (интерлейкинов 1β,
6 и 8). Приведены также данные многочисленных клинических исследований, свидетельствующие об эффективности Алфлутопа
при остеоартрите субклинической и развернутой стадий, заболеваниях околосуставных тканей, в качестве антивозрастной терапии у пожилых, о высоком профиле его безопасности у коморбидных больных, в частности у пациентов с гастропатиями, вызванными приемом нестероидных противовоспалительных препаратов, сахарным диабетом, артериальной гипертензией, дислипидемией.
Собранная на сегодняшний день доказательная база служит обоснованием широкого применения Алфлутопа в ревматологической, травматологической, ортопедической, неврологической, терапевтической практике, а также
в спортивной медицине.




Введение
Воспаление и дегенеративные изменения различных структур сустава являются самой частой причиной боли и нарушения функции опорно-двигательного аппарата. Целями лечения патологии суставов, а также околосуставных тканей являются снижение выраженности симптомов и замедление ее прогрессирования, что может улучшить мобильность и качество жизни пациентов [1, 2].
В настоящее время спектр терапевтических опций достаточно широкий [3, 4].
Уже более четверти века в России используется препарат Алфлутоп (компания Biotehnos S.A., Румыния). Это оригинальный комплексный биоактивный препарат, полученный из четырех видов мелкой морской рыбы. Важно и то, что он производится по стандартам Надлежащей производственной практики. В его состав входят сульфатированные гликозаминогликаны, аналогичные матриксу гиалинового хряща: хондроитина-4-сульфат, хондроитина-6-сульфат, дерматансульфат, кератансульфат, глюкуроновая кислота, низкомолекулярные полипептиды, свободные аминокислоты и микроэлементы (натрий, калий, кальций, магний, железо, медь, цинк), имеющие большое значение для обменных процессов и метаболизма соединительной ткани. Данный препарат показан при первичном и вторичном остеоартрите (ОА) различной локализации, а также при дегенеративно-дистрофических заболеваниях позвоночника и околосуставных тканей. Необходимо подчеркнуть, что указанные состояния являются одними из наиболее часто встречающихся в пожилом и старческом возрасте.
Изучение механизмов действия
В экспериментальных работах L. Olariu и соавт. был оценен пролиферативный статус хондроцитов после обработки препаратом Алфлутоп (0,1 и 0,2%) [5, 6]. Для этого определяли скорость митоза и последовательность генерации пролиферации с оценкой пролиферативного индекса и распределения фаз клеточного цикла в фазах S (синтез ДНК) и G2/M (начало митоза). В результате был доказан двойной механизм действия Алфлутопа на клеточные рецепторы. Во-первых, препарат препятствовал фрагментации внеклеточного матрикса, защищая рецепторы, вовлекаемые в воспалительные реакции, во-вторых – блокировал сигнальные пути, активируемые фрагментами матрикса, и таким образом уменьшал транслокацию ядерных провоспалительных факторов. Полагают, что именно через рецепторное воздействие Алфлутоп контролирует три компонента синовиального воспаления: клеточную инфильтрацию, высвобождение воспалительных медиаторов и ангиогенез. Данный теоретический анализ обосновывает целесообразность локальной доставки препарата в область повреждения, его парентерального введения.
В соответствии с новой противовоспалительной теорией терапевтическое воздействие Алфлутопа при ОА обусловлено, в частности, влиянием на внешние рецепторы клеток, такие как СD44, ICAM1, TL-4 (рис. 1).
Молекулярно-клеточные механизмы действия препарата Алфлутоп были исследованы еще в ряде экспериментальных работ. Установлено, что препарат стимулировал пролиферацию хондроцитов, активировал синтез внеклеточного матрикса посредством модуляции трансформирующего фактора роста β (Transforming Growth Factor β – TGF-β), ингибировал гиалуронидазу и окислительный стресс. В недавно проведенных исследованиях доказана способность Алфлутопа стимулировать противовоспалительные и антиангиогенные сигнальные пути, блокирующие активность генов провоспалительных цитокинов (интерлейкинов (Interleukins – IL) 6 и 8) и проангиогенного фактора роста эндотелия сосудов (Vascular Endothelial Growth Factor – VEGF) [5, 6].
Так, для создания точной модели in vitro молекулярных эффектов препарата Алфлутоп была выбрана стандартная линия хондроцитов CHON-001, стимулированных фактором некроза опухоли α (Tumor Necrosis Factor α – TNF-α), форболмиристатацетатом (Phorbol Myristate Acetate – PMA) и IL-1β. Оценка фенотипа и внеклеточной экспрессии генов IL-6, IL-8, IL-1β в хондроцитах, обработанных препаратом Алфлутоп, проводилась после их стимуляции и в контроле (нестимулированные клетки) методом проточной цитометрии с использованием мультиплексных микросфер и количественной полимеразной цепной реакции с детекцией в режиме реального времени (таблица).
Анализ полученных данных позволил сделать вывод, что противовоспалительное действие in vitro препарата Алфлутоп осуществляется через инициацию механизмов, участвующих в подавлении сигнальной активности генов IL-1β, IL-6 и IL-8 [5]. К его молекулярным эффектам следует отнести ингибирование экспрессии протеаз, ответственных за каскад деградации ядерного белка аггрекана (экспрессия мРНК ADAMTS-4), увеличение синтеза аггрекана и гиалуронана (активация экспрессии мРНК гиалуронансинтазы), а также активацию основного регулятора транскрипции SOX-9, ответственного за предотвращение деградации внеклеточного матрикса [6].
Приведенные доклинические исследования влияния препарата Алфлутоп на хондроциты на молекулярно-клеточном уровне были отмечены золотыми медалями на европейской выставке инноваций и изобретений в 2016 и 2018 гг.
Механизмы действия Алфлутопа на факторы прогрессирования ОА представлены на рис. 2.
Схемы применения
В различных научно-медицинских центрах накоплен значительный положительный опыт применения препарата Алфлутоп при заболеваниях суставов и позвоночника [7–9]. Схемы введения могут быть следующие:
- глубоко внутримышечно по 2 мл через день № 10 или по 1 мл ежедневно № 20 в случае вовлечения в патологический процесс множества суставов и остеохондроза;
- внутрисуставно по 1–2 мл в каждый пораженный сустав с интервалом три-четыре дня (пять-шесть введений) в случае вовлечения в процесс крупных суставов;
- паравертебрально по 0,25 мл в четыре точки (суммарно 1 мл) на уровне двух смежных сегментов два раза в неделю (три – пять введений) при поражении позвоночника;
- сочетание внутрисуставного и внутримышечного введения.
Курс лечения целесообразно повторять через шесть месяцев.
В недавно завершенном исследовании было продемонстрировано, что курс по 2 мл в/м через день так же эффективен и безопасен, как и стандартный курс по 1 мл в/м ежедневно № 20. Он удобнее стандартного курса по 1 мл № 20 и может способствовать повышению приверженности пациентов терапии.
Исследование эффективности и безопасности при разных нозологиях
Симптом- и структурно-модифицирующее действие Алфлутопа оценивалось Л.И. Алексеевой и соавт. в 2014 г. в двухлетнем многоцентровом слепом рандомизированном плацебоконтролируемом исследовании [10, 11]. В него были включены 90 больных ОА коленного сустава второй и третьей стадий по классификации Kellgren – Lawrence. Пациенты были рандомизированы на две группы: первая (n = 45) получала внутримышечные инъекции Алфлутопа по 1 мл курсами по 20 дней с шестимесячными интервалами в течение двух лет (всего четыре курса), вторая (n = 45) – инъекции плацебо (изотонический раствор натрия хлорида) по аналогичной схеме. В качестве сопутствующей терапии назначался ибупрофен в дозе 600–1200 мг/сут. Различие в абсолютной величине снижения интенсивности боли по индексу выраженности ОА Университетов Западного Онтарио и МакМастера (Western Ontario and McMaster Universities Osteoarthritis Index – WOMAC) между группами оказалось достоверным. Достоверное уменьшение скованности в группе Алфлутопа наблюдалось к третьему визиту, в группе плацебо такового не выявлено (p < 0,001). В группе Алфлутопа улучшение функции суставов, суммарного индекса WOMAC, общего состояния здоровья было отмечено после первого курса терапии и сохранялось в течение всего периода наблюдения (р = 0,001). Кроме того, к шестому визиту только в первой группе наблюдалось достоверное улучшение качества жизни (р = 0,0045). В первой группе на терапию ответили 73%, во второй – 40% (р = 0,001). На фоне лечения Алфлутопом у 79% больных удалось снизить суточную дозу нестероидных противовоспалительных препаратов (НПВП). Оставшиеся 21% полностью прекратили их прием. В группе плацебо снижение суточной потребности в НПВП наблюдалось только у 23% больных.
Достоверное замедление сужения суставной щели зафиксировано в группе Алфлутопа по сравнению с группой плацебо (критерий Уилкоксона, р = 0,0003). Об уменьшении деградации суставного хряща свидетельствовала динамика уровня С-телопептида коллагена II (CТХ-II). Так, в группе Алфлутопа через три месяца наметилась тенденция к его снижению, которая сохранялась до конца исследования. В группе плацебо показатель CТХ-II на протяжении периода наблюдения не менялся. На основании полученных результатов ученые сделали вывод о структурно-модифицирующих эффектах Алфлутопа при ОА коленного сустава. Установлено также, что препарат Алфлутоп оказывал ранний анальгетический эффект. Таковой наблюдался на второй неделе терапии и возрастал в течение трех месяцев по окончании курса терапии. Период последействия составил до шести месяцев [10].
В 2019 г. Л.И. Алексеева и соавт. исследовали новый режим введения Алфлутопа при ОА коленного сустава – по 2 мл через день № 10. Эффективность и безопасность данной схемы лечения были доказаны в многоцентровом исследовании с участием 130 больных [9]. Она обеспечивала такой же терапевтический результат, как стандартная схема с ежедневными инъекциями. Через два месяца динамика значений WOMAC в отношении боли, скованности и функции суставов, а также ответ на терапию по критериям OMERACT-OARSI оказались сопоставимыми (рис. 3) [9].
При этом назначение Алфлутопа не ассоциировалось с ухудшением течения таких коморбидных состояний, как артериальная гипертензия, сахарный диабет и ожирение.
Серьезные нежелательные реакции, связанные с получением исследуемого препарата, зарегистрированы не были.
Нежелательное взаимодействие Алфлутопа с другими лекарственными средствами также отсутствовало [9].
Полученные результаты позволили сделать заключение, что Алфлутоп обладает благоприятным профилем безопасности у коморбидных пациентов.
Оценка хондропротективного действия Алфлутопа у больных ОА проведена в 2003 г. Н.И. Коршуновым и соавт. [12]. Длительность наблюдения составила 12 месяцев. Действие Алфлутопа на структуры коленного сустава определяли с помощью магнитно-резонансной томографии коленного сустава. Измерение высоты суставного хряща проводилось в трех точках: в области передней и задней поверхности головки бедренной кости, а также в области наибольшего соприкосновения бедренной и большеберцовой костей коленного сустава. При этом в первой и второй точках измерялась высота суставного хряща бедренной кости, а в третьей – суммарная толщина хряща бедренной и большеберцовой костей. При визуальной оценке результатов магнитно-резонансной томографии независимым экспертом в основной группе улучшение наблюдалось у десяти (40%) пациентов, ухудшение – у трех (12%). У 12 (48%) больных изменения отсутствовали. В контрольной группе улучшение было зарегистрировано у четырех (17%) больных, ухудшение – у семи (29%). Изменения не отмечены у 13 (54%) пациентов. Таким образом, через 12 месяцев терапия Алфлутопом способствовала улучшению структур суставного хряща коленного сустава.
Данные, полученные И.Г. Салиховым (2003 г.) [13] и Н.А. Хитровым (2006 г.) [14], доказали эффективность параартикулярного введения Алфлутопа у больных гонартрозом с признаками поражения сухожильно-связочного аппарата, а также с энтезопатиями надостной и/или подлопаточной мышц. Курсовое введение препарата (2 мл с 15 мл 0,25%-ного раствора новокаина два раза в неделю, всего пять инъекций) в болевые точки, соответствующие энтезисам пораженных мышц, способствовало уменьшению боли в плечевом суставе, оцениваемой по визуальной аналоговой шкале, увеличению объема движений, снижению дозы принимаемых НПВП на 30–70%.
Эффект ранней (на субклинической стадии ОА) комбинированной хондропротективной терапии с применением Алфлутопа в 2019 г. изучали Д.А. Аршин и соавт. [15]. В исследование были включены 392 человека. Основную группу составил 361 пациент без клинических и рентгенологических признаков гонартроза, но с высоким риском его развития (субклинический гонартроз). Пациенты основной группы были разделены на две подгруппы. В течение двух лет первая группа (n = 190) не получала специфической терапии, вторая (n = 171) – применяла комбинированную хондропротективную терапию. Последняя предполагала назначение фиксированной комбинации хондроитина сульфата и глюкозамина гидрохлорида и внутримышечное введение препарата Алфлутоп. В контрольную группу вошел 31 человек без факторов высокого риска развития гонартроза. Исходно и через два года всем участникам исследования проведено ультразвуковое исследование коленных суставов. Анализировалась динамика минимальной толщины гиалинового хряща. У пациентов с факторами высокого риска развития гонартроза наблюдалось достоверное снижение минимальной высоты гиалинового хряща коленного сустава по сравнению с лицами в контрольной группе. Через два года наблюдения у получавших комбинированную хондропротективную терапию зафиксировано достоверно меньшее снижение минимальной толщины гиалинового хряща, чем у не применявших специфической терапии. Следовательно, назначение Алфлутопа в комплексном лечении раннего ОА замедляло его прогрессирование.
В недавно опубликованном клиническом исследовании К.А. Бердюгина и соавт. (2020 г.) сравнивались эффективность и безопасность внутрисуставного введения гиалуроновой кислоты у 76 больных ОА коленного сустава, получавших и не получавших курсовое лечение Алфлутопом [16]. Через шесть месяцев динамика всех показателей индекса WOMAC оказалась достоверно лучше в группе комбинированной терапии, чем в группе монотерапии.
Эффективность применения Алфлутопа при посттравматическом ОА коленного сустава оценивали Е.А. Трофимов и соавт. (2016 г.) [17]. В исследовании принял участие 61 пациент. Больных разделили на три группы. В первой группе использовали эторикоксиб в дозе 60 мг/сут, во второй – внутримышечные инъекции Алфлутопа, в третьей – внутрисуставные инъекции гиалуроновой кислоты. Через 12 месяцев наилучший результат по динамике WOMAC был получен у применявших Алфлутоп. Более того, данный препарат оказывал существенное положительное влияние на структуру хряща. Так, по данным магнитно-резонансной томографии, он способствовал замедлению деструктивных изменений.
В 2019 г. изучена клиническая эффективность внутримышечного или локального применения Алфлутопа (в виде монотерапии локальными инъекциями в пораженные зоны, комбинированной терапии с глюкокортикостероидами, сочетания локальных и внутримышечных введений) при заболеваниях околосуставных тканей различной локализации (энтезите, тендините и бурсите) [18, 19]. Алфлутоп продемонстрировал хороший эффект как в качестве моно-, так и в качестве комбинированной терапии. На фоне применения Алфлутопа отмечалось выраженное снижение интенсивности боли.
Алфлутоп зарекомендовал себя и в неврологической практике [20]. В частности, препарат оказался перспективным при хронической вертеброгенной люмбоишиалгии. В двойном слепом плацебоконтролируемом исследовании, проведенном О.С. Левиным и соавт. (2008 г.), Алфлутоп был наиболее эффективным у пациентов молодого и среднего возраста с относительно короткой продолжительностью заболевания и текущего обострения, при поражении фасеточных суставов [20]. Исследователи сравнивали эффективность внутримышечного (20 инъекций по 1 мл) у 32 больных и паравертебрального (по 0,25 мл в четыре точки два раза в неделю, всего пять введений) у 22 пациентов введения Алфлутопа. Состояние участников исследования оценивали через один, три и шесть месяцев. У всех больных исходно наблюдали некорешковую/корешковую вертеброгенную люмбоишиалгию, умеренный или выраженный болевой синдром, хроническое или рецидивирующее течение с длительностью обострения не менее месяца. Через месяц терапии Алфлутопом отмечено достоверное уменьшение и вертеброгенного синдрома, и боли по сравнению с плацебо. При этом более выраженный эффект получен в группе паравертебрального введения препарата. Через три месяца от начала курса лечения возрастание эффекта также было более значимым у получавших паравертебральные инъекции. Поэтому ученые рекомендовали при обострении вертеброгенной люмбоишиалгии начинать курс лечения с паравертебральных инъекций, затем переходить на внутримышечные. Это позволит достоверно улучшить функциональное состояние пациентов и купировать болевой синдром на длительный срок.
При синдроме хронической боли в нижней части спины после первого курса лечения Алфлутопом полное его купирование отметили 7,1% пациентов, после второго – 35,7%. В контрольной группе такого эффекта не наблюдалось. В основной группе также установлено статистически достоверное (p = 0,001) ступенчатое снижение показателя теста Томайера. Через три месяца он уменьшился в 3,6 раза по сравнению с исходными значениями. За период лечения у пациентов основной группы отмечено увеличение объема статической и динамической нагрузки на позвоночник в два – два с половиной раза, что оценивалось по индексу хронической нетрудоспособности Ваделя. По окончании лечения Алфлутопом 42,9% пациентов основной группы и только 5,6% контрольной прекратили прием НПВП [21, 22].
Данные, полученные в клинических исследованиях, послужили основанием для включения препарата Алфлутоп в рекомендации Ассоциации ревматологов России по лечению ОА и Консенсус по лечению боли в спине [23, 24].
Алфлутоп способен воздействовать и на воспаление, ассоциированное с возрастными изменениями в организме (inflammaging), за счет влияния на вовлеченные в этот процесс сигнальные пути. Установлено, что он может опосредованно способствовать профилактике некоторых гериатрических проблем, таких как запоры, депрессия и др. Поэтому его можно рассматривать в качестве препарата комплексной антивозрастной терапии (anti-age medicine) [25].
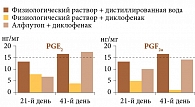
И.А. Куксгауз и соавт. (2019 г.) изучали гастропротективный эффект препарата Алфлутоп на модели индуцированной диклофенаком гастропатии у крыс [26]. Введение диклофенака в течение 20 дней привело к значимому снижению уровней простагландинов (Pg) E2 и F2α по сравнению с группами, не получавшими НПВП. После отмены диклофенака за 20 дней уровни Pg не восстановились. Напротив, наблюдалось еще большее снижение концентраций по сравнению с 21-м днем эксперимента. Применение Алфлутопа привело к нормализации уровней PGE2 и PGF2α в группах со сформированной гастропатией (рис. 4).
В.Н. Дроздов и Е.В. Коломиец (2005 г.) в ходе проспективного наблюдения установили, что включение Алфлутопа в комплексную терапию больных гонартрозом второй и третьей стадии позволило значительно сократить или полностью отказаться от приема НПВП, что снижало или исключало риск их повреждающего воздействия на желудочно-кишечный тракт [27].
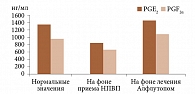
Алфлутоп ассоциируется с нормализацией уровня Pg, сниженного на фоне приема НПВП, и уменьшением времени эпителизации язвенных и эрозивных дефектов, возникших при их применении, на фоне стандартной противоязвенной терапии (рис. 5).
Заключение
Алфлутоп является одним из наиболее широко используемых симптоматических медленно действующих лекарственных средств при остеоартрите и остеохондрозе. Он действует на молекулярно-клеточном уровне. В частности, стимулирует пролиферацию хондроцитов, активирует синтез внеклеточного матрикса посредством модуляции TGF-β, ингибирует гиалуронидазу, окислительный стресс и активность внеклеточной экспрессии генов провоспалительных цитокинов IL-1β, IL-6 и IL-8 in vitro.
Многочисленные клинические исследования свидетельствуют о плейотропном эффекте Алфлутопа у пациентов с ОА, заболеваниями околосуставных тканей, а также у лиц пожилого возраста в качестве anti-age-терапии. Кроме того, отмечены длительный период ремиссии (до шести месяцев) и высокий профиль безопасности при коморбидных состояниях (НПВП-гастропатиях, сахарном диабете, артериальной гипертензии, дислипидемии).
Собранная к настоящему времени доказательная база обусловливает целесообразность применения Алфлутопа не только в ревматологической, но и в травматологической, ортопедической, неврологической, терапевтической практике и спортивной медицине.
Не так давно была предложена новая схема применения Алфлутопа при ОА – десять внутримышечных инъекций по 2 мл через день. Короткий курс терапии не уступает по эффективности стандартному 20-дневному курсу.
I.B. Belyayeva, MD, PhD, Prof., V.I. Mazurov, Academician of RAS, MD, PhD, Prof., Ye.A. Trofimov, PhD
North-Western State Medical University named after I.I. Mechnikov
Contact person: Irina B. Belyayeva, belib@mail.ru
Alflutop is an original complex injection drug, which is the bioactive concentrate of small marine fish and is produced according to the standards of good manufacturing practice. Currently, it is one of the most widely used symptomatic slow-acting drugs against osteoarthritis in Russia.
The article presents the results of experimental studies that proved the genetic, molecular and cellular mechanisms of Alflutop action. It was found that the drug stimulates the proliferation of chondrocytes, activates the synthesis of the extracellular matrix by modulating the transforming growth factor β, inhibits hyaluronidase, as well as oxidative stress and the activity of extracellular expression of proinflammatory cytokine genes (interleukins 1β, 6 and 8). In addition, the data of numerous clinical studies are presented, indicating the effectiveness of Alflutop in subclinical and advanced osteoarthritis, diseases of the periarticular tissues, as an anti-aging therapy in the elderly, and its high safety profile in comorbid patients, in particular in patients with gastropathies caused by taking nonsteroidal anti-inflammatory drugs, diabetes mellitus, arterial hypertension, dyslipidemia.
The evidence base collected to date serves as the justification for the widespread use of Alflutop in rheumatological, traumatological, orthopedic, neurological and therapeutic practice.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.