Прогнозирование исходов послеоперационного эндофтальмита: факторы риска и прогностические модели
- Аннотация
- Статья
- Ссылки
- English
Введение
Послеоперационный эндофтальмит (ПОЭ) является одним из наиболее грозных осложнений интраокулярной хирургии. Частота возникновения ПОЭ после плановых операций составляет 0,02–0,1%, при наличии факторов риска может достигать 0,5–1,0% [1, 2]. Несмотря на совершенствование методов диагностики и лечения, исходы ПОЭ остаются вариабельными: от полного восстановления зрительных функций до необратимой слепоты и утраты глаза [3].
Как показывает клинический опыт, течение заболевания и его исход определяются множеством факторов, которые можно разделить на несколько групп: связанные с пациентом (возраст, наличие сахарного диабета, иммунный статус), возбудителем (вид микроорганизма, его вирулентность и чувствительность к антибиотикам), клинической картиной на момент госпитализации (острота зрения, наличие гипопиона, вовлечение заднего сегмента), а также с лечебной тактикой (сроки начала терапии, выбор между интравитреальными инъекциями и витрэктомией) [4, 5].
Способность прогнозировать исход ПОЭ имеет критическое значение для практикующего офтальмолога по ряду причин:
- выбор тактики лечения: пациенты с высоким риском неблагоприятного исхода могут потребовать более агрессивного подхода (ранняя витрэктомия, комбинированная терапия);
- информирование пациента: реалистичная оценка прогноза позволяет пациенту и его семье подготовиться к возможным исходам, в том числе длительной реабилитации или утрате глаза;
- планирование реабилитации: раннее прогнозирование неблагоприятного исхода позволяет своевременно подключить психологическую поддержку и начать подготовку к протезированию;
- сравнительная оценка эффективности: стратификация по факторам риска необходима для корректного сравнения результатов лечения в разных центрах и при использовании различных методик [6, 7].
Цель настоящего обзора – систематизировать современные данные о факторах, влияющих на прогноз ПОЭ, проанализировать существующие прогностические модели и оценить перспективы их клинического применения.
Факторы, связанные с пациентом
Возраст
Роль возраста в исходах ПОЭ после хирургии катаракты изучалась в ряде исследований. Показано, что пожилой возраст ассоциирован с более высоким риском развития ПОЭ и менее благоприятным функциональным исходом, включая более низкую вероятность достижения высокой остроты зрения после операции. В крупных популяционных анализах пациенты старших возрастных групп (75–84 лет, особенно ≥ 85 лет) имели статистически значимо более высокий риск неблагоприятных исходов по сравнению с пациентами 60–74 лет даже после поправки на ряд клинических переменных. Предполагается, что это связано с возраст-зависимым снижением иммунного ответа, замедлением репаративных процессов и более высокой распространенностью сопутствующей патологии у пожилых пациентов, что ухудшает контроль инфекции и восстановление тканей. В то же время не во всех моделях возраст сохраняет значение независимого предиктора: в ряде многофакторных анализов после учета коморбидности, тяжести исходного состояния и особенностей течения инфекции вклад возраста утрачивал статистическую значимость, что указывало на опосредованный характер его влияния через функциональный статус и сопутствующие заболевания [8]. Вероятно, возраст сам по себе является суррогатным маркером общей соматической отягощенности и его эффект реализуется преимущественно через ассоциированную коморбидность и сниженный резерв адаптации.
Сахарный диабет
Сахарный диабет (СД) традиционно рассматривается как фактор риска развития и более тяжелого течения инфекционных осложнений, что связано с нарушениями иммунного ответа, микроангиопатией и замедленным заживлением тканей. У больных СД описаны изменения врожденного и адаптивного иммунитета, нарушение репарации эпителия и склонность к более вирулентной микрофлоре, что повышает вероятность тяжелого течения ПОЭ и задержки санации внутриглазной инфекции [9].
Ряд клинических исследований свидетельствует о худших функциональных исходах ПОЭ у пациентов с СД. В поданализе Endophthalmitis Vitrectomy Study только 39% пациентов с диабетом достигли конечной остроты зрения 20/40, что отражает более неблагоприятный зрительный прогноз у этой категории больных. Систематический обзор экзогенного эндофтальмита у пациентов с СД также показал, что у них существенно ниже доля глаз, достигающих удовлетворительного зрения (≥ 20/40 и ≥ 20/100), и выше частота тяжелой потери зрения по сравнению с пациентами без СД. Современные данные указывают и на повышенный риск самого ПОЭ у больных диабетом после внутриглазных вмешательств (включая операцию катаракты), что дополнительно усиливает значимость СД как фактора неблагоприятного исхода [10].
Иммуносупрессия
Пациенты, получающие иммуносупрессивную терапию (глюкокортикостероиды, цитостатики, биологические агенты), имеют повышенный риск тяжелого течения инфекционных заболеваний.
В исследовании F.M. Recchia и соавт. доля иммуносупрессии составила 12% всех случаев ПОЭ, но с ней связан 31% неблагоприятных исходов (p < 0,01) [11].
Факторы, связанные с возбудителем
Вид микроорганизма
Вид возбудителя является одним из наиболее значимых предикторов исхода ПОЭ:
- коагулазонегативные стафилококки, прежде всего Staphylococcus epidermidis, ассоциированы с наиболее благоприятным прогнозом;
- S. aureus связан с более агрессивным течением, особенно при метициллин-резистентности;
- Streptococcus spp.: быстрое прогрессирование и высокая частота неблагоприятных исходов;
- Enterococcus spp.: высокая вирулентность, нередко множественная лекарственная устойчивость и, как следствие, неблагоприятный прогноз;
- грамотрицательные бактерии (Pseudomonas aeruginosa, Klebsiella spp.): агрессивное течение, часто с развитием необратимых изменений;
- грибы (Candida spp., Aspergillus spp.): торпидное течение, трудности диагностики, необходимость специфической терапии [12].
M. Ather и соавт. провели стратифицированный анализ исходов в зависимости от типа патогена. Пациенты, инфицированные вирулентными патогенами, не являющимися комменсалами поверхности глаза (Streptococcus spp., Enterococcus spp.), имели значительно худшую конечную остроту зрения по сравнению с пациентами, инфицированными коагулазонегативными стафилококками (средний logMAR 2,14 против 0,77; p < 0,001), а также более высокие показатели третьих вмешательств (27,5 против 10,1%), развития фтизиса (15,4 против 1,1%) и энуклеации/эвисцерации (12,8 против 0%) [9].
Антибиотикорезистентность
Резистентность возбудителя к антибиотикам первой линии существенно ухудшает прогноз. В исследовании F.Z.A. Ali и соавт., посвященном MRSA-эндофтальмиту, только у 56% пациентов отмечалось улучшение остроты зрения через месяц, у 33% – через три месяца и у 22% – через шесть месяцев. Осложнения включали эвисцерацию и фтизис [13].
Особую проблему представляют инфекции, вызванные ванкомицин-резистентными энтерококками (ВРЭ). M. Khera и соавт. описали шесть случаев ВРЭ-эндофтальмита, акцентировав внимание на сложности лечения и неблагоприятных исходах [14].
Микробная нагрузка и биопленки
Образование бактериальных биопленок на поверхности интраокулярных линз (ИОЛ) затрудняет эрадикацию инфекции и ухудшает прогноз. Биопленки формируются преимущественно стафилококками и энтерококками, защищая микроорганизмы от антибиотиков и иммунного ответа. В таких случаях может потребоваться удаление ИОЛ для достижения санации [15].
Факторы, связанные с клинической картиной
Острота зрения при госпитализации
Острота зрения на момент установления диагноза является одним из наиболее значимых предикторов конечного исхода. В исследовании показано, что исходная острота зрения менее 5/200 (счет пальцев у лица) ассоциирована с худшим прогнозом независимо от выбранной тактики лечения [6].
В многофакторном анализе A. Combey de Lambert и соавт. исходная острота зрения вошла в финальную прогностическую модель как независимый фактор с наибольшим весовым коэффициентом [16].
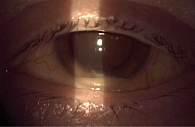
Наличие и высота гипопиона
Гипопион – классический признак ПОЭ, однако его прогностическое значение неоднозначно. С одной стороны, наличие гипопиона подтверждает диагноз и свидетельствует о выраженности воспаления, с другой – небольшая высота гипопиона может наблюдаться при синдроме токсического поражения переднего отрезка глаза, а также на ранних стадиях эндофтальмита (рис. 1). В исследовании G.A. Lalwani и соавт. высота гипопиона > 1,5 мм коррелировала с худшим прогнозом [17].
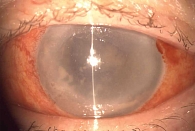
Вовлечение заднего сегмента
Отсутствие рефлекса с глазного дна, наличие экссудата в стекловидном теле по данным В-сканирования, вовлечение сетчатки и зрительного нерва ассоциированы с неблагоприятным прогнозом (рис. 2). В исследовании пациенты с отсутствием рефлекса имели лучшие исходы при проведении витрэктомии по сравнению с интравитреальными инъекциями [6].
Факторы, связанные с лечебной тактикой
Сроки начала терапии
Время от появления симптомов до начала адекватной терапии критически влияет на исход. Задержка начала терапии более чем на 24 часа связана с худшими функциональными исходами (относительный риск (ОР) неблагоприятного исхода 2,3; 95%-ный доверительный интервал (ДИ) 1,5–3,5) [18].
Выбор метода лечения
Установлено, что пациенты с исходной остротой зрения менее 5/200 имеют лучшие исходы при выполнении немедленной витрэктомии по сравнению с интравитреальными инъекциями [6]. Однако для пациентов с лучшей исходной остротой зрения различий между подходами не выявлено.
Современные исследования подтверждают эти данные. Показано, что витрэктомия предпочтительна при тяжелых формах ПОЭ, особенно вызванных высоковирулентными микроорганизмами [19].
Повторные вмешательства
Повторные хирургические вмешательства (ревизия передней камеры, повторная витрэктомия, введение силикона) служат маркером тяжелого течения и ассоциированы с худшим прогнозом. В исследовании M. Ather и соавт. частота третьих вмешательств была в 2,7 раза выше при инфекциях, вызванных вирулентными патогенами [9].
Прогностические модели
Модель EVS (1995)
Классическая модель EVS основана на исходной остроте зрения:
- при остроте зрения ≥ 5/200 прогноз относительно благоприятный, различий между тактиками нет;
- при остроте зрения < 5/200 прогноз хуже, витрэктомия предпочтительнее.
Чувствительность и специфичность модели ограниченны, поскольку она учитывает только один фактор [6].
Модель A. Combey de Lambert (2013)
Во французском многоцентровом исследовании (n = 102) была разработана прогностическая модель на основании многофакторного анализа. В модель вошли:
- исходная острота зрения (весовой коэффициент 3);
- сахарный диабет (2);
- возраст > 75 лет (1);
- вид возбудителя (Streptococcus/Enterococcus – 3, прочие – 0).
Модель позволяет рассчитать индивидуальный риск неблагоприятного исхода с чувствительностью 82% и специфичностью 79% [16].
Модель M. Ather (2025)
Это наиболее современная модель, разработанная на основании анализа данных 240 пациентов с острым ПОЭ. Методом множественной логистической регрессии выделены независимые предикторы:
- вирулентный патоген (ОР 4,2; 95% ДИ 2,1–8,4);
- исходная острота зрения < 0,05 (ОР 3,1; 95% ДИ 1,6–5,9);
- возраст > 80 лет (ОР 2,2; 95% ДИ 1,1–4,3);
- сахарный диабет (ОР 1,9; 95% ДИ 1,0–3,6);
- задержка лечения > 24 ч (ОР 2,5; 95% ДИ 1,3–4,8).
Модель продемонстрировала хорошую дискриминационную способность (площадь под ROC-кривой (AUC) – 0,84) [9].
Перспективные подходы: машинное обучение и искусственный интеллект
Современные методы машинного обучения (machine learning, ML) открывают новые возможности для прогнозирования исходов ПОЭ. Преимущества ML-подходов:
- возможность учета нелинейных взаимодействий между факторами;
- обработка большого числа переменных;
- автоматическое выявление скрытых закономерностей;
- постоянное улучшение модели по мере накопления данных.
Исследование С.А. Абакарова в диссертации по посттравматическому эндофтальмиту
На основании однофакторного и многофакторного регрессионного анализа разработана прогностическая модель оценки вероятности развития эндофтальмита у пациентов с проникающим ранением глаза, в которую включены восемь независимых предикторов, проявивших статистическую значимость на уровне р < 0,1: возраст старше 55 лет, женский пол, локализация повреждений в зоне II, наложение менее четырех швов на 1 см2, наличие гнойного отделяемого, гипопион, тотальная гифема, выполнение факоэмульсификации катаракты [18].
Ограничения и перспективы
Несмотря на обнадеживающие результаты, применение ML в клинической практике ограничено:
- большими выборками для обучения;
- риском переобучения моделей;
- сложностями интерпретации результатов («черный ящик»);
- отсутствием валидации на независимых когортах.
Перспективными направлениями являются создание мультицентровых баз данных, унификация протоколов сбора информации и разработка интерпретируемых моделей (explainable AI) [20].
Клиническое применение прогностических моделей
Выбор тактики лечения
Исходя из прогноза риска неблагоприятного исхода, можно дифференцированно подходить к выбору тактики:
- при низком риске – терапия интравитреальными инъекциями, тщательное наблюдение;
- среднем риске – витрэктомия, комбинированная терапия;
- высоком риске – немедленная витрэктомия, раннее введение силикона, системная антибиотикотерапия, рассмотрение вопроса об удалении ИОЛ [21].
Информирование пациента
Прогностическая модель позволяет предоставить пациенту и его семье объективную информацию о вероятных исходах, что способствует реалистичным ожиданиям и лучшей приверженности лечению.
Планирование реабилитации
При высоком риске неблагоприятного исхода можно заблаговременно начинать психологическую подготовку к возможной утрате глаза, консультирование по вопросам протезирования, подключение служб медико-социальной помощи.
Заключение
Прогнозирование исходов ПОЭ – сложная многокомпонентная задача, требующая учета факторов, связанных с пациентом (возраст, коморбидность, иммунный статус), возбудителем (вид, вирулентность, резистентность), клинической картиной (острота зрения, гипопион, вовлечение заднего сегмента) и лечебной тактикой (сроки, метод, необходимость повторных вмешательств).
Наиболее значимыми независимыми предикторами неблагоприятного исхода служат:
- вид возбудителя (особенно Streptococcus spp., Enterococcus spp.);
- исходная острота зрения < 0,05;
- сахарный диабет;
- задержка начала адекватной терапии > 24 часов;
- возраст старше 75–80 лет.
Существующие прогностические модели (A. Combey de Lambert, M. Ather) обладают хорошей прогностической способностью (AUC 0,82–0,84) и могут использоваться в клинической практике. Перспективным направлением является применение методов машинного обучения, характеризующихся более точными индивидуальными прогнозами с учетом сложных взаимодействий между факторами.
Ключевыми направлениями для будущих исследований являются:
- валидация существующих моделей на крупных мультицентровых когортах;
- разработка удобных для клинического применения калькуляторов риска (веб-интерфейсы, мобильные приложения);
- интеграция прогностических моделей в клинические рекомендации;
- изучение возможности использования новых биомаркеров (цитокины, генетические маркеры) для улучшения прогноза.
Точное прогнозирование исхода ПОЭ позволит оптимизировать лечебную тактику, улучшить информирование пациентов и более эффективно планировать реабилитационные мероприятия, что в конечном итоге будет способствовать улучшению результатов лечения этого тяжелого осложнения.
S.A. Abakarov, PhD, M.S. Laouar, I.A. Loskutov, PhD
Moscow Regional Research and Clinical Institute
Contact person: Sapiyulla A. Abakarov, abakarov.s@moniki.ru
Postoperative endophthalmitis remains the most severe infectious complication in ophthalmic surgery, the outcomes of which range from complete restoration of visual functions to loss of the eye. The ability to predict the course of the disease and its outcome is crucial for choosing optimal treatment tactics, informing the patient and planning rehabilitation measures. The article systematizes current data on factors affecting the prognosis of postoperative endophthalmitis, predictors related to the patient (age, comorbidity), pathogen (type of microorganism, virulence, antibiotic resistance), clinical picture (visual acuity at admission, presence of hypopion, involvement of the posterior segment), as well as therapeutic tactics (timing of intervention, method selection). The existing prognostic models, their sensitivity and specificity, and the possibilities of application in clinical practice are analyzed. The prospects of using machine learning and artificial intelligence to create more accurate individual forecasts are considered.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.